一种治疗T细胞急性淋巴细胞白血病的复方纳米制剂及制备方法和应用与流程
本发明属于复方纳米制剂
技术领域:
,特别是一种用于治疗t细胞急性淋巴细胞白血病的复方纳米制剂药物,同时还涉及一种治疗t细胞急性淋巴细胞白血病的复方纳米制剂的制备方法,还涉及一种复方纳米制剂在制备治疗或预防t细胞急性淋巴细胞白血病药物中的用途。
背景技术:
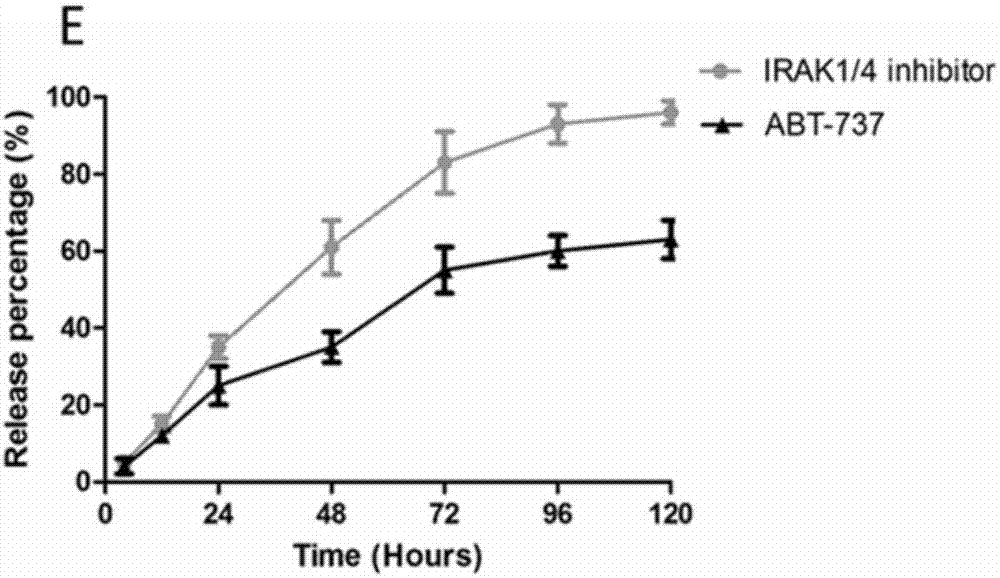
:t细胞急性淋巴细胞白血病(t-all)是由变异型t细胞祖细胞的克隆扩增引起的,被认为是高危白血病,占儿童急性淋巴细胞性白血病的15%左右,成人高达25%。随着当代化疗,儿童的完全缓解率高达85%,但在成人中并不理想。成人t-all患者复发后仅有15%-25%的患者预后良好,5年生存率低于50%。因此,更有效的治疗t-all患者的疗法是临床急需要开发拓展的。目前,有各种各样的激酶抑制剂正在被开发用于靶向细胞生长和差异的各种信号通路。这类激酶抑制剂能够阻止恶性细胞的分化和增殖,像常规化疗药物那样消除恶性细胞。然而,激酶抑制剂与化疗药物的组合具有产生协同效应和改善临床结果的潜力。白细胞介素-1(il-1)受体相关激酶4(irak4)可以激活各种转录因子以促进t细胞的存活或增殖。已经显示irak1/4抑制剂显著损害恶性t细胞系增殖,但对体外恶性t细胞的细胞存活率无显著影响。当irak1/4抑制剂与治疗化合物结合时,各种类型的抗白血病药物的细胞毒活性被irak1/4抑制剂增强。abt-737是一种破坏微管的药物,由于abt-737对b淋巴细胞瘤-2(bcl-2)和b淋巴细胞瘤-xl(bcl-xl)有抑制作用,而对mcl1无效。但是irak1/4抑制剂可以下调mcl1水平,这种相互补充的作用,使得这两种药物联合使用时对恶性t-all细胞的细胞毒性作用产生最大的协同效应。尽管通过irak1/4抑制剂和abt-737的组合,对恶性t-all细胞的细胞毒性作用有所改善,但是与此同时,对健康细胞相应的毒副作用也随之增加。然而化疗药物引起的全身性毒副作用是目前化疗药物在白血病临床治疗中的最大挑战和障碍。研究表明纳米颗粒的药物递送系统通过增强肿瘤细胞的通透性和保留时间,改善药代动力学特征,可以进一步加强这两种药物的协同效用,从而降低化疗药物的给药剂量,达到减少化疗毒副作用的目的。在这些基础上,本发明设计将激酶抑制剂irak1/4与化疗药物abt-737包封进聚合物纳米颗粒或者质脂体纳米颗粒中组成一种新的复方纳米药物,用于进一步加强这两种药物的协同效应,改善t细胞急性淋巴细胞白血病的治疗效果,并降低毒副作用。技术实现要素:针对上述存在的问题和目前化疗药物的毒副作用大的问题,本发明的目的是在于提供了一种治疗t细胞急性淋巴细胞白血病的复方纳米制剂,配方合理,使用方便,通过将irak1/4抑制剂和abt-737包裹进纳米颗粒组合成新的复方纳米制剂,通过纳米颗粒增加药物在肿瘤细胞内的吸收与分布,增强这两种药物的协同效应。与两种药物的溶液组合方式相比,纳米颗粒显著增加了两种药物对t细胞急性淋巴白血病细胞生长的制剂作用,使得wbc得到明显改善,存活率也相应延长。本发明的另一个目的是在于提供了一种治疗t细胞急性淋巴细胞白血病的复方纳米制剂的制备方法,方法易行,操作简便,通过乳化溶剂挥发将irak1/4抑制剂和abt-737共同包封进纳米颗粒中。通过本方法可以以较高的包封率将两种药物同时包封进纳米颗粒中,并具有缓控释的效果,使得两种药物能保持同时从纳米颗粒中缓慢释放出来,在体内被吸收时发挥协同效应。本发明还有一个目的是在于提供了一种复方纳米制剂在制备治疗或预防t细胞急性淋巴细胞白血病药物中的应用,复方纳米制剂通过增强肿瘤细胞的通透性和保留时间,改善药代动力学特征,可以进一步加强这两种药物的协同效用,从而降低化疗药物的给药剂量,达到减少化疗毒副作用的目的。为了实现上述的目的,本发明是通过以下技术方案实现:本发明的技术构思是:将irak1/4抑制剂和abt-737共同包封进纳米颗粒中,以增强irak1/4抑制剂和abt-737对t-all的协同治疗作用。使用试验设计对纳米颗粒配方进行优化以实现高的药物负载。考察药物从纳米颗粒中释放的情况,以及载药纳米颗粒对t-all细胞系生长的抑制率。依据ic50计算出协同效应,比较载药纳米药物与药物溶液组合的协同效果,纳米药物的协同效应高于药物溶液组合。然后在t-allpdx小鼠模型上,进一步对纳米药物的疗效和毒性进行评价,并与药物溶液组合进行比较。结果表明:载药纳米药物的治疗效果优于药物溶液组合,但毒副作用低于药物溶液组合。一种治疗t细胞急性淋巴细胞白血病的复方纳米制剂,它由以下重量份的原料制成:所述的irak1/4抑制剂与abt-737的混合物是由rak1/4抑制剂与abt-737按重量比1:1的比例混合配制成的。所述的聚乳酸-聚羟基乙酸的质量体积浓度0.5%-3.5%,优选为2.98%。所述的聚乙烯醇溶液的质量体积浓度为2%。一种治疗t细胞急性淋巴细胞白血病的复方纳米制剂,它由以下重量份的原料制成:(优选范围)一种治疗t细胞急性淋巴细胞白血病的复方纳米制剂,它由以下重量份的原料制成:(最好范围)一种治疗t细胞急性淋巴细胞白血病的复方纳米制剂,它由以下重量份的原料制成:(具体值)一种治疗t细胞急性淋巴细胞白血病的复方纳米制剂的制备方法,其步骤是:(1)将含有一定量的聚乳酸-聚羟基乙酸(plga)聚合物,irak1/4抑制剂和abt-737溶解在3ml乙腈溶液中,得到混合溶液;(2)将步骤(1)得到的混合溶液在12ml2%(w/v)的聚乙烯醇溶液中乳化以形成乳液,使用具有70w能量输出的微型探针超声波仪在冰浴上乳化2-4分钟,得到一种乳液;(3)将步骤(2)得到的乳液在室温(20-25℃,以下相同)下搅拌15-17小时以蒸发有机溶剂,得到irak1/4抑制剂和abt-737的复方纳米颗粒;(4)将步骤(3)得到的复方纳米颗粒在3-5℃超速离心机以30,000rpm超速离心28-32分钟收集纳米颗粒,并用蒸馏水洗涤两次,然后冻干保存,得到含有irak1/4抑制剂和abt-737的irak/abt-纳米颗粒(irak/abt-np)。本发明的另一方面,还提供了上述复方纳米制剂在制备治疗或预防t细胞急性淋巴细胞白血病药物中的应用。本发明与现有技术相比,具有以下优点和效果:针对目前成人t-all患者复发后预后效果不理想,5年生存率不到50%的现状。通过复方纳米制剂进一步加强药物的协同效应,增强对t-all的疗效,延长生存率。与现有的普通联合用药相比,复方纳米制剂通过缓控释作用,配方合理,使用方便,延长了药物的代谢时间;增加了药物在肿瘤细胞中的吸收,从而进一步增强了药物的协同作用。通过本方法可以以较高的包封率将两种药物同时包封进纳米颗粒中,并具有缓控释的效果,使得两种药物能保持同时从纳米颗粒中缓慢释放出来,在体内被吸收时发挥协同效应。复方纳米制剂通过增强肿瘤细胞的通透性和保留时间,改善药代动力学特征,可以进一步加强这两种药物的协同效用,从而降低化疗药物的给药剂量,达到了减少化疗毒副作用的目的。附图说明图1为irak/abt聚合物纳米颗粒扫描电子显微镜(sem)图像(左),粒径分布(中),透射电子显微镜(tem)图像(右);图2为irak/abt聚合物纳米颗粒体外释放药物;图3为用irak/abt聚合物纳米颗粒,单独的irak1/4抑制剂,单独的abt-737和一系列浓度的联合溶液处理的jurkat细胞的体外细胞活力;图4为在不同配方药物治疗后t-all异种移植小鼠中wbc的变化;图5为生存曲线显示每组治疗组的死亡率。具体实施方式实施例1:一种治疗t细胞急性淋巴细胞白血病的复方纳米制剂,它由以下重量份的原料制成:所述的irak1/4抑制剂与abt-737的混合物是由rak1/4抑制剂与abt-737按重量比1:1的比例混合配制成的。所述的聚乳酸-聚羟基乙酸的质量体积浓度为2.98%。所述的聚乙烯醇溶液的质量体积浓度为2%。一种治疗t细胞急性淋巴细胞白血病的复方纳米制剂的制备方法,其步骤是:(1)将含有一定量的聚乳酸-聚羟基乙酸(plga)聚合物(赢创工业股份公司),irak1/4抑制剂和abt-737溶解在3ml乙腈溶液中,得到混合溶液;(2)将步骤(1)得到的混合溶液在12ml2%(w/v)的聚乙烯醇溶液中乳化以形成乳液,使用具有70w能量输出的微型探针超声波仪(vc505,vibracellsonics,newtown,ct,usa)在冰浴上乳化3分钟,得到一种乳液;(3)将步骤(2)得到的乳液在室温下搅拌16小时以蒸发有机溶剂,得到irak1/4抑制剂和abt-737的复方纳米颗粒;(4)将步骤(3)得到的复方纳米颗粒在4℃超速离心机(sorvallultraspeedcentrifuge,kendro,usa)以30,000rpm超速离心30分钟收集纳米颗粒,并用蒸馏水洗涤两次,然后冻干保存,得到含有irak1/4抑制剂和abt-737的irak/abt-纳米颗粒(irak/abt-np)。通过本实施例可以以较高的包封率将irak1/4抑制剂和abt-737同时包封进纳米颗粒中,并具有缓控释的效果,使得两种药物能保持同时从纳米颗粒中缓慢释放出来,在体内被吸收时发挥协同效应。通过本实施例得到的irak/abt-纳米颗粒通过增强肿瘤细胞的通透性和保留时间,改善药代动力学特征,可以进一步加强这两种药物的协同效用,从而降低化疗药物的给药剂量,达到了减少化疗毒副作用的目的。实施例2-6:一种治疗t细胞急性淋巴细胞白血病的复方纳米制剂,它由以下重量份的原料制成:实施例2实施例3实施例4实施例5实施例6rak1/4抑制剂与abt-737的混合物1.52.53.54.55.5聚乳酸-聚羟基乙酸52708010040乙腈溶液12345聚乙烯醇溶液1224244545其制备步骤与实施例1相同。表征分析:动态光散射(dls)分析实施例1-6步骤(4)得到的irak/abt-np,结果表明,irak/abt-np的平均直径为100nm,单分散尺寸分布;通过sem和tem研究了表面形态,表明颗粒是球形(见图1)。实施例1步骤(4)得到的irak/abt-np体外释放试验:通过透析法对irak1/4抑制剂或abt-737的irak/abt-np进行体外释放。在实验之前,将透析膜(分子量截止值为10kda)在室温下浸入蒸馏水中过夜,并彻底冲洗以除去防腐剂。放置实施例1的步骤(4)得到的irak/abt-np后,透析袋密封。然后将其浸入50ml含有0.1%v/v吐温80的pbs(0.01m,ph7.4)的培养基中(以确保沉降条件),并保持在37℃和100rpm振荡培养箱中。分别在第24h,48h,72h,96h,120h,从振荡培养箱中取出0.5ml培养基(样品),并立即加入相同体积的新鲜培养基。将样品溶解在1ml乙腈溶液中。稀释样品中irak1/4抑制剂或abt-737的含量通过rp-hplc方法进行分析。使用流动相,其中含有0.1%(v/v)h3po4的乙腈溶液和0.1%(v/v)的h3po4水溶液。乙腈与水的比例为90:10(v/v)。使用四元泵在25℃下以0.8ml/min的流速输送流动相。通过在300nm处的紫外检测abt-737水平;通过在254nm处的紫外检测irak1/4抑制剂水平。实验一式三份进行。irak1/4抑制剂和abt-737均显示出peg-plganps的持续释放动力学,如图2所示。24h后,irak1/4抑制剂和abt-737分别从irak/abt-np释放出约35%和25%。然后,irak/abt-np呈现较慢的持续释放特征。超过80%的irak1/4抑制剂在72小时后释放,但在120小时后释放不到60%的abt-737。实施例1步骤(4)得到的irak/abt-np细胞毒性试验:通过基于mtt的比色测定法分析细胞毒性研究。测定单独irak1/4抑制剂、单独abt-737、irak1/4抑制剂和abt-737组合溶液(1:1,w/w)和实施例1的步骤(4)得到的irak/abt-np中不同浓度的irak1/4抑制剂和abt-737对jurkat细胞生长抑制的效力。将jurkat细胞接种在96孔板中并孵育24小时。用上述各种溶液不同浓度(0.01,0.10,1.00,2.00,5.00,10.00μm)的药物处理细胞,并在培养箱中孵育48小时。pbs(potassiumdihydrogenphosphate0.144g/l,sodiumchloride9g/l,disodiumphosphate0.795g/l,ph7.4)处理的细胞作为对照。仔细除去培养基,补充新鲜培养基(100μl)。然后向每个孔中加入10μl的5mg/ml的mtt,并在培养罩中37℃孵育3小时。再次除去培养基,向各孔中加入100μl二甲基亚砜。使用96孔格式elisa板读数器,用590nm的参考滤光片测量波长590nm处的吸光度。代谢活性细胞数量的减少导致吸光度的降低。通过比较代谢活性细胞的百分比与对照细胞的百分比来分析结果。如图3所示,单独irak1/4抑制剂在jurkat细胞中几乎没有杀伤作用。组合溶液的ic50为3.8μm,远低于单个abt-737的5.7μm。这些结果表明,irak1/4抑制剂在组合溶液中增强了abt-737的细胞毒活性。而irak/abt-np具有最低的ic50值为1.7μm,这意味着其具有比其他制剂更有潜力杀伤jurkat细胞。实施例1步骤(4)得到的irak/abt-np药效试验jurkat细胞(3×106个)尾静脉注射于25只雌性npg小鼠(beijingvitalstarbiotechnology,beijing,china)产生人类细胞系异种移植t-all小鼠模型。七天后,随机分为五组,每组五只。分别用irak抑制剂(10mg/kg)、abt-737(40mg/kg)、irak抑制剂+abt-737组合溶液(10mg/kg的irak抑制剂和40mg/kg的abt-737)、实施例1的步骤(4)得到的irak/abt-np分散于ph值7.4的磷酸盐缓冲液中((10mg/kg的irak抑制剂和40mg/kg的abt-737),pbs(potassiumdihydrogenphosphate0.144g/l,sodiumchloride9g/l,disodiumphosphate0.795g/l,ph7.4)作为对照,进行尾静脉注射,每周2次;四周后,各治疗组的小鼠外周血取出白血细胞(wbc)。如图4所示,用单一irak1/4抑制剂和abt-373处理的小鼠中的wbc数与pbs处理的小鼠没有显着差异。与pbs处理的小鼠相比,组合溶液处理的小鼠的wbc数明显减少。用irak/abt-np治疗的大约30%的小鼠恢复正常水平的白细胞数(2.6-10×103/μl)。wbc数据表明,irak/abt-np治疗的小鼠可以比其他制剂更好地改善t-all模型小鼠的淋巴细胞恶性增殖。与用组合溶液治疗的小鼠相比,具有irak/abt-np治疗的小鼠显示出显着更长的中位生存期(50vs65天,通过log-rank检验p<0.0001)(见图5)。实施例7:一种复方纳米制剂在制备治疗或预防t细胞急性淋巴细胞白血病药物中的应用,其步骤是:a、将干燥的复方纳米粉末制剂分散于注射用生理盐水中,浓度为2mg/ml;b、在涡旋器上震荡使得纳米混悬剂充分混匀,然后静脉注射或滴注。当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1