一种从多金属危险废物中分离精制铁、铬的方法与流程
本发明属于湿法冶金技术领域,具体涉及一种从多金属危险废物中分离精制铁、铬的方法。
背景技术:
目前,我国的含多金属危险废物主要是由电镀、表面处理、冶炼、化工等行业产生的污泥或废水,其中含有多种金属,包括铁、铬、铜、锌、镍、钴、锰等。而铬是一种毒性很强的重金属,容易进入人体细胞,对肝、肾等内脏器官和dna造成损伤,在人体内有蓄积作用,具有致癌性并可能诱发基因突变的危险性。含铬的污泥或废水排放到环境中不仅容易造成环境水体污染,同时对人类生命健康造成了直接威胁。因此,实现含铬废物的无害化处理至关重要。含铬废物的无害化处理技术总体上可分为两类:一类为固化稳定化技术,一类为再生利用技术。固化稳定化是利用固化剂将含铬废物固化在固化体中,以避免重金属铬流失到环境中,此法在有价金属回收利用方面显得略微不足。再生利用的特点是利用某种浸取剂浸出主要目标金属,再采用萃取、沉淀、电解等方法提取金属产品进行利用,以实现金属资源的循环再生。
金属铁与铬的化学性质非常相似,二者的分离一直是该研究领域的难题。目前铁铬分离的方法主要包括电解法、萃取法和沉淀法。某厂通过电解法使污泥酸浸滤液中的硫酸铬和硫酸铁转变为铬铵矾和铁铵矾,然后根据其在75°c条件下溶解度的不同而达到铬、铁分离的目的。祝万鹏等采用萃取法利用p204及p507作为萃取剂实现铁铬分离。邬建辉等用硫酸浸出废铬铁合金后,用莫尔盐结晶法分离溶液中的铁,此法需在70℃条件下反应6h,然后快速冷却结晶24h。王飞等人用双氧水将fe2+氧化为fe3+,再用碱沉淀除铁,实现铁铬分离。也有专利中用草酸与fe2+络合沉淀分离铁和铬。电解法能耗高,设备复杂,增加了危险废物的处置成本。萃取法中引进可循环利用的有机溶剂,但其使用寿命有限,增加了新的污染物。沉淀法利用不同种类及价态的金属与不同沉淀剂形成化合物的溶度积不同通过选择性沉淀而进行金属分离,能耗低,设备简单,但需要选择理想的沉淀剂并控制适当条件,一方面降低处理过程中的药剂成本和提高铁铬分离率,另一方面提高铁和铬二次金属资源的利用价值。
基于上述分析,一种全程无需加热,综合利用了危险废物中的铁离子和磷酸根,同时不会产生废水、废渣,对环境友好,提取的磷酸铁和氢氧化铬可进行二次利用的从多金属危险废物中分离精制铁、铬的方法是本行业目前急需的。
技术实现要素:
鉴于上述不足,本发明提供的从多金属危险废物中分离精制铁、铬的方法,全程无需加热,最大程度的利用了危险废物中的铁离子和磷酸根,制备过程不会产生废水、废渣,对环境友好。
为了达到上述目的,本发明采用了以下技术方案,本发明所使用的各物质浓度和ph值区间内分离的精制铁、铬均能用于化工业的二次使用。
一种多金属危险废物中分离精制铁、铬的方法包括以下步骤:
(1)酸浸:将含有金属元素的综合污泥进行配料,向污泥中加入水制浆,边搅拌边缓慢加入98%的h2so4,调节ph稳定在0.5时,停止加酸,继续溶解,使污泥中的各金属元素进入到溶液中;
(2)压滤:将酸浸后溶液进行压滤,压滤滤渣进行洗涤,洗涤水返回作调浆水用,洗涤后的渣进行纯化处理,压滤滤液进入下一道工序继续处理;
(3)粗制铁铬矾:将收集的滤液放入容器中搅拌,于常压下缓慢加入caco3浆液调节ph至4.0,继续反应,缓慢加入h2o2,同时用caco3浆液控制ph至3.8~4.1,直到h2o2将fe2+完全氧化为fe3+,然后压滤,得到的滤饼为粗制铁铬矾,滤液进入铜、锌、镍、钴、锰分离工序;
(4)溶解粗铁铬矾:将粗制铁铬矾滤饼与水制浆,向其中加入98%的h2so4调节ph至0.5使铁、铬进入到溶液中,然后压滤,滤饼为粗制石膏(主成分二水硫酸钙),经纯化洗涤得到石膏产品,滤液进入下一步工序;
(5)还原:向滤液中加入铁屑,并加98%的h2so4保持ph至1.0~1.5,将fe3+还原为fe2+,还原完毕后过滤;
(6)沉铬:向滤液中加入10%的caco3浆液调节ph至5.5沉淀cr3+,压滤后的滤饼为cr(oh)3;
(7)沉铁:将含fe2+的滤液返回粗制铁铬矾工序,并向其中补充铁量或者直接进一步加碱液沉淀,在空气中氧化得到fe(oh)3。
其中也提供了一种人为添加磷酸根从多金属危险废物中分离精制铁、铬的方法,具体为:
一种从多金属危险废物中分离精制铁、铬的方法包括以下步骤:
(1)酸浸:将含有金属元素的综合污泥进行配料,向污泥中加入水制浆,边搅拌边缓慢加入98%的h2so4,调节ph稳定在0.5时,停止加酸,继续溶解,使污泥中的各金属元素进入到溶液中;
(2)压滤:将酸浸后溶液进行压滤,压滤滤渣进行洗涤,洗涤水返回作调浆水用,洗涤后的渣进行纯化处理,压滤滤液进入下一道工序继续处理;
(3)粗制铁铬矾:将收集的滤液放入容器中搅拌,于常压下缓慢加入caco3浆液调节ph至4.0,继续反应,缓慢加入h2o2,同时用caco3浆液控制ph至3.8~4.1,直到h2o2将fe2+完全氧化为fe3+,然后压滤,得到的滤饼为粗制铁铬矾,滤液进入铜、锌、镍、钴、锰分离工序;
(4)溶解粗铁铬矾:将粗制铁铬矾滤饼与水制浆,向其中加入98%的h2so4调节ph至0.5使铁、铬进入到溶液中,然后压滤,滤饼为粗制石膏,经纯化洗涤得到石膏产品,滤液进入下一步工序;
(5)添加磷酸根制取磷酸铁:向滤液中加入85%的磷酸,使滤液中fe3+的浓度比磷酸根的浓度高2~3g/l,在室温及300r/min搅拌下,向滤液中缓慢加入10%氢氧化钠溶液调节ph值至1.5,开始有浅黄色fepo4沉淀生成,ph值达到2.0稳定后继续搅拌1h,得到浅黄色fepo4沉淀,压滤洗涤,滤饼为成品磷酸铁,滤液进入下一步工序;
(6)还原:向滤液中加入铁屑,并加98%的h2so4保持ph至1.0~1.5,将fe3+还原为fe2+,还原完毕后过滤;
(7)沉铬:向滤液中加入10%的caco3浆液调节ph至5.5沉淀cr3+,压滤后的滤饼为cr(oh)3;
(8)沉铁:将含fe2+的滤液返回粗制铁铬矾工序,并向其中补充铁量或者直接进一步加碱液沉淀,在空气中氧化得到fe(oh)3。
本发明还提供了一种从含有磷酸根的多金属危险废物中分离精制铁、铬的方法,具体为:
一种多金属危险废物中分离精制铁、铬的方法包括以下步骤:
(1)酸浸:将含有磷酸根和金属元素的综合污泥进行配料,向污泥中加入水制浆,边搅拌边缓慢加入98%的h2so4,调节ph稳定在0.5时,停止加酸,继续溶解,使污泥中的各金属元素进入到溶液中;
(2)压滤:将酸浸后溶液进行压滤,压滤滤渣进行洗涤,洗涤水返回作调浆水用,洗涤后的渣进行纯化处理,压滤滤液进入下一道工序继续处理;
(3)粗制铁铬矾:将收集的滤液放入容器中搅拌,于常压下缓慢加入caco3浆液调节ph至4.0,继续反应,缓慢加入h2o2,同时用caco3浆液控制ph至3.8~4.1,直到h2o2将fe2+完全氧化为fe3+,然后压滤,得到的滤饼为粗制铁铬矾,滤液进入铜、锌、镍、钴、锰分离工序;
(4)制取磷酸铁:将粗制铁铬矾滤饼与水制浆,向其中加入98%的h2so4调节ph至0.5使铁、铬进入到溶液中,然后压滤,向滤液中补充fe3+,使滤液中fe3+的浓度比磷酸根的浓度高2~3g/l,缓慢加入10%的氢氧化钠溶液调节ph至2.0,得到浅黄色fepo4沉淀,压滤洗涤,滤饼为成品磷酸铁,滤液进入下一步工序;
(5)还原:向滤液中加入铁屑,并加98%的h2so4保持ph至1.0~1.5,将fe3+还原为fe2+,还原完毕后过滤;
(6)沉铬:向滤液中加入10%的caco3浆液调节ph至5.5沉淀cr3+,压滤后的滤饼为cr(oh)3;
(7)沉铁:将含fe2+的滤液返回粗制铁铬矾工序,并向其中补充铁量或者直接进一步加碱液沉淀,在空气中氧化得到fe(oh)3。
进一步的,所述金属元素包括但不限于铁、铬、铜、锌、镍、钴、锰。
进一步的,步骤(1)所述综合污泥配料中,总铁与总铬的摩尔比为2.5~3.5:1;所述污泥与水以1:1~5质量比进行制浆。
进一步的,步骤(4)所述制浆是将粗制铁铬矾滤饼与水以1:1~3配制。
本发明和现有技术相比,具有以下优势:
(1)本发明全程无需加热,节省加工时间,降低加工成本;
(2)不会产生废水、废渣,对环境友好;
(3)提取的产品磷酸铁经济价值高,可用于电池材料、陶瓷等的原料,氢氧化铬可用于颜料、化工等行业原料;
(4)本发明采用针对不同情况(无磷酸根存在、有磷酸根存在、人为添加磷酸根)提供了三种方法来从多金属危险废物中分离精制铁、铬,扩大了应用范围;
(5)水溶液中cr3+完全沉淀的ph值为6.8,当有fe3+存在时,fe3+和cr3+在ph3.8~4.1条件下形成复盐沉淀铁铬矾,使得铬沉淀ph值大大降低,最终实现铬元素与铜、锌、镍、钴、锰等元素较好分离;
(6)向制铁铬矾溶液中补充过量铁元素,利用溶度积原理,控制一定ph值使有限的磷酸根只与fe3+形成沉淀而不与cr3+及其他杂质元素锌、镍、铜等形成沉淀,以达到在制取磷酸铁时利用过量的fe3+抑制磷酸根与cr3+形成沉淀而实现铁、铬的初步分离并制得纯度较高的磷酸铁产品的目的;
(7)采用金属铁还原fe3+,不引入其他杂质元素,将fe3+完全还原为fe2+后,控制适当条件,利用fe2+与cr3+沉淀ph差值,能使铬和铁得到较好分离,沉淀剂碳酸钙碱性弱,浆液ph值在5.4~6.0,不会产生溶液局部碱度过高的情况,有利于铬、铁分离;
(8)过量的碳酸钙还可以充当助滤剂改善过滤性能,其最终以硫酸钙副产物形式回收。
显然,根据本发明的上述内容,按照本领域的普通技术知识和手段,在不脱离本发明上述基本技术思想前提下,还可以做出其他多种形式的修改、替换或变更。
附图说明
图1为实施例3的工艺流程图。
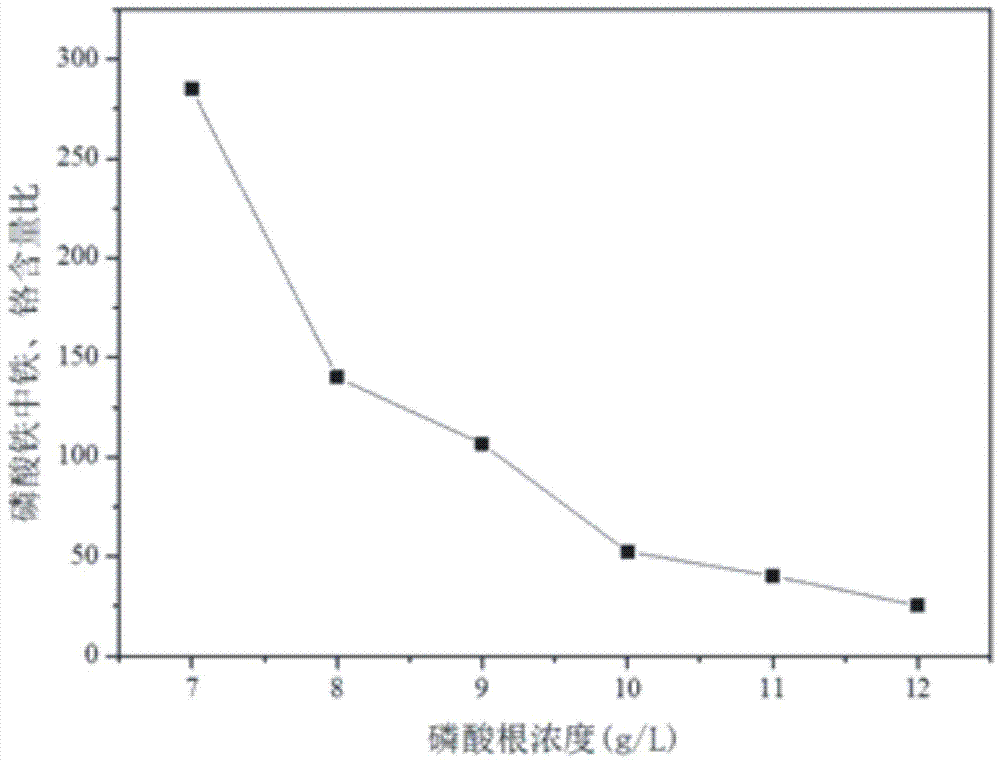
图2为实施例2中铁、铬含量比例与磷酸根量的关系。
图3为实施例2铁、铬沉淀率与ph值的关系。
具体实施方式
下面我们将结合具体实施方式对本发明作进一步的阐述。
实施例1
一种从多金属危险废物中分离精制铁、铬的方法(不含磷酸根的污泥)
(1)原料分析
取不含磷酸根的综合污泥,向污泥中补充fe盐混匀,使fe:cr=2.5~3.5:1,用火焰原子吸收分光光度计分析其金属含量,结果见表1。
表1综合污泥金属成分含量表
(2)酸浸实验
取上述混匀的综合污泥500g于2000ml烧杯中,加入1200ml水,将机械搅拌放入烧杯,调节转速300r/min使污泥浆化,然后向浆液中缓慢加入98%硫酸,过程中污泥逐渐溶解,加入硫酸至污泥不再反应,继续搅拌30min,且使ph值稳定在0.5左右以使污泥中金属完全浸出。浸出反应合格后过滤,得到滤液1360ml,用火焰原子吸收分光光度计分析金属浓度,结果见表2。
表2酸浸滤液中金属元素浓度表
过程中共计消耗98%硫酸116.45g,酸耗为23.29%。
(3)粗制铁铬矾
酸浸后的滤液用10%碳酸钙浆液调节ph值4.0,缓慢加入30%过氧化氢同时用碳酸钙浆液控制ph值3.8~4.1,直到过氧化氢将亚铁离子完全氧化为三价铁离子,然后压滤并洗涤滤饼至中性,得到的滤饼为粗铁铬矾,共计401.02g。
(4)粗铁铬矾溶解
将制得的粗铁铬矾置于2000ml烧杯中,加入600ml水,将机械搅拌放入烧杯,调节转速300r/min使污泥浆化,然后向浆液中缓慢加入98%硫酸至铁铬矾完全溶解,继续搅拌30min,且使ph值稳定在0.5左右以使铁和铬完全浸出。过滤,得滤液823ml,用火焰原子吸收分光光度计测滤液中金属的浓度,结果见表3。
表3含铁、铬滤液成分表
(5)还原-沉铬
向上述滤液中加入铁屑,并加98%硫酸保持ph值1.0~1.5,将三价铁离子还原为二价铁离子,还原完毕后过滤。用原子吸收测得滤液中铁和铬的浓度分别为16.87g/l和4.49g/l,向滤液中加入10%碳酸钙浆液调节ph值5.5,稳定后继续搅拌30min。过滤得滤液825ml,滤液中剩余铁、铬的浓度分别为15.94g/l和0.03g/l;得滤饼51.53g,将滤饼在105℃下烘至恒重即得铬产品,测得铬产品中铬、铁的质量百分率分别为12.74%、2.85%。
(6)沉铁
向上工序滤液中加入10%碳酸钠溶液调ph10.0,稳定30min后过滤,滤饼在105℃下烘至恒重即得铁产品,测得铁产品中铁、铬质量百分率分别为29.85%、0.05%。
实施例2
一种从多金属危险废物中分离精制铁、铬的方法(向不含磷酸根的污泥中添加磷酸根分离铁铬)
(1)含铁、铬滤液的制备
取实施例1中配好料的污泥500g,加入1000ml水浆化,按实施例1中的方法进行酸浸、粗制铁铬矾、粗铁铬矾溶解操作,最终得滤液816ml,用火焰原子吸收分光光度计测滤液中金属的浓度,结果见表4。
表4含铁、铬滤液成分表
(2)添加磷酸根制取磷酸铁
取5份150ml上述含铁、铬滤液(fe3+:11.05g/l,cr3+:4.48g/l,铁和铬浓度比为2.47),分别置于500ml烧杯中,向其中分别加入85%磷酸1.24、1.41、1.59、1.76、1.94、2.12g,使溶液中磷酸的浓度分别为7.00、8.00、9.00、10.00、11.00、12.00g/l。在室温及300r/min搅拌下,向滤液中缓慢加入10%氢氧化钠溶液调节ph值,ph值1.5左右开始有浅黄色磷酸铁沉淀生成,ph值达到2.0稳定后继续搅拌1h,分别压滤洗涤滤饼至中性。将制得的磷酸铁于60℃下烘至恒重,用火焰原子吸收分光光度计测其中金属成分,产品中铁、铬含量比例与磷酸根量的关系见图2。由图2可知,当溶液中磷酸根的浓度小于9g/l时,制得磷酸铁产品中铁、铬含量比均在100以上,铁、铬比扩大50倍以上,此时溶液中剩余三价铁的浓度在2g/l以上;当溶液中磷酸根的浓度逐渐增加时,制得磷酸铁产品中铁、铬含量比逐渐降低,即磷酸铁中铬含量逐渐升高。在实际工艺实施中,综合考虑磷酸铁产品质量和工艺效率,三价铁的浓度比磷酸根的浓度高2~3g/l为宜。
(3)还原-沉铬
上一步实验滤液合并共800ml,测得其中铁和铬的浓度分别为1.05g/l和3.98g/l,向滤液中加入铁屑,并加98%硫酸保持ph值1.0~1.5,将三价铁离子还原为二价铁离子,还原完毕后过滤。用原子吸收测得滤液中铁和铬的浓度分别为1.58g/l和3.98g/l,将滤液分成5份,每份150ml,向滤液中加入10%碳酸钙浆液分别调节ph值为3.5、4.0、4.5、5.0、5.5、6.0、6.5,稳定后继续搅拌30min,然后过滤,测滤液中剩余铬、铁的浓度。不同ph值条件下铬和铁的沉淀率见图3。由图3可知,在ph值5.5~6.0,可以实现铬基本完全沉淀,此时铁的沉淀率在10%以下,因此选择ph值5.5~6.0分离铬和铁。由于亚铁离子容易被吸附且容易被氧化,因此铁的沉淀率偏高。
实施例3
一种从多金属危险废物中分离精制铁、铬的方法(含磷酸根的污泥工艺流程见图1)
(1)原料分析
取含磷酸根的综合污泥,向污泥中补充fe3+盐混匀,使fe:cr-=2.5~3.5:1,用火焰原子吸收分光光度计分析其金属含量,用可见分光光度计分析磷酸根含量,结果见表5。
表5含磷酸根综合污泥金属成分表
(2)实验
取上述混匀的综合污泥500g于2000ml烧杯中,加入1000ml水,按实施例1中的方法进行酸浸、粗制铁铬矾、粗铁铬矾溶解步骤。最终得到主要含铁、铬、磷酸根的滤液1045ml,其浓度分别为:12.23g/l、4.59g/l、12.78g/l。
向上述滤液中补充三价铁溶液,使溶液中三价铁的浓度比磷酸根的浓度多2.5g/l,然后向溶液中加入10%氢氧化钠溶液调ph2.0,在该条件下铁和磷酸根以磷酸铁形式沉淀,且体系中三价铁的浓度大于磷酸根,可有效防止铬被磷酸根夹带沉淀下来。ph值稳定1h后,过滤,滤液进入下一工序;滤饼为磷酸铁产品,在60℃下烘至恒重,其成分分析见表6。
表6磷酸铁成分分析表
向上工序滤液中加入铁屑,并加98%硫酸保持ph值1.0~1.5,将三价铁离子完全还原为二价铁离子,过滤,测得滤液中铁、铬浓度分别为3.087g\l和5.850g\l(铬铁比为1.90)。向滤液中加入10%碳酸钙浆液调节ph值为5.5,稳定后继续搅拌30min,过滤洗涤滤饼至中性,该滤饼为一次提纯得到的氢氧化铬产品,测得滤饼中铬铁比为33.05。
继续将滤饼用硫酸溶解,加铁屑还原后重新沉淀,进行二次提纯,二次提纯得到的氢氧化铬产品在105℃下烘至恒重,测得铬的品位为25.67%,铁0.165%,铬铁比为155.30。
- 还没有人留言评论。精彩留言会获得点赞!