用天冬酰胺内肽酶(AEP)抑制剂以及相关组合物对神经退行性疾病的治疗的制作方法
本发明是在由美国国立卫生研究院(National Institutes of Health)资助的授权号RO1NS060680下由政府支持进行的。政府在本发明中具有一定权利。
相关申请的交叉引用
本申请要求于2014年4月11日提交的美国临时申请号61/978,362的优先权,将其通过引用以其全文特此结合。
背景
天冬酰胺内肽酶(AEP),又名豆荚蛋白,是切割天冬酰胺残基C-末端的肽键的溶酶体半胱氨酸蛋白酶。AEP涉及到各种细胞事件中,包括抗原加工、其他溶酶体酶类的切割、破骨细胞形成、以及适当的肾功能。在哺乳动物中,AEP在肾脏中高度表达;缺乏AEP的小鼠在其肾脏的近端小管细胞的内体和溶酶体中积累各种蛋白,这导致了由增生、纤维化和肾小球囊肿组成的病理学。AEP无效的小鼠展现出与噬血细胞性淋巴组织细胞增生症的症状相似的症状,表明该酶涉及此疾病的病理生理学。在生化上,该酶通过其对天冬酰胺残基和pH的特异性被高度调节。AEP用于识别其底物的具体基序尚未完全了解。失调的AEP活性已经牵涉多种疾病,包括癌症和神经变性。参见巴索托-伊斯拉斯(Basurto-Islas)等人,在阿尔茨海默病中天冬酰胺酰内肽酶的激活导致τ蛋白过度磷酸化(Activation of asparaginyl endopeptidase leads to tau hyperphosphorylation in Alzheimer disease),生物化学杂志(J Biol Chem)288,2013,17495-17507。陈(Chan)等人,缺乏天冬酰胺酰内肽酶的小鼠发展类似噬血细胞综合征的障碍(Mice lacking asparaginyl endopeptidase develop disorders resembling hemophagocytic syndrome),美国国家科学院院刊(Proc Natl Acad Sci U S A),2009,106,468-473。希思科维茨(Herskowitz)等人,天冬酰胺酰内肽酶切割脑中的TDP-43(Asparaginyl endopeptidase cleaves TDP-43 in brain),蛋白质组学(Proteomics),2012,12,2455-2463。
奥瓦特(Ovat)等人报道氮杂-肽基迈克尔受体以及环氧化物抑制剂作为曼氏裂体吸虫和蓖子硬蜱豆荚蛋白(天冬酰胺酰内肽酶)的抑制剂。参见药物化学杂志(J Med Chem),2009,52,7192-7210。
洛克(Loak)等人报道了天冬酰胺酰内肽酶的酰氧基甲基酮抑制剂。参见生物化学(Biol Chem),2003,384,1239-1246。
尼斯特罗伊(Niestroj)等人报道了哺乳动物豆荚蛋白被迈克尔受体和氮杂Asn-卤代甲基酮的抑制。参见生物化学(Biol Chem)(2002)383,1205-1214。
项(Xiang)等人报道了DNA疫苗靶向肿瘤血管系统和微环境并且抑制肿瘤生长和转移。参见免疫学综述(Immunol Rev),2008,222,117-128。
在此引用的参考文献并非对现有技术的承认。
概述
本披露涉及天冬酰胺内肽酶抑制剂及其相关的组合物和用途。在某些实施例中,这些天冬酰胺内肽酶抑制剂对于治疗或预防神经退行性疾病和认知障碍例如阿尔茨海默病是有用的。在某些实施例中,本披露涉及包括天冬酰胺内肽酶抑制剂和药学上可接受的赋形剂的药用组合物。在某些实施例中,本披露涉及治疗或预防神经退行性疾病的方法,这些方法包括将有效量的药用组合物给予至对其有需要的受试者,该药用组合物包括在此披露的天冬酰胺内肽酶抑制剂。
附图简述
图1展示了高通量筛选方案。用老鼠肾细胞裂解物筛选了Asinex库的54,384种化合物,然后用AEP敲除的细胞裂解物进行反向筛选,得到736个IC50值小于或等于40μM的命中化合物。将命中化合物用纯化的人类AEP进行进一步验证,并且将有前景的化合物归类为8个组。对来自每组的化合物进行测试,并且测定细胞毒性和特异性。
图2示出IC50值的测定数据。将纯化的重组酶与不同浓度的抑制剂在存在递增浓度的抑制剂的适当测定缓冲液中孵育。以一式两份的反应监测荧光产物的形成,并且将数据拟合为适当的方程以计算IC50值。
图3A-H示出在完整的Pala细胞中的IC50值的测定数据。将细胞与抑制剂孵育2小时,然后将细胞进行进行洗涤、收获并且裂解,并且测定残余的酶活性。将裂解产物通过布拉德福测定(Bradford assay)标准化,并且将实验一式三份地进行,并且对平均值结果和SEM进行绘图。
图4A-D示出化合物的细胞毒性和基因毒性的数据。A.MTT测定,其中将50μM的每种化合物与HepG2细胞孵育24小时。将含有化合物的培养基去除,并且将细胞与MTT溶液孵育3小时。随后,将MTT溶液用DMSO替代,并且观察OD570。B.LDH测定,其中将50μM的每种化合物与原代神经元培养物孵育48小时。然后将培养基收集,并且与LDH测定底物在室温下在黑暗中孵育30分钟。在反应淬灭后,观察OD490。C.COMET测定结果;将50μM的化合物与HepG2细胞孵育24小时。然后将细胞添加至低熔点琼脂糖并且涂布在显微镜载玻片上。将细胞裂解,并且使DNA变性并进行电泳。最后,将DNA用SYBE Green染色,并且在每个实验中,对于每个样品,100个细胞核被计数;一式三份地进行实验。D.微核测定结果;将50μM的化合物与HepG2细胞孵育24小时。将细胞固定并且将细胞核用DAPI染色,并且每个样品中1000个细胞被计数;进行三次独立的实验。
图5示出了指示DTT可逆性的数据。AEP和指定的抑制剂反应,15分钟后将10mM的DTT或L-半胱氨酸添加到反应中,并且读取荧光信号持续另外的15分钟。在孵化的第二个15分钟结束时,测定与DMSO对照反应相比在每种化合物存在时形成的产物的百分比。
图6A-H示出AEP的竞争性的、缓慢结合型的抑制剂的数据。通过在固定浓度的A.化合物11,B.化合物BB1下,改变底物Z-AAN-AMC,从拟合为竞争型抑制方程的米氏曲线测定稳态动力学参数。将每种抑制剂的KI值通过整体拟合到竞争型抑制方程中测定。C.使用时程失活测定产生进展曲线,该进展曲线描绘了以时间为函数的产物形成。准一级速率常数在化合物11的每个浓度下获得。D.准一级速率常数的再次描绘,kobs相对化合物11的浓度。E.使用时程失活测定产生进展曲线,该进展曲线描绘了以时间为函数的产物形成。准一级速率常数在化合物BB1的每个浓度下获得。F.准一级速率常数的再次描绘,kobs相对化合物BB1的浓度。
图7A-E示出在OGD处理的神经元中,AEP的抑制数据。A.用5μM Cbz-Ala-Ala-Asn-AMC在原代神经元培养物中测量的AEP活性(x轴代表用0.1μM或1.0μM的特定化合物处理的神经元)。B.用5μM Ac-Asp-Glu-Val-Asp-AMC在原代神经元培养物中测量的半胱天冬酶活性。C.用5μM D-Val-Leu-Lys-AMC在原代神经元培养物中测量的组织蛋白酶活性。D.APP切割的抑制。将与化合物预孵育30分钟、经历OGD处理4小时的原代皮质神经元的裂解物再灌注18小时(常氧神经元保持在常氧状态下)。E.APP能够以剂量依赖性形式被切割。将与化合物预孵育30分钟、经历OGD处理4小时的原代皮质神经元的裂解物再灌注18小时(常氧神经元保持在常氧状态下)。
图8A-B示出指示化合物11在脑中抑制AEP活性以及AEP介导的APP切割的数据。A.AEP活性测定。将5XFAD小鼠用10mg/kg的化合物11或运载体处理3个月。化合物11显著降低了脑中的AEP活性。*P<0.01。B.APP通过AEP和BACE1的处理。化合物11减少AEP产生的APP片段和BACE1产生的APP片段(C99),但是没有改变全长APP和BACE1的水平。
图9A-G示出指示化合物11在5XFAD小鼠中缓解Aβ沉积和认知损害的数据。A.在5XFAD小鼠的脑切片的海马体(HP)、运动皮质(MC)、和额皮质(FC)中的淀粉样蛋白斑的硫黄素-S染色。比例尺,50μm。B.淀粉样蛋白斑的定量分析。在5XFAD小鼠脑中斑块的密度被化合物11降低。*P<0.05,**P<0.01。C-D.在用化合物11或运载体处理的5XFAD小鼠中的Aβ1-40和Aβ1-42的ELISA。*P<0.05,**P<0.01,相对运载体处理的小鼠。E.莫里斯(Morris)水迷宫分析为用化合物11或运载体处理的小鼠的移动距离(mm)以及积分距离(AUC)。*P<0.05。F.在探索实验中在目标象限中所花费时间的百分比。用化合物11处理的小鼠比用运载体处理的小鼠在目标象限中花费更多的时间。**P<0.05。G.通过用化合物11处理,5XFAD小鼠的游泳速度没有改变。
图10A-F示出指示化合物11在5XFAD小鼠中改善突触损失并恢复突触功能障碍的数据。A.突触结构的代表性电子显微镜。箭头指示突触。B.在用运载体和化合物11处理的5XFAD小鼠中的突触密度的定量分析。数据用平均值±SEM示出(n=3只小鼠/组)。*p<0.01。C.高尔基体染色揭示了来自CA1区域的顶树突层的树突棘。比例尺,5μm。D.树突棘密度的定量分析。在5XFAD小鼠中,降低的树突棘密度被化合物11逆转。*P<0.01,**P<0.05。E.fEPSP的长时程增强(LTP)被3xTBS诱导(100Hz的4次脉冲,以200-ms为间隔重复3次)。所示的迹线是代表性fEPSP,是在时间点1和2(运载体处理的)和时间点3和4(化合物11处理的小鼠)记录。在5XFAD小鼠中,LTP的大小通过用化合物11处理而增强。数据用平均值±SEM来表示。*P<0.05,相对运载体处理的小鼠。F.通过在刺激强度和fEPSP斜率之间的输入/输出(I/O)关系评价的突触传递。I/O曲线在海马体切片中获得,海马体切片从运载体或化合物11处理的5XFAD小鼠中准备。
详细讨论
在更详细地描述本披露之前,应理解的是本披露不限于所描述的具体实施例,因此这些当然可以改变。还应当理解,在此使用的术语仅是为了描述特定实施例的目的,而并不意图是限制性的,因为本披露的范围将仅由所附权利要求限定。
除非另外定义,在此所用的全部技术术语和科学术语具有与本披露所属领域的普通技术人员通常所理解的相同意义。虽然与在此所述的那些方法和材料相似或等效的任何方法和材料也可以用于实施或测试本披露中,但现在描述优选的方法和材料。
在本说明书中引用的所有公开物和专利通过引用结合于此,就好像每个单独的公开物或专利被确切地并单独地指示为通过引用结合,并且通过引用结合于此从而结合引用的公开物披露和描述这些方法和/或材料。任何公开物的引用内容是针对在提交日之前的披露,并且不能理解为承认因为先前披露而本披露不能获得比这些公开物更早的申请日。此外,所提供的公开日期可能与实际的公开日期不同,实际的公开日期可能需要单独地确认。
如将对于本领域技术人员清楚的是,在阅读本披露时,在此描述和展示的单独实施例中的每一个具有离散的组成部分和特征,这些组成部分和特征可以在不偏离本披露的范围或精神的情况下易于与任何其他一些实施例的特征分离或组合。可以按照所叙述的事件的顺序或按照逻辑上可行的任何其他顺序来进行任何叙述的方法。
术语
除非另外说明,本披露的实施例将采用医学、有机化学、生物化学、分子生物学、药理学等的技术,这些技术是在本领域的技术之内。此类技术在文献中得到充分解释。
必须指出,如在说明书和所附权利要求书中所使用,单数形式“一个/一种(a/an)”和“该(the)”包括复数指示物,除非上下文另外清楚地规定。
如在此所用,当用于描述与一种另外的治疗一起给予时,术语“与...组合”意指该药剂可以在该另外的治疗之前、与其一起、或之后、或其组合被给予。
如本文所用的术语“衍生物”是指保留所鉴别类似物的足够功能特征的结构上类似的化合物。该衍生物可能是结构上类似的,因为缺乏一个或多个原子、被取代、呈盐形式、呈不同的水合/氧化状态,或因为分子内的一个或多个原子被转换,如(但不限于)氧原子被硫原子置换或氨基被羟基置换。所考虑的衍生物包括用杂环替换碳环、芳香环、或苯环,或用碳环、芳香环、或苯环替换杂环,通常情况下,环大小相同。衍生物可通过在合成或有机化学教科书中所呈现的任何种类的合成方法或适当改动来制备,诸如马奇的高等有机化学:反应、机理以及结构(March's Advanced Organic Chemistry:Reactions,Mechanisms,and Structure),威利出版社(Wiley),第6版(2007);迈克尔(Michael B.)史密斯(Smith)或有机合成中的多米诺反应(Domino Reactions in Organic Synthesis),威利出版社(Wiley)(2006)卢茨F.蒂策(Lutz F.Tietze)中所提供的那些,将所有这些化学教科书通过引用特此结合。
术语“被取代”是指其中至少一个氢原子被取代基置换的一个分子。当被取代时,一个或多个基团是“取代基”。该分子可被多重取代。在氧代取代基(“=O”)的情况下,两个氢原子被置换。在此背景内的实例取代基可以包括卤素、羟基、烷基、烷氧基、硝基、氰基、氧代、碳环基、碳环烷基、杂碳环基、杂碳环烷基、芳基、芳基烷基、杂芳基、杂芳基烷基、-NRaRb、-NRaC(=O)Rb、-NRaC(=O)NRaNRb、-NRaC(=O)ORb、-NRaSO2Rb、-C(=O)Ra、-C(=O)ORa、-C(=O)NRaRb、-OC(=O)NRaRb、-ORa、-SRa、-SORa、-S(=O)2Ra、-OS(=O)2Ra以及-S(=O)2ORa。这种情形中的Ra和Rb可以相同或不同并且独立地为氢、卤素、羟基、烷基、烷氧基、烷基、氨基、烷氨基、二烷氨基、碳环基、碳环烷基、杂碳环基、杂碳环烷基、芳基、芳基烷基、杂芳基以及杂芳基烷基。
如本文所用的术语“烷基”意味着一种非周期支链或者支链的、不饱和或者饱和烃,例如那些包含1至10个碳原子的烃。代表性饱和直链烷基包括甲基、乙基、正丙基、正丁基、正戊基、正己基、正庚基、正辛基、正壬基等;然而饱和支链烷基包括异丙基、仲丁基、异丁基、叔丁基、异戊基等。不饱和烷基类包含在相邻碳原子之间的至少一个双键或者三键(分别是指如“烯基”或者“炔基”)。代表性直链和支链烯基包括乙烯基、丙烯基、1-丁烯基、2-丁烯基、异丁烯基、1-戊烯基、2-戊烯基、3-甲基-1-丁烯基、2-甲基-2-丁烯基、2,3-二甲基-2-丁烯基等。而代表性直链和支链炔基包括乙炔基、丙炔基、1-丁炔基、2-丁炔基、1-戊炔基、2-戊炔基、3-甲基-1-丁炔基等。
非芳香族单环或多环烷基在此被称为“碳环”或“碳环基”基团。代表性的饱和碳环包括环丙基、环丁基、环戊基、环己基等;而不饱和碳环化合物包括环戊烯基和环己烯基等。
“杂碳环”或“杂碳环基”基团是可能饱和或不饱和(但不为芳香族)、单环或多环的包含从1个到4个独立地选自氮、氧和硫的杂原子的碳环,并且其中这些氮和硫杂原子可任选地被氧化,并且该氮杂原子可任选地被季铵化。杂碳环包括吗啉基、吡咯烷酮基、吡咯烷基、哌啶基、乙内酰脲基、戊内酰胺基、环氧乙烷基、氧杂环丁烷基、四氢呋喃基、四氢吡喃基、四氢吡啶基、四氢嘧啶基、四氢苯硫基、四氢硫代吡喃基、四氢嘧啶基、四氢苯硫基、四氢硫代吡喃基等。
“芳基”意指芳香族碳环单环或者多环环,诸如苯基或萘基。多环环系统可以(但不是必需)包含一个或多个非芳香族环,只要一个环是芳香族即可。
如本文所用的“杂芳基”或“杂芳香族”是指具有1到4个选自氮、氧以及硫的杂原子并且包含至少1个碳原子的一个芳香族杂碳环,包括单环与多环环系统。多环环系统可以(但不是必需)包含一个或多个非芳香族环,只要一个环是芳香族即可。代表性的杂芳基是呋喃基、苯并呋喃基、苯硫基、苯并苯硫基、吡咯基、吲哚基、异吲哚基、氮杂吲哚基、吡啶基、喹啉基、异喹啉基、噁唑基、异噁唑基、苯并噁唑基、吡唑基、咪唑基、苯并咪唑基、噻唑基、苯并噻唑基、异噻唑基、哒嗪基、嘧啶基、吡嗪基、三嗪基、噌啉基、酞嗪基、以及喹唑啉基。所考虑的是,术语“杂芳基”的使用包括N-烷基化衍生物,诸如1-甲基咪唑-5-基取代基。
如在此所用,“杂环”或“杂环基”是指具有1至4个选自氮、氧以及硫的杂原子并且包含至少1个碳原子的单环和多环环系统。这些单环和多环环系统可以是芳香族、非芳香族或芳香族与非芳香族环的混合物。杂环包括杂碳环、杂芳基等。
“烷硫基”是指通过一个硫基桥连接的如上文所定义的一个烷基基团。烷硫基的一个实例是甲硫基(即-S-CH3)。
“烷氧基”是指通过一个氧基桥连接的如上文所定义的一个烷基基团。烷氧基的实例包括,但并不限于,甲氧基、乙氧基、正丙氧基、异丙氧基、正丁氧基、仲丁氧基、叔丁氧基、正戊氧基以及仲戊氧基。优选的烷氧基是甲氧基、乙氧基、正丙氧基、异丙氧基、正丁氧基、仲丁氧基以及叔丁氧基。
“烷氨基”是指通过一个氨基桥附接的如上所定义的一个烷基基团。烷氨基的一个实例是甲氨基(即-NH-CH3)。
“链烷酰基”是指通过羰基桥附接的如上所定义的烷基(即-(C=O)烷基)。
“烷基磺酰基”是指通过磺酰基桥附接的如上所定义的烷基(即-S(=O)2烷基),诸如甲磺酰基等,并且“芳基磺酰基”是指通过磺酰基桥附接的芳基(即-S(=O)2芳基)。
“烷基氨磺酰基”是指通过氨磺酰基桥附接的如上文所定义的烷基(即-S(=O)2NH烷基),并且“芳基氨磺酰基”是指通过氨磺酰基桥附接的芳基(即-S(=O)2NH芳基)。
“烷基亚磺酰基”是指通过亚磺酰基桥连接的具有指定数目的碳原子的如上文所定义的烷基(即-S(=O)烷基)。
术语“卤素”和“卤”是指氟、氯、溴以及碘。
术语“芳酰基”是指连接到羰基基团的芳基基团(芳基基团可以如上所述的任选地被取代)(例如-C(O)-芳基)。
术语“氨磺酰基”是指磺酸的酰胺(即-S(=O)2NRR')
未指定的“R”基团可以是可以任选地被一个或多个相同或不同的取代基取代的氢、低级烷基、芳基、或杂芳基。
贯穿整个说明书中,基团和其取代基可以被选择为提供稳定的部分和化合物。
天冬酰胺内肽酶的抑制是神经保护的并且在阿尔茨海默病的小鼠模型中改善认知记忆
老化是阿尔茨海默病(AD)的最大的风险因素。在老化的过程中,脑中的pH逐渐降低。AEP在小鼠脑中被逐步上调,并且在年老的小鼠中被激活。此外,相比于正常对照,AEP在人类AD脑中也升高和激活。活性AEP切割在AD中两个主要的病原性参与者APP(淀粉样前体蛋白)以及τ蛋白两者。AEP处理APP促进了BACE1降解APP,这导致了β-淀粉样蛋白上调。从AD转基因小鼠模型中敲除AEP,逆转了在5XFAD和APP/PS1小鼠中的病理学事件,并且改善了认知损害。另一方面,活性AEP解蛋白性地降解τ蛋白,废除了它的维管装配功能,诱导了τ蛋白聚集,并且触发了神经变性。并且,AEP在τP301s转基因小鼠和人类AD脑中被激活,导致了在NFT中τ蛋白的截短。τP301S转基因小鼠中AEP的缺失实质性地降低了NFT沉积,减轻了突触损失并且挽救了损害的海马突触可塑性以及认知损害。AEP主要通过它对SET的切割负责τ蛋白的高度磷酸化,SET被切割后是PP2A的抑制剂,这将会导致负责70%τ蛋白磷酸酶活性的酶即蛋白磷酸酶-2A(PP2A)的抑制。参见巴索托-伊斯拉斯(Basurto-Islas)等人。AEP在AD的发作和发展中起到介导者的作用。AEP的抑制对于治疗神经退行性疾病(包括AD)可以是治疗上有用的。
AEP在年老的正常脑和人类阿尔茨海默病(AD)脑中被上调和激活,在介导AD的病理生理学中发挥关键作用。在此披露的是脑可渗透的并且口服有生物活性的AEP抑制剂,该抑制剂降低了在AD小鼠模型中的老年斑的形成并且缓解了认知损害。进行高通量的筛选。化合物的几种骨架家族被发现具有强有力的抑制活性。经鉴别的无毒的且特异性的AEP抑制剂选择性的阻滞AEP而不是其他的半胱氨酸相关的蛋白酶。5XFAD小鼠用口服给予抑制剂的慢性治疗改善了突触损失并且提高了长时程增强(LTP),导致在AD中的记忆丧失的保护。因此,这些发现指示这些AEP抑制剂可以是有效的临床治疗剂。
卒中、癫痫以及头部创伤都是脑组织缺血的原因,脑组织缺血上调脑组织中细胞凋亡和坏死的过程,暗示卒中、癫痫以及头部创伤是人类中神经变性的主要原因。剥夺脑的血液供应诱导兴奋性毒性效应,该效应通过非完全了解的机制引起神经元死亡。兴奋性毒性的主要特征是酸中毒,是在缓冲的脑间质中pH从7.3到6.0的转变,这是由细胞内兴奋性氨基酸谷氨酸的浓度增加导致的。响应于由兴奋性酸中毒引起的颅内pH降低,AEP被激活,并且已经示出显示对它的一个底物SET(DNAse抑制剂)的异常活性。SET是一种磷蛋白,并且主要定位于细胞核,在那里,它通过和组蛋白尾相互作用参与转录调控。在颗粒酶-A介导的细胞死亡途径中,SET还通过抑制DNA的切口形成起到细胞凋亡介导者的作用。在缺血和酸中毒诱导之后,AEP被激活,并且解蛋白地切割SET,这导致神经元细胞的死亡;然而,在AEP缺陷型小鼠中,SET保持完好,并且神经元细胞的死亡可以忽略不计。这个发现表明AEP的抑制提供了一种预防卒中、癫痫或头部创伤后的神经变性的方式。
AEP主要通过它对SET的切割负责τ蛋白的高度磷酸化,这会导致负责70%τ蛋白磷酸酶活性的酶即蛋白磷酸酶-2A(PP2A)的抑制。活性AEP以及被切割的SET的N端和C端片段的水平在AD患者的脑中升高。此外,发现酸中毒触发AEP和SET分别从溶酶体和细胞核的细胞质易位。这个发现指示AEP显现在阿尔茨海默病的发病机理中发挥一定作用。
AD是最普遍的神经退行性疾病。它表征为Aβ和不可溶性τ蛋白的沉积。我们发现在AD脑中,AEP切割APP和τ蛋白。相比于全长APP,AEP产生的APP片段是β-分泌酶的更好的底物,由此增强Aβ的产生。被AEP切割的τ蛋白将产生若干可以促进其沉积的片段。此外,被AEP进行的SET的切割促进由缺血诱导的神经元死亡,并且促进τ蛋白的磷酸化。所有的这些观察指示AEP抑制剂可以挽救在AD中的渐进式神经变性。为了检验这一假设,将5XFAD小鼠用化合物11处理3个月,并且监测该化合物对在该AD模型中的形态学的、电生理学的、生物化学的、以及行为学的改变的影响。化合物11的慢性给药推定是通过抑制由AEP对APP的切割而降低了Aβ的沉积。化合物11引起的认知功能的恢复指示AEP抑制剂在体外的的保护作用可以转变为临床益处。突触功能障碍是AD的早期的且不变的特征。在AD中,突触损失和痴呆相关联。5XFAD小鼠和非转基因小鼠相比,示出减少的突触密度以及LTP大小。如增加的突触密度和LTP大小所示,化合物11逆转了突触功能障碍,指示该化合物的“突触保护”效应。
天冬酰胺内肽酶抑制剂
本披露涉及天冬酰胺内肽酶抑制剂。在一些实施例中,天冬酰胺内肽酶抑制剂是经取代的苯并[c][1,2,5]噁二唑衍生物,例如具有以下化学式的化合物:
其前药、酯、衍生物、或盐,其中,
X是O或S;
R1选自氢、烷基、烯基、链烷酰基、卤素、硝基、氰基、羟基、氨基、巯基、甲酰基、羧基、氨甲酰基、烷氧基、烷硫基、烷氨基、二烷氨基、烷基亚磺酰基、烷基磺酰基、芳基磺酰基、碳环基、芳基、和杂环基,其中R1任选地被一个或多个相同或不同的R10取代;
R10选自烷基、烯基、链烷酰基、卤素、硝基、氰基、羟基、氨基、巯基、甲酰基、羧基、氨甲酰基、烷氧基、烷硫基、烷氨基、二烷氨基、烷基亚磺酰基、烷基磺酰基、芳基磺酰基、碳环基、芳基、和杂环基,其中R10任选地被一个或多个相同或不同的R11取代;
R11选自卤素、硝基、氰基、羟基、三氟甲氧基、三氟甲基、氨基、甲酰基、羧基、氨甲酰基、巯基、氨磺酰基、甲基、乙基、丙基、叔丁基、甲氧基、乙氧基、乙酰基、乙酰氧基、甲氨基、乙氨基、二甲氨基、二乙氨基、N-甲基-N-乙氨基、乙酰基氨基、N-甲基氨甲酰基、N-乙基氨甲酰基、N,N-二甲基氨甲酰基、N,N-二乙基氨甲酰基、N-甲基-N-乙基氨甲酰基、甲硫基、乙硫基、甲基亚磺酰基、乙基亚磺酰基、甲磺酰基、乙基磺酰基、甲氧基羰基、乙氧基羰基、N-甲基氨磺酰基、N-乙基氨磺酰基、N,N-二甲基氨磺酰基、N,N-二乙基氨磺酰基、N-甲基-N-乙基氨磺酰基、碳环基、芳基、和杂环基;
R2选自氢、烷基、烯基、链烷酰基、卤素、硝基、氰基、羟基、氨基、巯基、甲酰基、羧基、氨甲酰基、烷氧基、烷硫基、烷氨基、二烷氨基、烷基亚磺酰基、烷基磺酰基、芳基磺酰基、碳环基、芳基、和杂环基,其中R2任选地被一个或多个相同或不同的R20取代;
R20选自烷基、烯基、链烷酰基、卤素、硝基、氰基、羟基、氨基、巯基、甲酰基、羧基、氨甲酰基、烷氧基、烷硫基、烷氨基、二烷氨基、烷基亚磺酰基、烷基磺酰基、芳基磺酰基、碳环基、芳基、和杂环基,其中R20任选地被一个或多个相同或不同的R21取代;
R21选自卤素、硝基、氰基、羟基、三氟甲氧基、三氟甲基、氨基、甲酰基、羧基、氨甲酰基、巯基、氨磺酰基、甲基、乙基、丙基、叔丁基、甲氧基、乙氧基、乙酰基、乙酰氧基、甲氨基、乙氨基、二甲氨基、二乙氨基、N-甲基-N-乙氨基、乙酰基氨基、N-甲基氨甲酰基、N-乙基氨甲酰基、N,N-二甲基氨甲酰基、N,N-二乙基氨甲酰基、N-甲基-N-乙基氨甲酰基、甲硫基、乙硫基、甲基亚磺酰基、乙基亚磺酰基、甲磺酰基、乙基磺酰基、甲氧基羰基、乙氧基羰基、N-甲基氨磺酰基、N-乙基氨磺酰基、N,N-二甲基氨磺酰基、N,N-二乙基氨磺酰基、N-甲基-N-乙基氨磺酰基、碳环基、芳基、和杂环基;
R3选自氢、烷基、烯基、链烷酰基、卤素、硝基、氰基、羟基、氨基、巯基、甲酰基、羧基、氨甲酰基、烷氧基、烷硫基、烷氨基、二烷氨基、烷基亚磺酰基、烷基磺酰基、芳基磺酰基、碳环基、芳基、和杂环基,其中R3任选地被一个或多个相同或不同的R30取代;
R30选自烷基、烯基、链烷酰基、卤素、硝基、氰基、羟基、氨基、巯基、甲酰基、羧基、氨甲酰基、烷氧基、烷硫基、烷氨基、二烷氨基、烷基亚磺酰基、烷基磺酰基、芳基磺酰基、碳环基、芳基、和杂环基,其中R30任选地被一个或多个相同或不同的R31取代;
R31选自卤素、硝基、氰基、羟基、三氟甲氧基、三氟甲基、氨基、甲酰基、羧基、氨甲酰基、巯基、氨磺酰基、甲基、乙基、丙基、叔丁基、甲氧基、乙氧基、乙酰基、乙酰氧基、甲氨基、乙氨基、二甲氨基、二乙氨基、N-甲基-N-乙氨基、乙酰基氨基、N-甲基氨甲酰基、N-乙基氨甲酰基、N,N-二甲基氨甲酰基、N,N-二乙基氨甲酰基、N-甲基-N-乙基氨甲酰基、甲硫基、乙硫基、甲基亚磺酰基、乙基亚磺酰基、甲磺酰基、乙基磺酰基、甲氧基羰基、乙氧基羰基、N-甲基氨磺酰基、N-乙基氨磺酰基、N,N-二甲基氨磺酰基、N,N-二乙基氨磺酰基、N-甲基-N-乙基氨磺酰基、碳环基、芳基、和杂环基;
R4选自氢、烷基、烯基、链烷酰基、卤素、硝基、氰基、羟基、氨基、巯基、甲酰基、羧基、氨甲酰基、烷氧基、烷硫基、烷氨基、二烷氨基、烷基亚磺酰基、烷基磺酰基、芳基磺酰基、碳环基、芳基、和杂环基,其中R4任选地被一个或多个相同或不同的R40取代;
R40选自烷基、烯基、链烷酰基、卤素、硝基、氰基、羟基、氨基、巯基、甲酰基、羧基、氨甲酰基、烷氧基、烷硫基、烷氨基、二烷氨基、烷基亚磺酰基、烷基磺酰基、芳基磺酰基、碳环基、芳基、和杂环基,其中R40任选地被一个或多个相同或不同的R41取代;并且
R41选自卤素、硝基、氰基、羟基、三氟甲氧基、三氟甲基、氨基、甲酰基、羧基、氨甲酰基、巯基、氨磺酰基、甲基、乙基、丙基、叔丁基、甲氧基、乙氧基、乙酰基、乙酰氧基、甲氨基、乙氨基、二甲氨基、二乙氨基、N-甲基-N-乙氨基、乙酰基氨基、N-甲基氨甲酰基、N-乙基氨甲酰基、N,N-二甲基氨甲酰基、N,N-二乙基氨甲酰基、N-甲基-N-乙基氨甲酰基、甲硫基、乙硫基、甲基亚磺酰基、乙基亚磺酰基、甲磺酰基、乙基磺酰基、甲氧基羰基、乙氧基羰基、N-甲基氨磺酰基、N-乙基氨磺酰基、N,N-二甲基氨磺酰基、N,N-二乙基氨磺酰基、N-甲基-N-乙基氨磺酰基、碳环基、芳基、和杂环基。
在某些实施例中,R1是氨基。在某些实施例中,R2是氢。在某些实施例中,R3是氢。在某些实施例中,R4是杂环基。
在一些实施例中,天冬酰胺内肽酶抑制剂是经取代的3,7-二氢嘌呤-2,6-二酮衍生物,例如具有以下化学式的化合物:
其前药、酯、衍生物、或盐,其中,
R1选自氢、烷基、烯基、链烷酰基、卤素、硝基、氰基、羟基、氨基、巯基、甲酰基、羧基、氨甲酰基、烷氧基、烷硫基、烷氨基、二烷氨基、烷基亚磺酰基、烷基磺酰基、芳基磺酰基、碳环基、芳基、和杂环基,其中R1任选地被一个或多个相同或不同的R10取代;
R10选自烷基、烯基、链烷酰基、卤素、硝基、氰基、羟基、氨基、巯基、甲酰基、羧基、氨甲酰基、烷氧基、烷硫基、烷氨基、二烷氨基、烷基亚磺酰基、烷基磺酰基、芳基磺酰基、碳环基、芳基、和杂环基,其中R10任选地被一个或多个相同或不同的R11取代;
R11选自卤素、硝基、氰基、羟基、三氟甲氧基、三氟甲基、氨基、甲酰基、羧基、氨甲酰基、巯基、氨磺酰基、甲基、乙基、丙基、叔丁基、甲氧基、乙氧基、乙酰基、乙酰氧基、甲氨基、乙氨基、二甲氨基、二乙氨基、N-甲基-N-乙氨基、乙酰基氨基、N-甲基氨甲酰基、N-乙基氨甲酰基、N,N-二甲基氨甲酰基、N,N-二乙基氨甲酰基、N-甲基-N-乙基氨甲酰基、甲硫基、乙硫基、甲基亚磺酰基、乙基亚磺酰基、甲磺酰基、乙基磺酰基、甲氧基羰基、乙氧基羰基、N-甲基氨磺酰基、N-乙基氨磺酰基、N,N-二甲基氨磺酰基、N,N-二乙基氨磺酰基、N-甲基-N-乙基氨磺酰基、碳环基、芳基、和杂环基;
R2选自氢、烷基、烯基、链烷酰基、卤素、硝基、氰基、羟基、氨基、巯基、甲酰基、羧基、氨甲酰基、烷氧基、烷硫基、烷氨基、二烷氨基、烷基亚磺酰基、烷基磺酰基、芳基磺酰基、碳环基、芳基、和杂环基,其中R2任选地被一个或多个相同或不同的R20取代;
R20选自烷基、烯基、链烷酰基、卤素、硝基、氰基、羟基、氨基、巯基、甲酰基、羧基、氨甲酰基、烷氧基、烷硫基、烷氨基、二烷氨基、烷基亚磺酰基、烷基磺酰基、芳基磺酰基、碳环基、芳基、和杂环基,其中R20任选地被一个或多个相同或不同的R21取代;
R21选自卤素、硝基、氰基、羟基、三氟甲氧基、三氟甲基、氨基、甲酰基、羧基、氨甲酰基、巯基、氨磺酰基、甲基、乙基、丙基、叔丁基、甲氧基、乙氧基、乙酰基、乙酰氧基、甲氨基、乙氨基、二甲氨基、二乙氨基、N-甲基-N-乙氨基、乙酰基氨基、N-甲基氨甲酰基、N-乙基氨甲酰基、N,N-二甲基氨甲酰基、N,N-二乙基氨甲酰基、N-甲基-N-乙基氨甲酰基、甲硫基、乙硫基、甲基亚磺酰基、乙基亚磺酰基、甲磺酰基、乙基磺酰基、甲氧基羰基、乙氧基羰基、N-甲基氨磺酰基、N-乙基氨磺酰基、N,N-二甲基氨磺酰基、N,N-二乙基氨磺酰基、N-甲基-N-乙基氨磺酰基、碳环基、芳基、和杂环基;
R6选自氢、烷基、烯基、链烷酰基、卤素、硝基、氰基、羟基、氨基、巯基、甲酰基、羧基、氨甲酰基、烷氧基、烷硫基、烷氨基、二烷氨基、烷基亚磺酰基、烷基磺酰基、芳基磺酰基、碳环基、芳基、和杂环基,其中R6任选地被一个或多个相同或不同的R60取代;
R60选自烷基、烯基、链烷酰基、卤素、硝基、氰基、羟基、氨基、巯基、甲酰基、羧基、氨甲酰基、烷氧基、烷硫基、烷氨基、二烷氨基、烷基亚磺酰基、烷基磺酰基、芳基磺酰基、碳环基、芳基、和杂环基,其中R60任选地被一个或多个相同或不同的R61取代;
R61选自卤素、硝基、氰基、羟基、三氟甲氧基、三氟甲基、氨基、甲酰基、羧基、氨甲酰基、巯基、氨磺酰基、甲基、乙基、丙基、叔丁基、甲氧基、乙氧基、乙酰基、乙酰氧基、甲氨基、乙氨基、二甲氨基、二乙氨基、N-甲基-N-乙氨基、乙酰基氨基、N-甲基氨甲酰基、N-乙基氨甲酰基、N,N-二甲基氨甲酰基、N,N-二乙基氨甲酰基、N-甲基-N-乙基氨甲酰基、甲硫基、乙硫基、甲基亚磺酰基、乙基亚磺酰基、甲磺酰基、乙基磺酰基、甲氧基羰基、乙氧基羰基、N-甲基氨磺酰基、N-乙基氨磺酰基、N,N-二甲基氨磺酰基、N,N-二乙基氨磺酰基、N-甲基-N-乙基氨磺酰基、碳环基、芳基、和杂环基;
R7选自氢、烷基、烯基、链烷酰基、卤素、硝基、氰基、羟基、氨基、巯基、甲酰基、羧基、氨甲酰基、烷氧基、烷硫基、烷氨基、二烷氨基、烷基亚磺酰基、烷基磺酰基、芳基磺酰基、碳环基、芳基、和杂环基,其中R7任选地被一个或多个相同或不同的R70取代;
R70选自烷基、烯基、链烷酰基、卤素、硝基、氰基、羟基、氨基、巯基、甲酰基、羧基、氨甲酰基、烷氧基、烷硫基、烷氨基、二烷氨基、烷基亚磺酰基、烷基磺酰基、芳基磺酰基、碳环基、芳基、和杂环基,其中R70任选地被一个或多个相同或不同的R71取代;并且
R71选自卤素、硝基、氰基、羟基、三氟甲氧基、三氟甲基、氨基、甲酰基、羧基、氨甲酰基、巯基、氨磺酰基、甲基、乙基、丙基、叔丁基、甲氧基、乙氧基、乙酰基、乙酰氧基、甲氨基、乙氨基、二甲氨基、二乙氨基、N-甲基-N-乙氨基、乙酰基氨基、N-甲基氨甲酰基、N-乙基氨甲酰基、N,N-二甲基氨甲酰基、N,N-二乙基氨甲酰基、N-甲基-N-乙基氨甲酰基、甲硫基、乙硫基、甲基亚磺酰基、乙基亚磺酰基、甲磺酰基、乙基磺酰基、甲氧基羰基、乙氧基羰基、N-甲基氨磺酰基、N-乙基氨磺酰基、N,N-二甲基氨磺酰基、N,N-二乙基氨磺酰基、N-甲基-N-乙基氨磺酰基、碳环基、芳基、和杂环基。
在某些实施例中,R1是烷基。
在某些实施例中,R2是烷基。
在某些实施例中,R6是巯基。
在某些实施例中,R7是烷基。
在某些实施例中,天冬酰胺内肽酶抑制剂是经取代的1,3,4-噻二唑衍生物,例如具有以下化学式的化合物:
其前药、酯、衍生物、或盐,其中,
X是O或S;
R1选自氢、烷基、烯基、链烷酰基、卤素、硝基、氰基、羟基、氨基、巯基、甲酰基、羧基、氨甲酰基、烷氧基、烷硫基、烷氨基、二烷氨基、烷基亚磺酰基、烷基磺酰基、芳基磺酰基、碳环基、芳基、和杂环基,其中R1任选地被一个或多个相同或不同的R10取代;
R10选自烷基、烯基、链烷酰基、卤素、硝基、氰基、羟基、氨基、巯基、甲酰基、羧基、氨甲酰基、烷氧基、烷硫基、烷氨基、二烷氨基、烷基亚磺酰基、烷基磺酰基、芳基磺酰基、碳环基、芳基、和杂环基,其中R10任选地被一个或多个相同或不同的R11取代;
R11选自卤素、硝基、氰基、羟基、三氟甲氧基、三氟甲基、氨基、甲酰基、羧基、氨甲酰基、巯基、氨磺酰基、甲基、乙基、丙基、叔丁基、甲氧基、乙氧基、乙酰基、乙酰氧基、甲氨基、乙氨基、二甲氨基、二乙氨基、N-甲基-N-乙氨基、乙酰基氨基、N-甲基氨甲酰基、N-乙基氨甲酰基、N,N-二甲基氨甲酰基、N,N-二乙基氨甲酰基、N-甲基-N-乙基氨甲酰基、甲硫基、乙硫基、甲基亚磺酰基、乙基亚磺酰基、甲磺酰基、乙基磺酰基、甲氧基羰基、乙氧基羰基、N-甲基氨磺酰基、N-乙基氨磺酰基、N,N-二甲基氨磺酰基、N,N-二乙基氨磺酰基、N-甲基-N-乙基氨磺酰基、碳环基、芳基、和杂环基;
R2选自氢、烷基、烯基、链烷酰基、卤素、硝基、氰基、羟基、氨基、巯基、甲酰基、羧基、氨甲酰基、烷氧基、烷硫基、烷氨基、二烷氨基、烷基亚磺酰基、烷基磺酰基、芳基磺酰基、碳环基、芳基、和杂环基,其中R2任选地被一个或多个相同或不同的R20取代;
R20选自烷基、烯基、链烷酰基、卤素、硝基、氰基、羟基、氨基、巯基、甲酰基、羧基、氨甲酰基、烷氧基、烷硫基、烷氨基、二烷氨基、烷基亚磺酰基、烷基磺酰基、芳基磺酰基、碳环基、芳基、和杂环基,其中R20任选地被一个或多个相同或不同的R21取代;并且
R21选自卤素、硝基、氰基、羟基、三氟甲氧基、三氟甲基、氨基、甲酰基、羧基、氨甲酰基、巯基、氨磺酰基、甲基、乙基、丙基、叔丁基、甲氧基、乙氧基、乙酰基、乙酰氧基、甲氨基、乙氨基、二甲氨基、二乙氨基、N-甲基-N-乙氨基、乙酰基氨基、N-甲基氨甲酰基、N-乙基氨甲酰基、N,N-二甲基氨甲酰基、N,N-二乙基氨甲酰基、N-甲基-N-乙基氨甲酰基、甲硫基、乙硫基、甲基亚磺酰基、乙基亚磺酰基、甲磺酰基、乙基磺酰基、甲氧基羰基、乙氧基羰基、N-甲基氨磺酰基、N-乙基氨磺酰基、N,N-二甲基氨磺酰基、N,N-二乙基氨磺酰基、N-甲基-N-乙基氨磺酰基、碳环基、芳基、和杂环基。
在某些实施例中,R1是巯基。在某些实施例中,R2是氨基。
在一些实施例中,天冬酰胺内肽酶抑制剂是经取代的1-苯基-1H-吡咯-2,5-二酮衍生物,例如具有以下化学式的化合物:
其前药、酯、衍生物、或盐,其中,
R1选自氢、烷基、烯基、链烷酰基、卤素、硝基、氰基、羟基、氨基、巯基、甲酰基、羧基、氨甲酰基、烷氧基、烷硫基、烷氨基、二烷氨基、烷基亚磺酰基、烷基磺酰基、芳基磺酰基、碳环基、芳基、和杂环基,其中R1任选地被一个或多个相同或不同的R10取代;
R10选自烷基、烯基、链烷酰基、卤素、硝基、氰基、羟基、氨基、巯基、甲酰基、羧基、氨甲酰基、烷氧基、烷硫基、烷氨基、二烷氨基、烷基亚磺酰基、烷基磺酰基、芳基磺酰基、碳环基、芳基、和杂环基,其中R10任选地被一个或多个相同或不同的R11取代;
R11选自卤素、硝基、氰基、羟基、三氟甲氧基、三氟甲基、氨基、甲酰基、羧基、氨甲酰基、巯基、氨磺酰基、甲基、乙基、丙基、叔丁基、甲氧基、乙氧基、乙酰基、乙酰氧基、甲氨基、乙氨基、二甲氨基、二乙氨基、N-甲基-N-乙氨基、乙酰基氨基、N-甲基氨甲酰基、N-乙基氨甲酰基、N,N-二甲基氨甲酰基、N,N-二乙基氨甲酰基、N-甲基-N-乙基氨甲酰基、甲硫基、乙硫基、甲基亚磺酰基、乙基亚磺酰基、甲磺酰基、乙基磺酰基、甲氧基羰基、乙氧基羰基、N-甲基氨磺酰基、N-乙基氨磺酰基、N,N-二甲基氨磺酰基、N,N-二乙基氨磺酰基、N-甲基-N-乙基氨磺酰基、碳环基、芳基、和杂环基;
R2选自氢、烷基、烯基、链烷酰基、卤素、硝基、氰基、羟基、氨基、巯基、甲酰基、羧基、氨甲酰基、烷氧基、烷硫基、烷氨基、二烷氨基、烷基亚磺酰基、烷基磺酰基、芳基磺酰基、碳环基、芳基、和杂环基,其中R2任选地被一个或多个相同或不同的R20取代;
R20选自烷基、烯基、链烷酰基、卤素、硝基、氰基、羟基、氨基、巯基、甲酰基、羧基、氨甲酰基、烷氧基、烷硫基、烷氨基、二烷氨基、烷基亚磺酰基、烷基磺酰基、芳基磺酰基、碳环基、芳基、和杂环基,其中R20任选地被一个或多个相同或不同的R21取代;
R21选自卤素、硝基、氰基、羟基、三氟甲氧基、三氟甲基、氨基、甲酰基、羧基、氨甲酰基、巯基、氨磺酰基、甲基、乙基、丙基、叔丁基、甲氧基、乙氧基、乙酰基、乙酰氧基、甲氨基、乙氨基、二甲氨基、二乙氨基、N-甲基-N-乙氨基、乙酰基氨基、N-甲基氨甲酰基、N-乙基氨甲酰基、N,N-二甲基氨甲酰基、N,N-二乙基氨甲酰基、N-甲基-N-乙基氨甲酰基、甲硫基、乙硫基、甲基亚磺酰基、乙基亚磺酰基、甲磺酰基、乙基磺酰基、甲氧基羰基、乙氧基羰基、N-甲基氨磺酰基、N-乙基氨磺酰基、N,N-二甲基氨磺酰基、N,N-二乙基氨磺酰基、N-甲基-N-乙基氨磺酰基、碳环基、芳基、和杂环基;
R3选自氢、烷基、烯基、链烷酰基、卤素、硝基、氰基、羟基、氨基、巯基、甲酰基、羧基、氨甲酰基、烷氧基、烷硫基、烷氨基、二烷氨基、烷基亚磺酰基、烷基磺酰基、芳基磺酰基、碳环基、芳基、和杂环基,其中R3任选地被一个或多个相同或不同的R30取代;
R30选自烷基、烯基、链烷酰基、卤素、硝基、氰基、羟基、氨基、巯基、甲酰基、羧基、氨甲酰基、烷氧基、烷硫基、烷氨基、二烷氨基、烷基亚磺酰基、烷基磺酰基、芳基磺酰基、碳环基、芳基、和杂环基,其中R30任选地被一个或多个相同或不同的R31取代;
R31选自卤素、硝基、氰基、羟基、三氟甲氧基、三氟甲基、氨基、甲酰基、羧基、氨甲酰基、巯基、氨磺酰基、甲基、乙基、丙基、叔丁基、甲氧基、乙氧基、乙酰基、乙酰氧基、甲氨基、乙氨基、二甲氨基、二乙氨基、N-甲基-N-乙氨基、乙酰基氨基、N-甲基氨甲酰基、N-乙基氨甲酰基、N,N-二甲基氨甲酰基、N,N-二乙基氨甲酰基、N-甲基-N-乙基氨甲酰基、甲硫基、乙硫基、甲基亚磺酰基、乙基亚磺酰基、甲磺酰基、乙基磺酰基、甲氧基羰基、乙氧基羰基、N-甲基氨磺酰基、N-乙基氨磺酰基、N,N-二甲基氨磺酰基、N,N-二乙基氨磺酰基、N-甲基-N-乙基氨磺酰基、碳环基、芳基、和杂环基;
R4选自氢、烷基、烯基、链烷酰基、卤素、硝基、氰基、羟基、氨基、巯基、甲酰基、羧基、氨甲酰基、烷氧基、烷硫基、烷氨基、二烷氨基、烷基亚磺酰基、烷基磺酰基、芳基磺酰基、碳环基、芳基、和杂环基,其中R4任选地被一个或多个相同或不同的R40取代;
R40选自烷基、烯基、链烷酰基、卤素、硝基、氰基、羟基、氨基、巯基、甲酰基、羧基、氨甲酰基、烷氧基、烷硫基、烷氨基、二烷氨基、烷基亚磺酰基、烷基磺酰基、芳基磺酰基、碳环基、芳基、和杂环基,其中R40任选地被一个或多个相同或不同的R41取代;
R41选自卤素、硝基、氰基、羟基、三氟甲氧基、三氟甲基、氨基、甲酰基、羧基、氨甲酰基、巯基、氨磺酰基、甲基、乙基、丙基、叔丁基、甲氧基、乙氧基、乙酰基、乙酰氧基、甲氨基、乙氨基、二甲氨基、二乙氨基、N-甲基-N-乙氨基、乙酰基氨基、N-甲基氨甲酰基、N-乙基氨甲酰基、N,N-二甲基氨甲酰基、N,N-二乙基氨甲酰基、N-甲基-N-乙基氨甲酰基、甲硫基、乙硫基、甲基亚磺酰基、乙基亚磺酰基、甲磺酰基、乙基磺酰基、甲氧基羰基、乙氧基羰基、N-甲基氨磺酰基、N-乙基氨磺酰基、N,N-二甲基氨磺酰基、N,N-二乙基氨磺酰基、N-甲基-N-乙基氨磺酰基、碳环基、芳基、和杂环基;
R5选自氢、烷基、烯基、链烷酰基、卤素、硝基、氰基、羟基、氨基、巯基、甲酰基、羧基、氨甲酰基、烷氧基、烷硫基、烷氨基、二烷氨基、烷基亚磺酰基、烷基磺酰基、芳基磺酰基、碳环基、芳基、和杂环基,其中R5任选地被一个或多个相同或不同的R50取代;
R50选自烷基、烯基、链烷酰基、卤素、硝基、氰基、羟基、氨基、巯基、甲酰基、羧基、氨甲酰基、烷氧基、烷硫基、烷氨基、二烷氨基、烷基亚磺酰基、烷基磺酰基、芳基磺酰基、碳环基、芳基、和杂环基,其中R50任选地被一个或多个相同或不同的R51取代;
R51选自卤素、硝基、氰基、羟基、三氟甲氧基、三氟甲基、氨基、甲酰基、羧基、氨甲酰基、巯基、氨磺酰基、甲基、乙基、丙基、叔丁基、甲氧基、乙氧基、乙酰基、乙酰氧基、甲氨基、乙氨基、二甲氨基、二乙氨基、N-甲基-N-乙氨基、乙酰基氨基、N-甲基氨甲酰基、N-乙基氨甲酰基、N,N-二甲基氨甲酰基、N,N-二乙基氨甲酰基、N-甲基-N-乙基氨甲酰基、甲硫基、乙硫基、甲基亚磺酰基、乙基亚磺酰基、甲磺酰基、乙基磺酰基、甲氧基羰基、乙氧基羰基、N-甲基氨磺酰基、N-乙基氨磺酰基、N,N-二甲基氨磺酰基、N,N-二乙基氨磺酰基、N-甲基-N-乙基氨磺酰基、碳环基、芳基、和杂环基;
R6选自氢、烷基、烯基、链烷酰基、卤素、硝基、氰基、羟基、氨基、巯基、甲酰基、羧基、氨甲酰基、烷氧基、烷硫基、烷氨基、二烷氨基、烷基亚磺酰基、烷基磺酰基、芳基磺酰基、碳环基、芳基、和杂环基,其中R6任选地被一个或多个相同或不同的R60取代;
R60选自烷基、烯基、链烷酰基、卤素、硝基、氰基、羟基、氨基、巯基、甲酰基、羧基、氨甲酰基、烷氧基、烷硫基、烷氨基、二烷氨基、烷基亚磺酰基、烷基磺酰基、芳基磺酰基、碳环基、芳基、和杂环基,其中R60任选地被一个或多个相同或不同的R61取代;
R61选自卤素、硝基、氰基、羟基、三氟甲氧基、三氟甲基、氨基、甲酰基、羧基、氨甲酰基、巯基、氨磺酰基、甲基、乙基、丙基、叔丁基、甲氧基、乙氧基、乙酰基、乙酰氧基、甲氨基、乙氨基、二甲氨基、二乙氨基、N-甲基-N-乙氨基、乙酰基氨基、N-甲基氨甲酰基、N-乙基氨甲酰基、N,N-二甲基氨甲酰基、N,N-二乙基氨甲酰基、N-甲基-N-乙基氨甲酰基、甲硫基、乙硫基、甲基亚磺酰基、乙基亚磺酰基、甲磺酰基、乙基磺酰基、甲氧基羰基、乙氧基羰基、N-甲基氨磺酰基、N-乙基氨磺酰基、N,N-二甲基氨磺酰基、N,N-二乙基氨磺酰基、N-甲基-N-乙基氨磺酰基、碳环基、芳基、和杂环基;
R7选自氢、烷基、烯基、链烷酰基、卤素、硝基、氰基、羟基、氨基、巯基、甲酰基、羧基、氨甲酰基、烷氧基、烷硫基、烷氨基、二烷氨基、烷基亚磺酰基、烷基磺酰基、芳基磺酰基、碳环基、芳基、和杂环基,其中R7任选地被一个或多个相同或不同的R70取代;
R70选自烷基、烯基、链烷酰基、卤素、硝基、氰基、羟基、氨基、巯基、甲酰基、羧基、氨甲酰基、烷氧基、烷硫基、烷氨基、二烷氨基、烷基亚磺酰基、烷基磺酰基、芳基磺酰基、碳环基、芳基、和杂环基,其中R70任选地被一个或多个相同或不同的R71取代;并且
R71选自卤素、硝基、氰基、羟基、三氟甲氧基、三氟甲基、氨基、甲酰基、羧基、氨甲酰基、巯基、氨磺酰基、甲基、乙基、丙基、叔丁基、甲氧基、乙氧基、乙酰基、乙酰氧基、甲氨基、乙氨基、二甲氨基、二乙氨基、N-甲基-N-乙氨基、乙酰基氨基、N-甲基氨甲酰基、N-乙基氨甲酰基、N,N-二甲基氨甲酰基、N,N-二乙基氨甲酰基、N-甲基-N-乙基氨甲酰基、甲硫基、乙硫基、甲基亚磺酰基、乙基亚磺酰基、甲磺酰基、乙基磺酰基、甲氧基羰基、乙氧基羰基、N-甲基氨磺酰基、N-乙基氨磺酰基、N,N-二甲基氨磺酰基、N,N-二乙基氨磺酰基、N-甲基-N-乙基氨磺酰基、碳环基、芳基、和杂环基;
在一些实施例中,天冬酰胺内肽酶抑制剂是经取代的1-甲基哌嗪衍生物,例如具有以下化学式的化合物:
其前药、酯、衍生物、或盐,其中,
R1选自氢、烷基、烯基、链烷酰基、卤素、硝基、氰基、羟基、氨基、巯基、甲酰基、羧基、氨甲酰基、烷氧基、烷硫基、烷氨基、二烷氨基、烷基亚磺酰基、烷基磺酰基、芳基磺酰基、碳环基、芳基、和杂环基,其中R1任选地被一个或多个相同或不同的R10取代;
R10选自烷基、烯基、链烷酰基、卤素、硝基、氰基、羟基、氨基、巯基、甲酰基、羧基、氨甲酰基、烷氧基、烷硫基、烷氨基、二烷氨基、烷基亚磺酰基、烷基磺酰基、芳基磺酰基、碳环基、芳基、和杂环基,其中R10任选地被一个或多个相同或不同的R11取代;
R11选自卤素、硝基、氰基、羟基、三氟甲氧基、三氟甲基、氨基、甲酰基、羧基、氨甲酰基、巯基、氨磺酰基、甲基、乙基、丙基、叔丁基、甲氧基、乙氧基、乙酰基、乙酰氧基、甲氨基、乙氨基、二甲氨基、二乙氨基、N-甲基-N-乙氨基、乙酰基氨基、N-甲基氨甲酰基、N-乙基氨甲酰基、N,N-二甲基氨甲酰基、N,N-二乙基氨甲酰基、N-甲基-N-乙基氨甲酰基、甲硫基、乙硫基、甲基亚磺酰基、乙基亚磺酰基、甲磺酰基、乙基磺酰基、甲氧基羰基、乙氧基羰基、N-甲基氨磺酰基、N-乙基氨磺酰基、N,N-二甲基氨磺酰基、N,N-二乙基氨磺酰基、N-甲基-N-乙基氨磺酰基、碳环基、芳基、和杂环基;
R2选自氢、烷基、烯基、链烷酰基、卤素、硝基、氰基、羟基、氨基、巯基、甲酰基、羧基、氨甲酰基、烷氧基、烷硫基、烷氨基、二烷氨基、烷基亚磺酰基、烷基磺酰基、芳基磺酰基、碳环基、芳基、和杂环基,其中R2任选地被一个或多个相同或不同的R20取代;
R20选自烷基、烯基、链烷酰基、卤素、硝基、氰基、羟基、氨基、巯基、甲酰基、羧基、氨甲酰基、烷氧基、烷硫基、烷氨基、二烷氨基、烷基亚磺酰基、烷基磺酰基、芳基磺酰基、碳环基、芳基、和杂环基,其中R20任选地被一个或多个相同或不同的R21取代;
R21选自卤素、硝基、氰基、羟基、三氟甲氧基、三氟甲基、氨基、甲酰基、羧基、氨甲酰基、巯基、氨磺酰基、甲基、乙基、丙基、叔丁基、甲氧基、乙氧基、乙酰基、乙酰氧基、甲氨基、乙氨基、二甲氨基、二乙氨基、N-甲基-N-乙氨基、乙酰基氨基、N-甲基氨甲酰基、N-乙基氨甲酰基、N,N-二甲基氨甲酰基、N,N-二乙基氨甲酰基、N-甲基-N-乙基氨甲酰基、甲硫基、乙硫基、甲基亚磺酰基、乙基亚磺酰基、甲磺酰基、乙基磺酰基、甲氧基羰基、乙氧基羰基、N-甲基氨磺酰基、N-乙基氨磺酰基、N,N-二甲基氨磺酰基、N,N-二乙基氨磺酰基、N-甲基-N-乙基氨磺酰基、碳环基、芳基、和杂环基;
R3选自氢、烷基、烯基、链烷酰基、卤素、硝基、氰基、羟基、氨基、巯基、甲酰基、羧基、氨甲酰基、烷氧基、烷硫基、烷氨基、二烷氨基、烷基亚磺酰基、烷基磺酰基、芳基磺酰基、碳环基、芳基、和杂环基,其中R3任选地被一个或多个相同或不同的R30取代;
R30选自烷基、烯基、链烷酰基、卤素、硝基、氰基、羟基、氨基、巯基、甲酰基、羧基、氨甲酰基、烷氧基、烷硫基、烷氨基、二烷氨基、烷基亚磺酰基、烷基磺酰基、芳基磺酰基、碳环基、芳基、和杂环基,其中R30任选地被一个或多个相同或不同的R31取代;并且
R31选自卤素、硝基、氰基、羟基、三氟甲氧基、三氟甲基、氨基、甲酰基、羧基、氨甲酰基、巯基、氨磺酰基、甲基、乙基、丙基、叔丁基、甲氧基、乙氧基、乙酰基、乙酰氧基、甲氨基、乙氨基、二甲氨基、二乙氨基、N-甲基-N-乙氨基、乙酰基氨基、N-甲基氨甲酰基、N-乙基氨甲酰基、N,N-二甲基氨甲酰基、N,N-二乙基氨甲酰基、N-甲基-N-乙基氨甲酰基、甲硫基、乙硫基、甲基亚磺酰基、乙基亚磺酰基、甲磺酰基、乙基磺酰基、甲氧基羰基、乙氧基羰基、N-甲基氨磺酰基、N-乙基氨磺酰基、N,N-二甲基氨磺酰基、N,N-二乙基氨磺酰基、N-甲基-N-乙基氨磺酰基、碳环基、芳基、和杂环基。
在一些实施例中,天冬酰胺内肽酶抑制剂是经取代的喹啉-5-基甲胺衍生物,例如具有以下化学式的化合物:
其前药、酯、衍生物、或盐,其中,
R1选自氢、烷基、烯基、链烷酰基、卤素、硝基、氰基、羟基、氨基、巯基、甲酰基、羧基、氨甲酰基、烷氧基、烷硫基、烷氨基、二烷氨基、烷基亚磺酰基、烷基磺酰基、芳基磺酰基、碳环基、芳基、和杂环基,其中R1任选地被一个或多个相同或不同的R10取代;
R10选自烷基、烯基、链烷酰基、卤素、硝基、氰基、羟基、氨基、巯基、甲酰基、羧基、氨甲酰基、烷氧基、烷硫基、烷氨基、二烷氨基、烷基亚磺酰基、烷基磺酰基、芳基磺酰基、碳环基、芳基、和杂环基,其中R10任选地被一个或多个相同或不同的R11取代;
R11选自卤素、硝基、氰基、羟基、三氟甲氧基、三氟甲基、氨基、甲酰基、羧基、氨甲酰基、巯基、氨磺酰基、甲基、乙基、丙基、叔丁基、甲氧基、乙氧基、乙酰基、乙酰氧基、甲氨基、乙氨基、二甲氨基、二乙氨基、N-甲基-N-乙氨基、乙酰基氨基、N-甲基氨甲酰基、N-乙基氨甲酰基、N,N-二甲基氨甲酰基、N,N-二乙基氨甲酰基、N-甲基-N-乙基氨甲酰基、甲硫基、乙硫基、甲基亚磺酰基、乙基亚磺酰基、甲磺酰基、乙基磺酰基、甲氧基羰基、乙氧基羰基、N-甲基氨磺酰基、N-乙基氨磺酰基、N,N-二甲基氨磺酰基、N,N-二乙基氨磺酰基、N-甲基-N-乙基氨磺酰基、碳环基、芳基、和杂环基;
R2选自氢、烷基、烯基、链烷酰基、卤素、硝基、氰基、羟基、氨基、巯基、甲酰基、羧基、氨甲酰基、烷氧基、烷硫基、烷氨基、二烷氨基、烷基亚磺酰基、烷基磺酰基、芳基磺酰基、碳环基、芳基、和杂环基,其中R2任选地被一个或多个相同或不同的R20取代;
R20选自烷基、烯基、链烷酰基、卤素、硝基、氰基、羟基、氨基、巯基、甲酰基、羧基、氨甲酰基、烷氧基、烷硫基、烷氨基、二烷氨基、烷基亚磺酰基、烷基磺酰基、芳基磺酰基、碳环基、芳基、和杂环基,其中R20任选地被一个或多个相同或不同的R21取代;
R21选自卤素、硝基、氰基、羟基、三氟甲氧基、三氟甲基、氨基、甲酰基、羧基、氨甲酰基、巯基、氨磺酰基、甲基、乙基、丙基、叔丁基、甲氧基、乙氧基、乙酰基、乙酰氧基、甲氨基、乙氨基、二甲氨基、二乙氨基、N-甲基-N-乙氨基、乙酰基氨基、N-甲基氨甲酰基、N-乙基氨甲酰基、N,N-二甲基氨甲酰基、N,N-二乙基氨甲酰基、N-甲基-N-乙基氨甲酰基、甲硫基、乙硫基、甲基亚磺酰基、乙基亚磺酰基、甲磺酰基、乙基磺酰基、甲氧基羰基、乙氧基羰基、N-甲基氨磺酰基、N-乙基氨磺酰基、N,N-二甲基氨磺酰基、N,N-二乙基氨磺酰基、N-甲基-N-乙基氨磺酰基、碳环基、芳基、和杂环基;
R3选自氢、烷基、烯基、链烷酰基、卤素、硝基、氰基、羟基、氨基、巯基、甲酰基、羧基、氨甲酰基、烷氧基、烷硫基、烷氨基、二烷氨基、烷基亚磺酰基、烷基磺酰基、芳基磺酰基、碳环基、芳基、和杂环基,其中R3任选地被一个或多个相同或不同的R30取代;
R30选自烷基、烯基、链烷酰基、卤素、硝基、氰基、羟基、氨基、巯基、甲酰基、羧基、氨甲酰基、烷氧基、烷硫基、烷氨基、二烷氨基、烷基亚磺酰基、烷基磺酰基、芳基磺酰基、碳环基、芳基、和杂环基,其中R30任选地被一个或多个相同或不同的R31取代;
R31选自卤素、硝基、氰基、羟基、三氟甲氧基、三氟甲基、氨基、甲酰基、羧基、氨甲酰基、巯基、氨磺酰基、甲基、乙基、丙基、叔丁基、甲氧基、乙氧基、乙酰基、乙酰氧基、甲氨基、乙氨基、二甲氨基、二乙氨基、N-甲基-N-乙氨基、乙酰基氨基、N-甲基氨甲酰基、N-乙基氨甲酰基、N,N-二甲基氨甲酰基、N,N-二乙基氨甲酰基、N-甲基-N-乙基氨甲酰基、甲硫基、乙硫基、甲基亚磺酰基、乙基亚磺酰基、甲磺酰基、乙基磺酰基、甲氧基羰基、乙氧基羰基、N-甲基氨磺酰基、N-乙基氨磺酰基、N,N-二甲基氨磺酰基、N,N-二乙基氨磺酰基、N-甲基-N-乙基氨磺酰基、碳环基、芳基、和杂环基;
R4选自氢、烷基、烯基、链烷酰基、卤素、硝基、氰基、羟基、氨基、巯基、甲酰基、羧基、氨甲酰基、烷氧基、烷硫基、烷氨基、二烷氨基、烷基亚磺酰基、烷基磺酰基、芳基磺酰基、碳环基、芳基、和杂环基,其中R4任选地被一个或多个相同或不同的R40取代;
R40选自烷基、烯基、链烷酰基、卤素、硝基、氰基、羟基、氨基、巯基、甲酰基、羧基、氨甲酰基、烷氧基、烷硫基、烷氨基、二烷氨基、烷基亚磺酰基、烷基磺酰基、芳基磺酰基、碳环基、芳基、和杂环基,其中R40任选地被一个或多个相同或不同的R41取代;
R41选自卤素、硝基、氰基、羟基、三氟甲氧基、三氟甲基、氨基、甲酰基、羧基、氨甲酰基、巯基、氨磺酰基、甲基、乙基、丙基、叔丁基、甲氧基、乙氧基、乙酰基、乙酰氧基、甲氨基、乙氨基、二甲氨基、二乙氨基、N-甲基-N-乙氨基、乙酰基氨基、N-甲基氨甲酰基、N-乙基氨甲酰基、N,N-二甲基氨甲酰基、N,N-二乙基氨甲酰基、N-甲基-N-乙基氨甲酰基、甲硫基、乙硫基、甲基亚磺酰基、乙基亚磺酰基、甲磺酰基、乙基磺酰基、甲氧基羰基、乙氧基羰基、N-甲基氨磺酰基、N-乙基氨磺酰基、N,N-二甲基氨磺酰基、N,N-二乙基氨磺酰基、N-甲基-N-乙基氨磺酰基、碳环基、芳基、和杂环基;
R5选自氢、烷基、烯基、链烷酰基、卤素、硝基、氰基、羟基、氨基、巯基、甲酰基、羧基、氨甲酰基、烷氧基、烷硫基、烷氨基、二烷氨基、烷基亚磺酰基、烷基磺酰基、芳基磺酰基、碳环基、芳基、和杂环基,其中R5任选地被一个或多个相同或不同的R50取代;
R50选自烷基、烯基、链烷酰基、卤素、硝基、氰基、羟基、氨基、巯基、甲酰基、羧基、氨甲酰基、烷氧基、烷硫基、烷氨基、二烷氨基、烷基亚磺酰基、烷基磺酰基、芳基磺酰基、碳环基、芳基、和杂环基,其中R50任选地被一个或多个相同或不同的R51取代;
R51选自卤素、硝基、氰基、羟基、三氟甲氧基、三氟甲基、氨基、甲酰基、羧基、氨甲酰基、巯基、氨磺酰基、甲基、乙基、丙基、叔丁基、甲氧基、乙氧基、乙酰基、乙酰氧基、甲氨基、乙氨基、二甲氨基、二乙氨基、N-甲基-N-乙氨基、乙酰基氨基、N-甲基氨甲酰基、N-乙基氨甲酰基、N,N-二甲基氨甲酰基、N,N-二乙基氨甲酰基、N-甲基-N-乙基氨甲酰基、甲硫基、乙硫基、甲基亚磺酰基、乙基亚磺酰基、甲磺酰基、乙基磺酰基、甲氧基羰基、乙氧基羰基、N-甲基氨磺酰基、N-乙基氨磺酰基、N,N-二甲基氨磺酰基、N,N-二乙基氨磺酰基、N-甲基-N-乙基氨磺酰基、碳环基、芳基、和杂环基;
R6选自氢、烷基、烯基、链烷酰基、卤素、硝基、氰基、羟基、氨基、巯基、甲酰基、羧基、氨甲酰基、烷氧基、烷硫基、烷氨基、二烷氨基、烷基亚磺酰基、烷基磺酰基、芳基磺酰基、碳环基、芳基、和杂环基,其中R6任选地被一个或多个相同或不同的R60取代;
R60选自烷基、烯基、链烷酰基、卤素、硝基、氰基、羟基、氨基、巯基、甲酰基、羧基、氨甲酰基、烷氧基、烷硫基、烷氨基、二烷氨基、烷基亚磺酰基、烷基磺酰基、芳基磺酰基、碳环基、芳基、和杂环基,其中R60任选地被一个或多个相同或不同的R61取代;
R61选自卤素、硝基、氰基、羟基、三氟甲氧基、三氟甲基、氨基、甲酰基、羧基、氨甲酰基、巯基、氨磺酰基、甲基、乙基、丙基、叔丁基、甲氧基、乙氧基、乙酰基、乙酰氧基、甲氨基、乙氨基、二甲氨基、二乙氨基、N-甲基-N-乙氨基、乙酰基氨基、N-甲基氨甲酰基、N-乙基氨甲酰基、N,N-二甲基氨甲酰基、N,N-二乙基氨甲酰基、N-甲基-N-乙基氨甲酰基、甲硫基、乙硫基、甲基亚磺酰基、乙基亚磺酰基、甲磺酰基、乙基磺酰基、甲氧基羰基、乙氧基羰基、N-甲基氨磺酰基、N-乙基氨磺酰基、N,N-二甲基氨磺酰基、N,N-二乙基氨磺酰基、N-甲基-N-乙基氨磺酰基、碳环基、芳基、和杂环基;
R7选自氢、烷基、烯基、链烷酰基、卤素、硝基、氰基、羟基、氨基、巯基、甲酰基、羧基、氨甲酰基、烷氧基、烷硫基、烷氨基、二烷氨基、烷基亚磺酰基、烷基磺酰基、芳基磺酰基、碳环基、芳基、和杂环基,其中R7任选地被一个或多个相同或不同的R70取代;
R70选自烷基、烯基、链烷酰基、卤素、硝基、氰基、羟基、氨基、巯基、甲酰基、羧基、氨甲酰基、烷氧基、烷硫基、烷氨基、二烷氨基、烷基亚磺酰基、烷基磺酰基、芳基磺酰基、碳环基、芳基、和杂环基,其中R70任选地被一个或多个相同或不同的R71取代;并且
R71选自卤素、硝基、氰基、羟基、三氟甲氧基、三氟甲基、氨基、甲酰基、羧基、氨甲酰基、巯基、氨磺酰基、甲基、乙基、丙基、叔丁基、甲氧基、乙氧基、乙酰基、乙酰氧基、甲氨基、乙氨基、二甲氨基、二乙氨基、N-甲基-N-乙氨基、乙酰基氨基、N-甲基氨甲酰基、N-乙基氨甲酰基、N,N-二甲基氨甲酰基、N,N-二乙基氨甲酰基、N-甲基-N-乙基氨甲酰基、甲硫基、乙硫基、甲基亚磺酰基、乙基亚磺酰基、甲磺酰基、乙基磺酰基、甲氧基羰基、乙氧基羰基、N-甲基氨磺酰基、N-乙基氨磺酰基、N,N-二甲基氨磺酰基、N,N-二乙基氨磺酰基、N-甲基-N-乙基氨磺酰基、碳环基、芳基、和杂环基。
在一些实施例中,天冬酰胺内肽酶抑制剂是经取代的噻唑衍生物,例如具有以下化学式的化合物:
其前药、酯、衍生物、或盐,其中,
R1选自氢、烷基、烯基、链烷酰基、卤素、硝基、氰基、羟基、氨基、巯基、甲酰基、羧基、氨甲酰基、烷氧基、烷硫基、烷氨基、二烷氨基、烷基亚磺酰基、烷基磺酰基、芳基磺酰基、碳环基、芳基、和杂环基,其中R1任选地被一个或多个相同或不同的R10取代;
R10选自烷基、烯基、链烷酰基、卤素、硝基、氰基、羟基、氨基、巯基、甲酰基、羧基、氨甲酰基、烷氧基、烷硫基、烷氨基、二烷氨基、烷基亚磺酰基、烷基磺酰基、芳基磺酰基、碳环基、芳基、和杂环基,其中R10任选地被一个或多个相同或不同的R11取代;
R11选自卤素、硝基、氰基、羟基、三氟甲氧基、三氟甲基、氨基、甲酰基、羧基、氨甲酰基、巯基、氨磺酰基、甲基、乙基、丙基、叔丁基、甲氧基、乙氧基、乙酰基、乙酰氧基、甲氨基、乙氨基、二甲氨基、二乙氨基、N-甲基-N-乙氨基、乙酰基氨基、N-甲基氨甲酰基、N-乙基氨甲酰基、N,N-二甲基氨甲酰基、N,N-二乙基氨甲酰基、N-甲基-N-乙基氨甲酰基、甲硫基、乙硫基、甲基亚磺酰基、乙基亚磺酰基、甲磺酰基、乙基磺酰基、甲氧基羰基、乙氧基羰基、N-甲基氨磺酰基、N-乙基氨磺酰基、N,N-二甲基氨磺酰基、N,N-二乙基氨磺酰基、N-甲基-N-乙基氨磺酰基、碳环基、芳基、和杂环基;
R2选自氢、烷基、烯基、链烷酰基、卤素、硝基、氰基、羟基、氨基、巯基、甲酰基、羧基、氨甲酰基、烷氧基、烷硫基、烷氨基、二烷氨基、烷基亚磺酰基、烷基磺酰基、芳基磺酰基、碳环基、芳基、和杂环基,其中R2任选地被一个或多个相同或不同的R20取代;R20选自烷基、烯基、链烷酰基、卤素、硝基、氰基、羟基、氨基、巯基、甲酰基、羧基、氨甲酰基、烷氧基、烷硫基、烷氨基、二烷氨基、烷基亚磺酰基、烷基磺酰基、芳基磺酰基、碳环基、芳基、和杂环基,其中R20任选地被一个或多个相同或不同的R21取代;
R21选自卤素、硝基、氰基、羟基、三氟甲氧基、三氟甲基、氨基、甲酰基、羧基、氨甲酰基、巯基、氨磺酰基、甲基、乙基、丙基、叔丁基、甲氧基、乙氧基、乙酰基、乙酰氧基、甲氨基、乙氨基、二甲氨基、二乙氨基、N-甲基-N-乙氨基、乙酰基氨基、N-甲基氨甲酰基、N-乙基氨甲酰基、N,N-二甲基氨甲酰基、N,N-二乙基氨甲酰基、N-甲基-N-乙基氨甲酰基、甲硫基、乙硫基、甲基亚磺酰基、乙基亚磺酰基、甲磺酰基、乙基磺酰基、甲氧基羰基、乙氧基羰基、N-甲基氨磺酰基、N-乙基氨磺酰基、N,N-二甲基氨磺酰基、N,N-二乙基氨磺酰基、N-甲基-N-乙基氨磺酰基、碳环基、芳基、和杂环基;
R3选自氢、烷基、烯基、链烷酰基、卤素、硝基、氰基、羟基、氨基、巯基、甲酰基、羧基、氨甲酰基、烷氧基、烷硫基、烷氨基、二烷氨基、烷基亚磺酰基、烷基磺酰基、芳基磺酰基、碳环基、芳基、和杂环基,其中R3任选地被一个或多个相同或不同的R30取代;
R30选自烷基、烯基、链烷酰基、卤素、硝基、氰基、羟基、氨基、巯基、甲酰基、羧基、氨甲酰基、烷氧基、烷硫基、烷氨基、二烷氨基、烷基亚磺酰基、烷基磺酰基、芳基磺酰基、碳环基、芳基、和杂环基,其中R30任选地被一个或多个相同或不同的R31取代;并且
R31选自卤素、硝基、氰基、羟基、三氟甲氧基、三氟甲基、氨基、甲酰基、羧基、氨甲酰基、巯基、氨磺酰基、甲基、乙基、丙基、叔丁基、甲氧基、乙氧基、乙酰基、乙酰氧基、甲氨基、乙氨基、二甲氨基、二乙氨基、N-甲基-N-乙氨基、乙酰基氨基、N-甲基氨甲酰基、N-乙基氨甲酰基、N,N-二甲基氨甲酰基、N,N-二乙基氨甲酰基、N-甲基-N-乙基氨甲酰基、甲硫基、乙硫基、甲基亚磺酰基、乙基亚磺酰基、甲磺酰基、乙基磺酰基、甲氧基羰基、乙氧基羰基、N-甲基氨磺酰基、N-乙基氨磺酰基、N,N-二甲基氨磺酰基、N,N-二乙基氨磺酰基、N-甲基-N-乙基氨磺酰基、碳环基、芳基、和杂环基。
在一些实施例中,天冬酰胺内肽酶抑制剂是经取代的6-甲基-5,6,7,8-四氢吡啶并[4,3-d]嘧啶-4(3H)-酮衍生物,例如具有以下化学式的化合物:
其前药、酯、衍生物、或盐,其中,
R1选自氢、烷基、烯基、链烷酰基、卤素、硝基、氰基、羟基、氨基、巯基、甲酰基、羧基、氨甲酰基、烷氧基、烷硫基、烷氨基、二烷氨基、烷基亚磺酰基、烷基磺酰基、芳基磺酰基、碳环基、芳基、和杂环基,其中R1任选地被一个或多个相同或不同的R10取代;
R10选自烷基、烯基、链烷酰基、卤素、硝基、氰基、羟基、氨基、巯基、甲酰基、羧基、氨甲酰基、烷氧基、烷硫基、烷氨基、二烷氨基、烷基亚磺酰基、烷基磺酰基、芳基磺酰基、碳环基、芳基、和杂环基,其中R10任选地被一个或多个相同或不同的R11取代;
R11选自卤素、硝基、氰基、羟基、三氟甲氧基、三氟甲基、氨基、甲酰基、羧基、氨甲酰基、巯基、氨磺酰基、甲基、乙基、丙基、叔丁基、甲氧基、乙氧基、乙酰基、乙酰氧基、甲氨基、乙氨基、二甲氨基、二乙氨基、N-甲基-N-乙氨基、乙酰基氨基、N-甲基氨甲酰基、N-乙基氨甲酰基、N,N-二甲基氨甲酰基、N,N-二乙基氨甲酰基、N-甲基-N-乙基氨甲酰基、甲硫基、乙硫基、甲基亚磺酰基、乙基亚磺酰基、甲磺酰基、乙基磺酰基、甲氧基羰基、乙氧基羰基、N-甲基氨磺酰基、N-乙基氨磺酰基、N,N-二甲基氨磺酰基、N,N-二乙基氨磺酰基、N-甲基-N-乙基氨磺酰基、碳环基、芳基、和杂环基;
R2选自氢、烷基、烯基、链烷酰基、卤素、硝基、氰基、羟基、氨基、巯基、甲酰基、羧基、氨甲酰基、烷氧基、烷硫基、烷氨基、二烷氨基、烷基亚磺酰基、烷基磺酰基、芳基磺酰基、碳环基、芳基、和杂环基,其中R2任选地被一个或多个相同或不同的R20取代;
R20选自烷基、烯基、链烷酰基、卤素、硝基、氰基、羟基、氨基、巯基、甲酰基、羧基、氨甲酰基、烷氧基、烷硫基、烷氨基、二烷氨基、烷基亚磺酰基、烷基磺酰基、芳基磺酰基、碳环基、芳基、和杂环基,其中R20任选地被一个或多个相同或不同的R21取代;并且
R21选自卤素、硝基、氰基、羟基、三氟甲氧基、三氟甲基、氨基、甲酰基、羧基、氨甲酰基、巯基、氨磺酰基、甲基、乙基、丙基、叔丁基、甲氧基、乙氧基、乙酰基、乙酰氧基、甲氨基、乙氨基、二甲氨基、二乙氨基、N-甲基-N-乙氨基、乙酰基氨基、N-甲基氨甲酰基、N-乙基氨甲酰基、N,N-二甲基氨甲酰基、N,N-二乙基氨甲酰基、N-甲基-N-乙基氨甲酰基、甲硫基、乙硫基、甲基亚磺酰基、乙基亚磺酰基、甲磺酰基、乙基磺酰基、甲氧基羰基、乙氧基羰基、N-甲基氨磺酰基、N-乙基氨磺酰基、N,N-二甲基氨磺酰基、N,N-二乙基氨磺酰基、N-甲基-N-乙基氨磺酰基、碳环基、芳基、和杂环基。
药用组合物
在某些实施例中,本披露涉及包括在此披露的化合物和药学上可接受的赋形剂的药用组合物。在某些实施例中,药用组合物是处于丸剂、胶囊、片剂、或盐水水性缓冲液的形式。在某些实施例中,该药学上可接受的赋形剂选自糖类、二糖、蔗糖、乳糖、葡萄糖、甘露醇、山梨糖醇、多糖、淀粉、纤维素、微晶纤维素、纤维素醚、羟丙基纤维素(HPC)、木糖醇、山梨糖醇、麦芽糖醇、明胶、聚乙烯吡咯烷酮(PVP)、聚乙二醇(PEG)、羟丙基甲基纤维素(HPMC)、交联的羧甲基纤维素钠、二碱式磷酸钙、碳酸钙、硬脂酸、硬脂酸镁、滑石、碳酸镁、二氧化硅、维生素A、维生素E、维生素C、棕榈酸视黄酯、硒、半胱氨酸、甲硫氨酸、柠檬酸和柠檬酸钠、对羟基苯甲酸甲酯、对羟基苯甲酸丙酯及其组合。
在此披露的药用组合物可以呈药学上可接受的盐类的形式,通常如以下所描述的。适合的药学上可接受的有机和/或无机酸的某些优选但不限定的实例是盐酸、氢溴酸、硫酸、硝酸、乙酸以及柠檬酸,连同其他本身已知的药学上可接受的酸(在以下提到的引用文件中进行引用)。
当本披露的这些化合物包含一个酸基和一个碱基的时候,本披露的这些化合物还可能形成一个内盐,并且这类化合物在本披露的范围内。当本披露的这些化合物包含一个给氢的杂原子(如NH)的时候,本披露涵盖通过将所述氢原子在该分子内转移到一个碱基或原子上形成的盐类和/或异构体。
这些化合物的药学上可接受的盐类包括该酸加成以及它的碱性盐类。适合的酸加成盐由形成无毒的盐的酸形成。实例包括乙酸盐、己二酸盐、天冬氨酸盐、苯甲酸盐、苯碳酸盐、碳酸氢盐/碳酸盐、硫酸氢盐/硫酸盐、硼酸盐、樟脑磺酸盐、柠檬酸盐、环己烷氨基磺酸盐、乙二磺酸盐、乙磺酸盐、甲酸盐、富马酸盐、葡庚糖酸盐、葡萄糖酸盐、葡糖醛酸盐、六氟磷酸盐、羟苯酰苯酸盐、盐酸化物/氯化物、氢溴化物/溴化物、氢碘化物/碘化物、羟乙磺酸盐、乳酸盐、苹果酸盐、马来酸盐、丙二酸盐、甲磺酸盐、甲基硫酸盐、萘酚盐、2-萘磺酸盐、烟酸盐、硝酸盐、乳清酸盐、草酸盐、棕榈酸盐、扑酸盐、磷酸盐/磷酸/磷酸二氢盐、焦谷氨酸盐、糖质酸盐、硬脂酸盐、琥珀酸盐、鞣酸盐、酒石酸盐、甲苯磺酸盐、三氟乙酸盐以及昔萘酸盐盐类。适合的碱盐从形成无毒盐的碱形成。实例包括铝、精氨酸、苄星青霉素G、钙、胆碱、二乙胺、二乙醇胺、甘胺酸、细胞溶素、镁、甲基葡胺、环匹罗司乙醇胺、钾、钠、氨丁三醇以及锌盐。酸类和碱类的半盐也可能形成,例如半硫酸盐和半钙盐。作为适合的盐类的一个综述,参见斯特尔(Stahl)和韦穆特(Wermuth)所著的药用盐手册:特性、选择以及使用(威利-VCH,2002),通过引用结合在此。
在此描述的这些化合物可能以药物前体的形式给予。前药可以包括共价结合的载体,该载体当给予哺乳动物受试者时释放该活性母体药物。前药可以通过修饰存在于这些化合物中的功能基团制备,其方式是使得这些修饰在常规操作中或者在体内是可切割的,以形成这些母体化合物。例如,药物前体包括羟基结合到任意基团的化合物,当给予到哺乳动物受试者中时,羟基断裂形成游离的羟基。前药的实例包括,但不限于,在这些化合物中的醇功能基团的乙酸盐、甲酸盐以及苯甲酸盐衍生物类。将一种化合物构建为前药的方法可以在特斯塔(Testa)和迈耶(Mayer)的书,药物的水解和前药新陈代谢(Drug and Prodrug Metabolism),威利(2006)中找到。典型的前药通过水解酶转化前药,酰胺、内酰胺、肽、羧酸酯、环氧化合物的水解,或者无机酸类酯的切割形成活性代谢产物。制造酯前药例如游离羟基基团的乙酰基酯是本领域中的普通技术。众所周知,酯前药容易在体内降解释放相应的醇。参见例如今井(Imai),药物代谢药代动力学(Drug Metab Pharmacokinet)(2006)21(3):173-85,标题为“人类羧酸酯酶同工酶:催化特性和合理药物设计”(“Human carboxylesterase isozymes:catalytic properties and rational drug design.”)。
典型地,用于本披露的药用组合物包括有效量的化合物和适合的药学上可接受的载体。这些制剂能以本身已知的方式制备,该方式通常涉及将根据本披露所述的至少一种化合物与一种或多种药学上可接受的载体混合,并且,如果是所希望的,与其他药用活性化合物组合,此时有必要在无菌条件下进行。参考美国专利号6,372,778、美国专利号6,369,086、美国专利号6,369,087、美国专利号6,372,733以及以上提及的进一步的参考,连同标准手册,例如最新版本的雷明顿制药科学(Remington's Pharmaceutical Sciences)。
通常来说,对于药物使用,这些化合物可以被配制为一种药物制剂,该药物制剂包括至少一种化合物以及至少一种药学上可接受的载体、稀释剂或赋形剂和/或佐剂,以及任选地一种或多种另外的药用活性化合物。
被披露的这些药物制剂优选以一种单位剂型的形式,并且可以被适当地封装,例如在一个盒子、疱、管形瓶、瓶子、小药囊、针剂或者任意其他适合的单剂量或者多剂量的夹持器或者容器中(可以被适当地标记);可任选地用一个或多个包含产品信息和/或使用说明的宣传单。通常来说,这类单位剂量将在至少本披露的一种化合物包含1mg至1000mg,并且通常在5mg至500mg之间,如每单元剂量10mg、25mg、50mg、100mg、200mg、300mg或者400mg。
这些化合物可以通过多种途径给予,包括口服、眼睛、直肠、经皮、皮下、静脉内、肌内或者鼻内途径,主要取决于所使用的具体制剂。通常来说,该化合物将以一个“有效量”给予,由此意味着在适当的给药下,一种化合物的任意量足够在它给予的受试者中达到所希望的治疗或者预防效果。通常,取决于待预防或者治疗的情况以及给药的途径,这种有效量将通常为每天每千克病人体重0.01mg至1000mg之间,更经常在0.1mg至500mg之间,如1mg至250mg,例如每天每千克病人体重大约5mg、10mg、20mg、50mg、100mg、150mg、200mg或250mg,该剂量可以作为被划分成一个或多个日常剂量的单一的日常剂量。给予的量,给药的途径以及进一步的治疗方案可能由治疗的临床医师决定,取决与因素,如年龄、性别、以及病人的一般条件以及待治疗的疾病/症状的性质和严重性。参考美国专利号6,372,778、美国专利号6,369,086、美国专利号6,369,087、美国专利号6,372,733以及以上提及的进一步的参考,连同标准手册,例如最新版本的雷明顿制药科学(Remington's Pharmaceutical Sciences)。
对于口服给药形式,该化合物可以与适合的添加剂混合,如赋形剂、稳定剂或者惰性稀释剂,并且通过常规方法引入适合的给药形式,如片剂、包衣片剂、硬胶囊、水、醇或油溶液。适合的惰性载体的实例是阿拉伯树胶、氧化镁、碳酸镁、磷酸钾、乳糖、葡萄糖或者淀粉,特别是玉米淀粉。在这种情况下,该制备可以通过干法或者湿法造粒实行。适合的油性赋形剂或者溶剂是蔬菜或者动物油,如葵花籽油或者鱼肝油。水或者醇溶液的适合的溶剂是水、乙醇、糖溶液或者它们的混合物。聚乙二醇以及聚丙二醇也被用作其他给药形式的另外的助剂。作为立即释放的片剂,这些组合物可能包含微晶纤维素、磷酸二钙、淀粉、硬脂酸镁以及乳糖和/或其他本领域已知的赋形剂、粘合剂、增充剂、分解剂、稀释剂以及润滑剂。
当通过鼻吸气雾剂或吸入剂给予时,这些化合物可能根据药物配制品的本领域公认的技术制备,并且制备成盐溶液,使用苯甲醇以及其他适合的防腐剂,吸收促进剂来增强生物利用率,碳氟化合物和/或本领域已知的溶解或分散剂。以气雾剂或者喷雾的形式给药的适合的药物配制品是,例如,在本披露中的这些化合物的溶液、悬浮液或乳液或者它们的生理上可耐受的溶剂,如乙醇或水,或者这类溶剂的一个混合物。如果需要,该配制品可以包含其他药物助剂,如表面活性剂、乳化剂以及稳定剂,连同推进剂。
对于皮下或者静脉给药,如果是所希望的,因此,这些具有常规物质的化合物如增溶剂、乳化剂或者另外的助剂被引入溶液、悬浮液或者乳液。这些化合物还可以被低压冻干,并且这些冷冻干燥物可以用于,例如,注射或者浸出制剂的生产。例如,适合的溶剂是水、生理盐溶液或低级醇类,如乙醇、丙醇、丙三醇,糖溶液,如葡萄糖或者甘露醇溶液,或者提及的多种溶剂的混合物。这些可注射的溶液或者悬浮液可能根据已知的技术配置,使用适合的无毒的、不经肠可接受的稀释剂或者溶剂,如甘露醇、1,3-丁二醇、水、林格式溶液或者等渗氯化钠溶液,或者适合的分散或润湿以及助悬剂,如包含合成的甘油单酯或甘油二酯无菌的、温和的非挥发油,以及包含油酸的脂肪酸类。
当以栓剂的形式经直肠给予的时候,这些配制品可能通过将化学式I的这些化合物与一种适合的无刺激性的赋形剂混合,如可可脂、合成甘油酯类或者聚乙二醇类,这些赋形剂在常温下是固体,但是在直肠腔内液化和/或溶解以便释放药物。
在某些实施例中,考虑到这些组合物可以是延长释放的配制品。典型的延长释放配制品利用一种肠溶衣。典型地,在口服治疗中应用一种屏障,以便控制在其被吸收的消化系统的位置。
肠溶衣防止药物在到达小肠之前释放。肠溶衣可能包含多糖类的聚合物,如麦芽糊精、黄胞胶、硬葡聚糖、淀粉、藻酸盐、短梗霉多糖、透明质酸、甲壳质、聚葡萄胺糖等;其他天然聚合物,如蛋白质类(白蛋白、明胶等)、聚左旋赖氨酸;聚丙烯酸钠;聚(甲基丙烯酸羟烷酯)(例如聚(甲基丙烯酸羟烷酯));羧聚乙烯(例如聚羰乙烯TM);丙烯酸聚合物;聚乙烯吡咯酮;胶类,如古尔胶、阿拉伯胶、卡拉牙胶、阔叶榆绿木胶、刺槐豆胶、罗望子果胶、胞外多糖胶、黄芪胶、琼脂、果胶、谷蛋白等;聚乙烯醇;乙烯乙烯醇;聚乙二醇(PEG);以及纤维素醚,如羟甲香豆素(HMC)、羟乙基纤维素(HEC)、羟丙基纤维素(HPC)、甲基纤维素(MC)、e乙基纤维素(EC)、羧甲基纤维素(CEC)、乙羟基乙基纤维素(EHEC)、羧甲基纤维素(CMHEC)、羟丙基甲基纤维素(HPMC)、羟丙基乙基纤维素(HPEC)以及羧基甲基纤维素钠(Na CMC);以及任意以上的聚合物的共聚物和/或(简单的)混合物。某些上述聚合物可能通过标准技术进一步交联。
聚合物的选择将取决于施用于本发明的组合物的该活性成分/药物的性质连同所希望的释放率。特别是,它将经过普通技术人员的鉴别,例如在HPMC的情况下,通常一个较高的分子量将提供药物从该组合物中较低的释放率。此外,在HPMC的情况下,甲氧基团和羟丙基基团取代的不同程度将提高药物从该组合物中的释放率的变化。在这方面,以及以上所述的,可能令人希望的是提供以涂层形式的本发明的组合物,其中该聚合物载体通过混合两种或多种聚合物的方式提供,例如,不同的分子量以便生产一种特殊的所需的或所希望的释放特征。
聚交酯、聚乙醇酸交酯的微球,以及它们的共聚物聚(丙交酯共聚乙交酯)可能用于形成持续释放的蛋白质或化合物供应系统。蛋白质类和/或化合物可以通过多种方法加入该聚(丙交酯共聚乙交酯)微球储存,这些方法包括与水性蛋白质以及有机溶剂性聚合物形成水油相乳液(乳液法),与分散在溶剂型聚合物溶液中的固态蛋白质形成固油相悬浮液(悬浮法),或者通过将该蛋白质溶解在溶剂型聚合物溶液中(溶解法)。可以将聚(乙二醇)贴附在蛋白质类(聚乙二醇化药物修饰技术)来增加体内循环治疗蛋白质的半衰期,并且降低免疫应答的机会。
使用方法
在某些实施例中,这些天冬酰胺内肽酶抑制剂对于治疗或预防神经退行性疾病和认知障碍例如阿尔茨海默病是有用的。在某些实施例中,本披露涉及包括天冬酰胺内肽酶抑制剂和药学上可接受的赋形剂的药用组合物。在某些实施例中,本披露涉及治疗或预防神经退行性疾病的方法,这些方法包括将有效量的药用组合物给予至对其有需要的受试者,该药用组合物包括在此披露的天冬酰胺内肽酶抑制剂。
在某些实施例中,受试者处于展现出AD症状的风险。
在某些实施例中,本披露考虑将在此披露的化合物和成像剂(如florbetapir(18F)和/或涉及治疗或改善AD的一种或多种症状的治疗剂组合给药。
在某些实施例中,本披露考虑把此披露的化合物和用于记忆丧失的药物、用于行为改变的治疗、用于睡眠改变的治疗组合给药。
在某些实施例中,本披露考虑把此披露的化合物和选自胆碱酯酶抑制剂如多奈哌齐、利伐斯的明、加兰他敏、和他克林和/或用于阻滞NMDA受体的药剂如美金刚组合给药,以治疗阿尔茨海默病的认知症状(记忆丧失、困惑以及在思考和推理方面的问题)。
在某些实施例中,本披露考虑将在此披露的化合物和维生素E组合给药。
在某些实施例中,本披露考虑将在此披露的化合物和例如抗兴奋、抗焦虑、抗神经错乱、抗失眠以及抗抑郁药剂的药物组合给药。
在某些实施例中,本披露考虑将在此披露的化合物和淀粉样蛋白的单克隆抗体疫苗(包括但不限于solanuzemab、gantenerumab、以及bapineuzumab)组合给药。
在某些实施例中,本披露考虑将在此披露的化合物和用于卒中或创伤性脑损伤的药物组合给药。
在某些实施例中,本披露考虑将在此披露的化合物和重组组织纤溶酶原激活剂(rtPA)组合给药。
在某些实施例中,在此披露的化合物可以用于治疗与细胞凋亡相关的多种疾病,包括神经退行性障碍、缺血性损伤、获得性免疫缺陷综合征(AIDS)、以及骨质疏松症。细胞凋亡涉及肌萎缩侧索硬化(ALS)、亨廷顿病、阿尔茨海默病、帕金森病、以及脊髓性肌萎缩。在多发性硬化(MS)中,少突胶质细胞的死亡是神经胶质通过细胞凋亡而变性的重要例子。
在某些实施例中,在此披露的化合物可用于治疗亨廷顿病和其他神经退行性疾病如齿状红核苍白球吕伊斯体萎缩症(DRPLA)、3型小脑萎缩症(SCA-3)、以及脊延髓肌萎缩症(SBMA)。
神经元细胞凋亡还在急性损伤如卒中、创伤、和缺血后观察到。细胞凋亡已经在动物卒中模型中的纹状体的和皮质的神经元中被观察到。
实验
AEP的抑制剂通过高通量筛选来鉴定
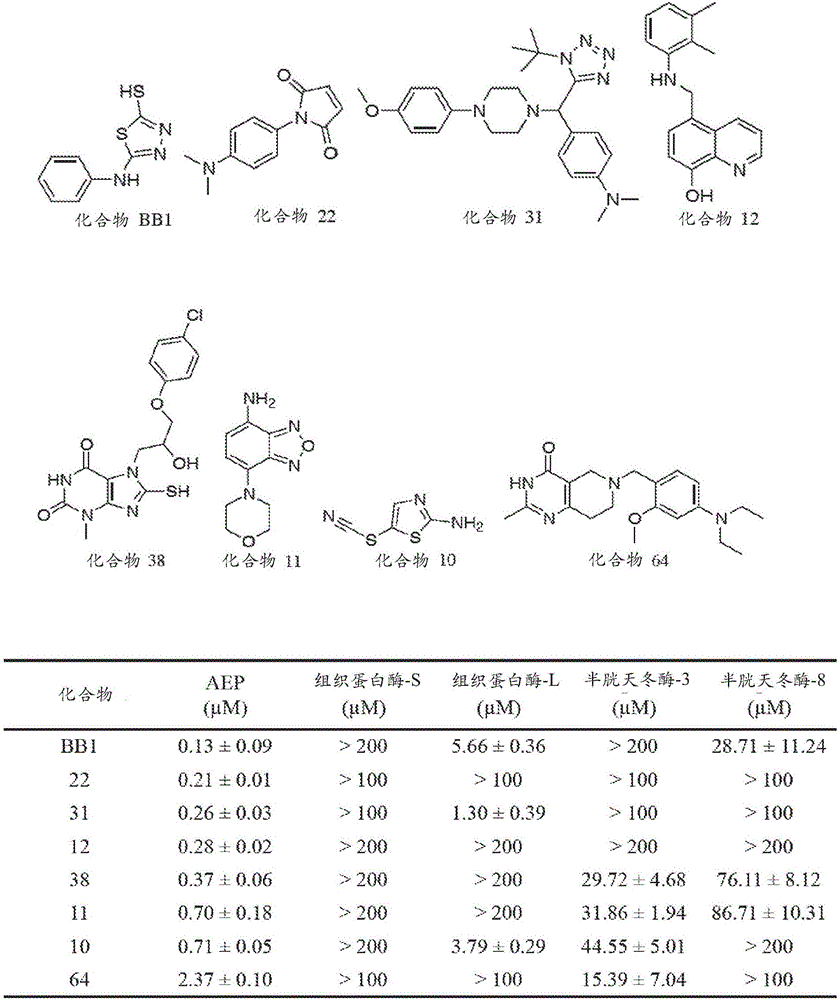
为了鉴定AEP的小分子抑制剂,协同爱默蕾化学生物发现中心(Emory Chemical Biology Discovery Center)设计高通量筛选。该筛选结合小鼠肾细胞裂解物以测定54,384种化合物的库。在用来自AEP-/-小鼠的肾细胞裂解物进行反向筛选时,736个命中化合物被确认针对细胞AEP显示小于或等于40μM的IC50值。用纯化的活性AEP进行第三次筛选,发现46个命中化合物展现出有前景的抑制活性(图1)。另外的结构分析和分类使这些化合物被归为8类不同的骨架家族。在来自每组的一些最强的化合物用纯化的活性AEP测试后,发现顶尖的8个候选化合物的IC50值。还使用四种主要的半胱氨酸蛋白酶来确定这些化合物的特异性(图2)。化合物BB1显现在大约130mM具有针对AEP最大的效力,并且它对AEP的选择性比对组织蛋白酶-L选择性高约38倍。另一方面,化合物22对于所有测试的半胱氨酸蛋白酶具有大于100μM的IC50。化合物11和38还显现是AEP的有力抑制剂,因为它们分别显示了大约700nM和370nM的IC50值,并且它们对AEP的选择性比对半胱天冬酶-3或半胱天冬酶-8的选择性至少高80倍。化合物64展现出在2.37μM的最高IC50。它是个低微摩尔抑制剂,并且它对AEP的选择性比对组织蛋白酶-S、组织蛋白酶-L和半胱天冬酶-8的选择性高超过40倍,并且比对半胱天冬酶-3的选择性高约6倍。
化合物的细胞渗透性
为了评价这些化合物在完整细胞中的活性,将这些化合物与人类的类B淋巴母细胞pala细胞孵育,这些人类B淋巴母细胞样pala细胞富含内源性AEP并且已经在细胞测定中被用于抑制AEP。大部分化合物能够以在亚微摩尔范围内的IC50值抑制酶,然而化合物BB1和10展现出略大的IC50值;许多化合物显现是细胞渗透性的(图3)。IC50值小于1μM的化合物的ADME特征被进一步评估。
体外ADMET特征
为了表征这些化合物的毒性,使用人类肝细胞癌HepG细胞和原代神经元培养物进行MTT测定去监测细胞活力。在HepG细胞中,化合物22(含马来酰亚胺的衍生物)揭示了和阳性对照依托泊苷相似的毒性,依托泊苷是一种拓扑异构酶抑制剂并且已知其诱导双链断裂(图4A)。将这些化合物在原代神经元培养物中的细胞毒性使用LDH测定测量细胞裂解来测定(图4B)。化合物的致癌性与它的微核诱导是成正比的。为了评价化合物是否具有任何致癌性,进行COMET测定和微核测定。在这些测定中,产生可测量的DNA切口的苯并(α)芘(B(a)p)被包括作为阳性对照。在用50μM化合物处理24小时后,化合物22是唯一一个示出基因毒性的测试化合物,因此将该化合物从进一步分析中排除(图4C和4D)。
为了探索这些化合物的体外ADME特征,进行另外的测试。进行Caco-2细胞单层渗透性筛选以评价这些化合物的吸收特征,并且发现化合物11和31是高度可渗透的,并且因此应该是生理上可较好吸收的(表1)。
表1.Caco-2渗透性。
LLOQ=在接受侧未检测到化合物
在BBB-PAMPA渗透性测定中,化合物11以高水平被检测到,并且因此被认为能够穿过血脑屏障(表2)。
表2.BBB-PAMPA渗透性。
LLOQ=在接受侧未检测到化合物
ND=由于生物分析问题未检测到峰
人类肝微粒体稳定性筛选证实了在孵育30分钟后,76%的化合物11和88%的化合物38保留在人类肝微粒体中(表3)。
表3.肝微粒体稳定性。
ND=由于生物分析问题(不良的离子化)未检测到峰
根据CYP抑制筛选,化合物31能够以69.2%抑制CYP2C9,并且以55.7%抑制CYP2C19,而化合物64在10μM的浓度下以58.3%抑制CYP2D6,表明这两种化合物能够产生潜在的药物-药物相互作用(表4)。
表4.CYP抑制。
化合物的DTT可逆转性
虽然并不预期本披露的实施例被任何具体机制所限制,但为了获得对由抑制剂采用以便去除AEP活性的机制的进一步深入了解,在游离硫醇基的存在下测定这些抑制剂的可逆转性。将强还原剂如DTT,或弱还原剂L-半胱氨酸添加到抑制的反应中,可以用于竞争胜过抑制药剂并且恢复带有活性位点硫醇基残基的酶的催化活性。这里,通过将还原剂DTT或L-半胱氨酸添加到反应中来使用类似的途径,其中为了逆转抑制剂的作用,AEP已经与指定的抑制剂孵育。含硫醇基的化合物BB1和38以及含硫氰酸酯部分的化合物10,都显现在还原剂的存在下已经重新获得实质性的量的活性,指示还原剂能够还原酶的活性位点半胱氨酸,并且由此增强活性酶的有效浓度。然而,在含硫化合物BB1、10和38的存在下,AEP重新获得实质性的量的活性。对于化合BB1和38,酶活的这种增加可以是由于在抑制剂和酶之间的二硫键的还原,因为这些化合物包含硫醇基。化合物10包含硫氰酸酯,并且可以经历被酶的活性位点硫醇盐进行亲核攻击,以形成硫代亚氨酸酯酶-抑制剂复合物。在酸性条件下,该复合物可由强还原剂如DTT或更弱的还原剂L-半胱氨酸还原。因此,可能的是化合物BB1、10和38可以和AEP的活性位点半胱氨酸形成共价键并竞争性地抑制该AEP的活性。
抑制剂表征
为了进一步评价由化合物采用的用以抑制AEP的机制,针对化合物11以及化合物BB1测定抑制动力学,从而确认硫醇部分竞争性地抑制该酶。为了确定化合物BB1和11的抑制模式,将稳态动力学参数在递增浓度的每种抑制剂的存在下进行测量(图6A-H)。产生的每种化合物的米氏图表显现指示竞争性抑制。竞争抑制剂和底物竞争结合酶的活性位点,因此在饱和的底物浓度下,抑制可以减弱。抑制剂常数KI,是产生半最大抑制的抑制剂浓度,是抑制剂效力的度量;化合物的KI值在图6A-B中被列出。化合物BB1和11的米氏图以及纳摩尔级抑制常数指示它们是AEP的竞争性抑制剂。因为BB1包含硫醇基,它能够和AEP的活性位点半胱氨酸形成二硫键。化合物11的反应性基团仍然不清楚,因此为了进一步表征它的抑制模式,在递增浓度的抑制剂下,测量进展曲线。所产生的曲线图指示化合物11以时间和浓度依赖性方式抑制AEP(图6C)。此外,描绘从进展曲线中测定的抑制的准一级速率常数kobs,得到双曲线,与失活的两步机制一致(图6D)。失活速率,kinact,被发现是0.075±0.002mm-1,因此二级速率常数kinact/KI是1.2x 106min-1M-1,表明化合物11不可逆地使AEP失活。化合BB1还显示了指示缓慢结合型抑制剂的进展曲线(图6E)。然而,kobs相对抑制剂浓度曲线得到一条直线,可能是因为快速的二硫化物形成反应(图6F)。抑制的二级速率常数kinact/KI能够从这条曲线的斜率中获得,并且是3.3x 106min-1M-1,并且对于化合物BB1而言,指示此化合物能够和AEP的活性位点硫醇基形成二硫键。
在酸中毒的细胞模型中的效力
剥夺细胞的氧和葡萄糖是被用于在所培养的细胞中触发酸中毒的细胞模型。在氧-葡萄糖剥夺(OGD)的细胞模型中,测定化合物的效力,从而模拟卒中在原代培养的神经元中的影响。作为剥夺了神经元的包含氧和葡萄糖的培养基的结果,AEP活性为双倍(图7A,‘DMSO-Norm’相比于‘DMSO-OGD'’),而半胱天冬酶-3以及组织蛋白酶活性仍然保持相对不变。在化合物11的存在下,AEP活性存在明显的剂量依赖性下降,这并没有在半胱天冬酶-3以及组织蛋白酶中观察到。化合物12还能够产生AEP活性的略微下降,并且选择性的只针对该酶(图7)。由于已经发现缺血在卒中后增加阿尔茨海默病的风险,淀粉样前体蛋白(APP)的切割在OGD处理后被评价(图7D和E)。作为仅对DMSO处理的响应,观察到APP的切割(图7D,泳道2),并且显现在1μM的化合物10、11和12以及仅仅0.1μM的化合物31、38和64处理时,切割被阻滞,推定是由于AEP抑制。图7E还示出响应于化合物10和12存在的剂量依赖性APP切割的降低。
化合物11具有神经保护作用,并且在AD小鼠中改善认知行为
将化合物11的急性和慢性毒性通过口服饲喂C57BL/6J小鼠100mg/kg的药物经30天时间而评估。在整个处理时间中,在体重方面未观察到显著的改变。此外,免疫组织化学染色证实运载体处理的和药物处理的动物之间没有大差别。还对用化合物11处理的小鼠进行全血球计数(CBC)分析,并且验证了所有的参数是在健康小鼠的正常范围内。综上,这些数据证实了化合物11在100mg/kg的剂量下,在小鼠中并没有展现全身毒性。化合物11具有非常有利的ADMET特征,具有突出的血脑屏障渗透性。
化合物11抑制AEP活性并且在AD的小鼠模型中降低由BACE进行的APP切割
活性AEP切割APP并且促进Aβ的产生。为了测试化合物11的口服给药是否可以减弱体内Aβ的产生,将5XFAD小鼠在2个月大小开始用化合物11或运载体处理3个月。5XFAD小鼠共表达总计五种与通常的AD相关联的突变,并且在早期发展脑淀粉样蛋白斑。AEP活性测定示出口服化合物11显著地抑制了在小鼠脑内AEP的活性(图8A)。AEP的阻滞减少了接下来在切割APP中的BACE活性。C99,是由β位点切割产生的APP的C端片段,在化合物11处理后减少,但是α位点切割产物C83的表达并没有被化合物11改变。化合物11处理并没有改变总的APP或β分泌酶(BACE1)的蛋白水平(图8B,第二和第三个图片)。这些结果指示化合物11在抑制脑中的AEP的活性,并且AEP活性的抑制降低了APP的β位点切割以及Aβ的产生。因此,化合物11抑制AEP并且在AD小鼠模型中降低由BACE进行的APP降解。
化合物11的慢性口服给药挽救在5XFAD小鼠中的记忆损害
为了研究化合物11的慢性口服给药是否能够逆转5XFAD小鼠的认知损害,将3个月大的小鼠用化合物11通过连续口服给药来处理,每日一次持续3个月。硫黄素S染色发现运载体处理的5XFAD小鼠具有在海马体(HC)、运动皮质(MC)、以及额皮质(FC)中有显著的蛋白斑块沉积,该沉积可以由化合物11减弱(图9A,B)。该结果是通过使用抗-Aβ抗体的淀粉样蛋白斑的免疫组织化学染色确认的。此外,化合物11降低在脑裂解物中的Aβ1-40和Aβ1-42的浓度(图9C,D)。为了研究化合物11对认知活动的治疗效力,我们使用莫里斯水迷宫测试评价空间记忆形成。在5个采集日中,当与运载体处理的小鼠比较时,用化合物11处理的小鼠示出到平台的降低的距离,指示改进了空间学习(图9E)。在探索测试中,化合物11处理的小鼠在之前包含平台的目标象限中花费了更多的时间,证实化合物11对空间记忆回想的挽救(图9F)。游泳速度并未受到化合物11的影响(图9G)。这些结果指示用化合物11的慢性处理改善了在5XFAD模型中的记忆损害。
化合物11在5XFAD小鼠中防止突触损失并且恢复突触可塑性
突触功能障碍是AD的早期特征,并且被认为是认知损害的基础。和非转基因对照小鼠相比,5XFAD小鼠示出降低的突触密度。为了研究化合物11对突触功能障碍的影响,在CA1区域中的突触密度用电子显微镜评价。化合物11显著增加了突触密度(图10A,B)。将沿着锥体神经元的单独树突的树突棘的密度通过高尔基体染色进行评价。再一次,化合物11增加了树突棘的密度(图10C,D)。长时程增强(LTP)是构成学习和记忆基础的突触可塑性的度量。5XFAD小鼠在谢弗侧枝-CA1途径中有降低的LTP大小。化合物11处理在5XFAD小鼠中显著逆转了LTP损害,指示由化合物11引起突触功能的恢复(图10E,F)。
方法
小鼠、细胞和试剂
5XFAD小鼠来自杰克逊(Jackson)实验室,并且根据爱默蕾医学院(Emory Medical School)指南在无病原环境中养殖。小鼠接受10mg/Kg/d剂量的运载体或11号化合物的饲喂处理。将抗APP、抗APP C、小鼠单克隆抗APP N585使用肽NH2-IKTEEISEVC-COOH发展,并且从蛋白G亲和柱中纯化。TUNEL原位细胞死亡检测试剂盒来自罗氏(印第安纳波利斯,印第安纳州(IN))。11号化合物购买自TCI(波特兰,奥勒冈州(OR))。化学品还购买自西格玛奥德里奇。天冬酰胺内肽酶(AEP,豆荚蛋白)从义翘神州生物技术有限公司(Sino Biological)获得,组织蛋白酶-S从雅典研究与技术公司(Athens Research and Technology)获得,半胱天冬酶-3和半胱天冬酶-8从密理博(Millipore)获得。Pala细胞是来自柯林沃茨(Colin Watts)博士的礼物,并且在37℃、5%CO2下被保存在加湿孵箱中的RPMI-1640培养基中,培养基中补充有10%FBS、2mg/mL谷氨酰胺、100U青霉素/链霉素。
高通量筛选
在微高通量筛选形式中,针对潜在的AEP抑制剂对Asinex化合物库进行筛选。在1536孔板中,将625μg/mL野生型小鼠肾细胞裂解物与16.7μM库中化合物孵育,并且通过EnVision多标记酶标仪进行读取(激发λ=360nm,发射λ=460nm),以获得背景读数。添加1μM Cbz-Ala-Ala-Asn-AMC以起始反应,并且在15分钟后,再次测量荧光,并且从最终结果中减去背景值。和对照孔相比,抑制的百分比被测定,并且将前736个化合物与来自AEP敲除小鼠的肾细胞裂解物和50nM纯的活性AEP(义翘神州)进行剂量-反应确证筛选。
酶学测定
组织蛋白酶-S-将100nM酶与抑制剂在测定缓冲液(100mM NaH2PO4 pH 6.5,100mM NaCl)中在37℃预孵育10分钟。该反应在添加25μM底物(Boc-Val-Leu-Lys-AMC(巴亨))时起始。
组织蛋白酶-L-将100nM酶与抑制剂在测定缓冲液(100mM乙酸钠pH5.5,1mM EDTA)中在37℃预孵育10分钟。该反应在添加25μM底物(D-Val-Leu-Lys-AMC(巴亨))时起始。
半胱天冬酶-3和半胱天冬酶-8-将酶与抑制剂在测定缓冲液(100mM HEPES pH 7.4,0.1%CHAPS,10%蔗糖)中在37℃预孵育10分钟。该反应在添加25μM底物(Ac-Asp-Glu-Val-Asp-AMC(巴亨))时起始。
AEP-将50nM酶与抑制剂在测定缓冲液(50mM乙酸钠pH 5.5,0.1%CHAPS,60mM Na2HPO4,1mM EDTA)中在37℃预孵育10分钟。该反应在添加10μM MAc-Asp-Glu-Val-Asp-AMC(巴亨)时起始。
在完整的Pala细胞中的IC50测定
将表达高浓度AEP的人类的类B淋巴母细胞Pala细胞培养于RPMI-1640中,补充有10%FBS、2mM L-谷氨酰胺、100单位/mL青霉素、100μg/mL链霉素。将不同浓度的每种化合物和Pala细胞在37℃孵育2小时。将细胞收集,用PBS洗涤两次并且在裂解缓冲液(20mM柠檬酸、60mM正磷酸氢二钠、1mM EDTA、0.1%CHAPS,pH 5.8)中裂解。将蛋白浓度通过布拉德福测定标准化,并且将裂解物用5μM Cbz-Ala-Ala-Asn-AMC测定。将IC50值通过把数据拟合到方程中测定:酶活性分数=1/(1+([I]/IC50)),其中,[I]=抑制剂浓度,并且IC50=产生半最大活性的抑制剂浓度。将数据用GraFit 5.0.11版本的软件安装包进行分析。
彗星测定(单细胞凝胶电泳)
人类肝细胞癌HepG2细胞被用于测定这些化合物的基因毒性。彗星测定根据Trevigen试剂盒(4250-050-K)提供的方案进行。简而言之,将细胞用运载体对照或50μM化合物预处理24小时。将细胞收获,嵌入到低熔点琼脂糖中,并在裂解缓冲液中在4℃浸泡45分钟。在碱解旋溶液(300mM NaOH,1mM EDTA)中孵育20分钟后,使细胞经受在碱解旋溶液中在300mA下进行30分钟电泳。将切片用70%乙醇洗涤、进行干燥并用SYBR Green在室温下染色30分钟。将产生切口的DNA测量为尾DNA的百分比。针对每种样品对一百个彗星图案进行评分。参见可泽斯(Kozics)等人(2011)黄酮类的结构在HepG2细胞中影响苯并(a)芘诱导的DNA损伤和微核的抑制程度,赘生物(Neoplasma)58,516-524。
微核测定
将HepG2细胞用运载体或50μM化合物处理24小时。将细胞用PBS清洗,然后以1:19在低渗溶液(0.075M KCl/0.9%NaCl)中37℃孵育10分钟。接下来,将细胞用甲醇:冰醋酸(3:1)在37℃固定15分钟,然后冲洗并干燥。将细胞用DAPI(2μg/mL)在室温下在黑暗中染色30分钟,用水冲洗、进行干燥并且用甘油安放。对于每个实验,对每个培养皿的一千个细胞进行分析;进行三次独立的实验。
DTT可逆转性测定
大约5倍的每种化合物IC50值被加入到AEP反应中,如上描述,并且允许反应15分钟。同时,将10mM(终浓度)二硫苏糖醇(DTT)或L-半胱氨酸添加到每个反应中并且孵育另外的15分钟。在第二个15分钟诱导时间结束时,测量每个样品的荧光。在DMSO存在下形成的产物的量被用于确定在每种药物的存在下AEP活性的百分比。
氧-葡萄糖剥夺
将化合物与原代神经元培养物DIV13预孵育30分钟。将培养基以不含葡萄糖的DMEM替换,并且对神经元进行脱气,并且在37℃下,在95%N2/5%CO2中用化合物孵育4小时。将培养基用DMEM替换,并且补充化合物,然后将神经元在常氧条件下被再灌注18小时。制备神经元裂解物用于AEP、半胱天冬酶-3和组织蛋白酶测定。此外,用神经元裂解物,使用抗-APP、抗-AEP抗体进行免疫印迹分析。
酶抑制测定
为了测定抑制常数以及化合物BB1、11和38抑制AEP的机制,在递增浓度的抑制剂不存在或存在的情况下测定肽底物Z-AAN-AMC水解的稳态动力学参数。在这些测定中,将指定浓度的抑制剂与底物在37℃预孵育10分钟,然后添加50 nM AEP以起始反应,将该反应在10分钟之后淬灭。将反应产物的RFU值用AMC标准曲线转化为微摩尔值,并且将最终的反应速率针对底物浓度进行绘制并且通过5.0.11版本的GraFit,使用非线性最小拟合二乘法,总体上拟合至代表竞争性抑制的方程(方程1)、代表非竞争性抑制的方程(方程2)、代表混合抑制的方程(方程3)、以及代表无竞争性抑制的方程(方程4)。
v=Vmax[S]/([S]+Km(1+[I]/Kis)) (方程1),
v=Vmax[S]/([S](1+[I]/Ki)+Km(1+[I]/Ki)) (方程2),
v=Vmax[S]/([S](1+[I]/Kii)+Km(l-[I]/Kis)) (方程3),
v=Vmax[S]/([S](1+[I]/Kii)+Km) (方程4)。
在方程中,Kii是截距Ki,Kis是斜率Ki。被化合物诱导的对AEP的抑制模式是通过数据到方程1-4的最佳拟合来测定。拟合的目测和标准误差的比较被用于确认这些赋值。
时程失活测定
进展曲线是通过在37℃下,在测定缓冲液中孵育5μM Z-AAN-AMC和指定浓度的抑制剂持续10分钟来产生。该反应通过添加50 nM AEP起始,并且在10分钟之后被淬灭。从AMC标准曲线中测定产物的浓度,并且通过非线性回归来拟合数据。因为曲线是非线性的,因此它们被使用5.0.11版本的GraFit软件安装包拟合至方程5,
[产物]=vi(1-e-kobs.app*t)/kobs.app (方程5),
其中vi是初始速率,kobs.app是失活的表观伪一级速率常数,并且t是时间。方程6:
kobs=((1+[S])/Km)kobs.app (方程6),
被用于修正从这个分析中获得的针对底物浓度的表观伪一级失活速率常数,并且由此获得的伪一级失活速率常数即kobs被针对测试的抑制剂浓度描绘。由于数据符合失活的两步机制,将它们拟合至方程7,
kobs=(kinact[I])/(KI+[I]) (方程7),
使用5.0.11版本的GraFit软件,其中KI是产生半最大失活的失活剂浓度,kinact是最大失活速率,并且[I]是失活剂浓度。
电子显微镜检查
将突触密度通过如之前描述的电子显微镜检查来测定(22)。在深麻醉后,将小鼠用在PBS中的2%戊二醛和3%多聚甲醛进行经心脏灌注。将海马体切片后固定在冷的1%OsO4中持续1小时。将样品使用标准程序进行制备并且检查。将超薄切片(90nm)用铀酰乙酸酯和乙酸铅染色,并且在100kV下,在JEOL 200CX电子显微镜下观察。突触通过突触小泡和突触后致密物的存在来鉴定。
小鼠脑组织制备和蛋白提取
在行为测试完成之后,小鼠被戊巴比妥深麻醉并且用盐水进行经心脏灌注,并且将脑迅速移除。将一个大脑半球固定在4%磷酸缓冲的多聚甲醛中,同时将另一半速冻以用于生化分析。为了脑蛋白的提取,首先将脑半球在PIPA缓冲液(25mM Tris-HCl,pH 7.5,150mM NaCl,1%NP 40,0.5%NaDOC,0.1%SDS)中提取,在100,000rpm离心30分钟,并且将包含不可溶Aβ的球粒进一步在2%SDS、25mM Tris-HCl(pH 7.5)中提取。
电生理学分析
如之前描述的进行电生理学分析(23)。简而言之,将运载体和11号化合物处理的5XFAD小鼠用异氟烷麻醉,头部被切下,并且将它们的脑滴进冰冷的人工脑脊液(a-CSF)中,该人工脑脊液包含124mM NaCl、3mM KCl、1.25mM NaH2PO4、6.0mM MgCl2、26mM NaHCO3、2.0mM CaCl2、以及10mM葡萄糖。将海马体用振动切片机切成400μm厚的横切片。在a-CSF中在室温(23℃-24℃)下孵育60-90分钟后,将切片放置在直立显微镜(奥林巴斯CX-31)的台子上的记录槽(RC-22C,华纳仪器)中,并且用a-CSF(包含1mMMgCl2)以3mL每分钟的速率在23℃-24℃下进行灌注。使用0.1MΩ的钨单极电极以刺激谢弗侧枝。将场兴奋性突触后电位(fEPSP)在CA1辐射层中由填充有具有3-4MΩ电阻的a-CSF的玻璃微电极来记录。刺激输出(Master-8;AMPI,耶路撒冷)被EPC9放大器的触发功能控制(HEKA Elektronik,兰布雷希特,德国)。将fEPSP在电流钳模式下记录。将数据在3kHz下过滤,并且在20kHz的采样速率下用Pluse软件(HEKA Elektronik)数字化。将刺激强度(0.1ms持续时间,10-30μA)设定为产生40%最大的f-EPSP并且以0.033Hz的速率施加测试脉冲。将fEPSP的LTP通过3θ-爆发刺激(TBS)诱导,它是在100Hz下的4次脉冲(以200ms间隔,重复3次)。配对脉冲易化(PPF)通过利用配对的脉冲来检查,以20-500ms的间隔分离开。LTP的大小用基线fEPSP初始斜率的平均百分比表示。
Western印迹分析
将小鼠脑组织或人类组织样品在裂解缓冲液(50mM Tris,pH 7.4,40mM NaCl,1mM EDTA,0.5%Triton X-100,1.5mM Na3VO4,50mM NaF,10mM焦磷酸钠,10mMβ-甘油磷酸钠,补充有蛋白酶抑制剂混合物)中裂解,并且在16,000g离心15分钟。将上清液在SDS装载缓冲液中煮沸。在SDS-PAGE后,将样品转移到硝酸纤维膜上。Western印迹分析用多种抗体进行。
免疫组织化学
将自由漂浮的30μm-厚的连续切片用0.3%的过氧化氢处理10分钟,并且然后用抗-AEP切割的APP(1:500)或抗-Aβ(1:500)孵育过夜。使用Histostain-SP试剂盒(#956543,英杰公司(invitrogen))根据厂商说明书发展信号。
Aβ蛋白斑染色
将淀粉样蛋白斑用硫黄素-S染色。将脱蜡和水合的切片在0.25%高锰酸钾溶液中孵育20分钟,在蒸馏水中冲洗,并且在包含2%草酸和1%焦亚硫酸钾的漂白溶液中孵育2分钟。在蒸馏水中冲洗后,将切片转移到包含1%氢氧化钠和0.9%过氧化氢的封闭溶液中持续20分钟。将切片在0.25%酸性酸中孵育5秒,然后在蒸馏水中冲洗,并用在50%乙醇中的0.0125%的硫黄素-S染色。将切片用50%乙醇清洗并放在蒸馏水中。然后切片用封固溶以及玻璃盖玻片覆盖。
Aβ42ELISA
将小鼠脑在8X质量的5M胍盐酸/50mM Tris HCl(pH 8.0)中均化,并且在室温下孵育3小时。然后将样品用冷的反应缓冲液(具有5%BSA和0.03%吐温20的磷酸盐缓冲盐水,补充有蛋白酶抑制剂混合物)稀释,并且在4℃在16000g离心20分钟。将上清液通过人类Aβ42ELISA试剂盒根据厂商说明书(KHB3441,英杰公司)进行分析。Aβ42的浓度通过和标准曲线比较来测定。
莫里斯水迷宫实验
将以标准引用水或11号化合物维持的雌性野生型和5XFAD小鼠在圆的充满水的桶(直径52英寸)中在富含额外的迷宫线索的环境中进行训练。将看不见的逃生平台定位在水下1cm处的一个固定空间位置上,独立于在具体试验中受试者的起始位置。以这种方式,受试者需要使用额外的迷宫线索来判定平台的位置。在每个试验开始时,将小鼠放进水迷宫中,用它们的爪子从4个不同的起始位点(N、S、E、W)之一处触摸墙壁。每个受试者每天被给予4次试验,持续连续的5天,试验间的间隔为15分钟。最大试验时长是60s,并且如果受试者不能在分配的时间中到达平台,它们被用手指导到达。在到达了不可见的逃生平台时,受试者留在其上面持续另外的5秒,以允许在环境中的空间线索的观察,以便指导到平台的未来行程。在每次试验后,将受试者干燥,并放在干的充满纸巾的塑料保持笼子中,以允许受试者变干。每小时监测水的温度,从而在22℃和25℃之间的水中测试小鼠。在5天任务采集后,呈现探索试验,在该探索试验期间将平台移除,并且在之前任务采集期间包含逃生平台的象限中所花费时间的百分比是经60s测量。对所有的试验借助于MazeScan(Clever Sys公司)针对潜伏期、游泳路线长度以及游泳速度进行分析。
高尔基体染色
将小鼠脑固定在10%的福尔马林中持续24小时,并且然后在黑暗中浸入3%重铬酸钾中持续3天。溶液每天更换。然后将脑转移到2%硝酸银溶液中并且在黑暗中孵育24小时。振动切片机将切片以60μm进行切割,空气干燥10分钟,通过95%和100%乙醇脱水,在二甲苯中进行清洗并进行封片。为了测量树突棘密度,仅对垂直于树突轴出现的树突棘进行计数。
- 还没有人留言评论。精彩留言会获得点赞!