用于治疗和诊断化学疗法抗性癌症的组合物和方法与流程
序列表
本申请含有序列表,所述序列表已经以ascii格式电子提交,并且在此通过提及完整收入。2015年12月22日创建的所述ascii拷贝命名为50474_092wo3_sequence_listing_12_22_15_st25,并且大小为4552字节。
发明领域
本发明涉及用于鉴定具有化学疗法抗性癌症的患者的方法。
发明背景
上皮卵巢癌(eoc)是妇科学恶性的死亡的首要原因,并且eoc的治疗继续呈现相当大的临床挑战。目前用于eoc的护理标准由攻击性手术细胞减少,随后是基于铂的和基于紫杉烷的辅助化学疗法组成。虽然对此治疗的响应率较高,但是20-30%的病例是抗性的,并且在初始疗法(primarytherapy)期间或完成初始疗法6个月之内进展。如此,抗性癌症患者自此治疗获得较少的益处,并且代表相当大的未满足的临床需要。为了预测对化学疗法的响应,并且为了开发新颖的策略以克服eoc中以及一般在癌症中的初始化学疗法抗性,需要更好地了解化学疗法抗性的分子特征。
已经暗示宿主基质微环境,通常称为“反应性基质”的活化为许多类型的癌症中癌症进展的一种至关重要的组分。癌症中的基质活化类似于正常组织中的伤口愈合过程,因为活化的基质细胞展现出升高的胞外基质(ecm)组分、生长因子、和基质重塑酶生成以创建促进癌细胞存活、增殖和侵入的肿瘤微环境。特别地,已经越来越认识到肿瘤微环境在eoc的发病机制中发挥重要的作用。然而,反应性基质的关键调节物和反应性基质影响肿瘤进展、治疗响应和eoc的临床结果的具体机制是了解不佳的。
因而,需要确定患者是否很可能响应基于化疗剂的疗法,以及还有开发用于治疗一般癌症的备选策略的方法。
发明概述
在一个方面,本发明特征在于鉴定具有化学疗法抗性癌症的患者的方法,所述方法包括:a)测定自患者获得的样品中一种或多种基质标签基因的表达水平,b)将所述一种或多种基质标签基因的表达水平与所述癌症类型中所述一种或多种基质标签基因的中值表达水平比较,并且c)确定所述患者的癌症是否是化学疗法抗性的,其中在所述患者样品中所述一种或多种基质标签基因以比所述癌症类型中所述一种或多种基质标签基因的中值表达水平多的水平表达指示所述患者具有化学疗法抗性癌症,例如在检测化学疗法(例如基于铂的化学疗法)抗性癌症中上调的一种或多种基质标签基因的表达水平的情况中。在检测化学疗法(例如基于铂的化学疗法)抗性癌症中下调的一种或多种基质标签基因的表达水平的情况中,检出降低的表达水平(例如比中值水平小的水平)也可以指示所述患者具有化学疗法抗性癌症。
在一个实施方案中,若已经确定所述患者的癌症以比所述癌症类型中所述一种或多种基质标签基因表达的第75百分位数多的水平表达所述一种或多种基质标签基因(例如在化学疗法(例如基于铂的化学疗法)抗性癌症中上调的一种或多种基质标签基因的情况中),则所述患者具有化学疗法抗性癌症。在上述方面的某些其它实施方案中,所述化学疗法抗性癌症是铂抗性癌症。
在某些实施方案中,所述方法进一步包括在确定所述患者具有化学疗法抗性癌症时将所述患者鉴定为很可能受益于vegf拮抗剂的施用的步骤。在某些其它实施方案中,所述方法进一步包括若确定所述患者具有化学疗法抗性癌症,则对所述患者以治疗有效量施用vegf拮抗剂的步骤。在优选的实施方案中,所述vegf拮抗剂是抗vegf抗体。优选地,所述抗vegf抗体是贝伐单抗。
在其它实施方案中,所述方法进一步包括在确定所述患者具有化学疗法抗性癌症时将所述患者鉴定为很可能受益于基质靶向疗法的步骤。在还有其它实施方案中,所述方法进一步包括若确定所述患者具有化学疗法抗性癌症,则对所述患者以治疗有效量施用基质靶向剂的步骤。
在另一个实施方案中,所述方法进一步包括在确定所述患者具有化学疗法抗性癌症时将所述患者鉴定为很可能受益于免疫疗法的步骤。在还有另一个实施方案中,所述方法进一步包括若确定所述患者具有化学疗法抗性癌症,则对所述患者以治疗有效量施用免疫调节剂的步骤。在优选的实施方案中,所述免疫调节剂包括tdo2、cd36、gzmk、cd247、cd1c、csf1r、ido1、il7r、或ccr7拮抗剂。
在第二个方面,本发明特征在于鉴定具有化学疗法敏感性癌症的患者的方法,所述方法包括:a)测定自患者获得的样品中一种或多种基质标签基因的表达水平,b)将所述一种或多种基质标签基因的表达水平与所述癌症类型中所述一种或多种基质标签基因的中值表达水平比较,并且c)确定所述患者是否具有化学疗法敏感性癌症,其中在所述患者样品中所述一种或多种基质标签基因以比所述癌症类型中所述一种或多种基质标签基因的中值表达水平少的水平表达指示所述患者具有化学疗法敏感性癌症(例如在化学疗法(例如基于铂的化学疗法)抗性癌症中上调的一种或多种基质标签基因的情况中)。
在某些实施方案中,若已经确定所述患者的癌症以比所述癌症类型中所述一种或多种基质标签基因表达的第25百分位数小的水平表达所述一种或多种基质标签基因,则所述患者具有化学疗法敏感性癌症。在其它实施方案中,所述方法包括若确定所述患者具有化学疗法敏感性癌症,则施用化学疗法方案中的一种或多种化学治疗剂的步骤。
在上述方面和实施方案的某些实施方案中,所述样品是肿瘤组织样品。在具体的实施方案中,在施用化学治疗剂前实施所述方法以提供施用前诊断。在某些实施方案中,所述患者尚未经历化学疗法或所述患者目前正在经历化学疗法。
在第三个方面,本发明特征在于鉴定可受益于vegf拮抗剂或免疫调节剂的施用的患有癌症的患者的方法,所述方法包括:a)测定自患者获得的样品中一种或多种基质标签基因的表达水平,其中所述一种或多种基质标签基因以比所述癌症类型中所述一种或多种基质标签基因的中值表达水平多的水平表达指示所述患者可受益于vegf拮抗剂或免疫调节剂的施用(例如在化学疗法(例如基于铂的化学疗法)抗性癌症中上调的一种或多种基质标签基因的情况中),并且任选地b)对所述患者以治疗有效量施用所述vegf拮抗剂或免疫调节剂。
在具体的实施方案中,上述方法进一步包括施用化学疗法方案中的一种或多种化学治疗剂的步骤。在一些实施方案中,所述化学治疗剂选自下组:her抗体、针对肿瘤关联抗原的抗体、抗激素化合物、保心药、细胞因子、egfr靶向性药物、抗血管生成剂、酪氨酸激酶抑制剂、cox抑制剂、非类固醇抗炎药、法尼基转移酶抑制剂、结合癌胚蛋白ca125的抗体、her2疫苗、her靶向疗法、raf或ras抑制剂、脂质体多柔比星、托泊替康、紫杉烷、双重酪氨酸激酶抑制剂、tlk286、emd-7200、治疗恶心的药物、预防或治疗皮疹的药物或标准痤疮疗法、预防或治疗腹泻的药物、体温降低药物、和造血生长因子。在其它实施方案中,所述一种或多种化学治疗剂是吉西他滨、卡铂、奥沙利铂、伊立替康、氟嘧啶(例如5-fu)、帕利他赛(例如nab-帕利他赛)、多西他赛、托泊替康、卡培他滨、甲酰四氢叶酸、替莫唑胺、干扰素-α、或脂质体多柔比星(例如peg化的脂质体多柔比星)。
在一个优选的实施方案中,所述化学疗法方案包括施用卡铂和帕利他赛;卡铂和吉西他滨;或帕利他赛、托泊替康、或peg化的脂质体多柔比星。在第二个优选的实施方案中,所述化学疗法方案包括施用卡培他滨和帕利他赛;或卡培他滨和多西他赛。在第三个优选的实施方案中,所述化学疗法方案包括施用替莫唑胺和任选地放射疗法。在第四个优选的实施方案中,所述化学疗法方案包括施用氟嘧啶、伊立替康、顺铂、氟嘧啶和奥沙利铂;氟嘧啶和伊立替康;氟嘧啶、甲酰四氢叶酸、和奥沙利铂;或伊立替康、氟嘧啶、和甲酰四氢叶酸。在第五个优选的实施方案中,所述化学疗法方案包括施用帕利他赛和托泊替康;或帕利他赛和顺铂。在第六个优选的实施方案中,所述化学疗法方案包括施用干扰素-α2a。
在一些实施方案中,所述一种或多种基质标签基因选自下组:postn、lox、timp3、fap、bgn、fgf1、fn1、angptl2、acta2、mmp11、rbp4、cd36、plvap、pecam1、gzmk、cd247、abcc9、pcolce、cd1c、ms4a1、cd44、pmepa1、il7r、fbln1、twist1、id1、rac2、gfra1、ccr7、man1a1、evi2a、ptprccd45ra、fcrl5、nnmt、cd27、sla、tdo2、nuak1、和col4a1。在优选的实施方案中,所述基质标签基因是postn。在其它优选的实施方案中,所述一种或多种基质标签基因是postn和fap;postn和timp3;postn和lox;postn、fap、和timp3;postn、fap、和lox;postn、timp3、和lox;或postn、fap、timp3、和lox。
在第四个方面,本发明特征在于治疗癌症患者的方法,所述方法包括对所述患者施用治疗有效量的基质靶向剂,其中已经确定所述患者的癌症以比所述癌症类型中所述一种或多种基质标签基因的中值表达水平多的水平表达所述一种或多种基质标签基因。
在上述方法的优选的实施方案中,所述基质靶向剂是抗骨膜蛋白(postn)抗体。在上述方法的某些实施方案中,所述癌症是原发性、晚期、不应性、或复发性的。在其它实施方案中,所述癌症是选自下组的妇科癌症:卵巢癌、腹膜癌、输卵管癌、宫颈癌、子宫内膜癌、阴道癌、和外阴癌。在优选的实施方案中,所述妇科癌症是卵巢癌。在上述方法的还有其它实施方案中,癌症选自下组:结肠直肠癌、乳腺癌、非小细胞肺癌(nsclc)、肾癌(肾细胞癌)、或脑癌(成胶质细胞瘤)。
在第五个方面,本发明提供了测定患者中的卵巢癌的阶段的方法。所述方法包括测定自所述患者获得的样品(例如肿瘤组织样品、血液样品、或血清样品)中postn的表达水平。在所述患者样品中检出相对于对照升高的postn表达水平指示卵巢癌的晚期阶段(例如figo卵巢癌iii或iv期)。在某些实施方案中,所述对照是具有卵巢癌的患者群体中postn表达的中值水平,而在其它实施方案中,所述对照是具有figoi期和/或figoii期卵巢癌的患者群体中postn表达的中值水平。任选地,所述方法还包括若确定所述患者具有晚期阶段的卵巢癌,则对所述患者施用疗法的步骤。
从详述、附图和权利要求书看,本发明的其它特征和优点会是显而易见的。
附图简述
图1a-1d显示了初始化学疗法抗性卵巢肿瘤中上调的“反应性基质”基因标签的鉴定。(a)32个plat-r原发性和26个plat-s原发性卵巢肿瘤之间前14种最差异表达的基因的分层群聚(假发现率(fdr)≤10%,倍数变化≥1.5)。在底部注释了对初始化学疗法的临床限定响应、tp53突变状态、和7种反复扩增基因(≥4个拷贝);(b)27个患者匹配的plat-r原发性和plat-r复发性卵巢肿瘤之间的前65种最差异表达的基因的分层群聚(fdr≤10%,倍数变化≥1.5);(c)plat-r原发性和复发性肿瘤中显著差异表达的共同标签基因的维恩(venn)图;(d)26个plat-s原发性、32个plat-r原发性、和27个plat-r复发性肿瘤中的四种反应性基质标签基因的基因表达。
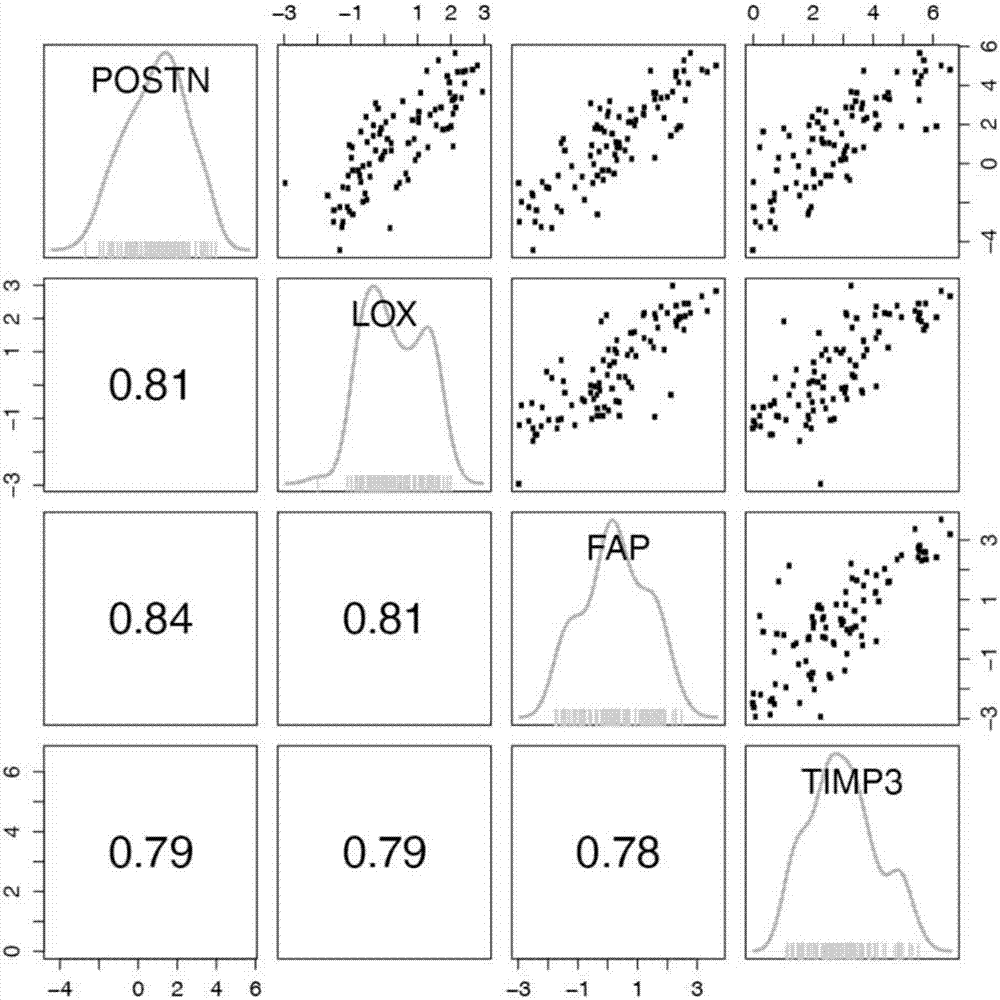
图2是一系列图,其显示彼此高度相关的4种反应性基质标签基因的mrna表达水平。
图3a-3b显示了通过rnaish和ihc对反应性基质标签基因postn、lox、和fap的原位分析。(a)来自plat-s原发性肿瘤、化学疗法前的患者匹配的plat-r原发性肿瘤、和疾病进展时化学疗法后的复发性肿瘤的代表性ish和ihc图像。左边两栏中的图像:用于检测postn、lox的2重生色rnaish,和用于检测fapmrna定位的单重(singleplex)rnaish。右边三栏中的图像:用于postn、fap、和asma蛋白定位的ihc染色。比例尺=100um。(b)所有85份样品(postn和fapish)或来自每个响应组的5份代表性肿瘤标本(loxish、postn、和fapihc)中的ish得分和ihc得分的汇总:plat-s原发性、患者匹配的plat-r原发性、和复发性肿瘤。分别在肿瘤和基质细胞中测定ishh得分(材料和方法,用均值和标准偏差绘图)和ihc总体得分两者。*p<0.05,**p<0.01。
图4a-4c显示了postn表达水平在体内与结缔组织生成表型相关联,并且postn在体外促进eoc细胞中的化学疗法抗性。(a)增加的结缔组织生成与postn表达和初始化学疗法抗性相关联。显示了肿瘤标本的苏木精和曙红(h&e)染色的代表性高放大率图像(上部小图)和postnish图像(下部小图)。如下定义结缔组织生成得分:0=无结缔组织生成,1=癌细胞邻近的少数分散的结缔组织增生病灶,2=癌细胞邻近的几个结缔组织增生病灶或中等汇合的(较宽的)结缔组织生成,但是不遍及切片存在,3=遍及切片的结缔组织增生反应,与大多数癌细胞有关。标签:ds=结缔组织增生基质,ns=正常基质,tc=肿瘤细胞。箭指向肿瘤细胞的例子。点线环绕含有肿瘤细胞的区域。大小比例尺,100μm。(b)21个plat-s原发性、18个plat-r原发性、和21个plat-r复发性肿瘤标本中结缔组织生成得分的汇总;(c)postn在体外促进化学疗法敏感性es2卵巢细胞中的化学疗法抗性。将96孔板用重组蛋白fn1或postn包被或保持未包被,之后将细胞分配入每孔中。然后,次日将10μm卡铂或10nm泰素添加至每孔。在化合物处理后72小时添加cell-titre
图5a-5b显示了反应性基质基因的表达预测icon7研究化学疗法处理分支中前线化学疗法的临床结果。(a)发现数据集(x轴)和独立的验证集(icon7对照分支)(y轴)之间的倍数变化(plat-r对plat-s)的关联。图上的5种基因是这两种数据集中显著差异表达的(p≤0.01和倍数变化≥1.5);(b)一项独立数据集(icon7化学疗法处理分支)中反应性基质标签基因表达(中值截留)与来自初始化学疗法的患者结果(pfs)的关联。
图6是一系列图,其显示了postn和卵巢癌中的已知预后因素之间的关联。
图7显示了4种基质标签基因的多变量分析。使用多变量cox回归模型分析使用中值截留二分的5种基因(postn、pgr、fap、lox、和timp3)的表达以评估每种基因的联系强度。仅postn的表达在此多变量分析中是显著的。另外,在对每名患者对4种基因的表达取平均值时,所得的总体基质得分不改善与pfs的联系(hr=2.0,95%ci:1.3-3.1,p=0.0013)。
图8提供了通过使用与初始化学疗法抗性有关的基因标签的途径分析(ingenuity)鉴定的头等活化网络和上游调节物的示意图。化学疗法抗性肿瘤中的下调基因是fgfr4、cxcl10、ido1、mmp10、和mmp7。剩余的基因在化学疗法抗性肿瘤中的上调程度上变化。
图9的图显示了postn表达与促血管发生标志物(plvap、pecam1、和angptl2)和m2样巨噬细胞标志物(cd68、cd163、和cd36)高度相关。
图10是分组点图,其显示了供应商获得的来自102名年龄匹配的正常健康受试者(nhs)、100名未知化学敏感性(卵巢癌)的上皮卵巢癌(eoc)患者、43名已知为铂抗性(plat-r卵巢癌)的eoc患者、96名肺癌(nsclc)患者、和29名胰腺癌患者的血清样品组中的postn表达范围。
图11是分组点图,其显示了供应商获得的来自i(25)和ii(6)期患者(31名组合)的血清样品和来自iii期患者的69份样品中的循环postn和疾病阶段之间的关联。
发明详述
i.导言
本发明提供了与卵巢癌中的初始化学疗法抗性特别相关并且在复发性肿瘤中进一步上调的反应性基质基因标签。对此标签的几种关键组分,包括骨膜蛋白(postn)、成纤维细胞活化蛋白(fap)、和赖氨酰氧化酶(lox)的原位分析揭示了这些基因在化学疗法抗性肿瘤中的肿瘤关联成纤维细胞中特别上调。在来自iii期临床的化学疗法治疗分组的独立数据集中验证了反应性基质基因标签,并且在此验证分析中显示了高postn表达水平与接收一线化学疗法(卡铂和帕利他赛)的患者的恶化结果(即无进展存活(pfs))有关。
因此,本发明提供了用于鉴定具有化学疗法抗性癌症(例如妇科癌症(例如卵巢、腹膜、输卵管、宫颈、子宫内膜、阴道或外阴癌))的患者的方法,其通过测定一种或多种基质标签基因的表达水平,并且将此表达水平与癌症类型中一种或多种基质标签基因的中值表达水平比较进行。一种或多种基质标签基因以比癌症类型中所述一种或多种基质标签基因的中值表达水平多的水平的表达的检出指示所述患者具有化学疗法抗性癌症。本发明还提供了用于治疗具有癌症(例如化学疗法抗性癌症)的患者的方法,其通过对患者施用基质靶向性或其它药剂进行。本发明进一步提供了鉴定具有癌症(例如化学疗法抗性癌症)的患者的方法,所述患者可受益于与化学疗法方案和/或基质靶向剂组合施用抗血管发生剂(例如vegf拮抗剂,诸如抗vegf抗体,例如贝伐单抗)或免疫调节剂。
ii.定义
除非另有定义,本文中使用的技术和科学术语与本发明所属领域的普通技术人员通常的理解具有相同的含义。singletonetal.,dictionaryofmicrobiologyandmolecularbiology第2版,j.wiley&sons(newyork,n.y.1994)及march,advancedorganicchemistryreactions,mechanismsandstructure第4版,johnwiley&sons(newyork,n.y.1992)为本领域技术人员提供本申请中使用的许多术语的一般指导。
为了解读本说明书,以下定义将适用,并且无论何时,以单数使用的术语也会包括复数,并且反之亦然。如果下文列出的任何定义与通过提及并入本文的任何文件矛盾,应当以下文列出的定义为准。
如本文中使用的,术语“施用”意指通过本领域中已知的用于施用治疗性抗体的任何合适的手段对需要此类治疗或医学干预的患者施用化学治疗剂(例如本文中描述的任何化学治疗剂,见下文)、基质靶向剂(例如抗postn抗体)、免疫调节剂、和/或抗血管发生剂(例如抗vegf抗体,诸如贝伐单抗)、和/或包含化学治疗剂(例如本文中描述的任何化学治疗剂,见下文)、基质靶向剂(例如抗postn抗体)、免疫调节剂、或抗血管发生剂(例如抗vegf抗体,诸如贝伐单抗)的药物组合物/治疗方案。非限制性施用路径包括口服、静脉内、腹膜内、皮下、肌内、表面、皮内、鼻内或支气管内施用(例如如通过吸入实现)。在本发明的上下文中特别优选的是肠胃外施用,例如静脉内施用。就用于治疗结肠直肠癌的贝伐单抗而言,依照emea的优选剂量是每2周给予一次的5mg/kg或10mg/kg体重或每3周给予一次的7.5mg/kg或15mg/kg体重。对于治疗nsclc,优选的剂量是与卡铂和帕利他赛组合通过输注每3周给予一次的15mg/kg。对于治疗肾细胞癌,优选的剂量是通过与干扰素α-2a一起输注或者作为单一疗法每2周给予一次的10mg/kg。对于治疗宫颈癌,优选剂量是通过输注每三周给予一次并且与下列化学疗法方案之一组合施用15mg/kg:帕利他赛和顺铂或帕利他赛和托泊替康。对于治疗成胶质细胞瘤,优选的剂量是通过输注每两周给予一次的10mg/kg。
用于鉴定多肽的激动剂或拮抗剂的方法可以包括使多肽与候选激动剂或拮抗剂分子接触并测量通常与多肽相关的一种或多种生物活性的可检测变化。
术语“抗体”在本文中以最广义使用,并且涵盖各种抗体结构,包括但不限于单克隆抗体、多克隆抗体、多特异性抗体(例如双特异性抗体)和抗体片段,只要它们展现出期望的抗原结合活性。结合靶物的抗体指能够以足够的亲和力结合靶物,使得该抗体可用作靶向靶物的诊断和/或治疗剂的抗体。在一个实施方案中,抗靶物抗体与无关非靶蛋白的结合程度小于抗体与靶物的结合的小于约10%,如例如通过放射免疫测定法(ria)或biacore测定法测量的。在某些实施方案中,结合靶物的抗体具有<1μm、<100nm、<10nm、<1nm、<0.1nm、<0.01nm、或<0.001nm(例如10-8m或更小,例如10-8m至10-13m,例如10-9m至10-13m)的解离常数(kd)。在某些实施方案中,抗靶物抗体结合不同物种间保守的靶物的表位。
“抗体片段”指除完整抗体之外的分子,其包含完整抗体中结合与完整抗体结合的抗原的一部分。抗体片段的例子包括但不限于fv、fab、fab’、fab’-sh、f(ab’)2;双抗体;线性抗体;单链抗体分子(例如scfv);和由抗体片段形成的多特异性抗体。
与参照抗体“结合相同表位的抗体”指在竞争测定法中将参照抗体对其抗原的结合阻断50%或更多的抗体,且相反,参照抗体在竞争测定法中将该抗体对其抗原的结合阻断50%或更多。
术语“益处”以最广义使用,指任何期望的效果,并且明确包括如本文中限定的临床益处。可以通过评估各种终点来测量临床益处,例如在某种程度上抑制疾病进展,包括减缓和完全阻滞;减少疾病事件和/或症状数目;减小损伤尺寸;抑制(即降低、减缓或完全阻止)疾病细胞渗入临近的周围器官和/或组织;抑制(即降低、减缓或完全阻止)疾病扩散;降低自身免疫应答(其可以但是不必导致疾病损伤的消退或消融);在某种程度上减轻一种或多种与病症有关的症状;延长治疗后无疾病表现(例如无进展存活)的长度;延长的总体存活;较高的应答率;和/或降低治疗后给定时间点的死亡率。
如本文中使用的,术语“生物学样品”或“样品”包括但不限于血液、血清、血浆、痰液、组织活组织检查、肿瘤组织、和鼻样品,包括鼻拭子或鼻息肉。
术语“癌症”和“癌性”指或描述哺乳动物中特征通常为细胞生长不受调控的生理疾患。此定义中包括良性和恶性癌症。癌症的例子包括但不限于癌、淋巴瘤、母细胞瘤、肉瘤、和白血病。此类癌症的更具体例子包括鳞状细胞癌、肺癌(包括小细胞肺癌、非小细胞肺癌、肺的腺癌、和肺的鳞癌)、腹膜癌、肝细胞癌、胃癌(gastricorstomachcancer)(包括胃肠癌)、胰腺癌、成胶质细胞瘤、宫颈癌、卵巢癌、肝癌(livercancerorhepaticcarcinoma)、膀胱癌、肝瘤(hepatoma)、乳腺癌、结肠癌、结肠直肠癌、子宫内膜癌或子宫癌、唾液腺癌、肾癌(kidneyorrenalcancer)、前列腺癌、外阴癌、甲状腺癌、及各种类型的头和颈癌,以及b细胞淋巴瘤(包括低级/滤泡性非何杰金氏淋巴瘤(nhl)、小淋巴细胞性(sl)nhl、中级/滤泡性nhl、中级弥漫性nhl、高级成免疫细胞性nhl、高级成淋巴细胞性nhl、高级小无核裂细胞性nhl、贮积病(bulkydisease)nhl、套细胞淋巴瘤、aids相关淋巴瘤、和瓦尔登斯特伦氏(waldenstrom)巨球蛋白血症)、慢性淋巴细胞性白血病(cll)、急性成淋巴细胞性白血病(all)、毛细胞性白血病、慢性成髓细胞性白血病、和移植后淋巴增殖性病症(ptld)、以及与瘢痣病(phakomatoses)、水肿(诸如与脑瘤有关的)和梅格斯氏(meigs)综合征有关的异常血管增殖。
“晚期”癌症指通过局部侵入或转移而扩散到最初的部位或器官之外的癌症。
“不应性”癌症指即使对癌症患者施用抗肿瘤剂,诸如化疗剂,仍然发生进展的癌症。不应性癌症的一个例子是铂不应性癌症。
“复发性”癌症指在对初始疗法的响应之后,在初始部位或远端部位再次生长的癌症。
“铂抗性”癌症意指虽然患者在接受基于铂的化学疗法但仍然进展的患者中的癌症或者已经在完成基于铂的化学疗法后的例如12个月内(例如6个月内)进展的患者中的癌症。此类癌症可以说成具有或展现出“铂抗性”。
“化学疗法抗性”癌症意指虽然患者在接受基于化学疗法方案但仍然进展的患者中的癌症或者已经在完成化学疗法方案后的例如12个月内(例如6个月内)进展的患者中的癌症。此类癌症可以说成具有或展现出“化学疗法抗性”。
术语“嵌合”抗体指其中的重和/或轻链的一部分自特定的来源或物种衍生,而重和/或轻链的剩余部分自不同来源或物种衍生的抗体。
抗体的“类”指其重链拥有的恒定域或恒定区的类型。抗体有5大类:iga、igd、ige、igg、和igm,并且这些中的几种可以进一步分成亚类(同种型),例如,igg1、igg2、igg3、igg4、iga1、和iga2。与不同类免疫球蛋白对应的重链恒定域分别称作α、δ、ε、γ、和μ。
“化疗剂”包括在治疗癌症中有用的化学化合物。化疗剂的例子包括厄洛替尼(erlotinib)(
化疗剂还包括(i)起调节或抑制激素对肿瘤作用的作用的抗激素剂,诸如抗雌激素类和选择性雌激素受体调控物类(serm),包括例如他莫昔芬(tamoxifen)(包括
化疗剂还包括抗体,诸如阿仑珠单抗(alemtuzumab)(campath),贝伐珠单抗(bevacizumab)(
化疗剂还包括“egfr抑制剂”,其指结合egfr或以其它方式直接与egfr相互作用并阻止或降低其信号传导活性的化合物,其另外还称作“egfr拮抗剂”。此类药剂的例子包括结合egfr的抗体和小分子。结合egfr的抗体的例子包括mab579(atcccrlhb8506),mab455(atcccrlhb8507),mab225(atcccrl8508),mab528(atcccrl8509)(参见美国专利no.4,943,533,mendelsohnetal.)及其变体,诸如嵌合化的225(c225或西妥昔单抗;
化疗剂还包括“酪氨酸激酶抑制剂”,包括前一段中提到的egfr靶向药物;小分子her2酪氨酸激酶抑制剂,诸如可从takeda获得的tak165;cp-724,714,一种口服erbb2受体酪氨酸激酶选择性抑制剂(pfizer和osi);优先结合egfr但抑制her2和egfr过表达细胞二者的双重her抑制剂,诸如ekb-569(可从wyeth获得);拉帕替尼(lapatinib)(gsk572016;可从glaxo-smithkline获得),一种口服her2和egfr酪氨酸激酶抑制剂;pki-166(可从novartis获得);泛her抑制剂,诸如卡奈替尼(canertinib)(ci-1033;pharmacia);raf-1抑制剂,诸如可从isispharmaceuticals获得的,抑制raf-1信号传导的反义药剂isis-5132;非her靶向tk抑制剂,诸如甲磺酸伊马替尼(
化疗剂还包括地塞米松(dexamethasone),干扰素,秋水仙素(colchicine),氯苯氨啶(metoprine),环孢霉素(cyclosporine),两性霉素(amphotericin),甲硝唑(metronidazole),阿仑单抗(alemtuzumab),阿利维a酸(alitretinoin),别嘌醇(allopurinol),氨磷汀(amifostine),三氧化二砷(arsenictrioxide),天冬酰胺酶(asparaginase),活的bcg,贝伐珠单抗(bevacuzimab),贝沙罗汀(bexarotene),克拉屈滨(cladribine),里本灵(clofarabine),darbepoetinalfa,地尼白介素(denileukin),右雷佐生(dexrazoxane),阿法依伯汀(epoetinalfa),厄洛替尼(elotinib),非格司亭(filgrastim),醋酸组氨瑞林(histrelinacetate),ibritumomab,干扰素α-2a,干扰素-2b,lenalidomide,左旋咪唑(levamisole),美司钠(mesna),甲氧沙林(methoxsalen),诺龙(nandrolone),奈拉滨(nelarabine),诺非单抗(nofetumomab),奥普瑞白介素(oprelvekin),palifermin,帕米膦酸盐(pamidronate),培加酶(pegademase),培门冬酶(pegaspargase),peg非格司亭(pegfilgrastim),培美曲塞二钠(pemetrexeddisodium),普卡霉素(plicamycin),卟吩姆钠(porfimersodium),喹纳克林(quinacrine),拉布立酶(rasburicase),沙格司亭(sargramostim),替莫唑胺(temozolomide),vm-26,6-tg,托瑞米芬(toremifene),tretinoin,atra,戊柔比星(valrubicin),唑来膦酸盐(zoledronate),和唑来膦酸(zoledronicacid),及其药学可接受盐。
“基于铂的化学治疗剂”或“platin”意指作为铂的配位络合物的抗肿瘤药。基于铂的化学治疗剂的例子包括卡铂、顺铂、沙铂(satraplatin)、吡铂(picoplatin)、奈达铂(nedaplatin)、triplatin、lipoplatin、和oxaliplatinum。
“基于铂的化学治疗剂”意指用一种或多种基于铂的化学治疗剂,任选与一种或多种其它化学治疗剂组合的疗法。
“效应器功能”指那些可归于抗体fc区且随抗体同种型而变化的生物学活性。抗体效应器功能的例子包括:c1q结合和补体依赖性细胞毒性(cdc);fc受体结合;抗体依赖性细胞介导的细胞毒性(adcc);吞噬作用;细胞表面受体(例如b细胞受体)下调;和b细胞活化。
“已经确定为表达”或“表达”下述水平的基质标签基因的样品、细胞、肿瘤或癌症是其中对于癌症类型,技术人员认为基质标签基因的表达水平是“高基质标签基因表达水平”的,所述水平超过所述癌症类型(或者在癌症类型中,其中“癌症类型”意图包含癌性细胞(例如肿瘤细胞、肿瘤组织)及围绕癌症/肿瘤环境的非癌症细胞(例如基质细胞、基质组织))中基质标签基因的中值表达水平。一般地,此类水平会在相对于相同癌症类型的样品、细胞、肿瘤或癌症的群体中基质标签基因水平的约50%直至约100%或更多(例如50%、55%、60%、65%、70%、75%、80%、85%、90%、95%、100%、或更多)的范围中。例如,用于达到中值表达水平的群体一般可以是卵巢癌样品,或其分组,诸如化学疗法抗性卵巢癌、铂抗性卵巢癌、及晚期、不应性、或复发性卵巢癌样品。
提及特定生物标志物(例如一种或多种基质标签基因,例如postn)使用的“确定或已经确定癌症表达”或“癌症表达”意指癌症关联生物学环境(例如肿瘤细胞中的生物标志物的表达)、肿瘤关联细胞(例如肿瘤关联基质细胞,诸如肿瘤关联成纤维细胞)中的生物标志物(例如一种或多种基质标签基因,例如postn)表达,如使用诊断测试、本文中描述的任何检测方法或相似方法测定的。例如,可以使用总骨膜蛋白或总postn测定法测定postn的表达。术语“总postn测定法”指测量生物学样品中的总postn水平的测定法。在一个实施方案中,使用抗postn抗体测量总postn水平。在另一个实施方案中,抗postn抗体是本文中描述的抗postn抗体。在另一个例子中,使用一种或多种与编码postn同等型1-4的mrna反义的核酸序列测量总postn水平。在一些实施方案中,总postn测定法包括使用(1)包含序列seqidno:1和seqidno:2(“25d4”抗体)的抗体和/或包含序列seqidno:3和seqidno:4(“23b9”抗体)的抗体以结合生物学样品中的postn,(2)包含seqidno:1和seqidno:2的可变区序列的抗体和/或包含seqidno:3和seqidno:4的可变区序列的抗体以结合生物学样品中的postn,(3)包含seqidno:1和seqidno:2的hvr序列的抗体和/或包含seqidno:3和seqidno:4的hvr序列的抗体以结合生物学样品中的postn,(4)包含与seqidno:1和seqidno:2的hvr序列为95%或更多相同的hvr序列的抗体和/或包含与seqidno:3和seqidno:4的hvr序列为95%或更多相同的hvr序列的抗体。
本文中的术语“fc区”用于定义免疫球蛋白重链中至少含有恒定区一部分的c端区。该术语包括天然序列fc区和变体fc区。在一个实施方案中,人igg重链fc区自cys226,或自pro230延伸至重链的羧基端。然而,fc区的c端赖氨酸(lys447)可以存在或不存在。除非本文中另有规定,fc区或恒定区中的氨基酸残基的编号方式依照eu编号系统,又称作eu索引,如记载于kabatetal.,sequencesofproteinsofimmunologicalinterest,第5版publichealthservice,nationalinstitutesofhealth,bethesda,md,1991。
治疗剂的“固定的”(fixed)或“平坦的”(flat)剂量在本文中指不考虑患者的体重(wt)和体表面积(bsa)而施用于人患者的剂量。因此,固定的或平坦的剂量不是作为mg/kg剂量或mg/m2剂量提供的,而是作为治疗剂的绝对量提供的。
“框架”或“fr”指除高变区(hvr)残基外的可变域残基。一般地,可变域的fr由4个fr域组成:fr1、fr2、fr3、和fr4。因而,hvr和fr序列在vh(或vl)中一般以如下的顺序出现:fr1-h1(l1)-fr2-h2(l2)-fr3-h3(l3)-fr4。
术语“全长抗体”、“完整抗体”、和“全抗体”在本文中可互换使用,指与天然抗体结构具有基本上类似的结构或者具有含有如本文中所限定的fc区的重链的抗体。
“人抗体”指拥有与由人或人细胞生成的或利用人抗体全集或其它人抗体编码序列自非人来源衍生的抗体的氨基酸序列对应的氨基酸序列的抗体。人抗体的此定义明确排除包含非人抗原结合残基的人源化抗体。
“人共有框架”指代表人免疫球蛋白vl或vh框架序列选集中最常存在的氨基酸残基的框架。通常,人免疫球蛋白vl或vh序列选集来自可变域序列亚组。通常,序列亚组是如kabatetal.,sequencesofproteinsofimmunologicalinterest,第五版,nihpublication91-3242,bethesdamd(1991),第1-3卷中的亚组。在一个实施方案中,对于vl,亚组是如kabat等,见上文中的亚组κi。在一个实施方案中,对于vh,亚组是如kabat等,见上文中的亚组iii。
“人源化”抗体指包含来自非人hvr的氨基酸残基和来自人fr的氨基酸残基的嵌合抗体。在某些实施方案中,人源化抗体会包含至少一个,通常两个基本上整个可变域,其中所有或基本上所有hvr(例如,cdr)对应于非人抗体的那些,且所有或基本上所有fr对应于人抗体的那些。任选地,人源化抗体可以至少包含自人抗体衍生的抗体恒定区的一部分。抗体,例如非人抗体的“人源化形式”指已经经历人源化的抗体。
如本文中使用的,术语“高变区”或“hvr”指抗体可变域中在序列上高变的和/或形成结构上限定的环(“高变环”)的每个区。一般地,天然的4链抗体包含6个hvr;三个在vh中(h1、h2、h3),且三个在vl中(l1、l2、l3)。hvr一般包含来自高变环和/或来自“互补决定区”(cdr)的氨基酸残基,后一种通常是最高序列变异性的和/或牵涉抗原识别。如本文中使用的,hvr区包含任何数目位于位置24-36(对于hvrl1)、46-56(对于hvrl2)、89-97(对于hvrl3)、26-35b(对于hvrh1)、47-65(对于hvrh2)、和93-102(对于hvrh3)内的残基。
“免疫缀合物”指与一种或多种异源分子,包括但不限于细胞毒剂缀合的抗体。
术语“免疫调节剂”指诱导、增强或阻抑免疫应答的药剂。设计为引发或放大免疫应答的免疫调节剂是活化免疫调节剂。设计为降低或阻抑免疫应答的免疫调节剂是阻抑免疫调节剂。例如,阻抑免疫调节剂可以是tdo2、cd36、gzmk、cd247、cd1c、csf1r、ido1、il7r、或ccr7拮抗剂。术语“拮抗剂”以最广义使用,并且包括部分或完全阻断、抑制、或中和天然多肽的生物学活性的任何分子。此类药剂(例如拮抗剂)包括多肽(例如抗体,诸如抗csf1r抗体(rg7155)、免疫粘附素或肽体(peptibody))、适体或可以结合蛋白质的小分子或可以结合编码本文中鉴定的靶物的核酸分子的核酸分子(即sirna),其直接或间接靶向免疫系统的细胞(例如t效应细胞、t调节细胞、b细胞、nk细胞、炎性细胞、抗原呈递细胞(例如树突细胞,巨噬细胞)等)。在一些实施方案中,免疫调节剂可以特异性结合免疫系统的细胞上的受体以影响免疫细胞的活性。在其它实施方案中,免疫调节剂靶向信号传导途径中牵涉的基因和/或调控免疫细胞的活性。
“个体”或“受试者”是哺乳动物。哺乳动物包括但不限于驯养的动物(例如,牛、绵羊、猫、犬、和马)、灵长类(例如,人和非人灵长类诸如猴)、家兔、和啮齿类(例如,小鼠和大鼠)。在某些实施方案中,个体或受试者是人。
“分离的”抗体指已经与其天然环境的组分分开的抗体。在一些实施方案中,抗体纯化至大于95%或99%的纯度,如通过例如电泳(例如,sds-page、等电聚焦(ief)、毛细管电泳)或层析(例如,离子交换或反相hplc)测定的。关于用于评估抗体纯度的方法的综述,见例如flatmanetal.,j.chromatogr.b848:79-87(2007)。
“分离的”核酸指已经与其天然环境的组分分开的核酸分子。分离的核酸包括通常含有核酸分子的细胞中含有的核酸分子,但是核酸分子在染色体外或在与其天然染色体位置不同的染色体位置处存在。
“编码抗靶物抗体的分离的核酸”指编码抗体重和轻链(或其片段)的一种或多种核酸分子,包括单一载体或不同载体中的此类核酸分子,和存在于宿主细胞中的一个或多个位置的此类核酸分子。
“加载”(loding)剂量在本文中一般包括施用于患者的治疗剂的初始剂量,后续其一个或多个维持剂量。一般而言,施用单个加载剂量,但本文中也设想了多个加载剂量。通常,所施用的加载剂量的量超过所施用的维持剂量的量,和/或加载剂量的施用比维持剂量更频繁,从而比使用维持剂量更早达到治疗剂的期望稳态浓度。
“维持”(maintenance)剂量或“延长”剂量在本文中指在治疗期间施用于患者的一个或多个剂量的治疗剂。通常,维持剂量以一定的治疗间隔施用,例如大约每周一次,大约每两周一次,大约每三周一次,或大约每四周一次。
如本文中使用的,术语“单克隆抗体”指从一群基本上同质的抗体获得的抗体,即构成群体的各个抗体是相同的和/或结合相同表位,除了例如含有天然存在的突变或在单克隆抗体制备物的生成期间发生的可能的变体抗体外,此类变体一般以极小量存在。与通常包含针对不同决定簇(表位)的不同抗体的多克隆抗体制备物不同,单克隆抗体制备物的每种单克隆抗体针对抗原上的单一决定簇。如此,修饰语“单克隆”指示抗体自一群基本上同质的抗体获得的特性,而不应解释为要求通过任何特定方法来生成抗体。例如,可以通过多种技术来生成要依照本文中提供的方法使用的单克隆抗体,包括但不限于杂交瘤方法、重组dna方法、噬菌体展示方法、和利用含有所有或部分人免疫球蛋白基因座的转基因动物的方法,本文中描述了用于生成单克隆抗体的此类方法和其它例示性方法。
“裸抗体”指未与异源模块(例如细胞毒性模块)或放射性标记物缀合的抗体。裸抗体可以存在于药物配制剂中。
“天然抗体”指具有不同结构的天然存在的免疫球蛋白分子。例如,天然igg抗体是约150,000道尔顿的异四聚糖蛋白,由二硫化物键合的两条相同轻链和两条相同重链构成。从n至c端,每条重链具有一个可变区(vh),又称作可变重域或重链可变域,接着是三个恒定域(chi、ch2、和ch3)。类似地,从n至c端,每条轻链具有一个可变区(vl),又称作可变轻域或轻链可变域,接着是一个恒定轻(cl)域。根据其恒定域氨基酸序列,抗体轻链可归入两种类型中的一种,称作卡帕(κ)和拉姆达(λ)。
依照本发明的短语“患有…的患者”指显示癌症(例如妇科癌症(例如卵巢、腹膜、输卵管、宫颈、子宫内膜、阴道或外阴癌)或乳腺癌(例如转移性mbc;还见下文))的临床体征的患者。短语“易受”或“易于”在癌症的上下文中指基于例如,可能的遗传素因、预先或最终暴露于危险的和/或致癌的化合物,或暴露于致癌性物理危险,诸如辐射,患者中的适应症疾病。
“患者响应”或“响应”(及其语法变型)可利用表明对患者有益处的任何终点来评估,包括但不限于:(1)一定程度地抑制疾病进展,包括减缓和完全阻滞;(2)减少疾病事件和/或症状的数目;(3)缩小损害尺寸;(4)抑制(即减轻、减缓或完全终止)疾病细胞浸润入临近周围器官和/或组织;(5)抑制(即减轻、减缓或完全终止)疾病扩散;(6)降低自身免疫应答,其可以但不必导致疾病损伤的消退或消融;(7)一定程度地减轻与病症有关的一种或多种症状;(8)治疗后无疾病呈现的长度延长;和/或(9)治疗后给定时间点的死亡率降低。
“放射疗法”指使用定向伽马射线或贝塔射线来诱发对细胞的足够损伤,以限制其正常发挥功能的能力或全然破坏细胞。应当领会,本领域知道许多方式来确定治疗的剂量和持续时间。典型的治疗作为一次施用来给予,而典型的剂量范围为每天10-200个单位(戈瑞(gray))。
术语“小分子”指具有50道尔顿至2500道尔顿之间的分子量的有机分子。
术语“基质标签基因”、“基质基因标签”、和“基质标签”指表1-4中列出的基因之一、表1-4中列出的基因的组合、或这些基因的子组合,它们的基因表达模式与癌症化学疗法抗性相关联。基质标签的每种个别的基因是“基质标签基因”。这些基因包括:postn、lox、bgn、fgf1、timp3、fn1、fap、angptl2、acta2、mmp11、rbp4、cd36、plvap、pecam1、gzmk、cd247、abcc9、pcolce、cd1c、ms4a1、cd44、pmepa1、il7r、fbln1、twist1、id1、rac2、gfra1、ccr7、man1a1、evi2a、ptprccd45ra、fcrl5、nnmt、cd27、sla、esr2、klk7、klk6、muc1、dtx4、fgfr4、tspan8、esr1、krt18、fut2、hoxd10、exo1、inadl、igfbp2、mycn、erbb3、tmem45b、prom1、ncam1、mki67、cdh3、ly6e、tjp3、slc7a11、bnip3、prame、esm1、vtcn1、ccl28、tdo2、nuak1、col4a1、abcb9、rb1、anxa1、foxo1、pgr、和alpp。
“基质靶向剂”意指直接或间接靶向肿瘤基质的组分(例如成纤维细胞、内皮细胞、周细胞、白细胞、胞外基质等)的药剂。基质靶向剂可以通过例如结合或以其它方式影响靶基因或其编码的蛋白质的活性来直接或间接影响本文中列出的基质标签基因的基因之任一种的活性。基质靶向剂也可以在不影响如本文中列出的基质标签的基因之任一种(或相应的多肽)的活性的情况中以不同方式靶向肿瘤基质。此类药剂可以包括例如小分子、适体、多肽(其包括例如免疫粘附素、抗体、多肽和肽)、和rna治疗剂(其包括例如小干扰rna(sirna)、微小rna(mirna)、反义寡核苷酸、和空间阻断寡核苷酸)。
“存活”指患者保持活着,并且包括总体存活及无进展存活。
“总体存活”指患者自诊断或治疗时间起保持限定时期活着,诸如1年、5年、等等。
短语“无进展存活”在本发明的上下文中指治疗期间和治疗后,依照治疗内科医生或调查人员的评估,患者的疾病不变坏,即不进展的时间长度。如技术人员会领会的,若与类似情况的患者的对照组的平均或均值无进展存活时间相比,患者经历更长的疾病不进展的时间长度,则患者的无进展存活得到改善或增强。
“延长存活”意指相对于未治疗的患者(即相对于未用基质靶向剂(例如抗postn抗体)、免疫调节剂、抗血管发生剂(例如vegf拮抗剂,例如抗vegf抗体,诸如贝伐单抗)治疗的患者),或相对于不以指定水平表达基质标签基因的患者,和/或相对于化学疗法敏感性的用化学治疗剂(例如本文中描述的任何化学治疗剂)治疗的患者,延长经治疗的患者中的总体或无进展存活。
“护理标准”在本文中意指常规用于治疗癌症的特定形式的一种或多种抗肿瘤剂。例如,对于铂抗性卵巢癌,护理标准是卡铂和帕利他赛的组合。
术语“治疗有效量”或“有效量”指在患者中有效治疗癌症的药物量。有效量的药物可减少癌细胞的数目;缩小肿瘤的尺寸;抑制(即一定程度的减缓和优选阻止)癌细胞浸润到周围器官中;抑制(即一定程度的减缓和优选阻止)肿瘤转移;一定程度的抑制肿瘤生长;和/或一定程度的减轻一种或多种与癌症有关的症状。根据药物可阻止现有癌细胞生长和/或杀死现有癌细胞的程度,它可以是抑制细胞的和/或毒害细胞的(细胞毒性的)。有效量可延长无进展存活(例如根据实体瘤的响应评估标准(responseevaluationcriteriaforsolidtumors,recist)或ca-125变化的测量),导致客观响应(包括部分响应,pr或完全响应,cr),改善存活(包括总体存活和无进展存活),和/或改善癌症的一种或多种症状(例如根据fosi的评估)。最优选地,所述药物的治疗有效量有效改善无进展存活(pfs)和/或总体存活(os)。
如本文中使用的,术语“总骨膜蛋白(postn)”至少指骨膜蛋白的同等型1、2、3和4。依照ncbi数据库(分别为us2012/0156194的seqidno:19-22,其通过提及结合这些序列和seqidno:23收入本文),人postn同等型1、2、3和4在本领域中已知分别包含以下氨基酸序列:np006466.2;np001129406.1、np001129407.1、和np001129408.1。us2012/0156194中描述了postn的别的形式。此同等型在本文中称为“同等型5”,并且已经部分得到测序。同等型5包含us2012/0156194的seqidno:23的氨基酸序列。在一个实施方案中,postn的同等型是人postn。在进一步的实施方案中,在同等型1-4外,术语总postn包括人postn的同等型5。在另一个实施方案中,总postn是总血清postn或总血浆postn(即分别来自获自全血的血清样品或获自全血的血浆样品的总postn,自患者获得全血)。
术语“骨膜蛋白(postn)抗体”或“抗postn抗体”指结合postn同等型的抗体。在一个实施方案中,postn是人postn。在一个实施方案中,抗体包含序列seqidno:l和seqidno:2(“25d4”抗体)或包含序列seqidno:3和seqidno:4(“23b9”抗体)。在另一个实施方案中,抗体包含seqidno:1和seqidno:2的可变区序列或包含seqidno:3和seqidno:4的可变区序列。在另一个实施方案中,抗体包含seqidno:1和seqidno:2的hvr序列或seqidno:3和seqidno:4的hvr序列。在另一个实施方案中,抗体包含与seqidno:1和seqidno:2的hvr序列为95%或更多相同的hvr序列和/或抗体包含与seqidno:3和seqidno:4的hvr序列为95%或更多相同的hvr序列。
如本文中使用的,“治疗/处理”指试图改变所治疗个体或细胞的自然进程的临床干预,并且可以是为了预防或在临床病理学的进程中进行。治疗的期望效果包括预防疾病的发生或复发、缓解症状、削弱疾病的任何直接或间接病理学后果、减缓疾病进展的速率、改善或减轻疾病状态、及免除或改善预后。在一些实施方案中,本发明的方法和组合物可用于试图延迟疾病或病症的发展。
术语“可变区”或“可变域”指抗体重或轻链中牵涉抗体结合抗原的域。天然抗体的重链和轻链可变域(分别为vh和vl)一般具有类似的结构,其中每个域包含4个保守的框架区(fr)和3个高变区(hvr)。(见例如kindtetal.kubyimmunology,第6版,w.h.freemanandco.,第91页(2007))。单个vh或vl域可以足以赋予抗原结合特异性。此外,可以分别使用来自结合抗原的抗体的vh或vl域筛选互补vl或vh域的文库来分离结合特定抗原的抗体。见例如,portolanoetal.,j.immunol.150:880-887(1993);clarksonetal.,nature352:624-628(1991)。
“vegf拮抗剂”或“vegf特异性拮抗剂”指能够结合vegf,降低vegf表达水平,或者中和、阻断、抑制、消除、降低或干扰vegf生物学活性(包括但不限于vegf与一种或多种vegf受体的结合、vegf信号传导及由vegf介导的血管发生和内皮细胞存活或增殖)的分子。例如,能够中和、阻断、抑制、消除、降低或干扰vegf生物学活性的分子可以通过结合一种或多种vegf受体(vegfr)(例如vegfr1、vegfr2、vegfr3、膜结合vegf受体(mbvegfr)、或可溶性vegf受体(svegfr))施加其效应。在本发明的方法中有用的vegf特异性拮抗剂包括特异性结合vegf的多肽、抗vegf抗体及其抗原结合片段、特异性结合vegf由此使其隔绝与一种或多种受体结合的受体分子和衍生物、融合蛋白(例如vegf-trap(regeneron))、和vegf121-白树毒素(peregrine)。vegf特异性拮抗剂还包括vegf多肽的拮抗剂变体、至少与编码vegf多肽的核酸分子的片段互补的反义核碱基寡聚物;至少与编码vegf多肽的核酸分子的片段互补的小rna;靶向vegf的核酶;针对vegf的肽体;和vegf适体。vegf拮抗剂还包括结合vegfr的多肽、抗vegfr抗体、及其抗原结合片段,和结合vegfr,从而阻断、抑制、消除、降低或干扰vegf生物学活性(例如vegf信号传导)的衍生物、或融合蛋白。vegf特异性拮抗剂还包括结合vegf或vegfr且能够阻断、抑制、消除、降低、或干扰vegf生物学活性的非肽小分子。如此,术语“vegf活性”明确包括vegf介导的vegf生物学活性。在某些实施方案中,vegf拮抗剂将vegf的表达水平或生物学活性降低或抑制了至少10%、20%、30%、40%、50%、60%、70%、80%、90%或更多。在一些实施方案中,由vegf特异性拮抗剂抑制的vegf是vegf(8-109)、vegf(1-109)、或vegf165。
如本文中使用的,vegf拮抗剂可以包括但不限于抗vegfr2抗体及相关分子(例如雷莫芦单抗(ramucirumab)、tanibirumab、阿柏西普(aflibercept))、抗vegfr1抗体及相关分子(例如icrucumab、阿柏西普(vegftrap-eye;
“抗vegf抗体”是以足够的亲和力和特异性结合vegf的抗体。在某些实施方案中,抗体会对vegf具有足够高的结合亲和力,例如抗体可以以100nm-1pm的kd值结合hvegf。可以例如通过基于表面等离振子共振的测定法(诸如如pct申请公开no.wo2005/012359中描述的biacore测定法);酶联免疫吸附测定法(elisa);和竞争测定法(例如ria)测定抗体亲和力。
在某些实施方案中,可以在靶向和干扰牵涉vegf活性的疾病或状况中使用抗vegf抗体作为治疗剂。还有,抗体可以进行其它生物学活性测定法,例如以评估其作为治疗剂的有效性。此类测定法是本领域中已知的,并且取决于靶抗原和抗体的意图使用。例子包括huvec抑制测定法;肿瘤细胞生长抑制测定法(如例如记载于wo89/06692);抗体依赖性细胞性细胞毒性(adcc)和补体介导的细胞毒性(cdc)测定法(美国专利no.5,500,362);和激动活性或造血测定法(见wo95/27062)。抗vegf抗体通常不会结合其它vegf同源物,诸如vegf-b或vegf-c,也不结合其它生长因子诸如plgf、pdgf、或bfgf。在一个实施方案中,抗vegf抗体是与由杂交瘤atcchb10709生成的单克隆抗vegf抗体a4.6.1结合相同表位的单克隆抗体。在另一个实施方案中,抗vegf抗体是依照prestaetal.(1997)cancerres.57:4593-4599生成的重组人源化抗vegf单克隆抗体,包括但不限于称为贝伐单抗(bv;
抗vegf抗体“贝伐单抗(bv)”,又称为“rhumabvegf”或
iii.预后、诊断和检测的方法
本发明涉及鉴定、选择和使用与对化学治疗剂(例如基于铂的化学治疗剂,例如顺铂、卡铂、奥沙利铂、沙铂、吡铂、dedaplatin、triplatin、lipoplatin、等等)的抗性有关的癌症(例如妇科癌症(例如卵巢、腹膜、输卵管、宫颈、子宫内膜、阴道或外阴癌))的生物标志物。在此方面,本发明涉及使用已经确定为具有化学疗法抗性癌症或化学疗法敏感性癌症的癌症(例如妇科癌症(例如卵巢、腹膜、输卵管、宫颈、子宫内膜、阴道或外阴癌))患者中的肿瘤基质组分(例如肿瘤关联成纤维细胞)表达序型,来鉴定与对化学疗法药剂(例如基于铂的化学治疗剂,诸如顺铂、卡铂、奥沙利铂、沙铂、吡铂、dedaplatin、triplatin、lipoplatin,等等)的抗性有关的生物标志物。在本文中(例如在表1-4中)列出了本发明的生物标志物。
本发明提供了用于鉴定具有化学疗法抗性癌症(例如妇科癌症(例如卵巢、腹膜、输卵管、宫颈、子宫内膜、阴道或外阴癌))的患者的方法,其通过测定一种或多种基质标签基因(例如表1-4中列出的一种或多种基因和/或其组合)的表达水平,并且将基质标签基因的表达水平与癌症类型中的基质标签基因的中值表达水平比较。在一些实施方案中,若基质标签基因(例如表1和3中的任何基因和/或其组合)的表达在比癌症类型中的基质标签基因的中值表达水平多的水平,则确定患者具有化学疗法抗性癌症。在其它实施方案中,若基质标签基因(例如表2和4中的任何基因和/或其组合)的表达在比癌症类型中的基质标签基因的中值表达水平小的水平,则确定患者具有化学疗法抗性癌症。本发明还提供了用于鉴定具有化学疗法敏感性癌症(例如妇科癌症(例如卵巢、腹膜、输卵管、宫颈、子宫内膜、阴道或外阴癌))的患者的方法,其通过测定基质标签基因(例如表1-4中列出的一种或多种基因和/或其组合)的表达水平,并且将基质标签基因的表达水平与癌症类型中的基质标签基因的中值表达水平比较。在一些实施方案中,若基质标签基因(例如表1和3中的任何基因和/或其组合)的表达在比癌症类型中的基质标签基因的中值表达水平小的水平,则确定患者具有化学疗法敏感性癌症。在其它实施方案中,若基质标签基因(例如表2和4中的任何基因和/或其组合)的表达在比癌症类型中的基质标签基因的中值表达水平多的水平,则确定患者具有化学疗法敏感性癌症。任选地,在施用化学治疗剂前实施这些方法以提供具有化学疗法抗性的施用前诊断的患者。
本发明还提供了关于受益于用特定化学治疗剂(例如卡铂、顺铂、奥沙利铂、或本文中描述的任何药剂,见上文)的化学疗法的可能性和/或受益于在化学疗法外或替换所述化学疗法的备选抗癌疗法(例如施用抗血管发生剂、免疫调节剂、和/或基质靶向剂(例如抗postn抗体))的可能性的预后方法。这些方法牵涉测定基质标签基因(例如表1-4中列出的一种或多种基因和/或其组合)的表达水平,并且将基质标签基因的表达水平与癌症类型中的基质标签基因的中值表达水平比较。在一些实施方案中,若基质标签基因(例如表1和3中的任何基因和/或其组合)的表达在比癌症类型中的基质标签基因的中值表达水平多的水平,则确定患者可能受益于在化学疗法外或替换所述化学疗法的抗癌疗法(例如抗血管发生疗法、免疫疗法、基质靶向疗法、等等)的施用。在其它实施方案中,若基质标签基因(例如表2和4中的任何基因和/或其组合)的表达在比癌症类型中的基质标签基因的中值表达水平小的水平,则确定患者可能受益于在化学疗法外或替换所述化学疗法的抗癌疗法(例如抗血管发生疗法、免疫疗法、基质靶向疗法、等等)的施用。任选地,这些方法包括与化学疗法方案组合或作为单一疗法对患者施用抗癌疗法(例如施用抗血管发生剂(例如vegf拮抗剂,诸如抗vegf抗体,例如贝伐单抗)、免疫调节剂、和/或基质靶向剂(例如抗postn抗体))。
表1:铂抗性对铂敏感性原发性卵巢肿瘤中差异表达的上调基因
表2:铂抗性对铂敏感性原发性卵巢肿瘤中差异表达的下调基因
表3:铂抗性复发性卵巢肿瘤对铂抗性原发性卵巢肿瘤中差异表达的上调基因
表4:铂抗性复发性卵巢肿瘤对铂抗性原发性卵巢肿瘤中差异表达的下调基因
*在2015年7月29日自于store.nanostring.com/search的nanostringtechnologies网页检索基因idno。
本发明还提供了测定患者中的癌症阶段的方法。在这些方法中,评估了如本文中描述的一种或多种基质标签基因的表达水平,并且基因的表达增加指示较晚期的癌症阶段。在一个例子中,在样品(例如血液样品,诸如血清样品)中评估例如postn的水平,并且基因(例如postn)的升高的表达水平的检出指示较晚期(例如figoiii期(例如iiia、iiib、或iiic期)或iv期)eoc阶段。一般地,将样品中的标签基因的表达水平与例如具有癌症类型的患者群体中基因的中值表达水平比较,或者可以与确定为与癌症类型的特定阶段(例如早期阶段,诸如figoi期或figoii期eoc)有关的水平比较。
可以通过本领域中已知的适合于测定患者样品中的特定蛋白质水平的任何方法评估基质标签基因的表达水平,并且优选地通过采用对基质标签基因特异性的抗体的免疫组织化学(“ihc”)方法测定。此类方法是本领域中公知且常规实施的,并且相应的商业抗体和/或试剂盒是容易可用的。优选地,使用抗体或试剂盒制造商的试剂和/或方案推荐评估本发明的标志物/指示剂蛋白的表达水平。熟练技术人员还会意识到通过ihc方法测定基质标签基因的表达水平的进一步手段。因此,可以由本领域技术人员在无需过度负担的情况中常规地且可重复地测定本发明的一种或多种标志物/指示剂的表达水平。然而,为了确保准确和可重现的结果,本发明还涵盖在可以确保测试规程的验证的专门实验室中测试患者样品。
优选地,在含有或怀疑含有癌细胞的生物学样品中评估基质标签基因的表达水平。样品可以是例如卵巢组织切除、卵巢组织活组织检查或自患有、疑似患有或诊断患有癌症(例如,妇科癌症,特别是卵巢癌)的患者获得的转移性损伤。优选地,样品是卵巢组织的样品、卵巢肿瘤的切除或活组织检查、已知或疑似的转移性卵巢癌损伤或切片、或者已知或怀疑包含循环癌细胞,例如卵巢癌细胞的血液样品,例如外周血样品。样品可以包含癌细胞(即肿瘤细胞)和非癌性细胞两者,并且在某些实施方案中,包含癌性和非癌细胞两者(例如优选地,样品含有基质细胞)。在包括测定基质组分中的基因表达的本发明的方面,样品包含癌/肿瘤细胞和例如与癌/肿瘤细胞相关的非癌性细胞(例如肿瘤关联成纤维细胞、内皮细胞、周细胞、胞外基质和/或各种类型的白细胞)两者。在其它方面,熟练技术人员(例如病理学家)可以容易地辨别癌细胞与非癌性(例如基质细胞,内皮细胞等)。获得生物学样品,包括组织切除、活组织检查和体液,例如包含癌/肿瘤细胞的血液样品的方法在本领域中是公知的。在一些实施方案中,在开始任何化学治疗或其它治疗方案或治疗,例如用于治疗癌症或管理或改善其症状的疗法前收集自患者获得的样品。因此,在一些实施方案中,在施用化学治疗剂或其它药剂,或开始化学疗法或其它治疗方案前收集样品。
在上文描述的方法外,本发明还涵盖用于评估一种或多种基质标签基因的表达水平的进一步的免疫组织化学方法,例如通过western印迹法和基于elisa的检测进行。如本领域中理解的,也可以通过本领域中已知的任何合适的方法,诸如northern印迹法、实时pcr、和rtpcr在mrna水平评估本发明的标志物/指示剂蛋白的表达水平。基于免疫组织化学的和基于mrna的检测方法和系统在本领域中是公知的,并且可以从诸如lottspeich(bioanalytik,spektrumakademisherverlag,1998)或sambrookandrussell(molecularcloning:alaboratorymanual,cshpress,coldspringharbor,n.y.,u.s.a.,2001)等标准教科书导出。在优选的实施方案中,使用rna原位杂交(rnaish)(例如见下文)实施用于检测基质标签基因的mrna水平的方法。描述的方法特别用于相对于在诊断为癌症(例如,妇科癌症,诸如卵巢癌)晚期阶段的群体中建立的对照水平测定患者或患者组中基质标签基因的表达水平。
为了在本文中描述的检测方法中使用,技术人员具有标记由本发明涵盖的多肽或寡核苷酸的能力。如本领域中常规实施的,可以依照本领域中已知的标准方法标记和显现用于检测用于ihc方法的mrna水平和/或抗体或抗体片段的杂交探针。通常使用的系统的非限制性例子包括使用放射性标记物、酶标记物、荧光标签、生物素-亲合素复合物、化学发光等。
也可以通过利用免疫凝集、免疫沉淀(例如免疫扩散、免疫电泳、免疫固定)、western印迹法技术(例如原位免疫组织化学、原位免疫细胞化学、亲和层析、酶免疫测定法)等在蛋白质水平上测定一种或多种基质标签基因的表达水平。也可以通过物理方法,例如光度测定法测定纯化的多肽的量。量化混合物中的特定多肽的方法通常依赖于例如抗体的特异性结合。
如上文提及的,也可以在编码基质标签基因的相应基因的增加或减少的表达中反映依照本发明的标志物/指示剂蛋白的表达水平。因此,可以实施翻译前的基因产物(例如剪接、未剪接或部分剪接的mrna)的定量评估,以评估相应基因的表达。本领域技术人员知道要在此情况中使用的标准方法或者可以从标准教科书(例如sambrook,2001)推导出这些方法。例如,可以通过northern印迹、实时pcr等获得编码本文中描述的一种或多种基质标签基因的mrna的相应浓度/量的定量数据。
iv.治疗方法
本发明提供了治疗癌症(例如化学疗法抗性癌症、化学疗法敏感性癌症、原发性癌症、晚期癌症、不应性癌症和/或复发性癌症)患者的方法。方法包括若已经确定患者的癌症以比癌症类型中的基质标签基因的中值表达水平多的水平表达基质标签基因(例如表1和3中描述的一种或多种基因)或确定为以比癌症类型中的基质标签基因的中值表达水平小的水平表达基质标签基因(例如表2和4中描述的一种或多种基因),则对患者施用治疗有效量的基质靶向剂(例如抗postn抗体)。在一些实施方案中,可以以单一疗法施用基质靶向剂。在其它实施方案中,可以与化学疗法方案、放射治疗和/或免疫疗法组合施用基质靶向剂。
在具体实施方案中,基质靶向剂是结合骨膜蛋白(postn)的药剂。在某些实施方案中,结合postn的药剂是分离的抗体(即抗骨膜蛋白(postn)抗体(抗postn抗体))。在具体实施方案中,抗postn抗体可以以良好的亲和力结合人postn的同等型1-4。
在一个实施方案中,抗体包含序列seqidno:1和seqidno:2(“25d4”抗体)或包含seqidno:3和seqidno:4的序列(“23b9”抗体)。在另一个实施方案中,抗体包含seqidno:1和seqidno:2的可变区序列或包含seqidno:3和seqidno:4的可变区序列。在另一个实施方案中,抗体包含seqidno:1和seqidno:2的hvr序列或seqidno:3和seqidno:4的hvr序列。在另一个实施方案中,抗体包含与seqidno:1和seqidno:2的hvr序列为95%或更多相同的hvr序列和/或抗体包含与seqidno:3和seqidno:4的hvr序列为95%或更多相同的hvr序列。
在任何上述实施方案中,抗postn抗体可以是人源化的。在一个实施方案中,抗postn抗体包含如上述任何实施方案的hvr,并且还包含受体人框架,例如人免疫球蛋白框架或人共有框架。
在另一方面,抗postn抗体包含与seqidno:1的氨基酸序列具有至少90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或100%序列同一性的重链可变域(vh)序列。在某些实施方案中,具有至少90%、91%、92%、93%、94%、95%、96%、97%、98%、或99%同一性的vh序列含有相对于参照序列的替代(例如保守替代)、插入或删除,但包含所述序列的抗postn抗体保留结合骨膜蛋白的能力。在某些实施方案中,已经在seqidno:1中替代、插入和/或删除总共1至10个氨基酸。在某些实施方案中,在hvr外部的区域中(即在fr中)发生替代、插入或删除。任选地,抗postn抗体包含seqidno:1中的vh序列,包括所述序列的翻译后修饰。
在另一方面,提供了抗postn抗体,其中抗体包含与seqidno:2的氨基酸序列具有至少90%>、91%>、92%、93%>、94%>、95%、96%、97%、98%、99%或100%序列同一性的轻链可变域(vl)。在某些实施方案中,具有至少90%>、91%>、92%、93%>、94%、95%、96%、97%、98%、或99%同一性的vl序列含有相对于参照序列的替代(例如保守替代)、插入或删除,但包含所述序列的抗postn抗体保留结合骨膜蛋白的能力。在某些实施方案中,已经在seqidno:2中替代、插入和/或删除总共1至10个氨基酸。在某些实施方案中,在hvr外部的区域中(即在fr中)发生替代、插入或删除。任选地,抗postn抗体包含seqidno:2中的vl序列,包括所述序列的翻译后修饰。
在另一方面,抗postn抗体包含与seqidno:3的氨基酸序列具有至少90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或100%序列同一性的重链可变域(vh)序列。在某些实施方案中,具有至少90%、91%、92%、93%、94%、95%、96%、97%、98%、或99%同一性的vh序列含有相对于参照序列的替代(例如保守替代)、插入或删除,但包含所述序列的抗postn抗体保留结合骨膜蛋白的能力。在某些实施方案中,已经在seqidno:3中替代、插入和/或删除总共1至10个氨基酸。在某些实施方案中,在hvr外部的区域中(即在fr中)发生替代、插入或删除。任选地,抗postn抗体包含seqidno:3中的vh序列,包括所述序列的翻译后修饰。
在另一方面,提供了抗postn抗体,其中抗体包含与seqidno:2的氨基酸序列具有至少90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或100%序列同一性的轻链可变域(vl)。在某些实施方案中,具有至少90%>、91%>、92%、93%>、94%、95%、96%、97%、98%、或99%同一性的vl序列含有相对于参照序列的替代(例如保守替代)、插入或删除,但包含所述序列的抗postn抗体保留结合骨膜蛋白的能力。在某些实施方案中,已经在seqidno:4中替代、插入和/或删除总共1至10个氨基酸。在某些实施方案中,在hvr外部的区域中(即在fr中)发生替代、插入或删除。任选地,抗postn抗体包含seqidno:4中的vl序列,包括所述序列的翻译后修饰。
在另一方面,提供了抗postn抗体,其中抗体包含如上文提供的任何实施方案中的vh,以及如上文提供的任何实施方案中的vl。
在别的方面,本发明采用与本文中提供的抗postn抗体结合相同表位的抗体。例如,在某些实施方案中,提供了与包含seqidno:1的vh序列和seqidno:2的vl序列的抗postn抗体结合相同表位的抗体。例如,在某些实施方案中,提供了与包含seqidno:3的vh序列和seqidno:4的vl序列的抗骨膜蛋白抗体结合相同表位的抗体。
在本发明的另一方面,依照上述任何实施方案的抗postn抗体是单克隆抗体,包括嵌合的、人源化的或人的抗体。在一个实施方案中,抗postn抗体是抗体片段,例如fv、fab、fab’、scfv、双抗体或f(ab’)2片段。在另一个实施方案中,抗体是全长抗体,例如完整的igg1或igg4抗体或如本文中定义的其它抗体类别或同种型。在另一个实施方案中,抗体是双特异性抗体。
本发明还提供了鉴定可能受益于抗血管生成剂(例如vegf拮抗剂,诸如抗vegf抗体,例如贝伐单抗)或免疫调节剂施用的患有癌症的患者的方法,其通过测定基质标签基因(例如表1-4中的任何基因或其组合)的表达水平进行,其中若基质标签基因(例如,表1和表3中的任何基因和/或其组合)的表达处于比癌症类型中基质标签基因的中值表达水平多的水平,则对患者施用抗血管生成剂或免疫调节剂。在其它实施方案中,若基质标签基因(例如,表2和表4中的任何基因和/或其组合)的表达处于比癌症类型中基质标签基因的中值表达水平小的水平,则对患者施用抗血管生成剂或免疫调节剂。可以与免疫调节剂、化学疗法方案或基质靶向剂(例如抗postn抗体)组合施用抗血管生成剂(例如,vegf拮抗剂,诸如抗vegf抗体,例如贝伐单抗)。
因此,本发明提供了用于治疗具有化学疗法抗性、化学疗法敏感性、不应性、原发性、晚期或复发性癌症(例如妇科癌症()例如卵巢、腹膜、输卵管、宫颈、子宫内膜、阴道或外阴癌))的患者的方法,其牵涉对患者施用治疗有效量的抗血管生成剂(例如vegf拮抗剂(例如抗vegf抗体,诸如贝伐单抗)),任选地,这些方法牵涉共施用vegf拮抗剂与一种或多种别的化学治疗剂(例如卡铂和/或帕利他赛),如下文进一步描述的。
优选地,用基质靶向剂、免疫调节剂和/或抗血管生成剂(例如,vegf拮抗剂(例如抗vegf抗体,诸如贝伐单抗)),任选地与一种或多种化学治疗剂(例如卡铂和/或帕利他赛)组合的疗法延长和/或改善存活,包括无进展生存(pfs)和/或总体存活(os)。在一个实施方案中,用基质靶向剂、免疫调节剂和/或抗血管生成剂(例如vegf拮抗剂(例如抗vegf抗体,诸如贝伐单抗))的疗法将存活延长为比通过施用对于治疗的癌症而言经批准的抗肿瘤剂或护理标准实现的存活多至少约20%。在优选的实施方案中,患者具有妇科癌症(例如卵巢、腹膜、输卵管、宫颈、子宫内膜、阴道或外阴癌)。
为了预防或治疗癌症,基质靶向剂、免疫调节剂和/或抗血管生成剂(例如,vegf拮抗剂(例如抗vegf抗体,诸如贝伐单抗))和/或化学治疗剂的剂量会取决于如上文定义的要治疗的癌症的类型、癌症的严重性和过程、抗体是否用于预防或治疗目的施用、先前疗法、患者的临床史和对药物的响应、和主治内科医生的判断。
在一个实施方案中,施用固定剂量的基质靶向剂、免疫调节剂和/或抗血管生成剂(例如,vegf拮抗剂(例如抗vegf抗体,诸如贝伐单抗))。可以一次或在一系列治疗里对患者适当施用固定剂量。在施用固定剂量的情况中,优选地,它在约20mg至约2000mg的范围中。例如,固定剂量可以是约420mg、约525mg、约840mg或约1050mg的药剂(例如基质靶向剂、免疫调节剂和/或抗血管生成剂(例如vegf拮抗剂(例如抗vegf抗体,诸如贝伐单抗))。在施用一系列剂量的情况中,这些可以例如约每周、约每2周、约每3周、或约每4周,但是优选地约每3周施用。固定剂量可以例如继续施用直到疾病进展、不利事件或如由内科医生确定的其它时间。例如,可以施用约2、3、或4、直至约17或更多个固定剂量。
在一个实施方案中,施用一种或多种加载剂量的基质靶向剂、免疫调节剂和/或抗血管生成剂(例如,vegf拮抗剂(例如抗vegf抗体,诸如贝伐单抗)),然后是一个或多个维持剂量。在另一个实施方案中,对患者施用多个相同的剂量。
虽然可以以单一抗肿瘤剂施用基质靶向剂、免疫调节剂、和/或抗血管生成剂(例如vegf拮抗剂(例如抗vegf抗体,诸如贝伐单抗)),但是任选地用基质靶向剂、免疫调节剂、和/或抗血管生成剂(例如vegf拮抗剂(例如抗vegf抗体,诸如贝伐单抗))和一种或多种(别的)化学治疗剂的组合治疗患者。本文中的例示性化学治疗剂包括:吉西他滨、卡铂、奥沙利铂、伊立替康、氟嘧啶(例如5-fu)、帕利他赛(例如nab-帕利他赛)、多西他赛、托泊替康、卡培他滨、替莫唑胺、干扰素-α、和/或脂质体多柔比星(例如peg化的脂质体多柔比星)。在一些实施方案中,至少一种化学治疗剂是卡铂或帕利他赛。组合施用包括使用分开的配制剂或单一药物配制剂的共施用或同时施用,和任意次序的连续施用,其中优选地,存在有这两种(或所有)活性剂同时发挥其生物活性的时间段。如此,可以在施用基质靶向剂、免疫调节剂、和/或抗血管生成剂(例如vegf拮抗剂(例如抗vegf抗体,诸如贝伐单抗))之前或之后施用化学治疗剂。在此实施方案中,在化学治疗剂的至少一次施用和基质靶向剂、免疫调节剂、和/或抗血管生成剂(例如vegf拮抗剂(例如抗vegf抗体,诸如贝伐单抗))的至少一次施用之间的时机优选是约1个月或更少(3周、2周、1周、6天、5天、4天、3天、2天、1天)。或者,在单一配制剂或分开的配制剂中对患者同时施用化学治疗剂和基质靶向剂、免疫调节剂、和/或抗血管生成剂(例如vegf拮抗剂(例如抗vegf抗体,诸如贝伐单抗))。用化学治疗剂(例如卡铂和/或帕利他赛)和基质靶向剂(例如抗postn抗体)、免疫调节剂、和/或抗血管生成剂(例如vegf拮抗剂(例如抗vegf抗体,诸如贝伐单抗))的组合的治疗可以导致对患者的协同、或大于叠加的治疗益处。
用于与基质靶向剂(例如抗postn抗体)、免疫调节剂、和/或抗血管生成剂(例如vegf拮抗剂(例如抗vegf抗体,诸如贝伐单抗))组合(例如用于卵巢癌疗法)的特别期望的化学治疗剂包括:化学治疗剂诸如铂化合物(例如卡铂)、泰素诸如帕利他赛或多西他赛、托泊替康、或脂质体多柔比星。
用于与基质靶向剂(例如抗postn抗体)、免疫调节剂、和/或抗血管生成剂(例如vegf拮抗剂(例如抗vegf抗体,诸如贝伐单抗))组合(例如用于晚期阶段上皮卵巢癌、输卵管癌、或原发性腹膜癌疗法)的特别期望的化学治疗剂包括:化学治疗剂诸如卡铂和帕利他赛。
用于与基质靶向剂(例如抗postn抗体)、免疫调节剂、和/或抗血管生成剂(例如vegf拮抗剂(例如抗vegf抗体,诸如贝伐单抗))组合(例如用于铂敏感性上皮卵巢癌、输卵管癌、或原发性腹膜癌疗法)的特别期望的化学治疗剂包括:化学治疗剂诸如卡铂和吉西他滨。
用于与基质靶向剂(例如抗postn抗体)、免疫调节剂、和/或抗血管生成剂(例如vegf拮抗剂(例如抗vegf抗体,诸如贝伐单抗))组合(例如用于铂抗性复发性上皮卵巢癌、输卵管癌、或原发性腹膜癌疗法)的特别期望的化学治疗剂包括:化学治疗剂诸如帕利他赛、托泊替康、或peg化的脂质体多柔比星。
用于与基质靶向剂(例如抗postn抗体)、免疫调节剂、和/或抗血管生成剂(例如vegf拮抗剂(例如抗vegf抗体,诸如贝伐单抗))组合(例如用于乳腺癌疗法)的特别期望的化学治疗剂包括:化学治疗剂诸如卡培他滨、和泰素诸如帕利他赛(例如nab-帕利他赛)或多西他赛。
用于与基质靶向剂(例如抗postn抗体)、免疫调节剂、和/或抗血管生成剂(例如vegf拮抗剂(例如抗vegf抗体,诸如贝伐单抗))组合(例如用于成胶质细胞瘤疗法)的特别期望的化学治疗剂包括:化学治疗剂诸如替莫唑胺,任选地与放射疗法组合。
用于与基质靶向剂(例如抗postn抗体)、免疫调节剂、和/或抗血管生成剂(例如vegf拮抗剂(例如抗vegf抗体,诸如贝伐单抗))组合(例如用于结肠直肠癌疗法)的特别期望的化学治疗剂包括:化学治疗剂诸如氟嘧啶(例如5-fu)、帕利他赛、顺铂、托泊替康、伊立替康、氟嘧啶-奥沙利铂、氟嘧啶-伊立替康、folfox4(5-fu、甲酰四氢叶酸、奥沙利铂)、和ifl(伊立替康、5-fu、甲酰四氢叶酸)。
用于与基质靶向剂(例如抗postn抗体)、免疫调节剂、和/或抗血管生成剂(例如vegf拮抗剂(例如抗vegf抗体,诸如贝伐单抗))组合(例如用于肾细胞癌疗法)的特别期望的化学治疗剂包括:化学治疗剂诸如干扰素-α2a。
用于与基质靶向剂(例如抗postn抗体)、免疫调节剂、和/或抗血管生成剂(例如vegf拮抗剂(例如抗vegf抗体,诸如贝伐单抗))组合(例如用于宫颈癌疗法)的特别期望的化学治疗剂包括:化学治疗剂诸如帕利他赛、顺铂、托泊替康、与顺铂组合的帕利他赛、和与托泊替康组合的帕利他赛。
因此,化学治疗剂(若施用的话)通常以已知的剂量施用,或任选地由于药物的组合作用或可归因于化学治疗剂施用的负面副作用而降低。可以依照制造商的用法说明或者如由熟练从业人员凭经验确定的那样使用用于此类化学治疗剂的制备和给药日程表。在化学治疗剂是帕利他赛的情况中,优选地,以约130mg/m2至200mg/m2之间的剂量(例如约175mg/m2)例如在3小时里每3周一次施用它。在化学治疗剂是卡铂的情况中,优选地,通过使用calvert公式计算卡铂的剂量施用它,所述calvert公式基于患者先前存在的肾功能或肾功能和期望的血小板最低值。肾排泄是用于卡铂的主要消除路径。如与基于体表面积的经验剂量计算相比此给药公式的使用允许补偿治疗前肾功能的患者变化,其在其它情况中可以导致给药不足(在具有高于平均值的肾功能的患者中)或过度给药(在具有受损的肾功能的患者中)。使用单一药剂卡铂的4-6mg/ml/min靶标auc似乎在先前经治疗的患者中提供最合适的剂量范围。
除了基质靶向剂(例如抗postn抗体)、免疫调节剂、和/或抗血管生成剂(例如vegf拮抗剂(例如抗vegf抗体,诸如贝伐单抗))和化学治疗剂外,可以与其组合其它治疗方案。例如,可以施用第二(第三、第四、等等)化学治疗剂,其中第二化学治疗剂是抗代谢物化学治疗剂,或不是抗代谢物的化学治疗剂。例如,第二化学治疗剂可以是紫杉烷(诸如帕利他赛或多西他赛)、卡培他滨、或基于铂的化学治疗剂(诸如卡铂、顺铂、或奥沙利铂)、蒽环类抗生素(诸如多柔比星,包括脂质体多柔比星)、托泊替康、培美曲塞、长春花生物碱(诸如长春瑞滨)、和tlk286。可以施用不同化学治疗剂的“混合物”。
可以与基质靶向剂、免疫调节剂、抗血管生成剂(例如vegf拮抗剂(例如抗vegf抗体,诸如贝伐单抗))、和/或化学治疗剂组合的其它治疗剂包括下列任一项或多项:her抑制剂、her二聚化抑制剂(例如生长抑制性her2抗体诸如trastuzumab或诱导her2过表达细胞凋亡的her2抗体诸如7c2、7f3或其人源化变体);针对不同肿瘤相关抗原诸如egfr、her3、her4的抗体;抗激素化合物,例如抗雌激素化合物诸如他莫昔芬,或芳香酶抑制剂;心脏保护剂(以预防或减轻与治疗有关的任何心肌功能障碍);细胞因子;egfr靶向药物(诸如
任何上文记录的共施用药剂的合适的剂量是那些目前使用的,并且可以由于药剂和基质靶向剂、免疫调节剂、和/或抗血管生成剂(例如vegf拮抗剂(例如抗vegf抗体,诸如贝伐单抗))的组合作用(协同)而降低。在上述治疗方案外,患者可以进行肿瘤和/或癌细胞的手术除去和/或放射疗法。
在基质靶向剂(例如抗postn抗体)、免疫调节剂、和/或抗血管生成剂(例如vegf拮抗剂(例如抗vegf抗体,诸如贝伐单抗))是抗体的情况下,优选地,施用的抗体是裸抗体。施用的基质靶向剂(例如抗postn抗体)、免疫调节剂、和/或抗血管生成剂(例如vegf拮抗剂(例如抗vegf抗体,诸如贝伐单抗))可以是与细胞毒剂缀合的。优选地,缀合物和/或其结合的抗原受到细胞内在化,导致缀合物杀伤其所结合的癌细胞的治疗功效提高。在一个优选的实施方案中,细胞毒剂靶向或干扰癌细胞中的核酸。此类细胞毒剂的例子包括美登木素生物碱类(maytansinoids)、加利车霉素(calicheamicin)、核糖核酸酶和dna内切核酸酶。
可以通过基因疗法施用基质靶向剂(例如抗postn抗体)、免疫调节剂、和/或抗血管生成剂(例如vegf拮抗剂(例如抗vegf抗体,诸如贝伐单抗))。关于使用基因疗法产生细胞内抗体,见例如1996年3月14日公开的wo96/07321。有两种主要方法使核酸(任选包含在载体中)进入患者的细胞,即体内(invivo)和回体(exvivo)。对于体内投递,通常在需要抗体的部位将核酸直接注射到患者体内。对于回体治疗,取出患者的细胞,将核酸导入这些分离的细胞,并将经过修饰的细胞或是直接施用于患者,或是例如封装入多孔膜内并植入患者体内(参见例如美国专利第4,892,538号和第5,283,187号)。有多种技术可用于将核酸导入可存活细胞。这些技术根据是将核酸转移至体外培养细胞还是目的宿主的体内细胞而有所变化。适于在体外将核酸转移到哺乳动物细胞中的技术包括使用脂质体、电穿孔、显微注射、细胞融合、deae-右旋糖苷、磷酸钙沉淀法等。常用于回体投递基因的载体是逆转录病毒。目前优选的体内核酸转移技术包括用病毒载体(诸如腺病毒、i型单纯疱疹病毒或腺伴随病毒)和基于脂质的系统(可用于脂质介导的基因转移的脂质有例如dotma、dope和dc-chol)进行的转染。在有些情况中,希望与靶向靶细胞的试剂一起提供核酸源,所述试剂诸如对细胞表面膜蛋白或靶细胞特异的抗体、靶细胞上受体的配体等。在采用脂质体时,与胞吞作用相关细胞表面膜蛋白结合的蛋白质可用于靶向和/或促进摄入,例如对特定细胞类型具有向性的衣壳蛋白或其片段、在循环中发生内在化的蛋白质的抗体、及靶向细胞内定位和延长细胞内半衰期的蛋白质。受体介导的胞吞技术记载于例如wuetal.,j.biol.chem.262:44294432(1987);wagneretal.,proc.natl.acad.sci.usa87:3410-3414(1990)。关于目前已知的基因标记和基因治疗方案的综述参见andersonetal.,science256:808-813(1992)。还可参见wo93/25673及其引用的参考文献。
v.剂量和配制剂
可以通过任何合适的手段,包括胃肠外、肺内、和鼻内,及若期望用于局部治疗的话,损伤内施用来施用基质靶向剂(例如抗postn抗体)、免疫调节剂、和/或抗血管生成剂(例如vegf拮抗剂(例如抗vegf抗体,诸如贝伐单抗))。胃肠外输注包括肌肉内、静脉内、动脉内、腹膜内、或皮下施用。部分根据施用是短暂的还是长期的,剂量给药可以通过任何合适的路径,例如通过注射,诸如静脉内或皮下注射进行。本文中涵盖各种剂量给药日程表,包括但不限于单次施用或在多个时间点里的多次施用、推注施用、和脉冲输注。
基质靶向剂(例如抗postn抗体)、免疫调节剂、和/或抗血管生成剂(例如vegf拮抗剂(例如抗vegf抗体,诸如贝伐单抗))应当以一种符合良好的医学实践的方式配制、确定剂量及给药。关于这一点考虑的因素包括在治疗的特定病症、在治疗的特定哺乳动物、患者个体的临床状态、病因、药物递送部位、给药方法、服药日程以及其它为开业医生所知的因素。基质靶向剂(例如抗postn抗体)、免疫调节剂、和/或抗血管生成剂(例如vegf拮抗剂(例如抗vegf抗体,诸如贝伐单抗))无需但可任选地与一种或多种目前用于预防或治疗所述病症的药物一起配制。上述其它药物的有效量取决于配方中所存在的抗体的量、病症或治疗的类型、以及其它上述讨论的因素。这些药物通常以相同的剂量使用并具有本文中所描述的给药途径,或以约1-99%的本文所描述的剂量使用,或以任何剂量并通过任何途径使用,所述剂量和途径是凭经验确定的/经临床测定合适的。
为了预防或治疗疾病,本发明的治疗剂(当单独或与一种或多种其它别的治疗剂联合使用时)的合适剂量应取决于所要治疗的疾病的类型、药剂的种类、疾病的严重性和病程、施用的药剂的预防或治疗目的、先前疗法、患者的临床史和对药剂的响应、以及主治内科医生的判断。适当地,在一次或一系列的治疗中对患者施用药剂。取决于疾病的类型和严重性,对患者施用约1μg/kg-15mg/kg的抗体可作为首次候选用量,无论是例如通过一次或多次单独的给药或通过连续输注。取决于上述提及的因素,一种典型的日剂量可在约1μg/kg-100mg/kg或更多的范围内。对于几天或更长时间的重复给药,取决于病情,治疗应通常持续直至出现病症得到期望的抑制为止。药剂的一种例示性的剂量会在约0.05mg/kg至约10mg/kg的范围中。如此,可以对患者施用一剂或多剂约0.5mg/kg、2.0mg/kg、4.0mg/kg或10mg/kg(或其任何组合)。此类剂量可间歇施用,如每周或每三周施用一次(如使得患者得到约2-约20个,或例如约6个剂量的抗体)。然而,可使用其它给药方案。通过常规技术和测定方法易于监测该治疗的进展。
在某些实施方案中,以平坦剂量(即非重量依赖性)37.5mg、或平坦剂量125mg、或平坦剂量250mg施用基质靶向剂(例如抗postn抗体)、免疫调节剂、和/或抗血管生成剂(例如vegf拮抗剂(例如抗vegf抗体,诸如贝伐单抗))。在某些实施方案中,通过每4周一次皮下注射一段时间施用剂量。在某些实施方案中,时间段是6个月、1年、2年、5年、10年、15年、20年、或患者一生。
在另一个实施方案中,确定患者具有化学疗法抗性癌症,并且选择用抗postn抗体或如上文描述的任何治疗剂治疗。在一个实施方案中,癌症患者是18岁以上的年龄。在一个实施方案中,癌症患者的年龄是12至17岁,并且以平坦剂量250mg或平坦剂量125mg施用治疗剂。在一个实施方案中,癌症患者的年龄是6至11岁,并且以平坦剂量125mg施用治疗剂。
vi.制品
在本发明的另一个方面中,提供了含有可用于治疗、预防和/或诊断上文描述的病症的材料的制品。制品包含容器和容器上的或与所述容器相连的标签或包装插页。合适的容器包括例如瓶、管形瓶、注射器、iv溶液袋等。容器可以由多种材料制成,诸如玻璃或塑料。容器容纳自身或与另一种组合物组合有效治疗、预防和/或诊断状况的组合物,并且可以具有无菌存取口(例如,容器可以是具有由皮下注射针可穿过的塞子的管形瓶或静脉内溶液袋)。组合物中的至少一种活性剂是本发明的药剂(例如基质靶向剂(例如抗postn抗体)、免疫调节剂、和/或抗血管生成剂(例如vegf拮抗剂(例如抗vegf抗体,诸如贝伐单抗))。标签或包装插页指示使用组合物来治疗选择的状况。此外,制品可以包含(a)具有其中含有的组合物的第一容器,其中组合物包含药剂(例如基质靶向剂(例如抗postn抗体)、免疫调节剂、和/或抗血管生成剂(例如vegf拮抗剂(例如抗vegf抗体,诸如贝伐单抗));和(b)具有其中含有的组合物的第二容器,其中组合物包含别的细胞毒性或其它方面治疗性的药剂。在本发明的此实施方案中的制品可以进一步包含包装插页,其指示可以使用组合物来治疗特定的状况。或者/另外,制品可进一步包括第二(或第三)容器,其包含药学可接受缓冲液,诸如抑菌性注射用水(bwfi)、磷酸盐缓冲盐水、林格(ringer)氏溶液和右旋糖溶液。它可以进一步包括从商业和用户立场出发期望的其它物质,包括其它缓冲液、稀释剂、滤器、针头、和注射器。应当理解,替换药剂(例如基质靶向剂(例如抗postn抗体)、免疫调节剂、和/或抗血管生成剂(例如vegf拮抗剂(例如抗vegf抗体,诸如贝伐单抗))或除此之外,任何上述制品可以包含本发明的免疫缀合物。
实施例
实施系统且深入的分析以寻找、功能表征并且独立验证与对初始治疗的化学疗法抗性相关的关键分子特征。为了发现,选择一组患者,其具有临床上充分限定的对初始化学疗法治疗的响应和匹配的临床病理特征。对于独立验证研究,使用来自在具有代表性意图治疗(itt)患者群体和平衡良好的临床特征、良好注释的临床响应、和患者结果的iii期临床试验的化学疗法对照分组中登记的患者的组织样品。自发现研究,鉴定反应性基质标签与铂抗性(plat-r)原发性肿瘤特别相关,并且在plat-r复发性肿瘤中进一步上调。在独立数据集中进一步验证此标签,并且证明了在对基于铂的一线化学疗法预测患者结果中的临床效用。这些发现提供了用于鉴定初始化学疗法抗性卵巢癌患者的诊断策略,并且提供了用于预测对初始化学疗法的响应的基于生物标志物的测试。
材料与实验方法
患者和肿瘤标本
本研究分别由用于发现和验证目的的两组卵巢患者分组组成。
发现组由来自58名患者的85例高度浆液性或子宫内膜样卵巢癌组成。在表6中描述了这些患者的临床特征,并且表示具有高度上皮卵巢癌的患者的典型临床概况。最初用铂和紫杉烷组合治疗所有58名患者。在这些中,32名患者具有原发性铂抗性肿瘤(基于铂的一线化学疗法完成后6个月内疾病复发或进展),并且26名患者具有铂敏感性肿瘤(一线化学疗法的12个月内无复发或恶化)。在一线化学疗法前自所有患者收集肿瘤标本。32名铂抗性患者中的27名也具有在复发性疾病时收集的患者匹配的肿瘤标本。所有发现组组织样品是自商业来源获得的,并具有合适的机构批准。
验证组由来自138名来自iii期试验的化学疗法治疗分组的患者的138例高级浆液性或子宫内膜样卵巢癌组成,在具有新诊断的卵巢癌的女性中检查标准化学疗法相对于对标准化学疗法添加贝伐单抗的效果。在表9中描述了这些患者的临床特征。
所有肿瘤组织均由病理学家审查以确认诊断和肿瘤含量。对福尔马林固定且石蜡包埋的(ffpe)肿瘤组织实施宏观解剖(macro-dissection)以将肿瘤百分比富集至大于70%。使用highpureffperna微型试剂盒(rochediagnostics,indianapolis,in,usa)纯化总rna。使用qiaampdnaffpe组织试剂盒(qiagen,ca)制备ffpe肿瘤dna。
使用卵巢癌生物标志物nanostring组的基因表达序型分析
定制的nanostring800gxcodeset设计为测量与卵巢疾病生物学相关的800种生物标志物和对照的基因表达,包括亚型和预后分类器、流出abc转运蛋白、以及化学耐受性、免疫、和血管发生标志物(关于完整的基因列表,见表5)。使用nanostringncounter分析系统遵循制造商的方案(nanostringtechnologies)分析200ngrna。通过每份样品的所有800个测定法的中值计数标准化输出原始计数。
表5:完整基因列表
统计学分析
自随机化日至疾病进展或死亡的第一指征的日期(以先发生者为准)计算无进展存活;审查在无疾病进展的情况中存活的患者的数据到其最后一次非进展性疾病(pd)肿瘤评估日为止。自随机化日至来自任何原因的死亡的日期计算总体存活;在最后知道患者存活的日期时审查仍然存活的患者的数据。对生物标志物高和低组之间的无进展存活的分布的差异使用时序检验实施存活分析。通过kaplanmeier方法使用乘积极限估计计算中值存活时间。
为了比较plat-s和plat-r原发性肿瘤之间的基因表达差异,采用双样品t检验。为了比较plat-r匹配的原发性和转移性肿瘤之间的基因表达差异,使用配对t检验。导出两侧p值,并且通过使用benjaminihochberg法控制假发现率(fdr)调节用于多重比较。
rna原位杂交(rnaish)测定法
在advancedcelldiagnostics,hayward,ca设计、实施和评分双重postn/lox和单重fap
免疫组织化学
对载玻片上安装的4μm厚的福尔马林固定的、石蜡包埋的组织切片实施免疫组织化学(ihc)。使用针对fap(gne,克隆10d2.1.1)、α平滑肌肌动蛋白(sma)(abcam,cambridge,ma)和postn(biovendor,asheville,nc)的一抗。利用trilogy(cellmarque,rocklin,ca)抗原恢复在dako自动染色器上实施fap染色。检测采用马抗小鼠生物素化二抗(vectorlabs,burlingame,ca),接着是tsa增强(perkinelmer,waltham,ma)和dab显现(pierce,rockford,il)的链霉亲合素-hrp。在ventanadiscoveryxt自动化平台(ventanamedicalsystems;tucson,az)上实施sma和postn染色。用cellconditioner1处理切片,标准时间。通过在omnimap抗家兔hrp(ventanamedicalsystems;tucson,az)中温育切片,接着是通过chromomapdab(ventanamedicalsystems;tucson,az)检测特异性结合的一抗。用苏木精复染切片,脱水,并且盖上盖玻片。
结缔组织生成的h&e评估
对发现肿瘤样品(总共85份,包括原发性plat-s、患者匹配的plat-r原发性、和复发性肿瘤)的代表性h&e染色切片检查与肿瘤损伤相关的基质活化的证据,并且分配结缔组织生成得分。由于组织损伤、坏死、水肿或存在的有限基质,认为一些病例太难以对可用的代表性切片评分。将结缔组织生成鉴定为纤维化区域,其以与驻留的非活化成纤维细胞不同的肌成纤维细胞的增加的密度和瓦解为代表。使用的结缔组织生成评分系统类似于由tothilletal.,clincancerres.14:5198-5298,2008报告的。结缔组织生成得分定义如下:0=无结缔组织生成,1=癌细胞邻近的少数分散的结缔组织增生病灶,2=癌细胞邻近的几个结缔组织增生病灶或中等汇合的(较宽的)结缔组织生成,但是不遍及切片存在,3=遍及切片的结缔组织增生反应。
tp53突变状态
使用先前开发的mmp-seq靶向癌组对整个tp53基因的所有外显子和外显子-内含子接合实施深度测序。使用trak2qpcr“标尺测定法(rulerassay)”将ffpedna样品的质量量化为功能性拷贝的数目。使用来自每份样品的5000个功能性dna拷贝作为靶物富集和文库构建的输入,其使用fluidigmaccess阵列,接着在illuminamiseq测序仪上深度测序进行。tp53基因的平均覆盖是每个扩增子约1000倍。实施序列比对、主要变体调用和过滤,如记载于bourgonetal.,clincancerres20:2080-2091(2014)的。
通过实时pcr的拷贝数目变异分析
对使用各50nm的35对基因特异性引物合并物和taqman预扩增主混合物(lifetechnologies)依照制造商的方案对经福尔马林固定的石蜡包埋的(ffpe)基因组dna(200ng)进行17个循环的预扩增。稀释预扩增的样品,并且在biomarktm系统上使用fluidigm96.96dynamic阵列实施qpcr。简言之,样品混合物含有dna、taqman基因表达主混合物(lifetechnologies)、dna结合样品加载试剂(fluidigm)、和evagreen染料(biotium)。测定混合物含有基因特异性引物对和样品加载试剂(fluidigm)。使用fluidigm基因分析软件实施ct测定和熔解曲线分析。使用全局δδct法计算相对基因拷贝数目。首先,使用每份样品中的所有基因的中值ct作为参照以标准化样品dna输入,并且计算δct。然后,使用个别基因的所有样品的中值δct作为2拷贝校准物样品。结果是每种基因的三种引物对的平均值。
基于细胞的测定法
自atcc获得卵巢细胞系es-2,并且在具有10%fbs和2mm谷氨酰胺的rpmi1640培养基中培养。首先将96孔板用重组全长fn1(产品目录号f2006,sigma-aldrich,st.louis,mo)、postn(产品目录号3548-f2,r&dsystems,minneapolis,mn)包被或保持未包被,于37℃持续2小时或于4℃持续16小时。然后,将细胞以3,000个细胞/孔铺在经包被的板中。次日将10μm卡铂或10nm帕里他赛添加至每孔。在化合物处理后72小时时添加
实施例1:鉴定在初始化学疗法抗性卵巢肿瘤中上调的“反应性基质”基因标签
为了鉴定与eoc中的初始化学疗法抗性有关的分子特征,选择了对初始化学疗法具有临床上完全定义的响应的一组高级浆液性或子宫内膜样卵巢肿瘤(表6)。此发现组由来自32名具有初始化学疗法抗性的患者和26名对初始化学疗法敏感的患者的肿瘤标本组成。用铂和紫杉烷的组合作为一线化学疗法治疗所有患者。基于在完成基于铂的一线化学疗法后6个月内已经具有疾病复发或进展选择初始化学疗法抗性患者,而基于在自初始化学疗法起12个月内尚未具有复发或进展选择化学疗法敏感性患者。32名化学疗法抗性患者之27名具有在化学疗法前收集的患者匹配的原发性肿瘤标本和在疾病进展时在疗法后收集的复发性肿瘤标本(分别称为plat-r原发性和plat-r复发性)。对于26名化学疗法敏感性患者,仅在疗法前的原发性肿瘤标本可用于分析(称为plat-s原发性)。
表6:发现研究中的患者临床病理特征
寻求与对基于铂的化学疗法的响应相关的基因表达标签。使用在nanostring平台上开发的800基因的卵巢癌生物标志物组(表5)对plat-r原发性、plat-r复发性和plat-s原发性样品实施基因表达序型分析。在化学疗法前比较32个plat-r和26个plat-s原发性肿瘤的两样品t检验鉴定出在两组间显著差异表达的14种基因(fdr≤10%和倍数变化≥1.5,表7)。plat-r肿瘤中的上调基因代表了独特的“反应性基质”标签(图1a),其在ecm生成和重塑基因(即postn、fap、lox、timp3、col4a1)、牵涉细胞迁移和侵入的基因(即nuak1)、以及牵涉免疫调节的基因(即tdo2)中高度富集。另一方面,与化学疗法敏感性肿瘤有关的关键基因包括孕酮受体(pgr)、胎盘碱性磷酸酶(alpp)、和成纤维细胞生长因子4(fgfr4)基因。对于在疗法前收集患者匹配的原发性肿瘤标本且在疾病进展时在疗法后收集的复发性肿瘤标本的27名plat-r患者,实施进一步分析以搜索表征复发性肿瘤的基因标签。配对t检验鉴定出在原发性和复发性抗性肿瘤之间显著差异表达的65种基因(fdr≤10%和倍数变化≥1.5,表8)。再次,代表肿瘤基质成分的标志基因在复发性肿瘤中的36种显著上调基因间高度富集(图1b),包括活化成纤维细胞标志物(acta2)、ecm生成和重塑酶(即postn、fap、fn1、timp3、lox、mmp11),生长因子(即fgf1),免疫相关基因(即cd36,gzmk,cd247)以及血管内皮标志物(即plvap和pecam(抗原cd31))和生长因子(即angpl2)。与疗法前的原发性肿瘤相比,复发性plat-r肿瘤中的29种显著下调的基因是雌激素受体(esr1和esr2)和其它分化的上皮细胞标志物(muc1、klk6、klk7)(图1b)。表征原发性和复发性plat-r肿瘤的两种标签的比较鉴定出具有下述表达水平的4种共同的反应性基质标签基因,即postn、fap、timp3和lox,所述表达水平(1)彼此高度相关(图2);(2)与plat-s原发性肿瘤相比在plat-r原发性肿瘤中显著上调,以及(3)进一步诱导了plat-r复发性肿瘤中的化学疗法后治疗(图1c和1d)。这些结果一起指示反应性基质基因的上调可以在调控eoc中的化学疗法抗性中起重要作用。
先前已经将肿瘤阻抑物基因tp53中的突变和细胞周期蛋白e1(ccne1)的扩增与卵巢癌中的初始化学疗法抗性关联起来。使用mmp-seq靶向癌症组对整个tp53基因的所有外显子实施深度测序。在32之32个(100%)plat-r原发性肿瘤和26之23个(88%)plat-s原发性肿瘤中找到了tp53突变(图1a)。tp53突变的观察到的总体高频率与高级浆液性卵巢肿瘤中的tcga发现一致。这些结果也指示了tp53突变状态不可能是决定对化学疗法治疗的响应中的主要驱动力。也对已经报告为在许多癌症类型中频繁改变的35种基因实施了基于qpcr的拷贝数分析。在此研究中鉴定出9种反复扩增的基因(图1a,拷贝数≥4)。在这些中,仅在plat-s肿瘤中鉴定出rsf1、akt1、和akt3扩增,而仅在plat-r肿瘤中鉴定出fgfr1和znf703扩增。然而,在对化学疗法的响应和这些基因之任一种(包括ccne1)或组合的扩增之间没有观察到显著关联。
表7:plat-r原发性对plat-s原发性肿瘤之间的14种差异表达基因(发现数据集)
表8:plat-r复发性对plat-r原发性肿瘤之间的65种差异表达基因(发现数据集)
实施例2:在肿瘤关联成纤维细胞中特异性衍生和调控反应性基质标签基因
为了确定哪些特定的细胞类型表达反应性基质标签基因,对来自整组的85个肿瘤标本的肿瘤标本的全载玻片实施postn和faprnaish分析。另外,也对15个代表性肿瘤标本实施postn和fapihc,以及loxrnaish分析。在图3a中显示了显示这些标志物的ish和ihc的代表性图像。在plat-s原发性肿瘤中,无一或显著较低水平的反应性基质标签基因通过ish或ihc在基质或肿瘤细胞中检出。比较而言,在plat-r原发性和复发性肿瘤中,发现了仅在肿瘤关联成纤维细胞中表达postn,而主要在肿瘤关联成纤维细胞中并且以较低水平在肿瘤细胞中表达lox和fap。表达postn/lox/fap的肿瘤关联成纤维细胞也显示强烈的α-平滑肌肌动蛋白(αsma)染色,其是活化的成肌纤维细胞的建立的标志物。与来自nanostring基因表达序型分析(图1d)的结果一致,ish和ihc分析确认了与plat-s原发性肿瘤相比,反应性基质基因的表达在plat-r原发性肿瘤中显著更高,并且在plat-r复发性肿瘤中进一步上调(图3b)。反应性基质基因表达的观察到的调控主要限于与原发性和复发性plat-r肿瘤中的肿瘤细胞直接并列的基质区室(图3b),这显示了肿瘤关联基质区室可以是介导卵巢癌中的化学疗法抗性中的特定作用位点。如此,使用原位分析,包括ihc和rnaish两者,将反应性基质标签基因鉴定为仅仅或主要由与肿瘤细胞直接并列的活化的成纤维细胞表达。
实施例3:postn的基质表达与结缔组织生成表型有关
结缔组织生成是许多癌症类型中找到的共同的病理学表型。结缔组织生成的组织学表现包括胞外基质蛋白的显著过度生成,和成肌纤维细胞样细胞的广泛增殖和瓦解。基质细胞增殖和胞外基质组分沉积的变化导致总体组织异质性和弹性的显著变化,以及伴随的间隙液压力。已经提示了这些变化促成癌症中的化学疗法抗性。为了评估反应性基质分子标签和结缔组织生成生理特征之间的潜在联系,在此研究中的整组肿瘤标本的经h&e染色的全组织切片上对结缔组织生成程度评分。在评分的85个标本中,认为它们中的26个由于组织损伤、坏死、水肿、或存在的有限基质而太难以评分。剩余的标本包含21个plat-s原发性、18个plat-r原发性和21个plat-r复发性肿瘤。如图4a和4b中显示的,虽然在大多数plat-s原发性肿瘤中没有观察到结缔组织增生性病症或者仅仅观察到几个分散的结缔组织增生性病症,但是在plat-r原发性和复发性肿瘤中高度富集中等至广泛的结缔组织生成。此外,结缔组织生成的程度与postn(表征初始化学疗法抗性的反应性基质标签的关键组分之一)的基质表达水平高度相关。为了进一步建立这些反应性基质标签基因在介导化学疗法抗性中的直接作用,证明了在存在重组postn的情况中培养的化学疗法敏感性卵巢细胞在体外对卡铂和帕利他赛处理变得有抗性。
实施例4:postn在体外促进eoc细胞的化学疗法抗性
接着调查反应性基质标签基因是否在促进卵巢肿瘤细胞中的化学疗法抗性中起特定的作用。对此,使用重组人postn蛋白包被组织培养皿以直接测试其对es-2细胞(无内源postn表达的化学疗法敏感性卵巢癌细胞系)中对化学试剂的抗性的影响(图4c)。由于已经显示了纤连蛋白(fn)(ecm的一种糖蛋白和关键组分)调控卵巢癌细胞中的多西他赛抗性,使用fn蛋白包被作为此实验中的对照。如图4c中显示的,发现了经postn包被的板上培养的es-2细胞比未处理的培养皿上培养的细胞对卡铂或帕利他赛处理显著更有抗性。虽然单独的postn包被在缺乏化学疗法处理的情况中也显示了细胞生长的少量增加,但是其对化学疗法处理后提供存活益处的影响是卓越且显著的。比较而言,与postn相比,fn包被提供少得多的对促进es-2细胞中对卡铂或帕利他赛处理的药物抗性的影响。本研究证明了postn可以在体外促进eoc细胞中的化学疗法抗性。这些结果一起提供了进一步的支持证据,即postn和其它反应性基质组分可以在促进体内化学疗法抗性中起直接作用。
实施例5:与初始化学疗法抗性关联的反应性基质标签的独立验证
为了在独立数据集中进一步验证反应性基质标签和初始化学疗法抗性之间的直接联系,使用来自iii期试验的化学疗法治疗分组的卵巢肿瘤组织样品的亚组,所述iii期试验评估对标准化学疗法添加贝伐单抗作为卵巢癌(icon7)的一线治疗的益处。在化学对照分组中登记的510名患者中,138名具有高级浆液性或子宫内膜样卵巢肿瘤的患者具有可用于nanostring卵巢癌生物标志物组上的基因表达序型分析的组织(表9)。在生物标志物亚群中没有发现就plat-r和plat-s患者的分布,或临床病理学特征而言的显著偏倚,提示了它代表意图治疗(itt)群体(表10)。使用发现研究中使用的相同临床定义将来自iii期试验的化学对照分组的患者分类入plat-s和plat-r组中(实施例1,上文)。在化学疗法前对49个plat-r和86个plat-s原发性肿瘤的两样品t-检验分析鉴定出在两组间显著差异表达的10种基因(p≤0.01和倍数变化≥1.5,表11)。来自此数据集和发现数据集的差异表达的基因列表的比较显示了构成初始化学疗法抗性肿瘤中前4种显著上调基因的所有四种反应性基质标签基因(postn、fap、timp3、和lox)(图5a)。这些结果独立确认了反应性基质标签是eoc中的一种强力且可再现的化学疗法抗性标签。pgr的表达在发现和验证数据集两者中在化学疗法抗性组中组成性下调至少2倍(在发现数据集中p<0.001和倍数变化=3.3;和在验证数据集中p=0.0058和倍数变化=2),这提示了孕酮信号传导可以在介导卵巢癌中对化学疗法的敏感性中起重要作用。
表9:来自iii期临床研究的标准化学疗法分组的验证集中患者临床病理学特征
表10:icon7化学治疗分组(生物标志物群体对itt)的人口统计数据汇总
表11:在plat-r原发性对plat-s原发性肿瘤(icon数据集)之间的10种差异表达的基因
实施例6:postn预测eoc中基于铂的一线化学疗法的临床结果
为了检查反应性基质标签基因是否可以预测eoc中的一线化学疗法的临床结果,使用四种预先规定的反应性基质标签基因postn、fap、timp3、和lox之每种,以及pgr对iii期试验的化学对照分组患者实施单变量存活分析。如图5b中显示的,与具有低postn表达的患者中的27个月相比,具有高postn表达(中值截留)的患者具有显著更短的无进展存活(pfs),中值pfs为12个月(hr=2.4,95%ci:1.6-3.7,p=0.0001)。虽然在postn表达水平和几种已知的临床预后因素(包括减缩状态、血清ca125水平、和figo阶段)之间观察到弱关联(图6),但是postn水平和pfs之间的关联在针对这些协变量调节后仍然是显著的(hr=1.76,p=0.015)。还发现了timp3表达在单变量cox模型中与pfs显著有关(hr=1.8,95%ci:1.2-2.8,p=0.0073)(图5b)。另一方面,使用中值截留得到的fap或lox表达和pfs之间的关联不是统计学显著的,但是在使用75百分位数截留时是高度显著的(对于fap,hr=2.2,95%ci:1.4-3.4,p<0.001;对于lox,hr=1.9,95%ci:1.2-3.0,p=0.005)。接着,在多变量cox回归模型中分析使用中值截留二分的所有四种基因(postn、fap、lox、和timp3)的表达以评估每种基因的关联强度。仅postn的表达在此多变量分析中是显著的,这提示了postn是主要驱动力,并且提供了用于预测一线化学疗法的患者结果的卓越能力(图7)。另外,在对于每名患者对四种基因的表达取平均值时,所得的总体基质得分不改善与pfs的关联(hr=2.0,95%ci:1.3-3.1,p=0.0013),这确认了postn在预测化学疗法下一线卵巢癌存活中作为限定基质因素的作用。标签基因无一显示与总体存活(os)的显著关联。为了评估pgr是否提供患者存活的别的预测能力,用二分postn和pgr作为协变量实施多变量cox模型分析(图7)。在针对postn表达水平调节后,发现具有较高的pgr表达的患者经历卵巢癌进展风险的35%降低,然而,效果仅仅是微小的,p值为0.055(hr=0.65,95%ci:0.42-1.01)。
实施例7:克服癌症中的化学疗法抗性的治疗策略
自此研究鉴定的反应性基质、化学疗法抗性和较差的临床结果之间的特定关联突出显示了卵巢癌生物学和治疗中癌症和肿瘤微环境之间的重要的相互作用。如此,与直接靶向肿瘤细胞的药剂组合靶向肿瘤基质的组分可以提供用于克服抗性和改善效力的潜在的新颖方法。例如,postn可以是潜在的治疗性靶物之一。已经在许多癌症类型,诸如乳腺、肺、结肠、胰腺和卵巢癌中观察到postn的上调。postn与多种细胞表面受体,最值得注意地整联蛋白相互作用,并且主要经由pi3k/akt和fak介导的途径发信号以促进癌细胞存活、血管发生、上皮-间质转化(emt)、侵入、和转移。最近的研究已经证明了基质postn通过调节乳腺癌干细胞之间的相互作用对于转移性定殖是至关重要的。此外,在卵巢癌细胞系中用中和性抗体靶向内源postn抑制动物模型中的卵巢肿瘤生长和转移。总之,癌症开发、进展和治疗响应中postn的重要作用使它成为用于克服化学疗法抗性的有希望的新颖治疗性靶物。在个别的基质组分外,我们的研究已经揭示了表征化学疗法抗性的反应性基质标签是创伤愈合的正常过程中牵涉的基因中高度富集的。与先前的实验证据一致,我们的数据已经提示了tgf-β(一种在创伤修复中的基质应答的关键介导物)可能在调节肿瘤细胞与其关联基质之间的广泛串扰中起重要的作用(图8)。因此,靶向tgf-β信号传导途径可以是用于克服化学疗法抗性的另一种潜在的有希望的治疗策略。
分析下述基因揭示了可以牵涉促进化学疗法抗性的其它生物学过程,所述基因表达水平与反应性基质标签基因显著相关。例如,我们发现了postn表达水平与plvap、pecam1、和angptl2(促进血管发生和血管形成中的关键组分)高度相关(图9)。因此,对化学疗法主链(诸如贝伐单抗)添加抗血管发生试剂可以对卵巢患者提供额外的益处,所述卵巢患者在本质上对初始化学疗法有抗性。另外,用于克服初始化学疗法抗性的另一种治疗策略源自下述观察,即postn表达水平与cd68和cd163高度相关,两者都是已知在创伤愈合过程期间的炎性和免疫应答中牵涉的m2巨噬细胞的完善表征的表面标志物(图9)。此观察与下述最近报告一致,即基质响应表达标签与m2巨噬细胞浸润相关联,并且预测胃癌和卵巢癌中的不良预后。如此,想得到的是直接靶向m2巨噬细胞或关联的趋化因子、细胞因子或生长因子的抗炎药物可以代表用于克服eoc中的初始化学疗法抗性的另一种新颖治疗策略。
实施例8:循环postn作为预测铂抗性eoc的标志物
为了调查是否可以使用循环postn预测eoc患者中的化学抗性,采用elisa测定法测量血清中的循环postn。在来自102名年龄匹配的正常健康受试者(nhs)、100名未知化学敏感性的eoc患者、43名已知为铂抗性的eoc患者、96名肺癌(nsclc)患者、和29名胰腺癌患者的供应商获得的血清样品组中测量血清postn水平。化学敏感性状态和血清收集时间(在治疗之前和之后)对于100份供应商获得的样品是未知的,然而基于流行研究,可能的是至少30%的样品来自化学抗性患者。血清postnelisa下至1.88ng/ml是敏感的,并且在所有卵巢癌患者和nhs的血清中检出postn。图10中的分组点图显示了eoc患者中的postn表达范围与nhs和其它癌症患者的范围高度重叠。然而,循环postn的中值和范围在化学抗性卵巢癌和nsclc患者两者中比在nhs中显著更高。这些结果与在化学抗性卵巢癌患者中较高的组织postn表达一致。
也在来自i(25)和ii(6)期患者(31名组合)的供应商获得的血清样品和69份来自iii期患者的样品中测量循环postn水平(如通过卵巢癌的figo分期测定的)。在循环postn和疾病阶段之间发现正相关(图11)。基于这些结果,也可以使用循环postn的测量作为测定eoc患者的阶段的非侵入性方法。
序列表索引
虽然已经为了理解清楚的目的通过例示和实施例相当详细地描述了前述发明,但是描述和实施例不应解释为限制本发明的范围。为了所有目的通过提及完整明确收录本文中引用的所有专利、专利申请、科学参考文献的公开内容,就像通过提及明确且单独收录每篇专利、专利申请、科学参考文献一样。
序列表
<110>基因泰克公司(genentech,inc.)
豪夫迈·罗氏有限公司(f.hoffmann-larocheag)
<120>用于治疗和诊断化学疗法抗性癌症的组合物和方法
<130>50474-092wo3
<150>us62/200,340
<151>2015-08-03
<150>us62/096,355
<151>2014-12-23
<160>4
<170>patentinversion3.5
<210>1
<211>127
<212>prt
<213>小鼠(musmusculus)
<400>1
glnvalhisleuglnglnserglyalagluleualalysproglyala
151015
servalhismetsercyslysalaserglytyrthrphethrthrtyr
202530
trpmethistrpvallysglnargproglyglnglyleuglutrpile
354045
glytyrileasnproasnthrglytyralaasptyrasnglnlysphe
505560
argasplysalathrleuthralaasplysserserserthralatyr
65707580
metglnleuserserleuthrsergluaspserthrvaltyrphecys
859095
alaargargargthrglythrsertyrpheasptyrtrpglyglngly
100105110
thrthrleuthrvalserserthrlysthrthrproproserval
115120125
<210>2
<211>102
<212>prt
<213>小鼠(musmusculus)
<400>2
glnthrvalleuserglnserproalaileleuseralaserprogly
151015
glulysvalthrmetthrcysargalaserserservalthrtyrmet
202530
histrptyrglnglnlysproglyserserprolysprotrpilephe
354045
alathrserasnleualaserglyvalproalaargpheserglyser
505560
glyserglythrsertyrserleuthrileserargvalglualaglu
65707580
aspalaalathrtyrtyrcysglnglntrpthrserasnproleuthr
859095
pheglyalaglythrlys
100
<210>3
<211>127
<212>prt
<213>小鼠(musmusculus)
<400>3
glnvalglnleuglnglnserglyalagluleualaargproglyala
151015
servallysleusercyslysalaserglytyrserphethrhistyr
202530
trpmetglntrpvallysglnargproglyglnglyleuglutrpile
354045
glyalailetyrproglyaspglyaspthrargtyrthrglnargleu
505560
lysglylysalathrleuthralaasplysserserserthralatyr
65707580
metgluleuserserleualasergluaspseralavaltyrtyrcys
859095
alaarggluglygluglyasnseralametasptyrtrpglyglngly
100105110
thrservalthrvalserseralalysthrthrproproserval
115120125
<210>4
<211>103
<212>prt
<213>小鼠(musmusculus)
<400>4
aspilevalmetthrglnserglnlysphemetserthrservalgly
151015
aspargvalservalthrcyslysalaserglnasnvalglyserser
202530
valalatrppheglnglnlysproglyglnserprolysthrleuile
354045
tyrseralasertyrargaspserglyvalproaspargphethrgly
505560
serglyserglythraspphethrleuthrilethrasnvalglnser
65707580
gluaspleuthrasptyrphecysleuglntyrglythrtyrprotyr
859095
thrpheglyglyglythrarg
100
- 还没有人留言评论。精彩留言会获得点赞!