多效调控蛋白CcpA及其在提升菌株发酵性能中的用途的制作方法
本发明涉及多效调控蛋白ccpa及其在提升菌株发酵性能中的用途。
背景技术:
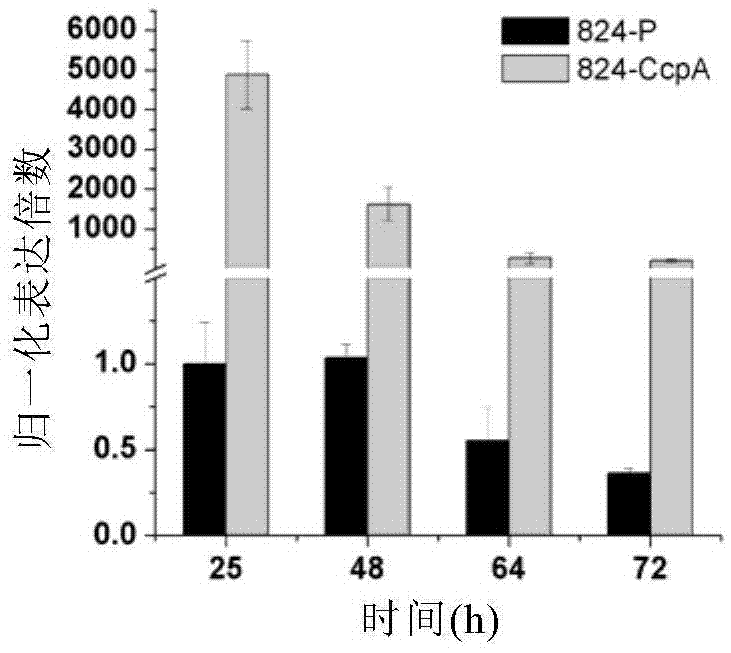
:产溶剂梭菌(solventogenicclostridia)是一种可以利用多种碳源合成各类化学品的革兰氏阳性厌氧菌。其中,丙酮丁醇梭菌(c.acetobutylicum)和拜氏梭菌(c.beijerinckii)作为典型的产溶剂梭菌受到研究者的广泛关注〔wang,y.,etal.,single-nucleotideresolutionanalysisofthetranscriptomestructureofclostridiumbeijerinckiincimb8052usingrna-seq.bmcgenomics,2011.12:p.479;ren,c.,etal.,identificationandinactivationofpleiotropicregulatorccpatoeliminateglucoserepressionofxyloseutilizationinclostridiumacetobutylicum.metabeng,2010.12(5):p.446-54〕。丙酮丁醇梭菌具有广泛的底物利用能力,可以利用淀粉、木糖、果糖、阿拉伯糖等多种糖类发酵生产丁醇、丙酮和乙醇。拜氏梭菌与丙酮丁醇梭菌相比其生长ph范围更广〔ezeji,t.andh.p.blaschek,fermentationofdrieddistillers'grainsandsolubles(ddgs)hydrolysatestosolventsandvalue-addedproductsbysolventogenicclostridia.bioresourtechnol,2008.99(12):p.5232-42〕、耐受水解液中抑制物能力更强〔liu,z.,etal.,butanolproductionbyclostridiumbeijerinckiiatcc55025fromwheatbran.jindmicrobiolbiotechnol,2010.37(5):p.495-501;ezeji,t.,n.qureshi,andh.p.blaschek,butanolproductionfromagriculturalresidues:impactofdegradationproductsonclostridiumbeijerinckiigrowthandbutanolfermentation.biotechnolbioeng,2007.97(6):p.1460-9〕,因而拜氏梭菌能够利用多种农林废弃物水解液进行发酵。此外,近年来出于节能减排的迫切需要,co2和co这类含碳气体的生物利用引起研究者们的兴趣。因此,可利用co2和co的产溶剂梭菌,如扬氏梭菌(clostridiumljungdahlii),也受到极大关注〔tanner,r.s.,l.m.miller,andd.yang,clostridiumljungdahliisp.nov.,anacetogenicspeciesinclostridialrrnahomologygroupi.intjsystbacteriol,1993.43(2):p.232-6;kopke,m.,etal.,clostridiumljungdahliirepresentsamicrobialproductionplatformbasedonsyngas.procnatlacadsciusa,2010.107(29):p.13087-92〕。分解代谢物控制蛋白a(catabolitecontrolproteina,ccpa)作为革兰氏阳性菌中的 全局性调控因子,广泛地参与到菌株的多项生理活动中,例如碳代谢〔cai,j.,etal.,ccpa-dependentcarbohydratecataboliterepressionregulatesgalactosemetabolisminstreptococcusoligofermentans.jbacteriol,2012.194(15):p.3824-32;warner,j.b.andj.s.lolkema,ccpa-dependentcarboncataboliterepressioninbacteria.microbiolmolbiolrev,2003.67(4):p.475-90;henkin,t.m.,theroleofccpatranscriptionalregulatorincarbonmetabolisminbacillussubtilis.femsmicrobiollett,1996.135(1):p.9-15〕,氮代谢〔nuxoll,a.s.,etal.,ccparegulatesargininebiosynthesisinstaphylococcusaureusthroughrepressionofprolinecatabolism.plospathog,2012.8(11):p.e1003033;tojo,s.,etal.,elaboratetranscriptionregulationofthebacillussubtilisilv-leuoperoninvolvedinthebiosynthesisofbranched-chainaminoacidsthroughglobalregulatorsofccpa,codyandtnra.molmicrobiol,2005.56(6):p.1560-73〕,生物膜形成〔sadykov,m.r.,etal.,ccpacoordinatescentralmetabolismandbiofilmformationinstaphylococcusepidermidis.microbiology,2011.157(pt12):p.3458-68〕以及毒性基因的表达〔kinkel,t.l.andk.s.mciver,ccpa-mediatedrepressionofstreptolysinsexpressionandvirulenceinthegroupastreptococcus.infectimmun,2008.76(8):p.3451-63〕等。研究表明,在产溶剂梭菌中ccpa可以通过发挥碳代谢物抑制效应(ccr)和碳代谢物激活效应(cca)来进行碳代谢物代谢调控。在ccr效应中,菌体内非速效碳源(葡萄糖,阿拉伯糖等)代谢相关基因的表达受到ccpa的抑制,菌株同时利用多种碳源的能力降低,这极大降低了菌株的发酵效率。为了缓解菌株的ccr效应,通过失活丙酮丁醇梭菌中的ccpa基因解除了菌株的ccr效应,该突变株可以同时实现葡萄糖与木糖的同步利用,但是由于ccpa具有多效调控的功能,失活ccpa后菌株的正常生理功能也受到影响,菌株生长变差,产溶剂能力降低〔ren,c.,etal.,identificationandinactivationofpleiotropicregulatorccpatoeliminateglucoserepressionofxyloseutilizationinclostridiumacetobutylicum.metabeng,2010.12(5):p.446-54〕,这不利于工业菌株的构建。相对而言,迄今尚未有涉及在微生物体内提高ccpa表达量的研究。因此,ccpa表达量的提高对微生物性能有何影响尚不得而知。技术实现要素:本文提供一种表达载体,用于表达产溶剂梭菌的ccpa蛋白。在一个或多个实施方案中,所述表达载体包括所述产溶剂梭菌ccpa蛋白的编码序列和与所述编码序列操作性连接的启动子。在一个或多个实施方案中,所述产溶剂梭菌选自丙酮丁醇梭菌、拜氏梭菌和扬氏梭菌。在一个或多个实施方案中,所述启动子选自thl启动子和ptb启动子。在一个或多个实施方案中,所述ccpa蛋白的氨基酸序列如seqidno:2、6或10所示。在一个或多个实施方案中,所述启动子序列如seqidno:3或7所示。在一个或多个实施方案中,所述ccpa蛋白的编码序列如seqidno:1、5或8所示。在一个或多个实施方案中,所述表达载体具有seqidno:4、8或11所示的核苷酸序列。本文还提供一种宿主细胞,包含本文所述的表达载体。在一个或多个实施方案中,宿主细胞为产溶剂梭菌。在一个或多个实施方案中,宿主细胞选自丙酮丁醇梭菌、拜氏梭菌和扬氏梭菌。在一个或多个实施方案中,在相同发酵条件下,与未转入ccpa蛋白的表达载体的对照相比,发酵结束时,所述产溶剂梭菌具有以下一个、任意多个或全部特征:(1)生物量提高至少10%,如至少15%、至少20%;(2)葡萄糖利用率提高至少5%,如至少8%、至少10%、至少15%、至少20%、至少25%、至少30%;(3)总溶剂产量提高至少5%,如至少10%、至少13%、至少15%、至少20%、至少25%、至少30%;(4)丙酮产量提高至少5%,如至少10%、至少13%、至少15%、至少20%、至少25%;(5)丁醇产量提高至少5%,如至少10%、至少13%、至少15%、至少20%、至少25%;和(6)乙醇产量提高至少15%,如至少20%、至少25%、至少30%。本文还提供一种提高产溶剂梭菌生产丙酮、丁醇和/或乙醇的能力的方法,所述方法包括使所述产溶剂梭菌中的ccpa蛋白过表达的步骤,优选地,过表达ccpa蛋白包括将表达ccpa蛋白的载体,尤其是本文所述的表达载体,转入所述产溶剂梭菌。本文还提供一种制备具有提高的糖利用能力和/或酸回用产溶剂能力的产溶剂梭菌的方法,所述方法包括对所述产溶剂梭菌进行基因工程操作,以使其ccpa蛋白过表达的步骤。在一个或多个实施方案中,所述方法包括将表达ccpa蛋白的载体,尤其是本文所述的表达载体,转入所述产溶剂梭菌中。本文还提供本文所述的ccpa蛋白、其编码序列或其表达载体,尤其是本文所述的表达载体,在提升产溶剂梭菌发酵性能尤其是糖利用能力和/或酸回用产溶剂能力中的用 途。附图说明图1:丙酮丁醇梭菌中过表达ccpa后的发酵结果。图中,空心圆圈代表含有空质粒的对照菌株(824-p),实心圆圈代表ccpa过表达菌株(824-ccpa)。图中显示为3次生物学重复的结果。图2:824-ccpa以及824-p菌株ccpa基因的转录分析。图中黑色柱形图为824-p菌株中ccpa基因的转录水平,灰色柱形图为824-ccpa菌株中ccpa基因的转录水平。将25h时824-p菌株中的ccpa基因的转录水平设为1。图3:拜氏梭菌中过表达ccpa后的发酵结果。图中显示为3次生物学重复的结果。图4:8052-ccpa以及8052-p菌株ccpa基因的转录分析。图中黑色柱形图为8052-p菌株中ccpa基因的转录水平,灰色柱形图为8052-ccpa菌株中ccpa基因的转录水平。将16h时8052-p菌株中的ccpa基因的转录水平设为1。图5:扬氏梭菌中过表达ccpa后发酵结果。其中,空心圆圈代表含有空质粒的对照菌株(cl-p),实心圆圈代表ccpa过表达菌株(cl-ccpa)。图中显示为2次生物学重复的结果。图6:cl-ccpa以及cl-p菌株ccpa基因的转录分析。图中黑色柱形图为cl-p菌株中ccpa基因的转录水平,灰色柱形图为cl-ccpa菌株中ccpa基因的转录水平。将48h时cl-p菌株中的ccpa基因的转录水平设为1。具体实施方式本文通过在产溶剂梭菌中过表达多效调控因子ccpa,有效提高产溶剂梭菌的生理性能(如发酵性能),促进其产物合成能力。本文中,发酵性能指菌株在糖、co或co2为原料时的产酸、酸回用以及溶剂合成能力;产物合成能力指合成丙酮、乙醇和丁醇等化学品和生物燃料的能力。产溶剂梭菌在发酵过程中可产生丙酮、乙醇和丁醇等化学品和生物燃料,是一类重要的工业微生物。本文中,产溶剂梭菌包括本领域周知的各种产溶剂梭菌,包括但不限于丙酮丁醇梭菌、拜氏梭菌和扬氏梭菌。本文中,ccpa蛋白包括来自本领域已知的各种产溶剂梭菌的ccpa蛋白,包括但不限于来自丙酮丁醇梭菌、拜氏梭菌和扬氏梭菌的ccpa蛋白。作为例子,来自丙酮丁醇梭菌的ccpa蛋白的氨基酸序列可如seqidno:2所示,来自拜氏梭菌的ccpa蛋白的氨基酸序列可如seqidno:6所示,来自扬氏梭菌的ccpa蛋白的氨基酸序列可如seqid no:10所示。可通过在本领域周知的数据库(例如ncbi)中进行序列同源性或相同性比对,例如使用本文公开的seqidno:2、6或10作为比对基础进行比对,同时结合数据库中对比对所得序列的注释获得来自不同产溶剂梭菌的ccpa蛋白。根据ncbiblast,seqidno:2与seqidno:6所示的氨基酸序列具有63%的序列相同性;seqidno:2与seqidno:10所示的氨基酸序列具有70%的序列相同性;seqidno:6和seqidno:10所示的氨基酸序列具有64%的序列相同性。因此,本发明的ccpa蛋白也包括与seqidno:2、6或10所示的氨基酸序列具有至少60%、至少65%、至少70%、至少75%、至少80%、至少85%、至少90%、至少95%、至少97%或至少99%的序列相同性,同时保留seqidno:2、6或10作为全局性调控因子所具备的生物学功能,尤其保留seqidno:2、6或10提升菌株发酵性能的能力的氨基酸序列。或者,本文的ccpa蛋白包括与seqidno:2、6或10所示的氨基酸序列相比,存在一个或多个(例如30个以内、25个以内、20个以内、15个以内、10个以内、5个以内)氨基酸突变(包括取代、缺失和/或插入),同时保留seqidno:2、6或10作为全局性调控因子所具备的生物学功能,尤其保留seqidno:2、6或10提升菌株发酵性能的能力的氨基酸序列。突变优选是保守性突变。例如,用性能相近或相似的氨基酸进行保守性取代时,通常不会改变蛋白质或多肽的功能。“性能相近或相似的氨基酸”包括例如,具有相似侧链的氨基酸残基的家族,这些家族包括具有碱性侧链的氨基酸(例如赖氨酸、精氨酸、组氨酸)、具有酸性侧链的氨基酸(例如天冬氨酸、谷氨酸)、具有不带电荷的极性侧链的氨基酸(例如甘氨酸、天冬酰胺、谷氨酰胺、丝氨酸、苏氨酸、酪氨酸、半胱氨酸)、具有非极性侧链的氨基酸(例如丙氨酸、缬氨酸、亮氨酸、异亮氨酸脯氨酸、苯丙氨酸、甲硫氨酸、色氨酸)、具有β-分支侧链的氨基酸(例如苏氨酸、缬氨酸、异亮氨酸)和具有芳香侧链的氨基酸(例如酪氨酸、苯丙氨酸、色氨酸、组氨酸)。在基因克隆操作中,常常需要设计合适的酶切位点,这势必在所表达的蛋白末端引入一个或多个不相干的残基,而这并不影响目的蛋白的活性。又如为了促进重组蛋白的表达,常常需要将一些氨基酸残基添加至重组蛋白的n-末端、c-末端或该蛋白内的其它合适区域内。应理解,这些氨基酸残基的存在不会影响到所得多肽的活性。因此,本发明也包括在产溶剂梭菌中过表达在seqidno:2、6或10所示的氨基酸序列的c末端和/或n末端添加一个或数个氨基酸所述氨基酸残基所得的氨基酸序列。可通过向产溶剂梭菌中转入含本文ccpa蛋白的编码基因的表达载体来实现产溶剂梭菌中ccpa蛋白的过表达。通常优选的是将含丙酮丁醇梭菌ccpa蛋白的编码基因的表达载体转入丙酮丁醇梭菌,将含拜氏梭菌ccpa蛋白的编码基因的表达载体转入拜氏梭菌 和将含扬氏梭菌ccpa蛋白的编码基因的表达载体转入扬氏梭菌,但应理解,在产溶剂梭菌中转入含异源ccpa编码基因的表达载体也能提高该产溶剂梭菌的发酵性能,如在丙酮丁醇梭菌中转入含来自拜氏梭菌和/或扬氏梭菌ccpa蛋白的编码基因的表达载体,或者在拜氏梭菌中转入含来自丙酮丁醇梭菌和/或扬氏梭菌ccpa蛋白的编码基因的表达载体,或者在扬氏梭菌中转入含来自丙酮丁醇梭菌和/或拜氏梭菌ccpa蛋白的编码基因的表达载体。同时,应理解的是,可将含来自不同产溶剂梭菌ccpa蛋白的编码基因的表达载体转入同一产溶剂梭菌菌株中,例如,可在丙酮丁醇梭菌中转入含丙酮丁醇梭菌ccpa蛋白的编码基因的表达载体、含拜氏梭菌ccpa蛋白的编码基因的表达载体和含扬氏梭菌ccpa蛋白的编码基因的表达载体中的一种、任意两种或全部三种。或者,也可提供能同时表达来自数种产溶剂梭菌的ccpa蛋白的表达载体,并将其转入感兴趣的产溶剂梭菌中。本文ccpa蛋白的编码基因的例子包括但不限于seqidno:1所示的编码丙酮丁醇梭菌ccpa蛋白的核苷酸序列,seqidno:5所示的编码拜氏梭菌ccpa蛋白的核苷酸序列,和seqidno:9所示的编码扬氏梭菌ccpa蛋白的核苷酸序列。根据ncbiblastn,seqidno:1与seqidno:9之间的序列相同性为74%。因此,本发明也包括与seqidno:1、5或9所示的核苷酸序列具有至少70%、至少75%、至少80%、至少85%、至少90%、至少95%、至少97%或至少99%的序列相同性的核苷酸序列。优选的是,这些核苷酸序列编码的氨基酸序列具有本文所述的ccpa蛋白的生物学功能。表达载体的一个重要特征是通常含有复制起点、启动子、标记基因和翻译控制元件。表达载体还可包括翻译起始用的核糖体结合位点和转录终止子。表达载体中,本文的编码序列和上述调控序列中的一种、多种或全部操作性连接在一起,用于在宿主细胞中表达本文的ccpa蛋白。重组表达载体可以是能够方便地经受重组dna方法并且可导致本文的编码序列表达的任何载体,如质粒或病毒,包括但不限于细菌质粒、噬菌体、酵母质粒、植物细胞病毒、哺乳动物细胞病毒如腺病毒、逆转录病毒或其它载体。只要能在宿主体内复制和稳定,任何质粒和载体都可以用。载体的选择一般取决于载体与其中被导入该载体的宿主细胞的相容性。该载体可以是线性或闭合的环形质粒。载体可以是自主复制的载体,即作为染色体外实体存在,其复制不依赖于染色体复制。这类载体包括质粒、染色体外元件、微型染色体或人工染色体。载体可包含用于保证自我复制的任何方式。或者,载体可以是当被导入宿主细胞时整合到基因组中并且与其已经被整合进入的染色体一起复制的载体。合适的启动子可以被转入了本发明表达载体的宿主细胞所识别,是在所选择的宿主 细胞中显示转录活性的任何核苷酸序列,包括突变的、截短的和杂合启动子,并且可以从编码与该宿主细胞同源或异源的胞外或胞内多肽的基因获得。启动子的代表性例子有:大肠杆菌的lac或trp启动子;λ噬菌体pl启动子;真核启动子包括cmv立即早期启动子、hsv胸苷激酶启动子、早期和晚期sv40启动子、反转录病毒的ltrs和其它一些已知的可控制基因在原核或真核细胞或其病毒中表达的启动子。示例性的启动子序列包括thl启动子和ptb启动子。seqidno:3示出了适用于本发明的thl启动子的核苷酸序列例子;seqidno:7示出了适用于本发明的ptb启动子的核苷酸序列例子。合适的转录终止子是宿主细胞识别的用以终止转录的序列。终止子可与编码序列的3′末端可操作连接。在选择的宿主细胞中有功能的任何终止子都可用于本发明。例如,用于细菌宿主的优选终止子可以是来自t7噬菌体的终止子。合适的标记基因的产物提供对抗生素或病毒的抗性、对重金属的抗性、原养型至营养缺陷型等。可采用本领域已知的载体来构建本发明的表达载体,如pimp1载体。可采用本领域技术人员熟知的方法构建含本文所述的编码序列和合适的转录/翻译控制信号的表达载体。这些方法包括体外重组dna技术、dna合成技术、体内重组技术等。本文因此包括一种表达载体,该表达载体用于在产溶剂梭菌中表达本文所述的ccpa蛋白。具体而言,该表达载体含有与编码本文所述的ccpa蛋白的核酸序列操作性连接的调控序列。调控序列包括前文所述的复制起点、启动子、标记基因、翻译控制元件、翻译起始用的核糖体结合位点和转录终止子中的一种、多种或全部。优选的,所述ccpa蛋白如seqidno:2、6或10所示。或者,所述核酸序列如seqidno:1、5或9所示。启动子可以是前文所述的thl启动子或ptb启动子;优选的,其核酸序列分别如seqidno:3和7所示。作为例子,本文表达载体的核酸序列可如seqidno:4、8或11所示。本文也包括宿主细胞,其转入了本文所述的表达载体。宿主细胞可以是制备本文所述的表达载体中使用到或用于保存本文的表达载体的宿主细胞,例如大肠杆菌细胞。宿主细胞也可以是本文所述的产溶剂梭菌,尤其是丙酮丁醇梭菌、拜氏梭菌和扬氏梭菌。因此,本文也包括一种产溶剂梭菌,其转入了本文所述的表达载体。优选的是,与未转入本文所述的编码序列的对照相比,本文的产溶剂梭菌具有提高的糖利用能力和/或酸回用产溶剂能力。举例而言,在相同发酵条件下,与未转入本文所述的编码序列的对照相比,发酵结束时,本文的产溶剂梭菌具有以下一个、任意多个或全部特征:(1)生物量提高至少10%,如至少15%、至少20%等;(2)葡萄糖利用率提高至少5%,如至少8%、至少10%、至少15%、至少20%、至少25%、至少30%等;(3)总溶剂(丙酮+丁醇+乙醇)产量提高至少5%,如至少10%、至少13%、至少15%、至少20%、至少25%、至少30%等;(4)丙酮产量提高至少5%,如至少10%、至少13%、至少15%、 至少20%、至少25%等;(5)丁醇产量提高至少5%,如至少10%、至少13%、至少15%、至少20%、至少25%等;和(6)乙醇产量提高至少15%,如至少20%、至少25%、至少30%等。将载体转入宿主细胞的方式是本领域周知的。例如,当宿主为原核生物如大肠杆菌时,在指数生长期后收获能吸收dna的感受态细胞,然后用cacl2法处理,所用的步骤在本领域众所周知。另一种方法是使用mgcl2。如果需要,转化也可用电穿孔的方法进行。当宿主是真核生物,可选用如下的dna转染方法:磷酸钙共沉淀法,常规机械方法如显微注射、电穿孔、脂质体包装等。优选地,转入了本文所述表达载体的宿主细胞能够稳定地表达本文所述的ccpa蛋白。本文还包括提高产溶剂梭菌生产丙酮、丁醇和/或乙醇的能力的方法,所述方法包括使产溶剂梭菌中的本文所述的ccpa蛋白过表达的步骤。过表达ccpa蛋白的方法可包括,将表达ccpa蛋白的载体,尤其是本文所述的表达载体,转入所述产溶剂梭菌中。本发明还包括一种制备具有提高的糖利用能力和/或酸回用产溶剂能力的产溶剂梭菌的方法,所述方法包括对所述产溶剂梭菌进行基因工程操作,以使其ccpa蛋白过表达的步骤。所述基因工程操作包括但不限于将表达ccpa蛋白的载体,尤其是本文所述的表达载体,转入所述产溶剂梭菌中。采用本发明上述方法获得的产溶剂梭菌优选具有前文所述的一个、任意多个或全部特征。下文将以具体实施例的方式阐述本发明。下列实施例中未注明具体条件的实验方法,通常按照常规条件如sambrook等,《分子克隆:实验室指南》(美国纽约州:冷泉港实验室出版社,1989)所述的条件,或按照制造厂商所建议的条件进行。对于试剂的用法和用量,除非另有说明,否则按照常规的用法和用量使用。实施例1:丙酮丁醇梭菌(c.acetobutylicum)中过表达ccpa提升菌株的发酵性能实验方法:通过在野生型丙酮丁醇梭菌中过表达其自身来源的ccpa基因,在p2培养基中进行发酵,验证发酵表型。实验材料:1)cgm培养基:(nh4)2so4(2g/l),k2hpo4(1g/l),kh2po4(0.5g/l),mgso4·7h2o(100mg/l),feso4·7h2o(15mg/l),cacl2(10mg/l),mnso4.h2o(10mg/l),cocl2(20mg/l),znso4(20mg/l),胰蛋白胨(2g/l),酵母抽提物(1g/l)以及葡萄糖(20g/l)。2)p2培养基:7%葡萄糖(w/v),k2hpo4(0.5g/l),kh2po4(0.5g/l),ch3coonh4 (2.2g/l),mgso4·7h20(200mg/l),mnso4·h20(10mg/l),nacl(10mg/l),feso4·7h20(10mg/l),对氨基苯甲酸(1mg/l),硫胺(1mg/l)以及生物素(10μg/l)。3)质粒pimp1-pthl由美国特拉华大学的eleftheriosterrypapoutsakis教授赠予。实验步骤:1)ccpa过表达质粒(pimp1-pthl-ccpacac)的构建:以丙酮丁醇梭菌基因组为模板,利用引物cac3037-for/cac3037-rev进行pcr扩增,经过琼脂糖电泳以及胶回收过程获得片段ccpa(cac3037)(seqidno:1),之后分别利用bamhi以及ecori对ccpa片段以及pimp1-pthl质粒进行酶切,酶切3h后利用胶回收试剂盒纯化回收酶切过的载体骨架以及ccpa片段,之后利用solutioni连接酶将酶切过的载体骨架以及ccpa片段进行重组连接。16℃连接4h后,将连接产物转化top10感受态,涂布含有amp+(100μg/ml)抗性的lb固体平板。第二天挑取平板上长出的菌落进行菌落pcr验证,将验证正确的单菌落转接至含有amp+(100μg/ml)抗性的lb液体培养基中,培养过夜。第二天,利用质粒提取试剂盒抽取质粒,经bamhi/ecori酶切验证正确后,将该质粒送测序公司测序,测序结果正确即获得pimp1-pthl-ccpacac质粒(序列如seqidno:4所示)。2)ccpa过表达质粒(pimp1-pthl-ccpacac)电转入丙酮丁醇梭菌中:将pimp1-pthl-ccpacac以及相应的对照质粒pimp1-pthl分别电转至野生型丙酮丁醇梭菌中得到824-ccpa(ccpa过表达菌株)以及824-p(对照菌株)菌株。3)ccpa过表达菌株及其对照菌株的发酵验证:将电转得到的824-ccpa以及824-p菌株分别接种至cgm培养基中进行过夜培养,12h后将菌液转接至p2培养基中进行发酵验证。发酵条件:p2培养基(30ml),5%的接种量(v/v),红霉素(10mg/l)。4)824-ccpa以及824-p菌株中ccpa基因的转录分析:利用p2培养基对824-ccpa以及824-p菌株进行发酵,分别在25h,48h,64h以及72h进行取样,液氮中研磨,保存于trizol(invitrogen)中,震荡均匀后离心(4℃,12000rpm,10min),取上清液加入200μl氯仿,涡旋15s,冰上放置5min;之后离心(4℃,12000rpm×10min)取上清;加入等体积的异丙醇,混匀,-20℃沉淀30min;4℃,12000rpm×15min,以1ml枪头吸弃上清液;加入75%乙醇1ml,4℃12000rpm×5min,以1ml枪头吸弃上清液。12000rpm再离心一次,用200ul枪吸掉剩余液体,晾干;加入50μl无rnase的水溶解rna,60℃×10min促进rna溶解,混合均匀后放冰上。之后利用primescriptrtreagentkit(takara)将rna反转录得到cdna,之后采用myiq2双色实时荧光定量pcr检测仪(bio-rad) 进行定量pcr,反应条件为:95℃反应2min,之后进行40个循环的如下反应:95℃反应15s,55℃反应20s,最后在72℃反应20s。qrt-pcr实验中利用已报道的cac2679(pullulanase)基因作为内参。qrt-pcr实验所用引物见下。实验所用引物:实验所用菌株及质粒:实验结果:通过在丙酮丁醇梭菌中利用pthl过表达来源于其自身ccpa基因后,在p2培养基中进行发酵发现:菌株的生长明显优于对照菌株,相对应的菌株的糖利用能力以及酸回用产溶剂能力均明显提升,其中发酵至72h时,824-ccpa较824-p多利用9.16g葡萄糖,多 合成2.15g丁醇,0.51g丙酮,0.7g乙醇以及3.36g总溶剂(图1)。发酵终点(72h)的发酵产物含量见表1。进一步通过qrt-pcr对824-p以及824-ccpa菌株中的ccpa的转录情况进行分析发现:过表达ccpa后,824-ccpa菌株中ccpa基因的转录水平明显高于824-p菌株(在25h,48h,64h以及72h824-ccpa较824-p菌株ccpa基因的转录量分别提升了4879倍,1574倍,493倍以及588倍),见图2。表1实施例2:拜氏梭菌(clostridiumbeijerinckii)中过表达ccpa提升菌株的发酵性能实验方法:通过在拜氏梭菌中过表达其自身来源的ccpa基因,在mp2培养基中进行发酵,验证发酵表型。实验材料:1)mp2培养基:7%葡萄糖(w/v),k2hpo4(0.5g/l),kh2po4(0.5g/l),ch3coona(6.56g/l),(nh4)2so4(2g/l),mgso4·7h20(200mg/l),mnso4·h20(10mg/l),nacl(10mg/l),feso4·7h20(10mg/l),对氨基苯甲酸(1mg/l),硫胺(1mg/l)以及生物素(10μg/l)。2)质粒pimp1-pptb:来源于pimp1-pthl质粒。实验步骤:1)ccpa过表达质粒的构建:以丙酮丁醇梭菌基因组为模板,利用引物pptb-for/pptb-rev扩增ptb启动子,之后利用psti/bamhi对ptb启动子以及pimp1-pthl质粒进行双酶切后,经过琼脂糖电泳以及胶回收获得酶切过的ptb启动子以及酶切过的pimp1-pthl质粒骨架。最后,利用solutioni连接酶将酶切过的pimp1-pthl质粒骨架以及ptb启动子进行重组连接得到pimp1-pptb质粒。以拜氏梭菌基因组为模板,利用引物cbei0047-for/cbei0047-rev进行pcr扩增,经过琼脂糖电泳以及胶回收过程获得片段ccpa(cbei0047)(seqidno:5),之后分别利用bamhi以及sali对ccpa片段以及pimp1-pptb质粒进行酶切,酶切3h后利用胶回收试剂盒纯化回收酶切过的载体骨架以及ccpa片段,之后利用solutioni连接酶将酶切过的载体骨架以及ccpa片段进行重组连接。16℃连接4h后,将连接产物转化top10感受态,涂布含有amp+(100μg/ml)抗性的lb固体平板。第二天挑取平板上长出的菌落进行菌落pcr 验证,将验证正确的单菌落转接至含有amp+(100μg/ml)抗性的lb液体培养基中,培养过夜。第二天,利用质粒提取试剂盒抽取质粒,经bamhi/sali酶切验证正确后,将该质粒送测序公司测序,测序结果正确即获得pimp1-pptb-ccpacbe质粒(seqidno:8)。2)ccpa过表达质粒(pimp1-pptb-ccpacbe)电转入拜氏梭菌中:将pimp1-pptb-ccpacbe以及相应的对照质粒pimp1-pptb分别电转至野生型拜氏梭菌中得到8052-ccpa(ccpa过表达菌株)以及8052-p(对照菌株)菌株。3)ccpa过表达菌株及其对照菌株的发酵验证:将电转得到的8052-ccpa以及8052-p菌株分别接种至cgm培养基中进行过夜培养,12h后将菌液转接至mp2培养基中进行发酵验证。发酵条件:mp2培养基(30ml),5%的接种量(v/v),红霉素(2mg/l)。4)8052-ccpa以及8052-p菌株中ccpa基因的转录分析:利用1lp2培养基对8052-ccpa以及8052-p菌株进行发酵,分别在16h,29h,40h以及64h进行取样,液氮中研磨,保存于trizol(invitrogen)中,震荡均匀后离心(4℃,12000rpm,10min),取上清液加入200μl氯仿,涡旋15s,冰上放置5min;之后离心(4℃,12000rpm×10min)取上清;加入等体积的异丙醇,混匀,-20℃沉淀30min;4℃,12000rpm×15min,以1ml枪头吸弃上清液;加入75%乙醇1ml,4℃12000rpm×5min,以1ml枪头吸弃上清液。12000rpm再离心一次,用200ul枪吸掉剩余液体,晾干;加入50μl无rnase的水溶解rna,60℃×10min促进rna溶解,混合均匀后放冰上。之后利用primescriptrtreagentkit(takara)将rna反转录得到cdna,之后采用myiq2双色实时荧光定量pcr检测仪(bio-rad)进行定量pcr,反应条件为:95℃反应2min,之后进行40个循环的如下反应:95℃反应15s,55℃反应20s,最后在72℃反应20s。qrt-pcr实验中利用16s基因作为内参。qrt-pcr实验所用引物见下表。实验所用引物:实验所用菌株及质粒:菌株或质粒基因型描述来源拜氏梭菌8052-patcc824,携带pimp1-pptb质粒本研究拜氏梭菌8052-ccpaatcc824,携带pimp1-pptb-ccpacbe质粒本研究大肠杆菌top10常规的克隆宿主菌invitrogenpimp1-pptbccpa(cbei0047)过表达中使用的对照载体,衍生自pimp1-pthl本研究pimp1-pptb-ccpacbeccpa(cbei0047)过表达载体,衍生自pimp1-pptb本研究实验结果:通过在拜氏梭菌中利用pptb过表达来源于其自身ccpa基因后,在mp2培养基中进行发酵发现:菌株的生长较对照菌株明显提升,与此同时菌株的糖利用能力以及酸回用产溶剂能力均明显提升,其中发酵至120h时,8052-ccpa较8052-p多利用19.52g葡萄糖,多合成4.01g丁醇,1.35g丙酮,0.31g乙醇以及5.67g总溶剂(图3)。发酵终点(120h)的发酵产物含量见表2。进一步通过qrt-pcr对8052-p以及8052-ccpa菌株中的ccpa的转录情况进行分析发现:过表达ccpa后,8052ccpa菌株中ccpa基因的转录水平明显高于8052-p菌株(在16h,29h,40h以及64h8052-ccpa较8052-p菌株ccpa基因的转录量分别提升了16倍,32倍,14倍以及8倍),见下图4。表2实施例3:扬氏梭菌(c.ljungdahlii)中过表达ccpa提升菌株的发酵性能实验方法:通过在野生型扬氏梭菌中过表达自身来源的ccpa基因,在atcc1754 培养基中进行发酵,验证发酵表型。实验材料:1)ytf培养基:10g/l酵母抽提物,16g/l胰蛋白胨,4g/l氯化钠,5g/l果糖,0.24g/ll-半胱氨酸,最终调节ph至6.0。2)atcc1754培养基(l):矿质元素贮存液30ml,维生素贮存液1ml,微量元素贮存液2ml,酵母抽提物0.5g,2-吗啉乙磺酸5g,还原剂5ml,最终调节ph至6.0。3)质粒pxy1-catp-pthl:由穿梭质粒pxy1改造而成。实验步骤:1)ccpa过表达质粒(pxy1-catp-pthl-ccpacl)的构建:以扬氏梭菌基因组为模板,利用引物clju1900-for/clju1900-rev进行pcr扩增,经过琼脂糖电泳以及胶回收过程获得片段ccpa(clju_c01900)(seqidno:9),之后分别利用bamhi以及smai对ccpa片段以及pxy1-catp-pthl质粒进行酶切,酶切3h后利用胶回收试剂盒纯化回收酶切过的载体骨架以及ccpa片段,之后利用solutioni连接酶将酶切过的载体骨架以及ccpa片段进行重组连接。16℃连接4h后,将连接产物转化top10感受态,涂布含有amp+(100μg/ml)抗性的lb固体平板。第二天挑取平板上长出的菌落进行菌落pcr验证,将验证正确的单菌落转接至含有amp+(100μg/ml)抗性的lb液体培养基中,培养过夜。第二天,利用质粒提取试剂盒抽取质粒,经bamhi/smai酶切验证正确后,将该质粒送测序公司测序,测序结果正确即获得pxy1-catp-pthl-ccpacl质粒(seqidno:11)。2)ccpa过表达质粒(pxy1-catp-pthl-ccpacl)电转入扬氏梭菌中:将pxy1-catp-pthl-ccpacl以及相应的对照质粒pxy1-catp-pthl分别电转至野生型扬氏梭菌中得到cl-ccpa(ccpa过表达菌株)以及cl-p(对照菌株)菌株。3)ccpa过表达菌株及其对照菌株的发酵验证:将电转得到的cl-ccpa以及cl-p菌株分别接种至ytf培养基中进行过夜培养,12h后将菌液转接至atcc1754培养基中进行发酵验证。发酵条件:atcc1754培养基(30ml),碳源为含碳气体,5%的接种量(v/v),甲砜氯霉素(5mg/l)。4)cl-ccpa以及cl-p菌株中ccpa基因的转录分析:利用800mlatcc1754培养基对cl-ccpa以及cl-p菌株进行发酵,分别在36h,60h以及84h进行取样,液氮中研磨,保存于trizol(invitrogen)中,震荡均匀后离心(4℃,12000rpm,10min),取上清液加入200μl氯仿,涡旋15s,冰上放置5min;之后离心(4℃,12000rpm×10min)取上清;加入等体积的异丙醇,混匀,-20℃沉淀30min; 4℃,12000rpm×15min,以1ml枪头吸弃上清液;加入75%乙醇1ml,4℃12000rpm×5min,以1ml枪头吸弃上清液。12000rpm再离心一次,用200ul枪吸掉剩余液体,晾干;加入50μl无rnase的水溶解rna,60℃×10min促进rna溶解,混合均匀后放冰上。之后利用primescriptrtreagentkit(takara)将rna反转录得到cdna,之后采用myiq2双色实时荧光定量pcr检测仪(bio-rad)进行定量pcr,反应条件为:95℃反应2min,之后进行40个循环的如下反应:95℃反应15s,55℃反应20s,最后在72℃反应20s。qrt-pcr实验中利用已报道的clju_c13280(reca)基因作为内参。qrt-pcr实验所用引物见下。实验所用引物:实验所用菌株及质粒:菌株或质粒基因型描述来源扬氏梭菌cl-ccpadsm13528,携带pxy1-catp-pthl-ccpacl质粒本研究扬氏梭菌cl-pdsm13528,携带pxy1-catp-pthl质粒本研究大肠杆菌top10常规的克隆宿主菌invitrogenpxy1-catp-pthlccpa(clju01900)过表达中使用的对照载体,衍生自pimp1本研究pxy1-catp-pthl-ccpaclccpa(clju01900)过表达载体,衍生自pxy1-pthl本研究实验结果:通过在扬氏梭菌中利用pthl过表达来源于自身ccpa基因后,在atcc1754培养基中进行发酵发现:菌株的生长明显优于对照菌株,相对应的菌株产溶剂能力明显提升,其中发酵至96h时,cl-ccpa较cl-p的生物量明显提高33%,乙醇产量增加1g,乙酸产量增加0.6g左右。发酵生长曲线及溶剂产量见图5。进一步通过qrt-pcr对cl-p以及cl-ccpa菌株中的ccpa的转录情况进行分析发现:cl-ccpa菌株中ccpa基因的转录水平明显高于cl-p菌株(在48h,72h时cl-ccpa较cl-p菌株ccpa基因的转录量分别提升了9倍以及4倍),见图6。当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1