黑曲霉菌株W35及其在降解赭曲霉毒素A中的应用的制作方法
本发明涉及微生物学及生物降解领域,具体地说,涉及黑曲霉菌株w35及其在降解赭曲霉毒素a中的应用。
背景技术:
赭曲霉毒素a(ota)污染粮谷类、干果、葡萄及葡萄酒、咖啡、可可和巧克力、中草药、调味料、罐头食品、油、橄榄、豆制品、啤酒、茶叶等多种农作物、食品及饲料,对人类的健康构成了极大的威胁。是继黄曲霉毒素后又一个引起世界广泛关注的霉菌毒素。ota的脱毒方法主要有三种:物理方法,化学方法和生物方法。利用微生物或酶制剂降解的生物脱毒方法成为控制赭曲霉毒素污染的理想方法。
技术实现要素:
本发明的目的是提供黑曲霉菌株w35及其在降解赭曲霉毒素a中的应用。
为了实现本发明目的,本发明的黑曲霉w35分离自落叶丛,并采用含ota的yes培养基进行筛选得到的。
菌株w35的微生物学特征如下:黑曲霉属于半知菌亚门,半知菌纲,壳霉目,杯霉科,黑曲霉属真菌中的一个常见种。分生孢子梗自基质中伸出,直径15~20μm,长约1~3mm,黑曲霉壁厚而光滑。顶部形成球形顶囊,其上全面覆盖一层梗基和一层小梗,小梗上长有成串褐黑色的球状,直径2.5~4.0μm。分生孢子头球状,直径700~800μm,褐黑色。蔓延迅速,初为白色,后变成鲜黄色直至黑色厚绒状,背面无色或中央略带黄褐色。分生孢子头褐黑色放射状,分生孢子梗长短不一。顶囊球形,双层小梗。分生孢子褐色球形。
菌株w35的理化特征如下:广泛分布于世界各地的粮食、植物性 产品和土壤中。是重要的发酵工业菌种,可生产淀粉酶、酸性蛋白酶、纤维素酶、果胶酶、葡萄糖氧化酶、柠檬酸、葡糖酸和没食子酸等。有的菌株还可将羟基孕甾酮转化为雄烯。生长适温37℃,最低相对湿度为88%,能引致水分较高的粮食霉变和其他工业器材霉变。
菌株w35的18srdna序列如seqidno:1所示,将其18srdna序列在genbank中进行比对,并构建菌株w35的系统进化树(图1)。
基于以上信息,将菌株w35鉴定为黑曲霉(aspergillusniger)。该菌现已保藏于中国微生物菌种保藏管理委员会普通微生物中心,地址北京市朝阳区北辰西路1号院3号,中国科学院微生物研究所,邮编100101,保藏编号cgmccno.12104,保藏日期2016年01月28日。
本发明还提供黑曲霉w35在降解赭曲霉毒素a中的应用。
在本发明的一个具体实施方式中,所述应用包括以下步骤:
将含105-107个孢子的黑曲霉w35孢子悬液接种于含有1-6μg/ml赭曲霉毒素a的500mlyes培养基中,接种量为0.5-3v/v%,于27℃-29℃静置培养13-19天;培养结束后,过滤去除菌丝体,所得上清再用0.45μm滤膜过滤,去除残留霉菌孢子,将500μl所得上清加至离心管中,同时加入终浓度为10-60g/l的赭曲霉毒素a,然后将离心管置于摇床上,36℃-38℃140-160rpm避光保温反应11-13h。
优选地,将含约106个孢子的黑曲霉w35孢子悬液接种于含有1μg/ml赭曲霉毒素a的500mlyes培养基中,接种量为2v/v%,于28℃静置培养14天;培养结束后,过滤去除菌丝体,所得上清再用0.45μm滤膜过滤,去除残留霉菌孢子,将500μl所得上清加至离心管中,同时加入浓度为10g/l的赭曲霉毒素a1μl,然后将离心管置于摇床上,37℃150rpm避光保温反应12h。
在本发明的另一个具体实施方式中,所述应用包括以下步骤:
将含105-107个孢子的黑曲霉w35孢子悬液接种于含有1-6μg/ml赭曲霉毒素a的500mlyes培养基中,接种量为0.5-3v/v%,于27℃-29 ℃静置培养13-19天;培养结束后,过滤去除菌丝体,向所得上清中加入硫酸铵固体,使硫酸铵的饱和度达到40%,4℃放置2h,12000rpm离心30min,沉淀用pbs溶液溶解,得溶液i;向溶液i中继续加入硫酸铵固体至硫酸铵饱和度达到60%,4℃放置2h,12000rpm离心30min,沉淀用pbs溶液溶解,得溶液ii;向溶液ii中继续加入硫酸铵固体至硫酸铵饱和度达到80%,4℃放置2h,12000rpm离心30min,沉淀用pbs溶液溶解,得粗酶液;将500μl粗酶液加至离心管中,同时加入终浓度为10-60g/l的赭曲霉毒素a,然后将离心管置于摇床上,36℃-38℃140-160rpm避光保温反应11-13h。
优选地,将含约106个孢子的黑曲霉w35孢子悬液接种于含有1μg/ml赭曲霉毒素a的500mlyes培养基中,接种量为2v/v%,于28℃静置培养14天;培养结束后,过滤去除菌丝体,向所得上清中加入硫酸铵固体,使硫酸铵的饱和度达到40%,4℃放置2h,12000rpm离心30min,沉淀用pbs溶液溶解,得溶液i;向溶液i中继续加入硫酸铵固体至硫酸铵饱和度达到60%,4℃放置2h,12000rpm离心30min,沉淀用pbs溶液溶解,得溶液ii;向溶液ii中继续加入硫酸铵固体至硫酸铵饱和度达到80%,4℃放置2h,12000rpm离心30min,沉淀用pbs溶液溶解,得粗酶液;将500μl粗酶液加至离心管中,同时加入终浓度为10g/l的赭曲霉毒素a,然后将离心管置于摇床上,37℃150rpm避光保温反应12h。
本发明还提供黑曲霉w35在制备赭曲霉毒素a生物降解剂中的应用。
本发明还提供由黑曲霉w35制备的赭曲霉毒素a生物降解剂,其活性成分为黑曲霉w35的发酵液、由其发酵液制备的粗酶液、菌体裂解液或孢子悬液。
本发明还提供由黑曲霉w35制备的酶制剂。
本发明进一步提供黑曲霉w35在受到赭曲霉毒素a污染的环境修 复中的应用。
本发明首次发现了能够降解赭曲霉毒素a的黑曲霉菌株w35,利用该菌的生物代谢、酶系统的作用,可简单、高效、快速地降解环境及水体中的赭曲霉毒素a。具体优点如下:
(一)黑曲霉w35降解赭曲霉毒素a的效率高、特异性强,且本解毒反应为不可逆降解。
(二)利用黑曲霉w35降解赭曲霉毒素a,解毒活性高,作用专一,作用效果温和。
(三)为后续研究黑曲霉w35的降解物质,以及降解酶的分离、纯化、鉴定提供了可能。
(四)提供一种宝贵的可高效降解赭曲霉毒素a的微生物资源。
附图说明
图1为本发明根据黑曲霉w35的18srdna序列构建的系统进化树。
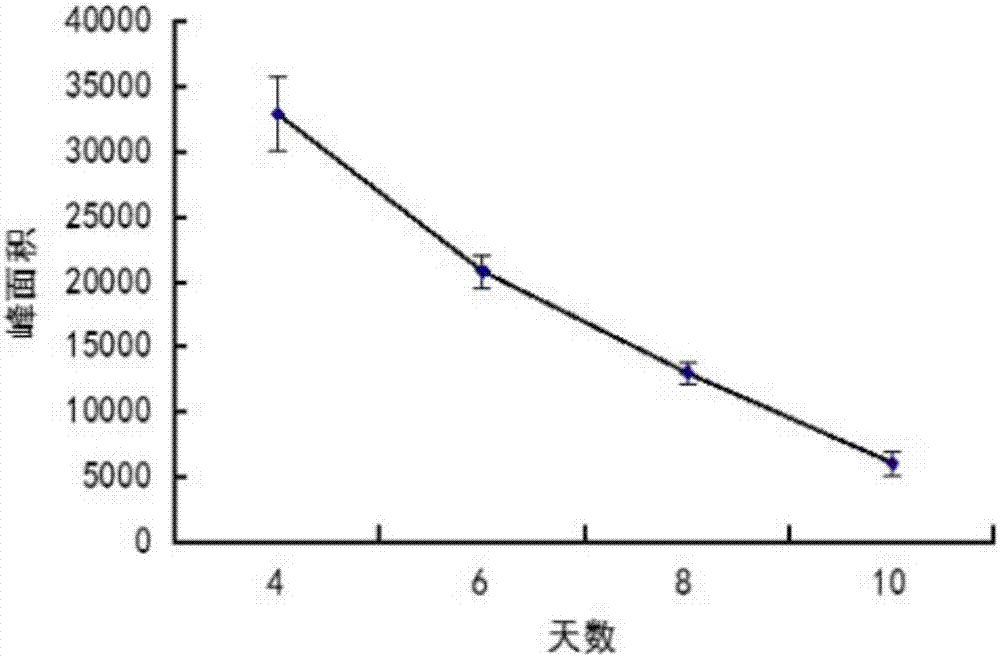
图2为本发明实施例1中菌株w35培养基中ota的含量变化。
图3为本发明实施例5中不同反应时间对ota降解率的影响。
图4为本发明实施例5中不同ph值对ota降解率的影响。
具体实施方式
以下实施例用于说明本发明,但不用来限制本发明的范围。若未特别指明,实施例均按照常规实验条件,如sambrook等分子克隆实验手册(sambrookj&russelldw,molecularcloning:alaboratorymanual,2001),或按照制造厂商说明书建议的条件。
本发明中使用的yes培养基中含有15%蔗糖和2%酵母提取物。
实施例1黑曲霉w35的筛选与鉴定
1、赭曲霉毒素a脱毒菌株的筛选
(1)在yes培养基中加入ota标准品,使得培养基中ota的浓度为2μg/ml。
(2)从落叶丛中分离出的霉菌,制备孢子悬液,将含约106个孢子的孢子悬液1ml接种于5ml上述含ota的yes培养基中,在10ml离心管中进行培养。设置两组平行。对照组接种1ml无菌水。28℃静置培养10天。
(3)从第4天起,每隔2天提取5ml培养基中的ota,hplc测定ota的含量。
(4)ota提取及hplc检测:通过离心去除真菌菌落,培养基用2m的盐酸1ml酸化处理,调ph至1~2,加入2ml的三氯甲烷,充分振荡,5000rpm离心10min,取下层三氯甲烷层,转移至新的离心管中。重复抽提两次,抽提液50℃氮吹干,4℃储存用于hplc检测。
hplc检测条件为流动相乙腈:水:乙酸=100:100:1(体积比);流动相流速1ml/min;c18色谱柱;激发波长333nm,检测波长460nm;上样量为15μl;检出限为0.02ng。
筛选获得对ota降解能力最好的菌株,命名为w35。菌株w35培养基中ota的含量变化见图2。
2、高效降解ota霉菌的鉴定
(1)18srdna鉴定
提取菌株w35的总dna,以其为模板,利用its1、its4为引物进行pcr扩增,得到长度为600bp左右的扩增产物,将扩增产物测序,结果如seqidno:1所示。
将测得的序列与genbank中的序列进行比对,菌株w35与黑曲霉(aspergillusniger)菌株s5p3、f5a1等有100%的同源性。从genbank数据库检索出与所测its片段序列同源性较高的序列,使用mega6.0.6软件分别构建菌株w35的系统进化树(图1)。
(2)菌株w35的微生物学特征如下:
黑曲霉属于半知菌亚门,半知菌纲,壳霉目,杯霉科,黑曲霉属真菌中的一个常见种。分生孢子梗自基质中伸出,直径15~20μm,长 约1~3mm,黑曲霉壁厚而光滑。顶部形成球形顶囊,其上全面覆盖一层梗基和一层小梗,小梗上长有成串褐黑色的球状,直径2.5~4.0μm。分生孢子头球状,直径700~800μm,褐黑色。蔓延迅速,初为白色,后变成鲜黄色直至黑色厚绒状,背面无色或中央略带黄褐色。分生孢子头褐黑色放射状,分生孢子梗长短不一。顶囊球形,双层小梗。分生孢子褐色球形。
(3)菌株w35的理化特征如下:
广泛分布于世界各地的粮食、植物性产品和土壤中。是重要的发酵工业菌种,可生产淀粉酶、酸性蛋白酶、纤维素酶、果胶酶、葡萄糖氧化酶、柠檬酸、葡糖酸和没食子酸等。有的菌株还可将羟基孕甾酮转化为雄烯。生长适温37℃,最低相对湿度为88%,能引致水分较高的粮食霉变和其他工业器材霉变。
基于以上信息,将高效降解ota的菌株w35鉴定为黑曲霉。
实施例2黑曲霉w35的培养及其胞外代谢上清的获得
将含约106个孢子的黑曲霉w35孢子悬液接种于含有1μg/ml赭曲霉毒素a的500mlyes培养基中,接种量为2v/v%,于28℃静置培养14天。培养结束后,用4层纱布过滤去除菌丝体,所得上清再用0.45μm滤膜过滤,去除残留霉菌孢子,所得上清用于赭曲霉毒素降解实验及硫酸铵分级沉淀。
实施例3黑曲霉w35的胞外上清对赭曲霉毒素a的降解作用
将500μl实施例2所得上清加至2ml离心管中,同时加入终浓度为1μg/ml的赭曲霉毒素a,然后将离心管用锡箔纸包裹,置于摇床上,37℃150rpm避光保温反应12h。以500μl的yes培养基加入同等的ota作为对照组。
首先,向离心管中加入1滴1m的hcl,调ph至1~2。加入500μl三氯甲烷,5000rpm离心10min,取出下层三氯甲烷层。为避免取出中间层,取出400μl的三氯甲烷。50℃空气浴氮吹至干,加入500μl100% 分析纯甲醇,过0.22μm的有机系滤膜,避光保存于-20℃。最后,用hplc检测ota的残留量。hplc检测条件同实施例2所述。
赭曲霉毒素a的降解率计算:
以对照中的ota含量为100%,则降解率计算公式为:
降解率(%)=(1-对照峰面积/样品峰面积)×100
结果表明,培养上清中的ota降解率达78%。
实施例4黑曲霉w35胞外上清硫酸铵分级沉淀产物的获得
向实施例2所得上清中加入硫酸铵固体,使硫酸铵的饱和度达到40%,4℃放置2h,12000rpm离心30min,沉淀用pbs溶液溶解,得溶液i。
向溶液i中继续加入硫酸铵固体至硫酸铵饱和度达到60%,4℃放置2h,12000rpm离心30min,沉淀用pbs溶液溶解,得溶液ii。
向溶液ii中继续加入硫酸铵固体至硫酸铵饱和度达到80%,4℃放置2h,12000rpm离心30min,沉淀用pbs溶液溶解,得粗酶液。
实施例5黑曲霉w35胞外上清硫酸铵分级沉淀产物对赭曲霉毒素a的降解作用
将500μl粗酶液加至2ml离心管中,同时加入终浓度为1μg/ml的赭曲霉毒素a,然后将离心管置于摇床上,37℃150rpm避光保温反应12h。以500μl的yes培养基加入同等的ota作为对照组。
首先,向离心管中加入1滴1m的hcl,调ph至1~2。加入500μl三氯甲烷,5000rpm离心10min,取出下层三氯甲烷层。为避免取出中间层,取出400μl的三氯甲烷。50℃空气浴氮吹至干,加入500μl100%分析纯甲醇,过0.22μm的有机系滤膜,避光保存于-20℃。最后,用hplc检测ota的残留量。hplc检测条件同实施例2所述。
赭曲霉毒素a的降解率计算:
以对照中的ota含量为100%,则降解率计算公式为:
降解率(%)=(1-对照峰面积/样品峰面积)×100
结果表明,与对照组相比,粗酶液能降解77.8%的ota。
实施例5不同反应时间、ph值对ota降解率的影响以及活性蛋白的初步分离纯化
实验方法:
1.不同反应时间对ota降解率的影响
(1)将菌株w35的发酵液透析以除去培养基中的蔗糖等物质。
(2)在500μl发酵液中,加入ota标准液使ota终浓度为6μg/ml。37℃,200rpm孵育12、24、36、48、60、72h。设置两个平行。
(3)加盐酸调节体系的ph值为1~2,加入500μl的三氯甲烷,5000rpm离心10min,取下层三氯甲烷层,转移至新的离心管中。
(4)氮吹至干加入40%的甲醇溶液,适当稀释至elisa试剂盒检测浓度范围内。
2.不同ph值对ota降解率的影响
(1)将菌株w35的发酵液透析以除去培养基中的蔗糖等物质。
(2)设置体积为500μlph值为6.5、7.5、8.5、9.5的四个不同反应体系,加入ota标准液使ota终浓度为6μg/ml。37℃,200rpm孵育48h。设置两个平行。
(3)加盐酸调节体系的ph值为1~2,加入500μl的三氯甲烷,5000rpm离心10min,取下层三氯甲烷层,转移至新的离心管中。
(4)氮吹至干加入40%的甲醇溶液,适当稀释至elisa试剂盒检测浓度范围内。
3.降解物质的初步分离纯化
(1)上柱样品的准备
①将菌株w35的发酵液经超滤管或冻干浓缩一定倍数。
②将发酵液使用50mm,ph值为7.5磷酸盐缓冲液多次透析,使发酵液的培养基完全置换成磷酸盐缓冲液。
(2)离子交换层析
①首先使系统中充满浓度为50mm,ph值为7.5的磷酸盐缓冲液,连接柱子。使用gehealthcare公司生产的q-sepharosefastflow强阴离子交换柱,填料为sepharose。
②用5倍柱体积的上述磷酸盐缓冲液冲洗柱子,流速为5ml/min。
③用5倍柱体积的洗脱液冲洗柱子,以除去柱子上的杂质。
④再用5~10倍柱体积的磷酸盐缓冲液平衡。
⑤将准备好的样品上柱,流速为5ml/min。
⑥使用至少5倍柱体积的磷酸盐缓冲液冲洗,以去除没有吸附于柱子的杂蛋白。
⑦线性梯度洗脱:将磷酸盐缓冲液和洗脱液分别置于梯度混合器的右、左两侧量杯中,打开阀门,使左、右两个量杯中的液体在右边的量杯中混合均匀,混合后的氯化钠呈线性梯度,终浓度为0.75mol/l。用10~20个柱体积洗脱柱子,分步收集器收集洗脱液。
⑧柱子重生:用5倍柱体积的洗脱液冲洗柱子,然后用5~10倍柱体积的磷酸盐缓冲液冲洗,封存柱子,4℃保存。
4.分离物质的活性验证
(1)取出分布收集到的每管液体各500μl,加入ota标准液使ota终浓度为6μg/ml。37℃,200rpm孵育48h。
(2)加盐酸调节体系的ph值为1~2,加入500μl的三氯甲烷,5000rpm离心10min,取下层三氯甲烷层,转移至新的离心管中。
(3)氮吹至干加入40%的甲醇溶液,适当稀释至elisa试剂盒检测浓度范围内。
结果分析:
1、不同反应时间对ota降解率的影响
从结果可以看出,随着时间的变化,ota的浓度逐渐降低,降解率随之升高。与ck相比,12h内发酵液可以降解37.6%的ota,24h 内可以降解60.9%的ota,36h内可以降解68.9%的ota,48h内可以降解75.5%的ota,60h内可以降解81.2%的ota,72h内可以降解83.6%的ota,ota的浓度及降解率如图3所示。ota浓度也随时间的变化不断减少,从0h的4.22μg/ml降低到72h的0.69μg/ml,48h后ota浓度趋于平稳。
2、不同ph值对ota降解的影响
ph值为6.5、7.5、8.5、9.5的四个不同反应体系中的ota均有不同程度地减少,降解率的结果如图4所示。从结果可以看出,ph值为6.5时,降解率为56.0%;ph值为7.5时,降解率最高,达到93.53%;ph值为8.5时,降解率为90.6%;ph值为9.5时,降解率为73.9%。整体来看,该在偏碱性条件下降解活性较高。
以上实验结果表明,黑曲霉菌株w35对赭曲霉毒素a具有良好的降解作用,对于商品化饲料中赭曲霉毒素a的降解以及在食品、农业的商业化ota脱毒方面应用前景广阔。
虽然,上文中已经用一般性说明及具体实施方案对本发明作了详尽的描述,但在本发明基础上,可以对之作一些修改或改进,这对本领域技术人员而言是显而易见的。因此,在不偏离本发明精神的基础上所做的这些修改或改进,均属于本发明要求保护的范围。
- 还没有人留言评论。精彩留言会获得点赞!