间苯二腈化合物及其制备方法和药物组合物与流程
本发明涉及医药领域,特别涉及一种2,4,5-三氯-6-((2,4,6-三氯苯胺基)间苯二腈化合物及其制备方法和含有上述2,4,5-三氯-6-((2,4,6-三氯苯胺基)间苯二腈化合物的药物组合物。
背景技术:
现有制备的2,4,5-三氯-6-((2,4,6-三氯苯胺基)间苯二腈化合物(如WO2013135147公开的)均具有一定的吸湿性,具有较低的堆密度与较差的流动性,不利于药物制剂的加工处理,并且具有潜在的药物稳定性问题,并不适用于医药领域。
技术实现要素:
本发明旨在克服现有技术中的2,4,5-三氯-6-((2,4,6-三氯苯胺基)间苯二腈化合物并不适用于医药领域的问题,提供一种具有良好晶型,性质稳定,容易制备,适合作为药用的2,4,5-三氯-6-((2,4,6-三氯苯胺基)间苯二腈化合物。
为实现上述目的,本发明采用以下技术方案:
本发明提供了一种2,4,5-三氯-6-((2,4,6-三氯苯胺基)间苯二腈化合物,其在X-射线衍射的衍射角度2θ为9.84±0.2度、19.66±0.2度、21.94±0.2度、22.80±0.2度、25.08±0.2度、31.19±0.2度上有衍射峰。
一些实施例中,2,4,5-三氯-6-((2,4,6-三氯苯胺基)间苯二腈化合物在X-射线衍射的衍射角度2θ为9.84±0.2度、12.51±0.2度、11.71±0.2度、14.72±0.2度、14.88±0.2度、18.33±0.2度、19.12±0.2度、19.66±0.2度、20.19±0.2度、20.86±0.2度、21.94±0.2度、22.80±0.2度、24.61±0.2度、25.08±0.2度、25.41±0.2度、25.75±0.2度、28.09±0.2度、28.45±0.2度、29.62±0.2度、30.32±0.2度、31.19±0.2度、31.93±0.2度、33.10±0.2度上有衍射峰。
一些实施例中,2,4,5-三氯-6-((2,4,6-三氯苯胺基)间苯二腈化合物的熔点为250-257℃。
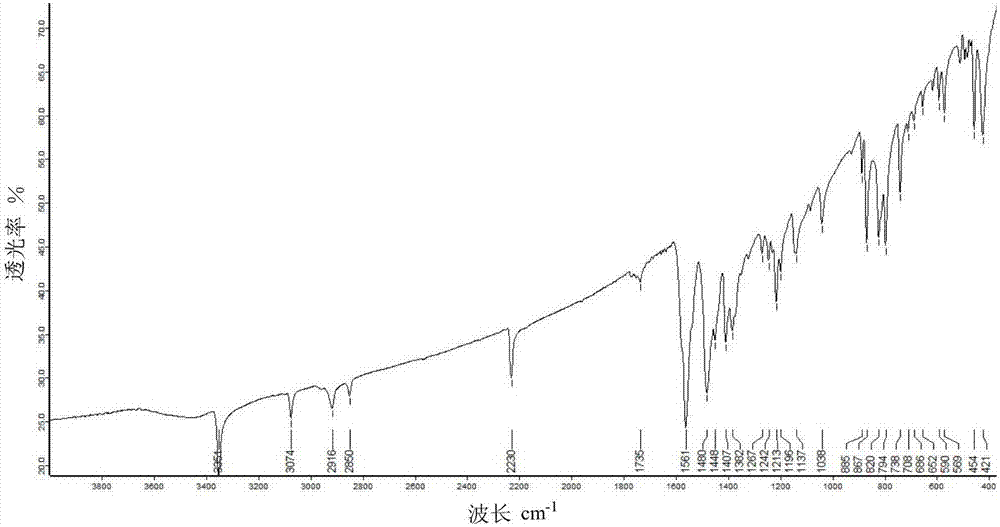
一些实施例中,2,4,5-三氯-6-((2,4,6-三氯苯胺基)间苯二腈化合物在红外光谱的波长3351.21cm-1、3073.79cm-1、2916.39cm-1、2849.80cm-1、2229.57cm-1、1560.66cm-1、1479.61cm-1、1407.23cm-1、1381.98cm-1、1213.29cm-1、1137.06cm-1、866.87cm-1、820.24cm-1、793.86cm-1、738.35cm-1、454.25cm-1、420.76cm-1上有吸收峰。
本发明同时还提供了一种2,4,5-三氯-6-((2,4,6-三氯苯胺基)间苯二腈化合物的制备方法,其步骤包括将含有无定型2,4,5-三氯-6-((2,4,6-三氯苯胺基)间苯二腈的化合物与溶剂混合,加热溶解,冷却析晶,制得上述2,4,5-三氯-6-((2,4,6-三氯苯胺基)间苯二腈化合物;所述含有无定型2,4,5-三氯
-6-((2,4,6-三氯苯胺基)间苯二腈的化合物与溶剂的质量体积比w/v为1g:
10-120ml。
一些实施例中,溶剂选自醇、取代苯、酯、氰类溶剂中的一种或几种。
一些实施例中,加热的温度为30-120℃。
一些实施例中,步骤包括将含有无定型2,4,5-三氯-6-((2,4,6-三氯苯胺基)间苯二腈的化合物置于反应器中,加入溶剂,搅拌加热使其溶解,保温0.5-2小时,冷却至10-15℃搅拌析晶,过滤,洗涤,干燥得上述2,4,5-三氯-6-((2,4,6-三氯苯胺基)间苯二腈化合物。
一些实施例中,析晶的时间为0.5-6小时。
本发明同时还提供了一种药物组合物,包括上述2,4,5-三氯-6-((2,4,6-三氯苯胺基)间苯二腈化合物。
本发明的有益效果在于:
本发明的发明人经过长期研究发现WO2013135147不适用于医药领域的原因是其制备的2,4,5-三氯-6-((2,4,6-三氯苯胺基)间苯二腈化合物是含有无定型的,且无定型含量比例难以控制,影响了药物制剂加工。而通过本发明的发明人的长期研究意外得到本发明的具有良好晶型的2,4,5-三氯-6-((2,4,6-三氯苯胺基)间苯二腈化合物,本发明的2,4,5-三氯-6-((2,4,6-三氯苯胺基)间苯二腈化合物具有良好理化性质,性质稳定,特别是利于药物制剂的加工处理,更适合作为药用。且本发明的制备方法简单,容易制备。
附图说明
图1为本发明实施例1制备的2,4,5-三氯-6-((2,4,6-三氯苯胺基)间苯二腈化合物的X-射线衍射(XRD)图;
图2为本发明实施例1制备的2,4,5-三氯-6-((2,4,6-三氯苯胺基)间苯二腈化合物的红外光谱图;
图3为本发明实施例1制备的2,4,5-三氯-6-((2,4,6-三氯苯胺基)间苯二腈化合物的差示扫描量热法分析(DSC)、热重分析(TGA)图。
具体实施方式
下面详细描述本发明的实施例,下面描述的具体实施例是示例性的,旨在用于解释本发明,而不能理解为对本发明的限制。
本发明提供了一种2,4,5-三氯-6-((2,4,6-三氯苯胺基)间苯二腈化合物,其在X-射线衍射的衍射角度2θ为9.84±0.2度、19.66±0.2度、21.94±0.2度、22.80±0.2度、25.08±0.2度、31.19±0.2度上有衍射峰。
一些实施例中,2,4,5-三氯-6-((2,4,6-三氯苯胺基)间苯二腈化合物在X-射线衍射的衍射角度2θ为9.84±0.2度、12.51±0.2度、11.71±0.2度、14.72±0.2度、14.88±0.2度、18.33±0.2度、19.12±0.2度、19.66±0.2度、20.19±0.2度、20.86±0.2度、21.94±0.2度、22.80±0.2度、24.61±0.2度、25.08±0.2度、25.41±0.2度、25.75±0.2度、28.09±0.2度、28.45±0.2度、29.62±0.2度、30.32±0.2度、31.19±0.2度、31.93±0.2度、33.10±0.2度上有衍射峰,物质晶型好,性质稳定,特别是利于药物制剂的加工处理,更适合作为药用。本发明较优的实施例中具体的2,4,5-三氯-6-((2,4,6-三氯苯胺基)间苯二腈化合物的X-射线衍射如图1及表1所示。
表1
其中,本发明的X-射线衍射测试是使用配备有位置敏感检测仪(OED)及一个作为X射线源的Cu阳极(CuKα1辐射,λ=1.5406A,40kV,40mA)的Bruker D8进阶衍射仪进行的测量。
一些实施例中,2,4,5-三氯-6-((2,4,6-三氯苯胺基)间苯二腈化合物的熔点为250-257℃。
一些实施例中,2,4,5-三氯-6-((2,4,6-三氯苯胺基)间苯二腈化合物在红外光谱的波长3351.21cm-1、3073.79cm-1、2916.39cm-1、2849.80cm-1、2229.57cm-1、1560.66cm-1、1479.61cm-1、1407.23cm-1、1381.98cm-1、1213.29cm-1、1137.06cm-1、866.87cm-1、820.24cm-1、793.86cm-1、738.35cm-1、454.25cm-1、420.76cm-1上有吸收峰,证明物质为2,4,5-三氯-6-((2,4,6-三氯苯胺基)间苯二腈化合物。
其中,红外光谱测试是采用SHIMADZU FTIR-8400型傅立叶变换红外光谱分析仪。
本发明同时还提供了一种2,4,5-三氯-6-((2,4,6-三氯苯胺基)间苯二腈化合物的制备方法,其步骤包括将含有无定型2,4,5-三氯-6-((2,4,6-三氯苯胺基)间苯二腈的化合物与溶剂混合,加热溶解,冷却析晶,制得上述2,4,5-三氯-6-((2,4,6-三氯苯胺基)间苯二腈化合物;所述含有无定型2,4,5-三氯-6-((2,4,6-三氯苯胺基)间苯二腈的化合物与溶剂的质量体积比w/v为1g:10-120ml。
优选,溶剂选自醇、取代苯、酯、氰类溶剂中的一种或几种。
优选,加热的温度为30-120℃。
优选,析晶后过滤,溶剂洗涤,干燥得目标晶体。其中,过滤、溶剂洗涤、干燥的方法为本领域技术人员公知,在此不再赘述。
具体的可以采用如下步骤进行制备:
将含有无定型2,4,5-三氯-6-((2,4,6-三氯苯胺基)间苯二腈的化合物置于反应器中,加入溶剂,搅拌加热使其溶解,保温0.5-2小时,冷却至10-15℃搅拌析晶0.5-6小时,过滤,洗涤,干燥得上述2,4,5-三氯-6-((2,4,6-三氯苯胺基)间苯二腈化合物。
本发明同时还提供了一种药物组合物,包括上述2,4,5-三氯-6-((2,4,6-三氯苯胺基)间苯二腈化合物。药物组合物可以还含有一种或多种惰性载剂及/或稀释剂,其中,惰性载剂和稀释剂可以并不限定为微晶纤维素、乳糖、硬脂酸镁等。药物组合物也可以含有多种药物,药物可以并不限定为紫杉醇、顺铂、阿霉素等。
本发明的2,4,5-三氯-6-((2,4,6-三氯苯胺基)间苯二腈化合物应用于药物组合物时,具体的配置方式可以采用本领域常用方式,例如直接给药,也可以配制成含有2,4,5-三氯-6-((2,4,6-三氯苯胺基)间苯二腈化合物的片剂,例如为薄膜包衣的圆形片剂,其可含有50mg、100mg和200mg的2,4,5-三氯-6-((2,4,6-三氯苯胺基)间苯二腈化合物,可口服给药释放活性成分。
含有2,4,5-三氯-6-((2,4,6-三氯苯胺基)间苯二腈化合物的片剂可以还含有填充剂、崩解剂、粘合剂、润滑剂、包衣剂等。具体可以由2,4,5-三氯-6-((2,4,6-三氯苯胺基)间苯二腈化合物、微晶纤维素、乳糖、交联羧甲基纤维素钠、聚维酮、硬脂酸镁、欧巴代等组成。
一些实施例中,可以使用湿法制粒、干混合、片剂压制和薄膜包衣方法制备含有50mg和100mg 2,4,5-三氯-6-((2,4,6-三氯苯胺基)间苯二腈化合物的片剂。具体的,可以称取配方量的原料药、乳糖一水合物、微晶纤维素和交联羧甲基纤维素钠,置于高剪切混合制粒机中混合均匀。将混合均匀的物料转移至流化床中,使用配制聚维酮水溶液喷入流化床制粒,在40±3℃的流化床干燥45分钟。将制得的颗粒经80目筛整粒,加入微晶纤维素和交联羧甲基纤维素钠混合物在混合机中混合20分钟,加入硬脂酸镁后再混合3分钟,压片机压制获得未包衣素片。将欧巴代溶于纯净水中,搅拌下制备薄膜包衣悬浮液。在包衣锅中对片剂进行薄膜包衣(重量增加大约3%)。
以下是本发明提供的具体实施例,用以说明上述方案及其各种条件的选取。本发明实施例中所用试剂均采用市购分析纯。
实施例1:
本实施例用于说明本发明的2,4,5-三氯-6-((2,4,6-三氯苯胺基)间苯二腈化合物。
在100mL单口瓶中,加入0.5g含有无定型2,4,5-三氯-6-((2,4,6-三氯苯胺基)间苯二腈化合物(采用WO2013135147的实施例1的方法自制的),60mL乙醇,80℃加热回流直至溶液澄清,保温1小时,停止加热,冷却至15℃搅拌析晶3小时,过滤,少量乙醇洗涤,室温干燥得灰白色固体晶体0.31g,收率62.0%。
采用配备有位置敏感检测仪(OED)及一个作为X射线源的Cu阳极(CuKα1辐射,λ=1.5406A,40kV,40mA)的Bruker D8进阶衍射仪进行X-射线衍射(XRD)测试,测试结果如附图1及表1。
采用SHIMADZU FTIR-8400型傅立叶变换红外光谱分析仪进行红外光谱测试,测试结果如图2所示。
采用NETZSCH STA 449F3进行DSC(差示扫描量热法分析)、TGA(热重分析)测量,升温速率5℃/分钟,N2氛围,测试结果如图3所示。
实施例2:
本实施例用于说明本发明的2,4,5-三氯-6-((2,4,6-三氯苯胺基)间苯二腈化合物。
在100mL单口瓶中,加入0.5g含有无定型2,4,5-三氯-6-((2,4,6-三氯苯胺基)间苯二腈化合物(采用WO2013135147的实施例1的方法自制的),50mL甲醇,80℃加热回流直至溶液澄清,保温1小时,停止加热,冷却至15℃搅拌析晶3小时,过滤,少量甲醇洗涤,室温干燥得灰白色固体晶体0.13g,收率26.0%。
采用与实施例1相同的方法进行XRD测试,红外光谱测试及DSC、TGA测试,结果与实施例1类似。
实施例3:
本实施例用于说明本发明的2,4,5-三氯-6-((2,4,6-三氯苯胺基)间苯二腈化合物。
在100mL单口瓶中,加入0.5g含有无定型2,4,5-三氯-6-((2,4,6-三氯苯胺基)间苯二腈化合物(采用WO2013135147的实施例1的方法自制的),20mL乙腈,85℃加热回流直至溶液澄清,保温1小时,停止加热,冷却至14℃搅拌析晶3小时,过滤,少量乙腈洗涤,室温干燥得灰白色固体晶体0.40g,收率80.0%。
采用与实施例1相同的方法进行XRD测试,红外光谱测试及DSC、TGA测试,结果与实施例1类似。
实施例4:
本实施例用于说明本发明的2,4,5-三氯-6-((2,4,6-三氯苯胺基)间苯二腈化合物。
在100mL单口瓶中,加入1.0g含有无定型2,4,5-三氯-6-((2,4,6-三氯苯胺基)间苯二腈化合物(采用WO2013135147的实施例1的方法自制的),10mL乙酸乙酯,85℃加热回流直至溶液澄清,保温1小时,停止加热,冷却至14℃搅拌析晶3小时,过滤,少量乙酸乙酯洗涤,室温干燥得灰白色固体晶体0.21g,收率21.0%。
采用与实施例1相同的方法进行XRD测试,红外光谱测试及DSC、TGA测试,结果与实施例1类似。
实施例5:
本实施例用于说明本发明的2,4,5-三氯-6-((2,4,6-三氯苯胺基)间苯二腈化合物。
在100mL单口瓶中,加入1.0g含有无定型2,4,5-三氯-6-((2,4,6-三氯苯胺基)间苯二腈化合物(采用WO2013135147的实施例1的方法自制的),15mL甲苯,120℃加热回流直至溶液澄清,保温1小时,停止加热,冷却至14℃搅拌析晶3小时,过滤,少量甲苯洗涤,室温干燥得灰白色固体晶体0.83g,收率83.0%。
采用与实施例1相同的方法进行XRD测试,红外光谱测试及DSC、TGA测试,结果与实施例1类似。
实施例6-15:
实施例6-15用于说明本发明的含有2,4,5-三氯-6-((2,4,6-三氯苯胺基)间苯二腈化合物的片剂,实施例6-15分别对应于包括50.00mg及100mg剂量的实施例1-5所得化合物的片剂。
称取如表2所示的配方量的2,4,5-三氯-6-((2,4,6-三氯苯胺基)间苯二腈化合物、乳糖一水合物、微晶纤维素和交联羧甲基纤维素钠,置于高剪切混合制粒机中混合均匀。将混合均匀的物料转移至流化床中,使用配制聚维酮水溶液喷入流化床制粒,在40±3℃的流化床干燥45分钟。将制得的颗粒经80目筛整粒,加入微晶纤维素和交联羧甲基纤维素钠混合物在混合机中混合20分钟,加入硬脂酸镁后再混合3分钟,压片机压制获得未包衣素片。将欧巴代溶于纯净水中,搅拌下制备薄膜包衣悬浮液。在包衣锅中对片剂进行薄膜包衣(重量增加大约3%)。
表2
对比例
称取如表3所示的配方量的2,4,5-三氯-6-((2,4,6-三氯苯胺基)间苯二腈化合物、乳糖一水合物、微晶纤维素和交联羧甲基纤维素钠,置于高剪切混合制粒机中混合均匀。将混合均匀的物料转移至流化床中,使用配制聚维酮水溶液喷入流化床制粒,在40±3℃的流化床干燥45分钟。将制得的颗粒经80目筛整粒,加入微晶纤维素和交联羧甲基纤维素钠混合物在混合机中混合20分钟,加入硬脂酸镁后再混合3分钟,压片机压制获得未包衣素片。将欧巴代溶于纯净水中,搅拌下制备薄膜包衣悬浮液。在包衣锅中对片剂进行薄膜包衣(重量增加大约3%)。
表3
实施例6-15所对应的药物片剂,相对于对比例的药物片剂的制备过程,实施例6-15更易操作,料的流动性好,整个加工操作过程不存在困难,制备的片剂良品率高,且产率也高。而对比例中的料易吸湿,料的流动性差,操作性能差,制备的片剂良品率低。
在本说明书的描述中,参考术语“一个实施例”、“一些实施例”、“示例”、“具体示例”、或“一些示例”等的描述意指结合该实施例或示例描述的具体特征、结构、材料或者特点包含于本发明的至少一个实施例或示例中。在本说明书中,对上述术语的示意性表述不一定指的是相同的实施例或示例。而且,描述的具体特征、结构、材料或者特点可以在任何的一个或多个实施例或示例中以合适的方式结合。
尽管上面已经示出和描述了本发明的实施例,可以理解的是,上述实施例是示例性的,不能理解为对本发明的限制,本领域的普通技术人员在不脱离本发明的原理和宗旨的情况下在本发明的范围内可以对上述实施例进行变化、修改、替换和变型。
- 还没有人留言评论。精彩留言会获得点赞!