一种富勒烯多氮杂桥水溶性衍生物的制备方法与流程
本发明属于碳纳米材料领域,涉及一种富勒烯多氮杂桥水溶性衍生物的制备方法。
背景技术:
以“明星分子”C60为典型代表的疏水性富勒烯材料可被特定亲水试剂经化学修饰成水溶性衍生物,如:富勒烯与羟基化试剂作用生成富勒醇;经Bingle-Hirsch反应生成水溶性的富勒烯丙二酸多加成衍生物;与多种氨基酸反应生成富勒烯氨基酸水溶性衍生物。此外,本研究组曾报道富勒烯在液相溶剂体系中经氮宾多加成反应生成富勒烯多氮杂桥水溶性衍生物(中国发明专利号:Zl201010522925.4.;He R.et al.Nanomedicine:Nanotechnology,Biology and Medicine,2016,12(2):525-526)。
富勒烯水溶性衍生物作为纳米生物材料生物相容性良好,自身具有优异的电子顺磁共振性能、弱顺磁性以及独特的结构尺寸和稳定的生物效应,成为探讨纳米粒与生物、环境相互作用产生纳米生物效应问题的模式材料。在纳米医学领域,已有文献展示富勒烯水溶性衍生物具有抗菌活性、抗氧化和清除自由基能力,可作化疗法抗肿瘤药物及用于光动力疗法杀死癌细胞;在纳米农业技术领域,其展现出调节植物生长及提高抗逆性方面的作用。然而,在纳米医学及纳米农业技术中有关富勒烯水溶性衍生物应用研究的报道依然极少,瓶颈就在于缺乏经济合理大规模制备具有良好生物相容性的富勒烯水溶性衍生物的方法,而导致无法提供充足产品应用于其纳米生物效应的研究。
目前,富勒烯可经羟基化、氨基酸化、Bingle-Hirsch反应及氮宾反应制备富勒烯水溶性衍生物,主流的制备方法均是富勒烯溶解于有机溶剂在液相体系发生反应。例如:富勒醇作为最具代表性的富勒烯水溶性衍生物,典型制备方法就是富勒烯溶解于甲苯在相转移催化剂作用下的NaOH处理法;氨基酸化反应是富勒烯溶于甲苯后在碱性条件下与过量的各种氨基酸反应;Bingle-Hirsch反应也是富勒烯溶解于甲苯溶液与丙二酸酯衍生物发生环加成反应;我们研究组报道的氮宾反应则是富勒烯溶解于邻二氯苯与亲水性叠氮有机化合物高温下发生多加成反应。综上所述,当前广泛制备富勒烯水溶性衍生物的液相反应技术方法,几乎千篇一律地采用甲苯或邻二氯苯等有机溶剂作为溶解富勒烯的反应溶剂。考虑到此二者溶解富勒烯能力较低(如:常温下甲苯、邻二氯苯分别能溶解C60为2.8、27mg/mL,RuoffR.et al.Journal of Physical Chemistry,1993,97:3379-3383),当开展工业化大规模制备时必将消耗巨大体积的甲苯或邻二氯苯,如此工艺将极大增加大批量生产的操作难度,且无法实现经济合理大规模制备水溶化的富勒烯产品。
在富勒烯类碳纳米材料领域,科研人员一直孜孜追求的目标就是通过更简便的制造技术大规模获得新型富勒烯水溶性衍生物。本发明的目的就是从改进富勒烯参与的液相反应系统着手,跳出拘泥于不断寻找高溶解性反应溶剂从而优化扩大反应规模的常规思路,通过免添加溶剂策略,利用富勒烯与液态的叠氮有机化合物直接发生氮宾反应,发明出一种在液相体系中便捷地大规模制备富勒烯多氮杂桥水溶性衍生物的新方法。
技术实现要素:
本发明要解决的技术问题是提供一种在液相体系中简便且能大规模制备富勒烯多氮杂桥水溶性衍生物的新方法,即免添加有机溶剂策略的氮宾多加成反应法。
本发明提供了一种富勒烯多氮杂桥水溶性衍生物的制备方法,含如下步骤:
(1)将富勒烯与室温时呈液态的叠氮有机化合物分别投料于反应器,无需添加有机溶剂直接在惰性气体氛围下机械搅拌,二者投料的物质的量之比为1:50~100;所述叠氮有机化合物的碳链一端键联亲水性官能团;
(2)将反应体系升温至回流,保温12~72小时后,停止加热;
(3)蒸除部分未反应的叠氮有机化合物,残留物经有机溶剂洗涤,进一步去除未反应物及加成数目较少的非水溶性衍生物,然后用水进行提取,提取液过滤后去除溶剂,得固化的粗产品;
(4)粗产品复溶于水并使用截留分子量为500-10000道尔顿透析袋透析,干燥得到纯净的富勒烯多氮杂桥水溶性衍生物的固态产品。
本发明所述的富勒烯和叠氮有机化合物的氮宾多加成反应以及产物为本领域技术人员所公知,步骤(4)所制得的富勒烯多氮杂桥类水溶性衍生物分子以富勒烯碳笼为核心,碳笼通过氮原子桥联多个亲水性侧链,每个侧链另一末端键联有亲水性官能团,如:-OH、-NH2,-COOH、-SO3H,由此保证整个衍生物分子具备水溶性。叠氮有机化合物与富勒烯品种可调控侧链数目的多寡及分布范围的宽窄。
本发明步骤(1)所述的富勒烯为分子由60~90个碳原子组成的具有球状或类球状结构并含有大量共轭碳碳双键的单质中的一种,分子式为C2n,富勒烯分子中的碳原子数目优选60、70、84或90个,更优选60或70,并以60个碳原子为最优。
本发明步骤(1)所述的叠氮有机化合物均可参考现有科技文献大量制备,优选其分子式为N3(CH2)mR或N3(CH2)m-1COOH,其中,R为OH、NH2或SO3H,m=2~6,含2~6个碳原子的饱和直碳链,且碳链两端必须分别键联叠氮基团(-N3)和亲水性官能团,如,-OH、-NH2、-COOH、-SO3H。优选叠氮有机化合物为2-叠氮基乙醇、2-叠氮基乙胺、2-叠氮基乙基磺酸、2-叠氮基乙酸、3-叠氮基丙酸或6-叠氮基己酸。特别值得注意的是上述叠氮有机化合物在室温时呈液态,以保证在高温反应过程中其既作反应物,又充作反应溶剂。如此,即可通过免添加有机溶剂策略,在液相反应体系中直接发生氮宾多加成反应,大规模制备富勒烯多氮杂桥水溶性衍生物。
本发明步骤(1)中,叠氮有机化合物相对于富勒烯的投料比必须介于指定范围之内,即物质的量之比为50~100:1。低于该指定投料比50:1下限时,随着反应的进程,反应体系迅速固化使反应被迫终止,如此主要获得加成数目相对较少且不具备水溶性的寡加成衍生物,这导致获得水溶性产品的收率大大降低,将不超过25%;超过该指定投料比100:1上限时,会大大增加叠氮有机化合物投料量而加大经济成本,并且极大增加后续纯化步骤的处理难度及成本;而在指定投料比范围内即可高性价比、高收率的获得富勒烯多氮杂桥水溶性衍生物。
本发明所述步骤(3)中,洗涤时可采用常规有机试剂,如:乙醚、二氯甲烷、三氯甲烷、乙酸乙酯等,以便优先去除未反应的叠氮有机化合物及加成数目较少的非水溶性寡加成衍生物。
本发明还提供了另一种富勒烯多氮杂桥水溶性衍生物的制备方法,含如下步骤:
(a)将富勒烯与室温时呈液态的叠氮有机化合物分别投料于反应器,无需添加有机溶剂直接在惰性气体氛围下机械搅拌,二者投料的物质的量之比为1:50~100;所述叠氮有机化合物的碳链一端键联-COOH或-SO3H;
(b)将反应体系升温至回流,保温12~72小时后,停止加热;
(c)蒸除部分未反应的叠氮有机化合物,残留物经有机溶剂洗涤,进一步去除未反应物及加成数目较少的非水溶性衍生物,然后用溶剂A进行提取,提取液过滤后去除溶剂,得固化的粗产品;所述的溶剂A为强亲水性溶剂和/或水,所述的强亲水性溶剂为甲醇、乙醇、乙酸或乙腈;
(d)将粗产品复溶于碱性溶液中,并使用截留分子量为500-10000道尔顿透析袋透析,干燥得到纯净的富勒烯多氮杂桥水溶性衍生物的固态产品。
本发明步骤(a)所述的富勒烯为分子由60~90个碳原子组成的具有球状或类球状结构并含有大量共轭碳碳双键的单质中的一种,分子式为C2n,富勒烯分子中的碳原子数目优选60、70、84或90个,更优选60或70,并以60个碳原子为最优。
本发明步骤(a)所述的叠氮有机化合物均可参考现有科技文献大量制备,优选其分子式为N3(CH2)mSO3H或N3(CH2)m-1COOH,其中,m=2~6,含2~6个碳原子的饱和直碳链,且碳链两端必须分别键联叠氮基团(-N3)和亲水性官能团-COOH、-SO3H。优选叠氮有机化合物为2-叠氮基乙基磺酸、2-叠氮基乙酸、3-叠氮基丙酸或6-叠氮基己酸。特别值得注意的是上述叠氮有机化合物在室温时呈液态,以保证在高温反应过程中其既作反应物,又充作反应溶剂。如此,即可通过免添加有机溶剂策略,在液相反应体系中直接发生氮宾多加成反应,大规模制备富勒烯多氮杂桥水溶性衍生物。
本发明步骤(a)中,叠氮有机化合物相对于富勒烯的投料比必须介于指定范围之内,即物质的量之比为50~100:1。低于该指定投料比50:1下限时,随着反应的进程,反应体系迅速固化使反应被迫终止,如此主要获得加成数目相对较少且不具备水溶性的寡加成衍生物,这导致获得水溶性产品的收率大大降低,将不超过25%;超过该指定投料比100:1上限时,会大大增加叠氮有机化合物投料量而加大经济成本,并且极大增加后续纯化步骤的处理难度及成本;而在指定投料比范围内即可高性价比、高收率的获得富勒烯多氮杂桥水溶性衍生物。
本发明所述步骤(c)中,洗涤时可采用常规有机试剂,如:乙醚、二氯甲烷、三氯甲烷、乙酸乙酯等,以便优先去除未反应的叠氮有机化合物及加成数目较少的非水溶性寡加成衍生物。
本发明所述步骤(c)中,产物的分离纯化可采用溶剂提取法,提取所用的溶剂A采用梯度改变强亲水性溶剂:水的体积比由100%:0%至0%:100%实现提取溶剂极性的调节,进而实现加成数目在较窄范围变化且平均加成数目由少到多变化的富勒烯多氮杂桥衍生物的相互分离。优选溶剂A为乙醇和/或水。
本发明所述步骤(d)中,碱性溶液优选为浓度>0.1mol/L且≤5mol/L的NaOH、KOH或氨水溶液,更优选1mol/L的NaOH或KOH溶液。
本发明步骤(d)所制得的富勒烯多氮杂桥类水溶性衍生物分子以富勒烯碳笼为核心,碳笼通过氮原子桥联多个亲水性侧链,每个侧链另一末端键联有亲水性官能团,如:-COOM、-SO3M(其中M为Na、K或NH4),由此保证整个衍生物分子具备水溶性。叠氮有机化合物与富勒烯品种及反应后处理中纯化时的提取方式可调控侧链数目的多寡及分布范围的宽窄。
与现有技术相比,本发明的有益效果在于:
a.本发明提供的大规模制备富勒烯多氮杂桥水溶性衍生物新方法的特点:①合成工艺更简便、更高效,合成过程中操作方法更简单;②实验室条件下,在0.5L反应容器内就可实现富勒烯多氮杂桥水溶性衍生物的百克量级制备,这为工业化大规模生产水溶性富勒烯衍生产品提供出崭新的工艺路线。
b.本发明提供的液相反应法的反应体系采用免添加有机溶剂策略,相较于以往采用二甲苯、氯苯、邻二氯苯作反应溶剂的反应体系其优势在于:①避免使用高污染的芳烃或卤代芳烃类有机溶剂溶解反应物,使得反应体系对环境污染影响降低到更小程度;②依据相似相溶原理,叠氮有机化合物自身作溶剂的反应氛围有利于形成的富勒烯寡加成衍生物分散于液相反应体系,促进其继续发生氮宾多加成反应,并最终产生更高加成数目的水溶性衍生产物;③利用同等反应容器反应时,免溶剂策略的反应规模可扩大10倍以上;④此法还适用于液态的多种加成试剂与富勒烯发生多加成反应大规模制备其它类型的水溶性富勒烯衍生物。
c.本发明所获得富勒烯多氮杂桥水溶性衍生物的水相溶解性能优异,自身为稳定自由基,可作为捕获其它自由基的纳米探针,体外自由基清除实验展示其清除自由基效果特别显著,此外,其还可受激发射荧光,使之在纳米生物医学领域和纳米农业技术领域中均具有重要的应用前景。
附图说明
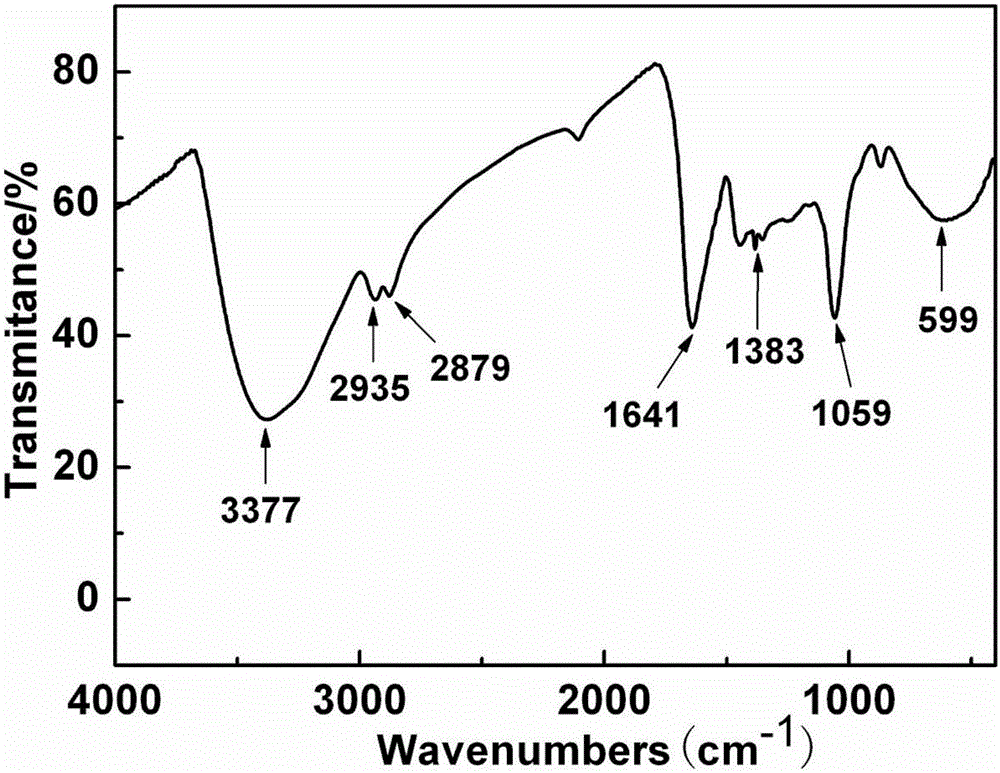
图1.实施例1中氮杂富勒醇1粉末的FT-IR谱图。
图2.实施例1中氮杂富勒醇1粉末的热重分析谱图。
图3.实施例1中氮杂富勒醇1的ESR分析谱图。
图4.实施例1中氮杂富勒醇1的荧光激发谱和发射谱。
图5.实施例9中C60(NCH2CH2OH)14水溶液处理ABTS+·后清除率与浓度的关联性。
图6.实施例9中C60(NCH2COONa)13水溶液处理ABTS+·后清除率与浓度的关联性。
图7.实施例10中C60(NCH2COONa)13处理对玉米种子萌发率的影响。
图8.实施例10中50μg/ml(左)、5μg/ml(中)、0μg/ml(右)C60(NCH2COONa)13水溶液处理对两叶一心期玉米根系的影响。
具体实施方式
以下实施例有助于进一步理解本发明,但本发明保护范围并不限于列举的实施例。
实施例中所述实验方法均为常规方法;所述试剂和材料均可从商业途径获得。其中,富勒烯C60和C70来源于河南省濮阳市永新富勒烯科技有限公司,纯度高于99.9%。所需的含短直碳链的亲水性叠氮基小分子有机化合物,如:叠氮乙醇、叠氮乙酸、叠氮乙胺、叠氮己酸等,由叠氮钠与相应的卤代物参考现有科技文献制成。
实施例1:大规模制备C60与叠氮乙醇的水溶性产物C60(NCH2CH2OH)14(氮杂富勒醇1)
(1)将60.0g C60固体粉末与362.8g液态的2-叠氮基乙醇(物质的量投料比为1:50)分别投料于500mL三口反应瓶,接冷凝管及机械搅拌装置,无需添加有机溶剂,直接在惰性气体氛围下机械搅拌;
(2)反应体系升温至回流,保温72小时后,停止加热;
(3)减压蒸馏去除部分未反应的2-叠氮基乙醇,残留物经乙醚、乙酸乙酯反复洗涤,以便进一步去除未反应的2-叠氮基乙醇及加成数目较少的非水溶性衍生化产物,然后添加去离子水超声提取多次至上清液无色后,合并提取液经滤膜过滤,去除溶剂,得固化的粗产品1;
(4)将粗产品1复溶于去离子水并使用截留分子量为500-10000道尔顿的透析袋于水相透析,微孔滤膜过滤,减压旋蒸干燥,由此精制得到纯净的侧链末端含羟基的富勒烯多氮杂桥水溶性衍生物的固态产品108.2g,产率84%,标记为氮杂富勒醇1。
氮杂富勒醇1的表征信息如下:
图1所示,红外光谱在3377cm-1处的强吸收峰归属为O-H伸缩振动、1383cm-1处弱吸收峰归属于O-H弯曲振动、1059cm-1归属于C-OH伸缩振动,此三组吸收峰证明氮杂富勒醇1分子中存在-OH,在2935、2879cm-1处的弱吸收峰归属于C-H对称与反对称伸缩振动,在1641cm-1处的强吸收峰归属于富勒烯碳笼中残余的C=C伸缩振动,在500-600cm-1之间的弱吸收宽峰为C60的骨架振动吸收。
图2所示TG-DTG-DSC同步分析结果表明,氮杂富勒醇1分子在温度区间133-695℃百分比质量从93.89%减少到44.26%,此区间减少的百分比质量(49.36%)完全归因于氮杂富勒醇1分子碳笼外接侧链基团-NCH2CH2OH的全部丢失,而695℃时残留的质量则归属于C60碳笼,其中碳笼式量为720,全部外接侧链(-NCH2CH2OH)的式量为59x,计算x=13.68,据此得氮杂富勒醇1的平均分子式为C60(NCH2CH2OH)14。
图3所示ESR图谱表明,氮杂富勒醇1粉末在室温下展现为3270G附近的无精细结构的宽峰,相应的g因子为2.0018,电子自旋量子数为S=1/2。其电子自旋态与文献报道富勒烯衍生物的结果一致,表明其可作为稳定的自由基离子。
图4所示荧光光谱显示氮杂富勒醇1在水溶液中能受激产生荧光,这意味着其免标记荧光染料自身即可作潜在的纳米荧光探针。
上述结果表明实验室条件下在0.5L反应容器内即可实现百克量级的富勒烯多氮杂桥水溶性衍生物产品制备。这为大规模工业化批量生产水溶性富勒烯衍生产品开辟了崭新的路径。所制得的富勒烯多氮杂桥类水溶性衍生物具有受激发射荧光性能及良好的电子顺磁共振性质,应用于生物体系可通过清除诸如活性氧等自由基而展现出优异的抗氧化性能,从而在纳米医药领域及在纳米农业技术领域具有巨大的潜在应用价值。
实施例2:制备C60与叠氮乙胺的水溶性加成产物C60(NCH2CH2NH2)12(氮杂富勒胺1)
(1)将12.0g C60固体粉末与143.5g液态的2-叠氮基乙胺(物质的量投料比为1:100)分别投料于250mL三口反应器,接冷凝管及机械搅拌装置,无需添加有机溶剂,直接在惰性气体氛围下机械搅拌;
(2)反应体系升温至回流,保温48小时后,停止加热;
(3)减压蒸馏去除部分未反应的2-叠氮基乙胺,残留物经乙醚、乙酸乙酯反复洗涤,以便进一步去除未反应的2-叠氮基乙胺及加成数目较少的非水溶性衍生化产物,然后添加去离子水超声提取多次至上清液无色后,合并提取液经滤膜过滤,去除溶剂,得固化的粗产品2;
(4)将粗产品2复溶于去离子水并使用截留分子量为500-10000道尔顿的透析袋透析,干燥,由此精制得到纯净的侧链末端含氨基的富勒烯多氮杂桥类水溶性衍生物的固态产品22.4g,产率95%,标记为氮杂富勒胺1。热重分析表征其平均分子式为C60(NCH2CH2NH2)12。
实施例3:制备C60与叠氮乙酸的富勒烯基聚甘氨酸水溶性衍生物C60(NCH2COOH)13
(1)将20.0g C60固体粉末与140.4g液态的2-叠氮基乙酸(物质的量投料比为1:100)分别投料于250mL三口反应器,接冷凝管及机械搅拌装置,无需添加有机溶剂,直接在惰性气体氛围下机械搅拌;
(2)反应体系升温至回流,保温12小时后,停止加热;
(3)减压蒸馏去除部分未反应的2-叠氮基乙酸,残留物经乙醚、乙酸乙酯反复洗涤,以便进一步去除未反应的2-叠氮基乙酸及加成数目较少的非水溶性衍生化产物,然后用去离子水超声提取多次至上清液无色,合并提取液,滤膜过滤,去除溶剂,得固化的粗产品3;
(4)将粗产品3复溶于去离子水并使用截留分子量为500-10000道尔顿的透析袋透析,干燥,由此精制得到纯净的侧链末端含羧基的富勒烯多氮杂桥类水溶性衍生物的固态产品,产率75%,标记为富勒烯基聚甘氨酸水溶性衍生物1。热重分析表征其平均分子式为C60(NCH2COOH)13。
实施例4:制备C60与叠氮乙酸的富勒烯基聚甘氨酸钠水溶性衍生物
实施例3的步骤(3)中,经去离子水多次超声提取粗产品3后的残留物继续添加乙醇超声提取多次至上清液无色,合并提取液,滤膜过滤,去除溶剂,得固化的粗产品4;提取粗产品4后的残留物继续添加体积比为50%:50%的乙醇-水的二元溶剂超声提取多次,合并提取液经滤膜过滤,去除溶剂,得固化的粗产品5。
将粗产品3、粗产品4、粗产品5复溶于1mol/L NaOH溶液并使用截留分子量为500-10000道尔顿的透析袋透析,微孔滤膜过滤,干燥,由此精制得到纯净的含甘氨酸钠的富勒烯多氮杂桥类水溶性衍生物的固态产品,依次标记为富勒烯基聚甘氨酸钠水溶性衍生物1、富勒烯基聚甘氨酸钠水溶性衍生物2、富勒烯基聚甘氨酸钠水溶性衍生物3。热重分析表征其平均分子式依次为C60(NCH2COONa)13、C60(NCH2COONa)6、C60(NCH2COONa)8。
如此,通过梯度调节提取溶剂极性的策略,即可实现加成数目在较窄范围变化且平均加成数目互异的富勒烯多氮杂桥水溶性衍生物的相互分离。
实施例5:制备C60与叠氮乙酸的富勒烯基聚甘氨酸钠水溶性衍生物C60(NCH2COONa)7
实施例3的步骤(3)中,经去离子水多次超声提取粗产品3后的残留物,直接添加体积比为50%:50%的甲醇-水的二元溶剂超声提取多次,合并提取液经滤膜过滤,去除溶剂,得固化的粗产品6。
将粗产品6复溶于1mol/L NaOH溶液并使用截留分子量为500-10000道尔顿的透析袋透析,微孔滤膜过滤,干燥,由此精制得到纯净的含甘氨酸钠的富勒烯多氮杂桥类水溶性衍生物的固态产品,依次标记为富勒烯基聚甘氨酸钠水溶性衍生物4。热重分析表征其平均分子式依次为C60(NCH2COONa)7。
实施例6:制备C60与叠氮丙酸的富勒烯基聚丙氨酸钠水溶性衍生物C60(NCH2CH2COONa)10
(1)将9.0g C60固体粉末与143.9g液态的3-叠氮基丙酸(物质的量投料比为1:100)分别投料于250mL反应器,无需添加有机溶剂直接在惰性气体氛围下机械搅拌;
(2)反应体系升温至回流,保温72小时后,停止加热;
(3)减压蒸馏去除部分未反应的3-叠氮基丙酸,残留物经乙醚、乙酸乙酯反复洗涤,以便进一步去除未反应的3-叠氮基丙酸及加成数目较少的非水溶性衍生化产物,然后添加体积比为50%:50%的乙腈与水的混合物超声提取多次,合并提取液经滤膜过滤,去除溶剂,得固化的粗产品;
(4)将粗产品复溶于1mol/L NaOH溶液,并使用截留分子量为500-10000道尔顿的透析袋透析,微孔滤膜过滤,干燥,由此精制得到纯净的侧链末端含羧酸盐的富勒烯多氮杂桥类水溶性衍生物的固态产品17.0g,产率75%,标记为富勒烯基聚丙氨酸钠水溶性衍生物。热重分析表征其平均分子式为C60(NCH2CH2COONa)10。
实施例7:制备C60与叠氮己酸的富勒烯基聚己氨酸钠水溶性衍生物C60(NCH2CH2CH2CH2CH2COONa)8
(1)将10.0g C60固体粉末与109.1g液态的6-叠氮基己酸(物质的量投料比为1:50)分别投料于250mL反应器,无需添加有机溶剂直接在惰性气体氛围下机械搅拌;
(2)反应体系升温至回流,保温48小时后,停止加热;
(3)减压蒸馏去除部分未反应的6-叠氮基己酸,残留物经乙醚、乙酸乙酯反复洗涤,以便进一步去除未反应的2-叠氮基乙酸及加成数目较少的非水溶性衍生化产物,然后添加体积比为50%:50%的乙酸与水的混合物超声提取多次,合并提取液经滤膜过滤,去除溶剂,得固化的粗产品;
(4)将粗产品复溶于1mol/L NaOH溶液,并使用截留分子量为500-10000道尔顿的透析袋透析,微孔滤膜过滤,干燥,由此精制得到纯净的侧链末端含羧酸盐的富勒烯多氮杂桥类水溶性衍生物的固态产品14.8g,产率60%,标记为富勒烯基聚己氨酸钠水溶性衍生物。热重分析表征其平均分子式为C60(NCH2CH2CH2CH2CH2COONa)8。
实施例8:制备C70与叠氮乙醇的水溶性加成产物C70(NCH2CH2NH2)16(氮杂富勒醇2)
(1)将5.0g C70固体粉末与51.8g液态的2-叠氮基乙醇(物质的量投料比为1:100)分别投料于100mL三口反应器,接冷凝管及机械搅拌装置,无需添加有机溶剂,直接在惰性气体氛围下机械搅拌;
(2)反应体系升温至回流,保温72小时后,停止加热;
(3)减压蒸馏去除部分未反应的2-叠氮基乙醇,残留物经乙醚、乙酸乙酯反复洗涤,以便进一步去除未反应的2-叠氮基乙醇及加成数目较少的非水溶性衍生化产物,然后添加去离子水超声提取多次至上清液无色后,合并提取液经滤膜过滤,去除溶剂,得固化的粗产品;
(4)将粗产品复溶于去离子水并使用截留分子量为500-10000道尔顿的透析袋透析,干燥,由此精制得到纯净的侧链末端含羟基的富勒烯多氮杂桥类水溶性衍生物的固态产品9.4g,产率95%,标记为氮杂富勒醇2。热重分析表征其平均分子式为C70(NCH2CH2OH)16。
实施例9:C60(NCH2CH2OH)14和C60(NCH2COONa)13水溶液体外清除自由基能力的测试
清除自由基测试方法参考文献(Li X.et al.Chemistry Central Journal.2012;6:140)的光度检测法,结果显示C60(NCH2CH2OH)14(图5)和C60(NCH2COONa)13(图6)水溶液都能有效清除2,2'-联氮双(3-乙基苯并噻唑啉-6-磺酸)二铵盐自由基(ABTS+·),且清除效果与二者的浓度呈线性依赖性,最高清除率均超过90%。这初步证实侧链末端含不同亲水官能团的富勒烯多氮杂桥水溶性衍生物在体外条件下均具备高效清除自由基的能力。这也间接阐释其可清除生物体中活性氧等自由基,本法所大规模制备的新型富勒烯多氮杂桥水溶性衍生物具备清除活体生物体系中自由基的能力。
实施例10:C60(NCH2COONa)13水溶液处理玉米种子的测试
(1)C60(NCH2COONa)13促进玉米种子萌发
利用5μg/ml和50μg/ml的C60(NCH2COONa)13水溶液浸泡24小时并培养玉米种子,以水作为对照。结果表明:萌发的第二天,经50μg/ml处理的玉米种子发芽率已接近70%,对照则40%左右,而5μg/ml C60(NCH2COONa)13处理样品与对照没有显著差异(图7)。说明一定浓度的C60(NCH2COONa)13处理能够促进萌发,提高种子萌发的整齐度及出苗率。
(2)C60(NCH2COONa)13促进玉米幼苗生长及根系发育
在上述处理下,对两叶一心期的玉米幼苗的进行测定发现,处理样品显著的促进玉米整个植物(地下部分-根长,地上部分-芽长)的发育(表1)。说明C60(NCH2COONa)13能够促进幼苗的生长。此外,发现50μg/ml C60(NCH2COONa)13处理的两叶一心期幼苗55%根系有分支现象,根条数增多,根系较为发达(图8左),5μg/ml处理下,27%的处理样根系有分支,而对照仅有17.5%的样品有分支。
表1
- 还没有人留言评论。精彩留言会获得点赞!
- 苯并双(噻二唑)衍生物、包含其的油墨、以及使用了其的有机电子装置的制造方法
- 具有含硫取代基的杀有害生物活性杂环衍生物的制造方法与工艺
- 具有含硫取代基的杀有害生物活性杂环衍生物的制造方法与工艺
- 一种苯并噻咯类衍生物及其制备方法和有机发光器件与制造工艺
- 苯并噻吩并咔唑类衍生物及其制备方法和有机发光器件与制造工艺
- 苯并二氮杂*衍生物的2-萘磺酸盐及晶型和它们的制备方法与制造工艺
- 靛红杂合喹唑啉类化合物合成的靛红衍生物及其在制备抗肿瘤药物中的应用的制造方法与工艺
- 一种杂环衍生物及使用该杂环衍生物的有机发光器件的制造方法与工艺
- 一种二氰基甲烯基苯并四氢呋喃衍生物及其制备方法与制造工艺
- 一种含氮杂环衍生物及使用该含氮杂环衍生物的有机发光器件的制造方法与工艺