一种即用型的核酸磁珠提取试剂的制作方法
本发明属于一种生物技术核酸提取纯化领域,特别是涉及一种微量的病毒核酸提取纯化试剂及其使用方法,尤其是人体体液如血清、血浆、全血、尿液、脑脊液等样本中的核酸提取。
背景技术:
核酸的分离与纯化技术是生化与分子生物学的一项基本技术,核酸是遗传信息的携带者,是蛋白表达的物质基础。无论是进行核酸结构还是功能研究,首先需要对核酸进行分离纯化。目前核酸分离技术虽然发展迅速,但是均存在一些缺点:经典的酚氯仿抽提法,虽然核酸得率高,但其对人体有害,且容易造成环境污染,同时提取过程需要反复抽提,多次高速离心换管,步骤繁琐,会造成样本的丢失与交叉污染。碱裂解法:该法操作相对简单,但提取的核酸不容易保存,纯度低且不能用于rna提取。硅胶膜吸附柱法:操作简便易于标准化,提取的核酸dna/rna纯度高得率高,但难于实现自动化、成本高、单位时间的提取通量低、提取的核酸片段不够完整(条件剧烈导致断裂较多)。
磁珠是由四氧化三铁或三氧化二铁等磁性粒子与各种含功能基团的二氧化硅材料复合而成的球形微粒,磁珠表面可被赋予多种活性功能基团,如羧基、羟基等,也可共价结合寡聚核苷酸、酶、细胞、抗体等生物活性物质。磁珠在磁场条件下可以发生聚集或分散,当粒径处于一定范围时,具有很好的瞬时响应性,即超顺磁性,可避免发生磁团聚,可在外加磁场作用下被定位、导向和分离。表面结合的基团或活性物质可以特异吸附核酸或其他生物大分子,并在磁场作用下达到分离纯化生物大分子的作用。
当前,磁珠已在核酸提取纯化中得以广泛应用,然而绝大多数商售的磁珠法核酸提取试剂盒存在缺点:提取效率低(与qiagen或roche的硅膜吸附柱法比较明显逊色),操作步骤繁琐(宣称自动化、实际操作却涉及多次人工干预并且无法从试剂角度避免),不是即用型试剂(用户使用前需要加入乙醇或异丙醇等,还需要复溶蛋白酶,载体核酸或助沉剂等)。这些缺点限制了磁珠试剂的大规模应用,用户并没有获得比传统吸附柱法更好的结果,与其它方法比较,除了可以自动化之外几乎没有其它优点,当前磁珠法的现状是,用户多一种选择,仅此而已。
技术实现要素:
本发明致力于开发一种操作简捷、可自动化、可标准化的即用型磁珠法核酸提取试剂,并提供其大规模工业化制造的方法。该试剂盒操作简便,提取核酸片段完整、纯度高,得率高,适用于杂交分析、测序、pcr、电泳、基因芯片等分子克隆等下游实验。其组分如下:①裂解结合液、②磁珠悬液、③洗涤液a、④洗涤液b、⑤洗脱液。所述裂解结合液为含有表面活性剂的异硫氰酸胍/硫氰酸胍/盐酸胍溶液,并含乙醇/异丙醇的缓冲液。优选的是2m-5mguscn,20-200mm柠檬酸钠-柠檬酸,2%-20%tritonx-100,1-6%thesit,0.1-1%sds,10-30%乙醇,所述裂解液的ph值=6-7;所述洗涤液a,优选的是30%-60%乙醇、1-2mguscn、1-20mmtris;所述洗涤液b优选的是60%-80%乙醇、10-100mmnacl和1-20mmtris;所述洗脱液含有10mmtris-hcl,0.5mmedta,ph值=8.0或者纯水;所述磁珠悬浮液优选的是磁珠含量为20-100mg/ml,磁珠颗粒直径为直径在0.1-2.5μm。
上述的磁珠法核酸提取试剂的提取方法,包括以下步骤:
1)在一次性塑料耗材中加入含有磁珠及内标的工作裂解结合液500-800μl,加入样本200μl,吸打混匀一次,使样本裂解释放出dna/rna,并结合到磁珠上,10-15分钟结合充分后,在磁场作用下,磁珠富集,磁珠-核酸复合物与液体分离。
2)向磁珠-核酸复合物加入800-1000μl洗涤液a,洗去复合物表面蛋白质、脂类以及盐离子等杂质,在磁场作用下,得到洗涤后的复合物。
3)向磁珠-核酸复合物加入800-1000μl洗涤液b,洗去复合物表面胍盐及离子杂质,在磁场作用下,得到洗涤后的复合物;
4)向洗涤后的磁珠-核酸复合物加入60-100μl洗脱液,改变磁珠和核酸结合情况,将核酸在磁珠上面洗脱下来,约需5分钟,在磁场作用下,磁珠和核酸分离,得到纯化的dna/rna。
本试剂盒适用的样本包括血清、血浆、全血、组织提取液、拭子洗液、分泌物浸泡液、粪便预处理液、病毒培养液和其他体液等。本发明所提取的核酸可直接进行pcr及rt-pcr等分子生物学实验研究以及临床检测。本试剂盒可配合自动化仪器提取病毒核酸。速度快,通量高。以下实施例仅仅是例证,本发明并不局限于这些实施例。
附图说明:
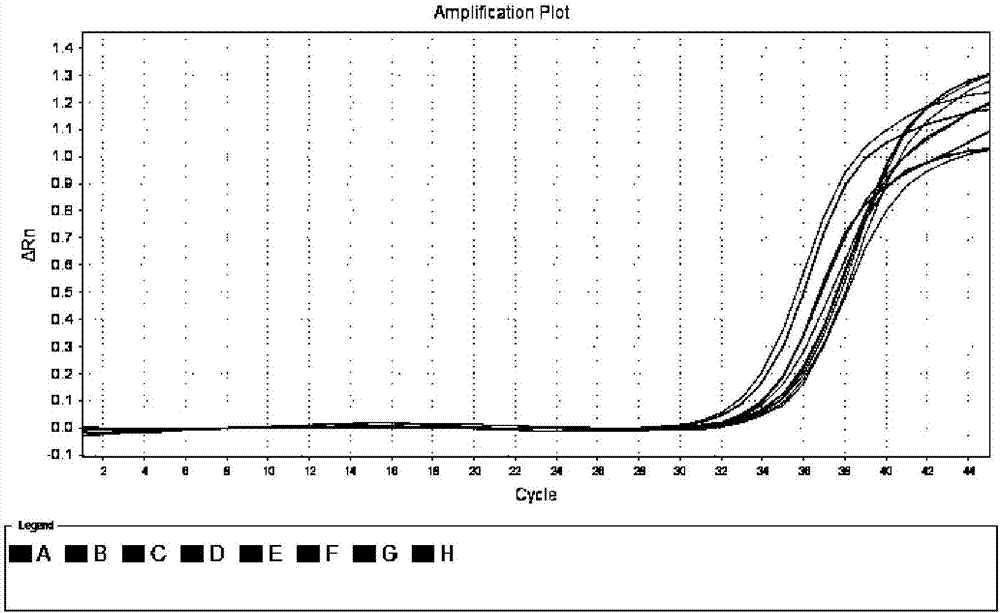
图1-1是本发明对hbvdna国家线性标准品为待测样本进行提取后用荧光pcr法检测hbvdna的结果图,横坐标代表扩增循环数,纵坐标代表荧光值强度。
图1-2是本发明对hbvdna国家线性标准品为待测样本进行提取后用荧光pcr法检测内标的结果图,横坐标代表扩增循环数,纵坐标代表荧光值强度。
图1-3是本发明对hcvrna国家线性标准品为待测样本进行提取后用荧光pcr法检测hcvrna的结果图,横坐标代表扩增循环数,纵坐标代表荧光值强度。
图1-4是本发明对hcvrna国家线性标准品为待测样本进行提取后用荧光pcr法检测内标的结果图,横坐标代表扩增循环数,纵坐标代表荧光值强度。
图2-1是本发明对待测全血样本进行提取后测定吸光度的结果图,od260值反应为浓度,a260/280、a260/230值反应为纯度。
图2-2是本发明对另一个待测全血样本进行提取后测定吸光度的结果图,od260值反应为浓度,a260/280、a260/230值反应为纯度。
实施案例1:血清或血浆中病毒核酸的提取纯化,特点是快捷、灵敏、自动化、易于与全自动平台集成
①裂解结合液:4.5mguscn、0.5%dtt、0.1m柠檬酸钠、1mm柠檬酸、0.5%sds、3%thesit、5%tritonx-100、25%乙醇
②磁珠悬液:40mg/ml硅基磁珠
③洗涤液a:30%乙醇、2mguscn、6mmtris、1.2mm柠檬酸
④洗涤液b:80%乙醇、20mmnacl、2mmtris
⑤洗脱液:含有0.04%nan3的纯水
以中检院乙型肝炎核酸(hbvdna)国家标准品线性灵敏度l0-l7为待测样本,l7为l611倍稀释所得,浓度为10iu/ml,用上述试剂及操作方法对样本进行核酸提取及荧光pcr检测。所用提取仪为西安天隆生物科技的np968磁珠法核酸提取系统和abi7500荧光pcr仪,在提取板上加含磁珠、内标的裂解结合液600μl(磁珠10μl,内标1μl),样本200μl,洗涤液a800μl、洗涤液b800μl、洗脱液100μl。上机执行提取程序,20-30分钟完成提取。结果如附图1-1:采用本发明试剂提取中检院hbv国家参考品l0-l7扩增结果,图1-2:采用本发明试剂提取中检院hbv国家参考品l0-l7内标结果。
以中检院丙型肝炎核酸(hcvrna)国家标准品线性灵敏度l0为待测样本,以阴性血清10倍梯度稀释至l5,浓度为106~101iu/ml,同上试剂、仪器及操作,对样本进行核酸提取及荧光pcr检测。结果如附图1-3:采用本发明试剂提取中检院hcv国家参考品10倍系列稀释物扩增结果,图1-4:采用本发明试剂提取中检院hcv国家参考品10倍系列稀释物内标结果。
实施案例2:全血基因组dna的提取纯化(纯度得率高,无人工干预)
1)在提取板一个操作单元(六孔)上分别加含磁珠的裂解结合液600μl(含磁珠10μl)、洗涤液a800μl、洗涤液a800μl、洗涤液b800μl、洗涤液b800μl,洗脱液100μl。
2)在裂解孔中加入全血200μl,蛋白酶(蛋白酶k干粉复溶成20mg/ml,复溶液采用5mmcacl2,10mmtris-hcl,ph7.5)10μl,混匀一次后,移入自动化提取仪,运行全血程序即可。具体为60℃裂解结合15min、洗涤a洗涤2min×2次、洗涤b洗涤2min×2次,80℃5min洗脱。取洗脱液1μl在微量紫外分光光度计上测定od260、od280及od230。如附图2-1采用本发明试剂提取全血1结果(101ng/μla260/280=1.86a260/230=1.37)及图2-2采用本发明试剂提取全血2结果(161ng/μla260/280=1.74a260/230=2.73)。
以上描述了本发明的基本原理、主要特征和本发明的优点。本行业的技术人员应该了解,本发明不受上述实施例的限制,上述实施例和说明书中描述的只是说明本发明的原理,在不脱离本发明精神和范围的前提下本发明还会有各种变化和改进,这些变化和改进都落入要求保护的本发明范围内。
- 还没有人留言评论。精彩留言会获得点赞!