人KRAS基因多点突变单管联检荧光PCR方法、试剂盒及体系与流程
本发明涉及基因甲基化水平检测技术领域,尤其涉及一种人KRAS基因多点突变单管联检荧光PCR方法、试剂盒及体系。
背景技术:
粪便既含有脱落的正常结直肠上皮细胞和游离的DNA,也含有大量从结直肠癌上脱落的癌细胞和游离的癌DNA;又由于肠道是碱性环境,有利于DNA的保存,使从粪便中提取的DNA质量较好。因此粪便基因甲基化作为一种新的、敏感度高、特异性中等的无创性结直肠肿瘤标志物,能根据其阳性结果对疑似病例进行进一步检测,作为相关肿瘤的早期筛查手段具有很重要的临床价值。
石蜡组织切片不仅用于观察正常细胞组织的形态结构,还用于研究、观察及判断细胞组织的形态变化的主要手段,由于生物组织经过固定、石蜡包埋后能够完好的保存其形态结构,大量的细胞内DNA遗传物质得以完好保存在石蜡组织当中,经过脱蜡、细胞消化、DNA提取等步骤能够将这些保存下来的DNA遗传物质释放出来。同时,石蜡组织切片也是一种短期内获取大量人体新鲜组织标本的有效方式,且部分研究涉及回顾性分析,也需要借助于病理科等长期保存的福尔马林固定石蜡包埋组织。因此,无论是作为相关肿瘤的早期筛查手段,还是从基因水平阐明肿瘤发病机制,石蜡切片组织都具有很重要的早期检测、研究用临床价值。
RAS基因家族与人类肿瘤密切相关的基因有三种HRAS、KRAS和NRAS,这三种基因编码的蛋白质大约有90%的氨基酸序列同源,分子量均为21KDa,又称为RASp21蛋白。KRAS信号通路是EGFR和其他信号转导的下游通路,当RAS基因发生突变时,其编码的RAS蛋白水解GTP-RAS能力下降,使得信号转导通路一直处于持续激活状态,刺激细胞不断增殖分化,最终导致细胞恶变。KRAS突变基因是一种常见的致癌基因,多见于恶性肿瘤,结直肠癌患者中约有30%~40%存在KRAS基因突变,肺腺癌患者中约有15%~30%存在KRAS突变。KRAS突变主要定位在第12、13、61和63号密码子,其中有7个突变热点:Gly12Asp、Gly12Val、Gly12Ser、Gly12Cys、Gly12Ala、Gly12Arg和Gly13Asp共7类热点突变,占KRAS基因总突变的90%以上。
研究表明,KRAS基因突变与NSCLC对吉非替尼、厄洛替尼等靶向治疗药物的原发性耐药有关。有研究发现KRAS基因的突变使结直肠癌患者对西妥昔单抗的治疗产生耐药性。NCCN(非小细胞肺癌临床实践指南2016版)指出KRAS基因突变会使肺癌患者对EGFR酪氨酸激酶抑制剂(EGFT-TKI)产生耐药;使结直肠癌患者对抗EGFR抗体类药物产生耐药。所以NCCN(非小细胞肺癌临床实践指南2016版)提出肺腺癌患者接受EGFR靶向药物治疗之前,必须进行KRAS基因突变检测,根据检测结果决定是否使用EGFR靶向药物作为临床治疗措施。因此对KRAS基因突变继续风险预测,可作为EGFR靶向治疗耐药性产生与否的重要预测指标。
目前临床检测DNA中基因突变的方法主要有3种:1)直接测序法,是目前应用最多的一种检测方法,主要是Sanger测序,当突变基因得到有效富集之后,才能被测序,优点是结果准确可靠,能读取到被检测序列信息,但其有效富集突变基因区域,及在突变基因含量低的情况下面临极大的挑战,一般用来确认其他检测阳性结果。2)荧光定量PCR法,在荧光定量PCR平台上,利用特异的引物对DNA突变靶序列进行PCR扩增,利用荧光标记探针对扩增产物进行突变检测,这样检测方法特异性强、灵敏度高,可检测到DNA含量低至1%的突变,但目前单管单一突变检测通量低,探针成本昂贵,很难适应临床大通量样本的风险预测。3)高通量测序技术法,一般利用PCR技术对目标区域进行富集,然后构建适合于NGS上机测序的文库,最后上机测序,信息分析获得感兴趣目标区域序列信息。但是在目前对目标区域富集过程中,富集的特异性和有效性在不同的实验平台差距大,而且普通的建库流程繁杂,周期长,成本高,这些因素都造成是否需要进行高通量测序的限制因素。
因此,目前急需一种提高通量、结果判别快速清晰的各种生物样本当中KRAS 基因突变进行风险预测的方法,为临床提供是否需要进行进一步区分突变类型、或进行高通量测序提供判断依据。
技术实现要素:
本发明提供一种人KRAS基因多点突变单管联检荧光PCR方法、试剂盒及体系,在单管PCR反应中联合检测KRAS基因第12位和第13位密码子上的7种热点突变。
根据本发明的第一方面,本发明提供一种人KRAS基因多点突变单管联检荧光PCR方法,包括:
在荧光PCR体系中,以含有人KRAS基因突变位点的DNA作为模板进行荧光PCR反应,其中上述荧光PCR体系中包括:
(a)用于检测KRAS Gly12Asp突变位点的上游引物序列:
GAATATAAACTTGTGGTAGTTGGAGCdIGA(SEQ ID NO:1),
用于检测KRAS Gly12Ala突变位点的上游引物序列:
GGAATATAAACTTGTGGTAGTTGGAGCdIGC(SEQ ID NO:2),
用于检测KRAS Gly12Val和Gly12Ser突变位点的上游引物序列:
GAATATAAACTTGTGGTAGTTGGAGCdIGT(SEQ ID NO:3),
用于检测KRAS Gly12Arg和Gly12Cys突变位点的上游引物序列:
GGAATATAAACTTGTGGTAGTTGGAGdITC(SEQ ID NO:4),
用于检测KRAS Gly13Asp突变位点的上游引物序列:
GGAATATAAACTTGTGGTAGTTGGAGCTGGdIGT(SEQ ID NO:5),
其中,上述上游引物序列中的dI表示脱氧次黄嘌呤核苷酸;
(b)用于检测KRAS各种突变位点的下游引物序列:
CCTCTATTGTTGGATCATATTCGT(SEQ ID NO:6);
(c)用于检测KRAS各种突变位点的荧光探针序列:
GAGTGCCTTGACGATACAGCTAATTC(SEQ ID NO:7),
其中,上述荧光探针序列的5’端具有荧光基团,3’端具有淬灭基团;
(d)Taq酶、UNG酶(Uracil-N-glycosylase,尿嘧啶-N-糖基化酶)、dNTPs(包括dATP、dCTP、dGTP、dTTP)、dUTP、Mg2+和PCR缓冲液;
(e)第一添加剂和第二添加剂,上述第一添加剂包括牛血清白蛋白,上述第二添加剂包括二甲基亚砜、NH4Cl和山梨糖醇水溶液。
进一步地,上述荧光基团是FAM,上述淬灭基团是BHQ1。当然,荧光基团也可以是HEX、TET等其他荧光基团,淬灭基团也可以是TAMRA等其他淬灭基团。
进一步地,上述荧光PCR体系中还包括:
用于KRAS监控的内标序列,包括:
上游引物序列为:CCTAGTAGGAAATAAATGTGATTTGCC(SEQ ID NO:8),
荧光探针序列为:
TAGAACAGTAGACACAAAACAGGCTCAGGACTT(SEQ ID NO:9),
下游引物序列为:CTGTCTTGTCTTTGCTGATGTTTCA(SEQ ID NO:10),
其中,上述荧光探针序列的5’端具有荧光基团VIC,3’端具有淬灭基团BHQ1。
进一步地,每50μL上述荧光PCR体系中含有:
Taq酶、UNG酶2个单位;10mM的dNTPs和2.5mM的dUTP 0.4μL;50mM的Mg2+1.5μL;10×PCR缓冲液5μL;10μM的引物序列各自1~2μL,10μM的探针序列3~4μL;含有人KRAS基因突变位点的DNA 20~40ng;10mg/mL牛血清白蛋白2μL,二甲基亚砜、250mM NH4Cl和60%山梨糖醇水溶液1.25μL,以及余量的水。
进一步地,上述每50μL上述荧光PCR体系中还含有:
10μM的上述内标的引物序列各自1μL,以及10μM的上述内标的探针序列0.5μL;上述内标的引物序列和探针序列包括:
用于KRAS监控的内标序列,包括:
上游引物序列为:CCTAGTAGGAAATAAATGTGATTTGCC(SEQ ID NO:8),
荧光探针序列为:
TAGAACAGTAGACACAAAACAGGCTCAGGACTT(SEQ ID NO:9),
下游引物序列为:CTGTCTTGTCTTTGCTGATGTTTCA(SEQ ID NO:10),
其中,上述荧光探针序列的5’端具有荧光基团VIC,3’端具有淬灭基团BHQ1。
进一步地,上述荧光PCR反应的程序为:
50℃反应2min;95℃反应5min;95℃反应15s然后60℃反应30s进行15个循环;95℃反应15s然后60℃反应30s进行30个循环并收集荧光信号;20℃反应2min。
根据本发明的第二方面,本发明提供一种人KRAS基因多点突变单管联检荧光PCR试剂盒,包括:
(a)用于检测KRAS Gly12Asp突变位点的上游引物序列:
GAATATAAACTTGTGGTAGTTGGAGCdIGA(SEQ ID NO:1),
用于检测KRAS Gly12Ala突变位点的上游引物序列:
GGAATATAAACTTGTGGTAGTTGGAGCdIGC(SEQ ID NO:2),
用于检测KRAS Gly12Val和Gly12Ser突变位点的上游引物序列:
GAATATAAACTTGTGGTAGTTGGAGCdIGT(SEQ ID NO:3),
用于检测KRAS Gly12Arg和Gly12Cys突变位点的上游引物序列:
GGAATATAAACTTGTGGTAGTTGGAGdITC(SEQ ID NO:4),
用于检测KRAS Gly13Asp突变位点的上游引物序列:
GGAATATAAACTTGTGGTAGTTGGAGCTGGdIGT(SEQ ID NO:5),
其中,上述上游引物序列中的dI表示脱氧次黄嘌呤核苷酸;
(b)用于检测KRAS各种突变位点的下游引物序列:
CCTCTATTGTTGGATCATATTCGT(SEQ ID NO:6);
(c)用于检测KRAS各种突变位点的荧光探针序列:
GAGTGCCTTGACGATACAGCTAATTC(SEQ ID NO:7),
其中,上述荧光探针序列的5’端具有荧光基团,3’端具有淬灭基团;
(d)Taq酶、UNG酶、dNTPs、dUTP、Mg2+和PCR缓冲液;
(e)第一添加剂和第二添加剂,上述第一添加剂包括牛血清白蛋白,上述第二添加剂包括二甲基亚砜、NH4Cl和山梨糖醇水溶液;
任选地,(f)用于KRAS监控的内标序列,包括:
上游引物序列为:CCTAGTAGGAAATAAATGTGATTTGCC(SEQ ID NO:8),
荧光探针序列为:
TAGAACAGTAGACACAAAACAGGCTCAGGACTT(SEQ ID NO:9),
下游引物序列为:CTGTCTTGTCTTTGCTGATGTTTCA(SEQ ID NO:10),
其中,上述荧光探针序列的5’端具有荧光基团VIC,3’端具有淬灭基团BHQ1。
进一步地,上述荧光基团是FAM,上述淬灭基团是BHQ1。
根据本发明的第三方面,本发明提供一种人KRAS基因多点突变单管联检荧光PCR反应体系,每50μL上述荧光PCR反应体系包括:
(1)10μM的引物序列各自1~2μL,10μM的探针序列各自3~4μL;其中,上述引物序列和探针序列包括:
(1a)用于检测KRAS Gly12Asp突变位点的上游引物序列:
GAATATAAACTTGTGGTAGTTGGAGCdIGA(SEQ ID NO:1),
用于检测KRAS Gly12Ala突变位点的上游引物序列:
GGAATATAAACTTGTGGTAGTTGGAGCdIGC(SEQ ID NO:2),
用于检测KRAS Gly12Val和Gly12Ser突变位点的上游引物序列:
GAATATAAACTTGTGGTAGTTGGAGCdIGT(SEQ ID NO:3),
用于检测KRAS Gly12Arg和Gly12Cys突变位点的上游引物序列:
GGAATATAAACTTGTGGTAGTTGGAGdITC(SEQ ID NO:4),
用于检测KRAS Gly13Asp突变位点的上游引物序列:
GGAATATAAACTTGTGGTAGTTGGAGCTGGdIGT(SEQ ID NO:5),
其中,上述上游引物序列中的dI表示脱氧次黄嘌呤核苷酸;
(1b)用于检测KRAS各种突变位点的下游引物序列:
CCTCTATTGTTGGATCATATTCGT(SEQ ID NO:6);
(1c)用于检测KRAS各种突变位点的荧光探针序列:
GAGTGCCTTGACGATACAGCTAATTC(SEQ ID NO:7),
其中,上述荧光探针序列的5’端具有荧光基团,3’端具有淬灭基团;
(2)Taq酶、UNG酶2个单位;10mM的dNTPs和2.5mM的dUTP 0.4μL;50mM的Mg2+1.5μL;10×PCR缓冲液5μL;
(3)第一添加剂2μL,第二添加剂1.25μL,上述第一添加剂包括10mg/mL牛血清白蛋白,上述第二添加剂包括二甲基亚砜、250mM NH4Cl和60%山梨糖醇水溶液;
(4)含有人KRAS基因突变位点的DNA 20~40ng;以及
(5)余量的水。
进一步地,上述每50μL上述荧光PCR体系中还含有:
(6)10μM的内标的引物序列各自1μL,以及10μM的内标的探针序列0.5μL,其中上述内标的引物序列和探针序列包括用于KRAS监控的内标序列,包括:
上游引物序列为:CCTAGTAGGAAATAAATGTGATTTGCC(SEQ ID NO:8),
荧光探针序列为:
TAGAACAGTAGACACAAAACAGGCTCAGGACTT(SEQ ID NO:9),
下游引物序列为:CTGTCTTGTCTTTGCTGATGTTTCA(SEQ ID NO:10),
其中,上述荧光探针序列的5’端具有荧光基团VIC,3’端具有淬灭基团BHQ1。
本发明的有益效果体现在:本发明解决了单管反应中联合检测KRAS基因7类热点突变的难题,以往的试剂盒通常为单管反应检测单个热点突变,该项KRAS基因联合检测手段节省了物力和人力成本,为大量样本的KRAS基因突变检测提供了途径。此外,以往的试剂盒通常采用△△CT的算法对检测结果进行判读,100ng野生型人DNA即易产生较强非特异性扩增,造成结果判别不清导致的假阳性结果。而本发明检测结果判读快速直观,KRAS基因联合检测手段无需△△CT的算法,在200ng人DNA中无扩增信号,有突变即有扩增信号,结果判别快速清晰。
附图说明
图1为突变型序列可以检测出荧光信号,野生型序列检测无荧光信号的原理示意图,其中dI(deoxyInosine)为脱氧次黄嘌呤修饰3’端倒数第3个碱基,其结合力弱;
图2为阴性参照人DNA 200ng(100%)KRAS基因7类热点突变目标区域检测信号FAM荧光曲线图;
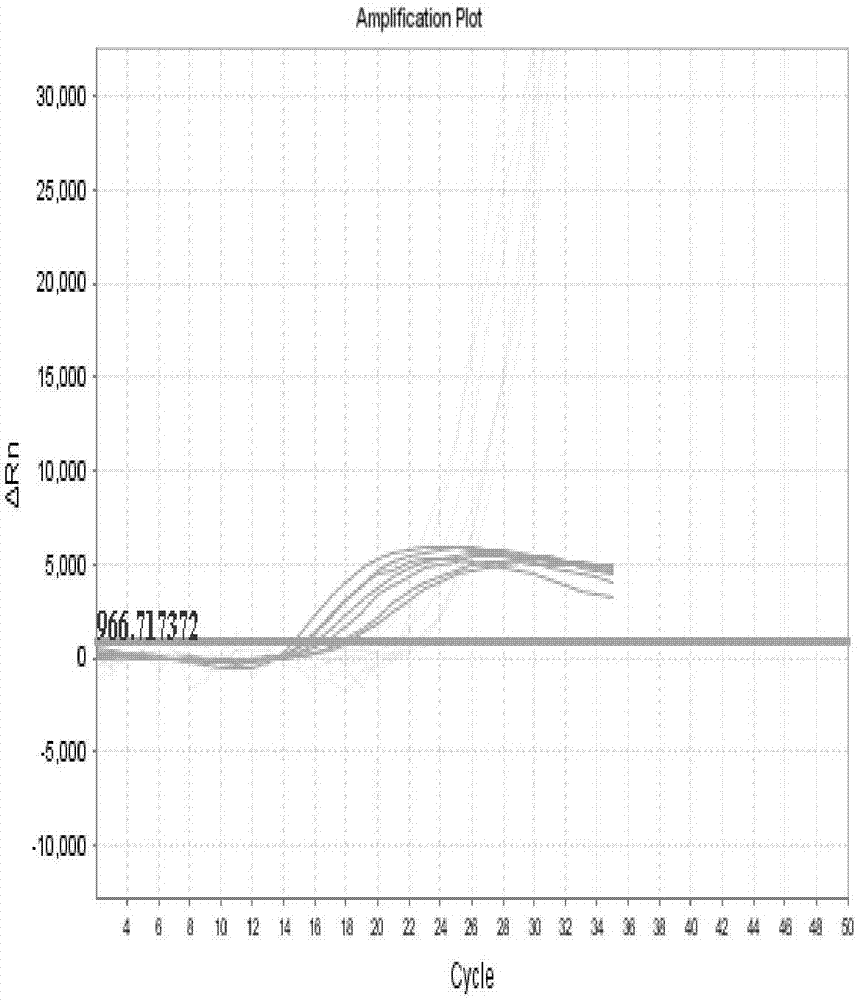
图3为阴性参照人DNA 200ng(100%)KRAS基因7类热点突变内标区域检测信号VIC荧光曲线图;
图4为KRAS基因7类突变质粒5*102拷贝(1%)+人DNA 200ng(99%)目标区域检测信号FAM荧光曲线图;
图5为KRAS基因7类突变质粒5*102拷贝(1%)+人DNA 200ng(99%)内标区域检测信号VIC荧光曲线图;
图6为KRAS基因7类突变质粒5*104拷贝(50%)+人DNA 200ng(50%)目标区域检测信号FAM荧光曲线图;
图7为KRAS基因7类突变质粒5*104拷贝(50%)+人DNA 200ng(50%)内标区域检测信号VIC荧光曲线图;
图8为人粪便样本DNA 100ng(100%)KRAS基因7类热点突变目标区域检测信号FAM荧光曲线图;
图9为人粪便样本DNA 100ng(100%)KRAS基因7类热点突变内标区域检测信号VIC荧光曲线图;
图10为人游离血DNA 3ng(100%)KRAS基因7类热点突变目标区域检测信号FAM荧光曲线图;
图11为人游离血DNA 3ng(100%)KRAS基因7类热点突变内标区域检测信号VIC荧光曲线图。
具体实施方式
下面通过具体实施方式结合附图对本发明作进一步详细说明。
本发明人进行了一系列研究,并在研究人粪便DNA、石蜡切片DNA的KRAS突变基因检测时发明了一种新的人KRAS基因多点突变单管联检荧光PCR方法和试剂盒,有非诊断性用途。本发明的检测方法针对人KRAS基因7类热点突变(表1)设计引物及其探针,即通过对上述生物样本中KRAS基因7类热点突变基因的上游特异性ARMS引物设计与碱基修饰(图1),下游共用Taq-man探针与引物,结合优化的PCR反应液及高效Taq酶,并进一步对PCR扩增体系当中dNTPs、Mg离子、NH4Cl、牛血清白蛋白(BSA)、二甲基亚砜(DMSO)、山梨糖醇等化学试剂特定比例组成的添加,以达到ARMS-PCR引物工作的最佳反应体系条件,对PCR扩增步骤的优化,结合q-PCR平台,实现KRAS基因7类热点突变基因的联合检测(不区分具体突变类型),同时在200ng/反应的野生型人DNA背景下无扩增信号,不出现假阳性情况,检测结果快速、直观、方便进行判别。
表1 KRAS基因7种常见突变
本发明所使用的特异性引物及其探针序列包括:
(a)用于检测KRAS Gly12Asp突变位点的上游引物序列:
GAATATAAACTTGTGGTAGTTGGAGCdIGA(SEQ ID NO:1),
用于检测KRAS Gly12Ala突变位点的上游引物序列:
GGAATATAAACTTGTGGTAGTTGGAGCdIGC(SEQ ID NO:2),
用于检测KRAS Gly12Val和Gly12Ser突变位点的上游引物序列:
GAATATAAACTTGTGGTAGTTGGAGCdIGT(SEQ ID NO:3),
用于检测KRAS Gly12Arg和Gly12Cys突变位点的上游引物序列:
GGAATATAAACTTGTGGTAGTTGGAGdITC(SEQ ID NO:4),
用于检测KRAS Gly13Asp突变位点的上游引物序列:
GGAATATAAACTTGTGGTAGTTGGAGCTGGdIGT(SEQ ID NO:5),
其中,上述上游引物序列中的dI表示脱氧次黄嘌呤核苷酸;
(b)用于检测KRAS各种突变位点的下游引物序列:
CCTCTATTGTTGGATCATATTCGT(SEQ ID NO:6);
(c)用于检测KRAS各种突变位点的荧光探针序列:
GAGTGCCTTGACGATACAGCTAATTC(SEQ ID NO:7),
其中,上述荧光探针序列的5’端具有荧光基团,3’端具有淬灭基团;
上游引物序列中的dI位于3’端倒数第3个碱基,该碱基的存在,使得其与目标区域的结合力变弱,从而使得一旦引物序列3’末端的碱基不能与目标区域配对,则难以发生扩增反应,也就是在野生型序列的情况下,3’末端的碱基不能发生配对,则无法发生扩增反应;而在突变型序列的情况下,3’末端的碱基依然能够发生配对,发生扩增反应。因此,上述特异性引物及其探针序列的巧妙设计,保证了单管反应中联合检测KRAS基因7类热点突变。
本发明还使用UNG酶,其选择性水解断裂含有dU的双链或单链DNA中的尿嘧啶糖苷键,形成的有缺失碱基的DNA链,在碱性介质以及高温下会进一步水解断裂。因此在UNG酶和dUTP存在的体系,能够消除和防止污染。例如,在PCR反应前设置50℃反应2min的步骤,使UNG酶作用于U碱基切断环境当中可能存在的扩增产物,以排除由此可能引起的假阳性结果,使检测结果更准确。
本发明使用牛血清白蛋白作为第一添加剂,以及含有二甲基亚砜、NH4Cl和山梨糖醇水溶液的第二添加剂,能够为探针和引物在对野生型序列/突变型序列不同的情况下,灵敏地结合或不结合目标区域。也就是说,第一添加剂和第二添加剂的存在,为探针和引物的结合提供有利的环境,使得在突变型序列的情况下,产生阳性的荧光PCR信号;而在野生型序列的情况下,不能产生阳性的荧光PCR信号。
此外,设置用于KRAS监控的内标序列,与目标基因采用不同的荧光标记探针,通过检测内标是否正常来监测待测样本有效DNA的量,同时监测样本中是否具有PCR抑制物,避免PCR假阴性。
发明人还对荧光PCR反应体系进行了优化,实现了最佳的扩增效果。发明人得到一个最佳的荧光PCR反应体系,每50μL荧光PCR体系中含有:Taq酶、UNG酶2个单位;10mM的dNTPs和2.5mM的dUTP 0.4μL;50mM的Mg2+1.5μL;10×PCR缓冲液5μL;10μM的引物序列各自1~2μL,10μM的探针序列3~4μL;含有人KRAS基因突变位点的DNA 20~40ng;10mg/mL牛血清白蛋白2μL,二甲基亚砜、250mM NH4Cl和60%山梨糖醇水溶液1.25μL,以及余量的水。
以下通过实施例详细说明本发明的技术方案和技术效果,应当理解,实施例仅是示例性的,不能理解为对本发明保护范围的限制。
以下实施例中,使用的特异性引物及其探针序列如下:
用于检测KRAS Gly12Asp突变位点的上游引物序列:
GAATATAAACTTGTGGTAGTTGGAGCdIGA(SEQ ID NO:1),
用于检测KRAS Gly12Ala突变位点的上游引物序列:
GGAATATAAACTTGTGGTAGTTGGAGCdIGC(SEQ ID NO:2),
用于检测KRAS Gly12Val和Gly12Ser突变位点的上游引物序列:
GAATATAAACTTGTGGTAGTTGGAGCdIGT(SEQ ID NO:3),
用于检测KRAS Gly12Arg和Gly12Cys突变位点的上游引物序列:
GGAATATAAACTTGTGGTAGTTGGAGdITC(SEQ ID NO:4),
用于检测KRAS Gly13Asp突变位点的上游引物序列:
GGAATATAAACTTGTGGTAGTTGGAGCTGGdIGT(SEQ ID NO:5),
其中,上述上游引物序列中的dI表示脱氧次黄嘌呤核苷酸;
用于检测KRAS各种突变位点的下游引物序列:
CCTCTATTGTTGGATCATATTCGT(SEQ ID NO:6);
用于检测KRAS各种突变位点的荧光探针序列:
FAM-GAGTGCCTTGACGATACAGCTAATTC-BHQ1(SEQ ID NO:7)。
用于KRAS监控的内标序列,包括:
上游引物序列为:CCTAGTAGGAAATAAATGTGATTTGCC(SEQ ID NO:8),
荧光探针序列为:
VIC-TAGAACAGTAGACACAAAACAGGCTCAGGACTT-BHQ1(SEQ ID NO:9),
下游引物序列为:CTGTCTTGTCTTTGCTGATGTTTCA(SEQ ID NO:10)。
检测KRAS基因7类热点突变的单管反应液的组成成分如下表2所示:
表2
荧光PCR反应的程序为:50℃反应2min;95℃反应5min;95℃反应15s然后60℃反应30s进行15个循环;95℃反应15s然后60℃反应30s进行30个循环并收集荧光信号;20℃反应2min。
图2示出了阴性参照人DNA 200ng(100%)KRAS基因7类热点突变目标区域检测信号FAM荧光曲线图,可见无荧光信号;图3示出了阴性参照人DNA 200ng(100%)KRAS基因7类热点突变内标区域检测信号VIC荧光曲线图,可见有荧光信号;图4示出了KRAS基因7类突变质粒5*102拷贝(1%)+人DNA 200ng(99%)目标区域检测信号FAM荧光曲线图,可见有荧光信号;图5示出了KRAS基因7类突变质粒5*102拷贝(1%)+人DNA 200ng(99%)内标区域检测信号VIC荧光曲线图,可见有荧光信号;图6示出了KRAS基因7类突变质粒5*104拷贝(50%)+人DNA 200ng(50%)目标区域检测信号FAM荧光曲线图,可见有荧光信号;图7示出了KRAS基因7类突变质粒5*104拷贝(50%)+人DNA 200ng(50%)内标区域检测信号VIC荧光曲线图,可见有荧光信号;图8示出了人粪便样本DNA 100ng(100%)KRAS基因7类热点突变目标区域检测信号FAM荧光曲线图,可见无荧光信号;图9示出了人粪便样本DNA 100ng(100%)KRAS基因7类热点突变内标区域检测信号VIC荧光曲线图,可见有荧光信号;图10示出了人游离血DNA 3ng(100%)KRAS基因7类热点突变目标区域检测信号FAM荧光曲线图,可见无荧光信号;图11示出了人游离血DNA 3ng(100%)KRAS基因7类热点突变内标区域检测信号VIC荧光曲线图,可见有荧光信号。
以上内容是结合具体的实施方式对本发明所作的进一步详细说明,不能认定本发明的具体实施只局限于这些说明。对于本发明所属技术领域的普通技术人员来说,在不脱离本发明构思的前提下,还可以做出若干简单推演或替换,都应当视为属于本发明的保护范围。
SEQUENCE LISTING
<110> 人和未来生物科技(长沙)有限公司
<120> 人KRAS基因多点突变单管联检荧光PCR方法、试剂盒及体系
<130> 17I23926
<160> 10
<170> PatentIn version 3.3
<210> 1
<211> 29
<212> DNA
<213> 人工序列
<220>
<221> misc_feature
<222> (27)..(27)
<223> n是脱氧次黄嘌呤
<400> 1
gaatataaac ttgtggtagt tggagcnga 29
<210> 2
<211> 30
<212> DNA
<213> 人工序列
<220>
<221> misc_feature
<222> (28)..(28)
<223> n是脱氧次黄嘌呤
<400> 2
ggaatataaa cttgtggtag ttggagcngc 30
<210> 3
<211> 29
<212> DNA
<213> 人工序列
<220>
<221> misc_feature
<222> (27)..(27)
<223> n是脱氧次黄嘌呤
<400> 3
gaatataaac ttgtggtagt tggagcngt 29
<210> 4
<211> 29
<212> DNA
<213> 人工序列
<220>
<221> misc_feature
<222> (27)..(27)
<223> n是脱氧次黄嘌呤
<400> 4
ggaatataaa cttgtggtag ttggagntc 29
<210> 5
<211> 33
<212> DNA
<213> 人工序列
<220>
<221> misc_feature
<222> (31)..(31)
<223> n是脱氧次黄嘌呤
<400> 5
ggaatataaa cttgtggtag ttggagctgg ngt 33
<210> 6
<211> 24
<212> DNA
<213> 人工序列
<400> 6
cctctattgt tggatcatat tcgt 24
<210> 7
<211> 26
<212> DNA
<213> 人工序列
<400> 7
gagtgccttg acgatacagc taattc 26
<210> 8
<211> 27
<212> DNA
<213> 人工序列
<400> 8
cctagtagga aataaatgtg atttgcc 27
<210> 9
<211> 33
<212> DNA
<213> 人工序列
<400> 9
tagaacagta gacacaaaac aggctcagga ctt 33
<210> 10
<211> 25
<212> DNA
<213> 人工序列
<400> 10
ctgtcttgtc tttgctgatg tttca 25
- 还没有人留言评论。精彩留言会获得点赞!