用于诊断、预测肝癌疗效和预后的基因甲基化面板的制作方法
本发明涉及基因表观遗传学技术领域,尤其是一种用于诊断、预测肝癌疗效和预后的基因甲基化面板,以及利用该基因甲基化面板诊断肝癌、预测疗效和复发情况,以及预测肝癌预后和死亡风险的方法。
背景技术:
肝细胞肝癌(hepatocellularcarcinoma,hcc)是我国常见恶性肿瘤之一。由于肝癌起病隐匿,早期没有症状,且多数患者缺乏普查意识,往往出现症状才到医院就诊而被诊断为晚期肝癌,而晚期肝癌治疗效果很不理想,平均生存期一般只有3-6个月。对于肝癌患者而言,如果早期发现和诊断肝癌,就更有可能接受根治性治疗(手术、消融等),其治疗效果和预后均明显优于晚期肝癌。因此,肝癌的早期诊断意义非常重大。
正常生理条件下,人体血循环中存在由凋亡和坏死的细胞释放的游离dna(cellfreedna,cfdna),肿瘤患者的血循环中还可检测到游离循环肿瘤dna(circulatingtumordna,ctdna),由于ctdna携带有与原发肿瘤组织相一致的分子遗传学改变,并且能全面的反映患者体内肿瘤细胞的遗传信息和演变进程,可以作为理想的肿瘤标志物,用于肿瘤的诊断、分子分型、疗效评价和追踪以及预后评估。
肿瘤细胞中的遗传学异常表现多样且存在明显的个体性,包括突变(mutation),拷贝数变异(copy-numbervariation),微卫星不稳定(microsatelliteinstability),杂合性缺失(lossofheterozygosity)等。这些异常不仅在不同肿瘤之间差异很大,即使在同一肿瘤的不同患者之间也具有高度的个体异质性(individualheterogeneity),使得在ctdna中检测这些改变和结果分析异常复杂。与此相比,在多种肿瘤的ctdna中可检测到相似的甲基化改变,而同一类型肿瘤ctdna的甲基化谱则更为稳定和一致。随着甲基化特异性pcr、二代测序(next-generationsequencing,ngs)等技术的飞速发展,使得高通量、准确、相对廉价的dna甲基化谱检测成为可能,也促使ctdna甲基化谱的检测日益成为目前液体活检技术的热点之一,可以准确筛查早期或超早期癌症,有助于癌症的早期诊断、早期评估、早期预防、早期治疗。
技术实现要素:
本发明公开了一种用于诊断、预测肝癌疗效和预后的基因甲基化面板,以及利用该面板诊断肝癌、预测疗效和复发情况,以及预测肝癌预后和死亡风险的方法
第一个方面,本发明提供一种用于诊断、预测肝癌疗效和预后的基因甲基化面板,所述基因甲基化面板包括第一组甲基化基因和第二组甲基化基因,所述第一组甲基化基因包括bmpr1a,psd4,arhgap25,klf3,plac8,atxn1,chr6:170,chr6:3,atad2和chr8:20,所述第二组甲基化基因包括sh3pxd2a,c11orf9,ppfia1,chr17:78,serpinb5,notch3,grhl2和tmem8b。
进一步地,所述基因甲基化面板测定肝癌患者血浆中的bmpr1a,psd4,arhgap25,klf3,plac8,atxn1,chr6:170,chr6:3,atad2和chr8:20的甲基化水平改变,以诊断肝癌和预测肝癌的治疗疗效、预测肝癌复发。
进一步地,所述基因甲基化面板测定肝癌患者血浆中的sh3pxd2a,c11orf9,ppfia1,chr17:78,serpinb5,notch3,grhl2和tmem8b的甲基化水平改变,以预测肝癌患者的预后和死亡风险。
第二个方面,本发明提供一种上述用于预测肝癌复发和预后的基因甲基化面板的检测方法,包括以下步骤:
第一步,在血浆中提取ctdna;
第二步,对提取的所述ctdna进行亚硫酸盐转化,使所述ctdna中未发生甲基化的胞嘧啶脱氨基转变成尿嘧啶,而甲基化的胞嘧啶保持不变,得到亚硫酸盐转化ctdna;
第三步,用深度测序的方法测定所述亚硫酸盐转化ctdna的甲基化水平的改变;
第四步,探针的设计和合成;
第五步,通过所述探针对所述亚硫酸盐转化ctdna进行捕获扩增并进行测序;
第六步,数据的分析和模型的建立。
在本发明的检测方法的第一步中,血浆可以是正常人的血浆或者肝癌患者的血浆。ctdna(circulatingtumordna)是指循环肿瘤dna。
在本发明中,深度测序也称高通量测序技术,为本领域技术人员所知晓的一种测序技术。
进一步地,第四步所述探针的设计和合成采取以下步骤;
首先,对tcga和gse数据库里的肝癌组织样本和正常人血浆样本的450k基因甲基化芯片数据进行分析,找出甲基化水平明显差异的基因;
然后,在同一患者的肝癌组织和血浆样本中用深度测序的方法测定上一步筛选出的所述基因的甲基化水平的改变,进一步筛选出同时能在患者肝癌组织和血浆中检测出来且甲基化水平变化一致的基因;其中,“测定上一步筛选出的所述基因的甲基化水平的改变”是指对450k基因甲基化芯片数据进行分析的步骤中所筛选出的甲基化水平明显差异的基因,对这些基因的甲基化水平的改变进行测定。
针对筛选出来的甲基化水平变化一致的基因设计探针并合成。
在本发明中,采用常规探针设计软件设计探针,例如采用ppdesigner软件设计上述同时能在同一患者的肝癌组织和血浆里检测出来且甲基化水平变化一致的基因探针。探针的合成方法采用现有成熟技术即可,例如可应用核酸杂交技术,用单独的寡核苷酸进行探针合成。
在本发明中,可以通过本领域常用方法使用探针捕获亚硫酸盐转化ctdna,经扩增后进行相应测序。或者,采用以下步骤进行捕获扩增后并测序:
首先,将所述亚硫酸盐转化ctdna与第四步中合成的所述探针混合于反应缓冲液中形成反应液,在所述反应液上加矿物油;
然后,对所述反应液进行退火和变性,pcr扩增并给每个血浆样本附上条码,pcr反应建立文库,并保留有效的捕获,去除空白的捕获;
用illumina公司的适配引物和浓度以pcr方法纯化所建文库,采用illumina公司的miseq和hiseq2500系统来进行测序,得到测序结果。
在本发明中,所述反应缓冲液采用本领域中在进行dna捕获时的常用反应缓冲液即可。
优选地,所述亚硫酸盐转化ctdna与所述探针按照1:20000的摩尔比混合;在本发明中,在所述反应液上加矿物油的目的是防止反应液蒸发。
进一步地,在所述用于预测肝癌复发和预后的基因甲基化面板的检测方法中,还包括在第五步后进行优化捕获:对所述测序结果进行相对效率计算,混合探针时根据采用调节后的摩尔比率进行混合。
在本发明中,由于在第五步中,测序的原始捕获实验结果(即测序结果)在高效率的探针和低效率的探针中读取的结果有显著差异,为了改善这种情况,故需进行优化捕获,使测序的覆盖更加均匀、测序结果更加合理。
进一步地,第六步中,所述数据的分析和模型的建立采取以下步骤:
首先,通过将肝癌血浆样本和正常对照的血浆样本随机按2:1的比例分为训练集和验证集,选用lasso和随机森林的方法对第五步中的所述基因的甲基化测序结果进行筛选,两种方法重叠的基因有10个,分别为bmpr1a,psd4,arhgap25,klf3,plac8,atxn1,chr6:170,chr6:3,atad2,chr8:20;
然后,通过逻辑回归方法,采用这10个重叠的甲基化基因作为协变量建立诊断预测模型,计算联合诊断指数,并在所述验证集中进行验证;
同样,将肝癌血浆样本分为训练集和验证集,先通过对每一个基因作为协变量建立一个单变量cox比例风险模型,筛选出与患者预后相关(p<0.05)的基因进行下一步分析;
接着,采用lasso-cox多因素回归分析,最终筛选出8个甲基化基因进行预后的分析,分别为sh3pxd2a,c11orf9,ppfia1,chr17:78,serpinb5,notch3,grhl2,tmem8b;
最后,通过拟合多变量cox比例风险模型,在训练集确定这8个甲基化基因中每一个基因的系数,计算合并后的预后评分指数,并在验证集中进行验证。
在本发明中,联合诊断指数(combineddiagnosisscore)定义为cd-score。预后评分指数(combinedprognosticscore)定义为cp-score。
进一步地,在所述lasso方法中,采用二次抽样方法不重复抽样75%的数据集500次,选择出现频率超过450次的甲基化基因共30个。
进一步地,在所述随机森林方法中,使用oob误差最小化准则,通过设置变量每次重复的分数下降0.3的原则进行随机变量的消除,最后筛选出24个甲基化基因。在本发明中oob是指out-of-bag,泛化误差估计的方法。
第三个方面,本发明提供一种用于预测肝癌的复发的方法,包括以下步骤:
提供一种如上述的基因甲基化面板,包括第一组甲基化基因,所述第一组甲基化基因包括bmpr1a,psd4,arhgap25,klf3,plac8,atxn1,chr6:170,chr6:3,atad2和chr8:20;
以第一组甲基化基因构建诊断预测模型;
提供肝癌血浆样本,根据所述诊断预测模型计算出肝癌血浆样本的联合诊断指数,以预测肝癌的复发情况。
第四个方面,本发明提供一种用于预测肝癌的预后的方法,包括以下步骤:
提供一种如上述的基因甲基化面板,包括第二组甲基化基因,所述第二组甲基化基因包括sh3pxd2a,c11orf9,ppfia1,chr17:78,serpinb5,notch3,grhl2和tmem8b;
以第二组甲基化基因构建预后风险模型;提供肝癌血浆样本,根据所述预后风险模型计算出肝癌血浆样本的预后评分指数,以预测肝癌的预后情况。
本发明的技术效果:本发明提供一种用于诊断、预测肝癌疗效和预后的基因甲基化面板,同时提供了利用该基因甲基化面板诊断,预测肝癌复发和预后的方法,可用于早期诊断原发性肝癌,并可预测肝癌患者的治疗效果、复发和预后,该基因甲基化面板共包含18个基因,通过检测患者血浆中bmpr1a,psd4,arhgap25,klf3,plac8,atxn1,chr6:170,chr6:3,atad2,chr8:20共10个基因甲基化水平的改变,可以用于诊断肝癌和预测肝癌的治疗疗效,通过检测患者血浆中sh3pxd2a,c11orf9,ppfia1,chr17:78,serpinb5,notch3,grhl2,tmem8b共8个基因甲基化水平的改变,可以用于预测肝癌患者的预后和死亡风险,提高了通过肝癌患者血液诊断和预后预测的准确性。
附图说明
图1至图3是本发明用于诊断、预测肝癌疗效复发和预后的基因甲基化面板的示意图。
具体实施方式
下面将对本发明实施例中的技术方案进行清楚、完整地描述,显然,所描述的实施例仅是本发明一部分实施例,而不是全部的实施例。基于本发明中的实施例,本领域普通技术人员在没有做出创造性劳动前提下所获得的所有其他实施例,都属于本发明保护的范围。
需要说明的是,本发明实施例的术语“包括”和“具有”以及它们的任何变形,意图在于覆盖不排他的包含,例如,包含了一系列步骤或单元的过程、方法、系统、产品或设备不必限于清楚地列出的那些步骤或单元,而是可包括没有清楚地列出的或对于这些过程、方法、产品或设备固有的其它步骤或单元。
本实施例公开了一种用于诊断、预测肝癌疗效和预后的基因甲基化面板,该基因甲基化面板包括第一组甲基化基因和第二组甲基化基因,第一组甲基化基因包括bmpr1a,psd4,arhgap25,klf3,plac8,atxn1,chr6:170,chr6:3,atad2和chr8:20,第二组甲基化基因包括sh3pxd2a,c11orf9,ppfia1,chr17:78,serpinb5,notch3,grhl2和tmem8b。该基因甲基化面板测定肝癌患者血浆中的bmpr1a,psd4,arhgap25,klf3,plac8,atxn1,chr6:170,chr6:3,atad2和chr8:20的甲基化水平改变,用于诊断肝癌和预测肝癌的治疗疗效、预测肝癌复发。该基因甲基化面板测定肝癌患者血浆中的sh3pxd2a,c11orf9,ppfia1,chr17:78,serpinb5,notch3,grhl2和tmem8b的甲基化水平改变,用于预测肝癌患者的预后和死亡风险。
本实施例还公开了上述用于预测肝癌复发和预后的基因甲基化面板的检测方法,包括以下步骤:
第一步,在血浆中提取ctdna;
第二步,对提取的所述ctdna进行亚硫酸盐转化,使所述ctdna中未发生甲基化的胞嘧啶脱氨基转变成尿嘧啶,而甲基化的胞嘧啶保持不变,得到亚硫酸盐转化ctdna;
第三步,用深度测序的方法测定所述亚硫酸盐转化ctdna的甲基化水平的改变;
第四步,探针的设计和合成;具体是:首先,对tcga和gse数据库里的肝癌组织样本和正常人血浆样本的450k基因甲基化芯片数据进行分析,找出甲基化水平明显差异的基因;然后,在同一病人的组织和血浆样本中用深度测序的方法测定上一步筛选出的基因的甲基化水平的改变,并筛选出同时能在组织和血浆里检测出来且甲基化水平变化一致的基因;用ppdesigner软件设计筛选出来的甲基化水平变化一致的基因的探针,并进行合成,例如应用核酸杂交技术,用单独的寡核苷酸进行探针合成。
第五步,通过所述探针对所述亚硫酸盐转化ctdna进行捕获;具体是:将10ng亚硫酸盐转化dna与上述合成的探针按1:20000摩尔比混合于20ul反应缓冲液中形成反应液,反应液上加50ul矿物油以防止液体蒸发。对反应液进行退火和变性,pcr扩增并给每个血浆样本附上条码。pcr反应建立文库,并保留有效的捕获,去除空白的捕获。用illumina公司的适配引物和浓度以pcr方法纯化所建文库,采用illumina公司的miseq和hiseq2500系统来进行测序,得到测序结果。
接着,由于测序的原始捕获实验结果(即测序结果)在高效率的探针和低效率的探针中读取的结果有的显著差异,为了改善这种情况,对原始的测序结果进行相对效率计算,混合探针时根据采用调节后的摩尔比率进行混合。
第六步,数据的分析和模型的建立。具体是:将肝癌血浆样本和正常对照的血浆样本随机按2:1的比例分为训练集和验证集,选用lasso和随机森林的方法针对第五步中的测试结果进行基因筛选;
在lasso方法中,采用二次抽样方法不重复抽样75%的数据集500次,选择出现频率超过450次的甲基化基因共30个;
在随机森林的方法中,使用oob误差最小化准则,通过设置变量每次重复的分数下降0.3的原则进行随机变量的消除,最后筛选出24个甲基化基因;
上述两种方法重叠的甲基化基因有10个(如表1所示),分别是bmpr1a,psd4,arhgap25,klf3,plac8,atxn1,chr6:170,chr6:3,atad2和chr8:20。
然后,采用这10个重叠的甲基化基因作为协变量建立一个逻辑回归模型模型,并获得一个联合诊断指数(cd-score),并在验证集中进行验证;
同样,将肝癌血浆样本分为训练集和验证集,为方便计算分析:先通过对每一个基因作为协变量建立一个单变量cox比例风险模型,筛选出与患者预后相关(p<0.05)的基因进行下一步分析;
接着,采用lasso-cox多因素回归分析,最终筛选出8个甲基化基因进行预后的分析(如表2所示),分别为sh3pxd2a,c11orf9,ppfia1,chr17:78,serpinb5,notch3,grhl2,tmem8b;
最后,通过拟合多变量cox比例风险模型,在训练集确定这8个甲基化基因中每一个基因的系数,计算合并后的预后评分指数(cp-score),并在验证集中进行验证(如表3所示)。
应用例1:
通过逻辑回归方法,用基因甲基化面板(包括10个甲基化基因:bmpr1a,psd4,arhgap25,klf3,plac8,atxn1,chr6:170,chr6:3,atad2和chr8:20)构建了一个诊断预测模型。应用该模型诊断肝癌,在训练集中的敏感性94.3%,特异性85.7,验证集中的敏感性为90.5%,特异性83.2%)。这个模型可以非常好的区分肝癌与正常对照组在训练数据集(auc=0.966)和验证数据集(auc=0.944)(图1)。证实这10个基因甲基化面板可以用于区分肝癌和正常对照。
应用例2:
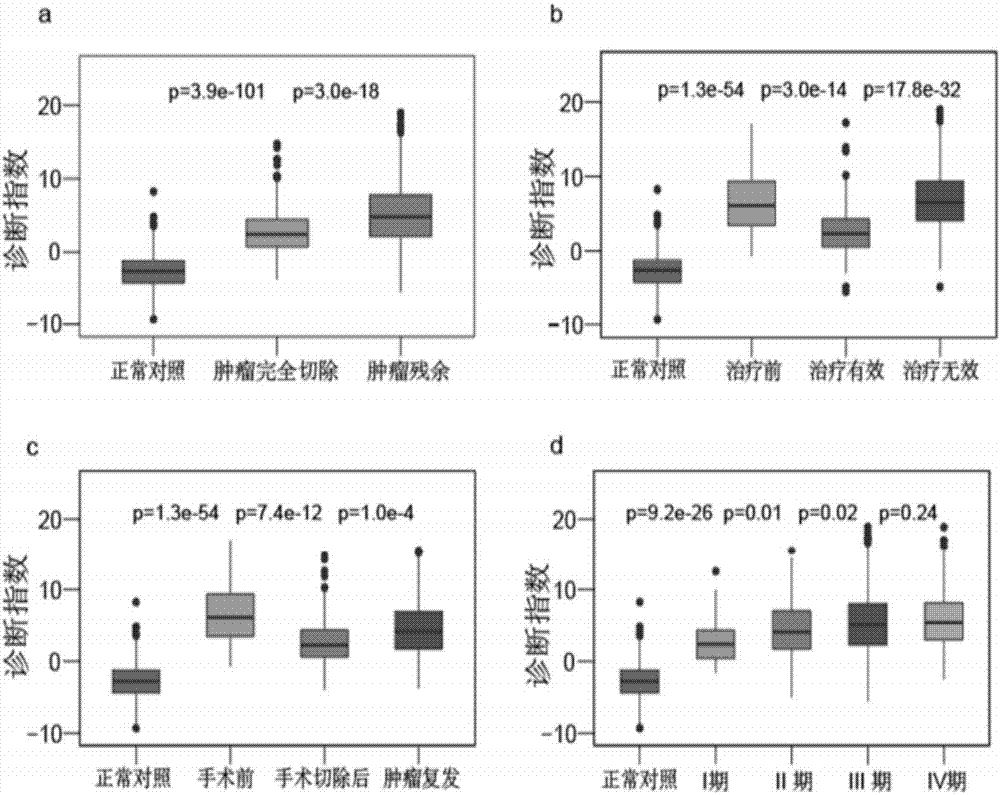
采用上述建立的诊断预测模型,计算出每个样本的联合诊断指数(cd-score),采用这个联合诊断指数,可以很好的预测肝癌患者的治疗疗效和肿瘤复发(如图2所示)。有肿瘤负荷的患者的cd-scores值明显高于肿瘤已切除的患者和正常对照组(p<0.0001,图2a)。同样,治疗前患者cd-scores明显高于治疗后有效的患者,而治疗无效肿瘤进展的患者cd-scores会进一步升高(p<0.0001,图2b)。此外,手术后病人的cd-scores较手术前明显降低,患者术后出现肿瘤复发,cd-scores则会再度升高(p<0.0001,图2c)。此外,cd-scores的值与肿瘤分期相关。早期患者(i,ii期)的cd-scores明显高于正常对照组,而明显低于晚期(iii,iv期)患者(p<0.05,图2d)。说明根据这10个基因甲基化水平建立的模型可用于肝癌的早期诊断、治疗疗效的判断、预测肿瘤的复发。
应用例3:
通过拟合多变量cox比例风险模型,用基因甲基化面板(包括8个甲基化基因:h3pxd2a,c11orf9,ppfia1,chr17:78,serpinb5,notch3,grhl2和tmem8b)构建了一个预后风险模型,并计算出每个样本的预后评分指数(指定为cp-score)。选取-0.24为cut-off值,将肝癌患者分为低风险组和高风险组。无论在训练集还是验证集,低风险组患者的生存均明显优于高风险组(如图3所示)。多元变量分析表明,cp-score与死亡风险显著相关,并且cp-score的生存是一个独立的危险因素(如表3所示)。分期也是肝癌患者的独立危险因素,而联合cp-score和分期,可进一步的改进对肝癌患者预后的预测能力(如图3所示)。
表1:10个用于诊断早期肝癌的基因
表2:8个用于预测预后的基因
表3:肝癌患者多变量生存分析
基于上述技术方案,本发明所述的基因甲基化面板及检测方法,可有效的用于诊断、预测肝癌疗效和预后。该甲基化面板共包含18个基因,通过检测患者血浆中bmpr1a,psd4,arhgap25,klf3,plac8,atxn1,chr6:170,chr6:3,atad2,chr8:20共10个基因甲基化水平的改变,可以用于诊断肝癌和预测肝癌的治疗疗效,通过检测患者血浆中sh3pxd2a,c11orf9,ppfia1,chr17:78,serpinb5,notch3,grhl2,tmem8b共8个基因的甲基化水平改变,可以用于预测肝癌患者的预后和死亡风险,并且通过检测方法来实现。从而提高了通过肝癌患者血液诊断和预后预测的准确性。
以上对本发明实施例公开的一种用于诊断、预测肝癌疗效和预后的基因甲基化面板及检测方法进行了详细介绍,本文中应用了具体个例对本发明的原理及实施方式进行了阐述,以上实施例的说明只是用于帮助理解本发明的方法及其核心思想;同时,对于本领域的一般技术人员,依据本发明的思想,在具体实施方式及应用范围上均会有改变之处,综上所述,本说明书内容不应理解为对本发明的限制。
- 还没有人留言评论。精彩留言会获得点赞!