一种用于检测绵羊肺炎支原体的引物和探针的制作方法
本发明涉及一种用于检测绵羊肺炎支原体的引物和探针,属于分子生物学领域。
背景技术:
绵羊肺炎支原体(mycoplasmaovipneumoniae,mo)是引起绵羊和山羊支原体性肺炎(mycoplasmapneumoniaofgoatsandsheep,mpgs)的主要病原。mpgs传染性强,主要通过呼吸道感染,也可垂直传播,病羊和耐过羊是该病的主要传染源(贺英等,2009;万一元等,2000)。mpgs临床症状表现为高热、咳嗽、喘气、渐进性消瘦、肺和胸膜发生浆液性和纤维素性炎症,病死率一般为30%~50%,有的高达80%(yangetal.,2014;rifatbegovicetal.,2011;dassnayakeetal.,2010;besseretal.,2008)。
当前国外非洲、西班牙、意大利、美国、约旦,国内四川、贵州、内蒙古、青海、广西、福建等地均有该病发生的报道。该病给养羊业造成了严重的经济损失,因此,亟需建立一种绵羊肺炎支原体特异、敏感、简便的检测方法。
taqman荧光pcr是在普通pcr的基础上,在反应体系中加入一对特异性引物的同时再加入一个特异性的荧光探针,使用荧光pcr检测仪来检测靶核苷酸序列的技术,具有特异性强、灵敏度高、定量准确等优点。通过查阅文献发现,当前国内虽有针对绵羊肺炎支原体检测的实时荧光定量pcr方法,但是主要是针对16srrna设计的引物,并且只有染料法荧光定量pcr方法,尚未见有绵羊肺炎支原体taqman荧光定量pcr检测方法。本发明的建立可以填补该领域的空白。
技术实现要素:
本发明的目的是提供一种用于检测绵羊肺炎支原体的引物和探针。
为实现上述目的,本发明采用以下技术方案:
用于检测绵羊肺炎支原体的实时荧光定量pcr引物,引物的核苷酸序列为:上游引物:5’-cttcgggacttattggag-3’,下游引物:5’-gatgcaaactgatttacttg-3’。
用于检测绵羊肺炎支原体的探针,序列为:5’-aagaccgattgtcaggccga-3’。
所使用的探针为两端分别标记荧光报告基团(r)和荧光淬灭基团(q)的寡核苷酸。
利用本发明的引物和探针可用于检测绵羊肺炎支原体的p113基因,尤其适用于基于荧光定量pcr技术的检测。通过对反应体系和反应条件的优化,建立一种可用于检测绵羊肺炎支原体的荧光定量pcr方法。
具体操作方法如下:
1、引物设计:根据genbank上公布的绵羊肺炎支原体kr270152.1基因组序列,利用primer6.0软件对p113基因序列进行引物和探针设计,探针合成同时进行两端荧光标记,探针5’端标记的荧光报告基团是fam,3’端标记的荧光淬灭基团为eclipse。
2、反应体系的优化:优化出的25μl最佳反应体系为:premixextaqtm(probeqpcr)12.5μl、上、下游引物(10μmol/l)各0.5μl、探针(5μmol/l)1μl、模板2μl、水8.5μl。最佳反应条件为:95℃,30s预变性;95℃5s,55℃10s,72℃20s共45个循环。
3、阳性标准品的制备:通过pcr对绵羊肺炎支原体fj-cl01株的p113基因进行扩增。20μlpcr扩增体系为:premixtaqtmversion2.0plusdye10μl、上下游引物(10μmol/μl)各1μl、fj-cl株dna2μl、灭菌无离子水补至20μl。pcr程序:94℃2min;94℃30s、55℃15s、72℃15s,共30个循环;72℃10min。用凝胶回收试剂盒纯化pcr产物并将目的片段连接到pmd19-t载体上,转化大肠杆菌dh5α感受态细胞,抽提质粒做pcr及酶切鉴定,并送至宝生物工程(大连)有限公司测序。以经过测序鉴定正确的重组质粒作为标准品。
4、标准曲线的建立:以优化的反应体系进行pcr扩增,以拷贝数为横坐标,以ct值为纵坐标建立标准曲线。
该方法可用于绵羊肺炎支原体的病原诊断和流行病学调查,为疾病的早期预防奠定技术基础。
有益效果
本发明根据genbank登录的kr270152.1的p113基因序列,设计特异性引物和探针,首此针对绵羊肺炎支原体p113基因建立taqman实时荧光定量pcr方法,该方法灵敏度高,最低可检测到10copies,特异性好、重复性好,可用于检测临床样品中绵羊肺炎支原体的含量。
附图说明
图1绵羊肺炎支原体实时荧光定量pcr方法的扩增曲线。
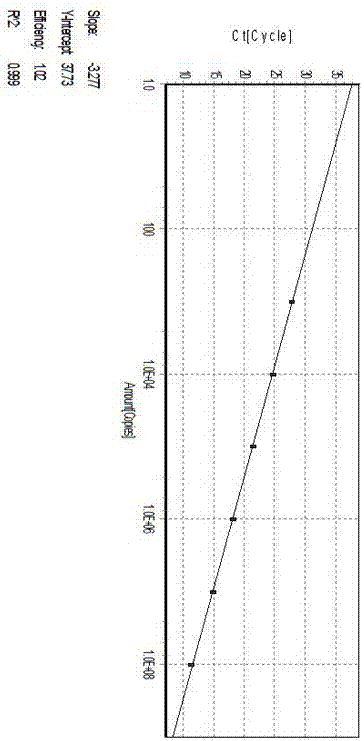
图2为绵羊肺炎支原体的实时荧光定量pcr的标准曲线。
具体实施方式
实施例1绵羊肺炎支原体的荧光定量pcr方法的建立
一、材料:
山羊支原体山羊肺炎亚种由中国农业科学院兰州兽医研究所储岳峰馈赠,大肠杆菌、巴氏杆菌、金黄色葡萄球菌等由福建省农业科学院畜牧兽医研究所禽病实验室程龙飞研究员馈赠;绵羊肺炎支原体fj-cl01株、丝状支原体山羊亚种fj-gt株、莱氏无胆甾原体fj-np株、牛支原体fj-hj株、羊口疮病毒fj-fz株为本室分离、鉴定、保存。
二、步骤
1、仪器与试剂:pmd19-t载体、sybrpremixextaqⅱ(2×)、dl2000marker均购自宝生物工程(大连)有限公司;荧光定量pcr管购自axygen(美国)公司;胶回收试剂盒购自康宁生命科学(吴江)有限公司;质粒小量抽提试剂盒购自omegabio-tek(美国)公司;mastercyclereprealplex荧光定量pcr仪,eppendorf(德国)公司产品。
2.引物和探针的特异性
引物和探针的特异性是本实验所建立方法的最重要因素。根据genbank登录的kr270152.1的p113基因序列,通过比对分析,设计引物和探针。
引物序列为:上游引物:5’-cttcgggacttattggag-3’,下游引物:5’-gatgcaaactgatttacttg-3’。
探针序列为:5’-aagaccgattgtcaggccga-3’。
3、阳性标准品的制备
通过pcr对绵羊肺炎支原体fj-cl01株的p113基因进行扩增。20μlpcr扩增体系为:premixtaqtmversion2.0plusdye10μl、上下游引物(10μmol/μl)各1μl、fj-cl株dna2μl、灭菌无离子水补至20μl。pcr程序:94℃2min;94℃30s、55℃15s、72℃15s,共30个循环;72℃10min。用凝胶回收试剂盒纯化pcr产物并将目的片段连接到pmd19-t载体上,转化大肠杆菌dh5α感受态细胞,抽提质粒做pcr及酶切鉴定,并送至宝生物工程(大连)有限公司测序。以经过测序鉴定正确的重组质粒作为标准品。
4.反应条件的优化
采用25条件反应体系premixextaqtm(probeqpcr)12.5μl、上、下游引物(10μmol/l)各0.5μl、探针(5μmol/l)1μl,倍比稀释后的阳性标准品2μl,补水至终体积25μl,以出现最高荧光值及最小的ct值为指标,分别对退火温度(51~60℃)、引物和探针浓度(5~10μmol/l)进行优化。
5、建立标准曲线
用easydilution将构建的标准品梯度稀释(109、108、107、106、105、104、103、102、101copies/μl)作为模板,以优化的条件进行扩增,以拷贝数为横坐标,以ct值为纵坐标建立标准曲线。
对阳性标准品的扩增曲线和标准曲线显示,荧光定量pcr方法对绵羊肺炎支原体的最低检测限为10copies,且ct与拷贝数在1×101~1×109拷贝/μl范围内有很好的线性关系,相关系数r2为0.999,扩增效率为102%。扩增曲线见图1,标准曲线见图2。
6特异性检测
6.1特异性检测
用优化的条件分别对绵羊肺炎支原体、山羊支原体山羊肺炎亚种、大肠杆菌、巴氏杆菌、金黄色葡萄球菌、副猪嗜血杆菌、莱氏无胆甾原体、牛支原体、丝状支原体山羊亚种及羊口疮病毒核酸样品进行检测,对该方法的特异性进行评价。检测结果显示,只有绵羊肺炎支原体核酸样品为阳性,其余核酸样品检测结果均为阴性。
6.2可重复性及再现性评估
对同一阳性标准品设3个重复管,用建立的实时荧光定量pcr进行检测,评价其重复性,计算组内变异系数;将阳性标准品置于-20℃保存,分别于第7、14、21d重检,评价其再现性,计算其组间变异系数。计算得组内变异系数为0.58%~1.29%,组间变异系数为0.19%~1.22%,可重复性好。
以上所述仅为本发明的较佳实施例,凡依本发明申请专利范围所做的均等变化与修饰,皆应属本发明的涵盖范围。
sequencelisting
<110>福建省农科院畜牧兽医研究所
<120>一种用于检测绵羊肺炎支原体的引物和探针
<130>3
<160>3
<170>patentinversion3.3
<210>1
<211>18
<212>dna
<213>人工序列
<400>1
cttcgggacttattggag18
<210>2
<211>20
<212>dna
<213>人工序列
<400>2
gatgcaaactgatttacttg20
<210>3
<211>20
<212>dna
<213>人工序列
<400>3
aagaccgattgtcaggccga20
- 还没有人留言评论。精彩留言会获得点赞!