诊断甲状腺功能减退的SNP及其应用的制作方法
本发明属于医学诊断领域,涉及一种诊断甲状腺功能减退的snp及其应用。
背景技术:
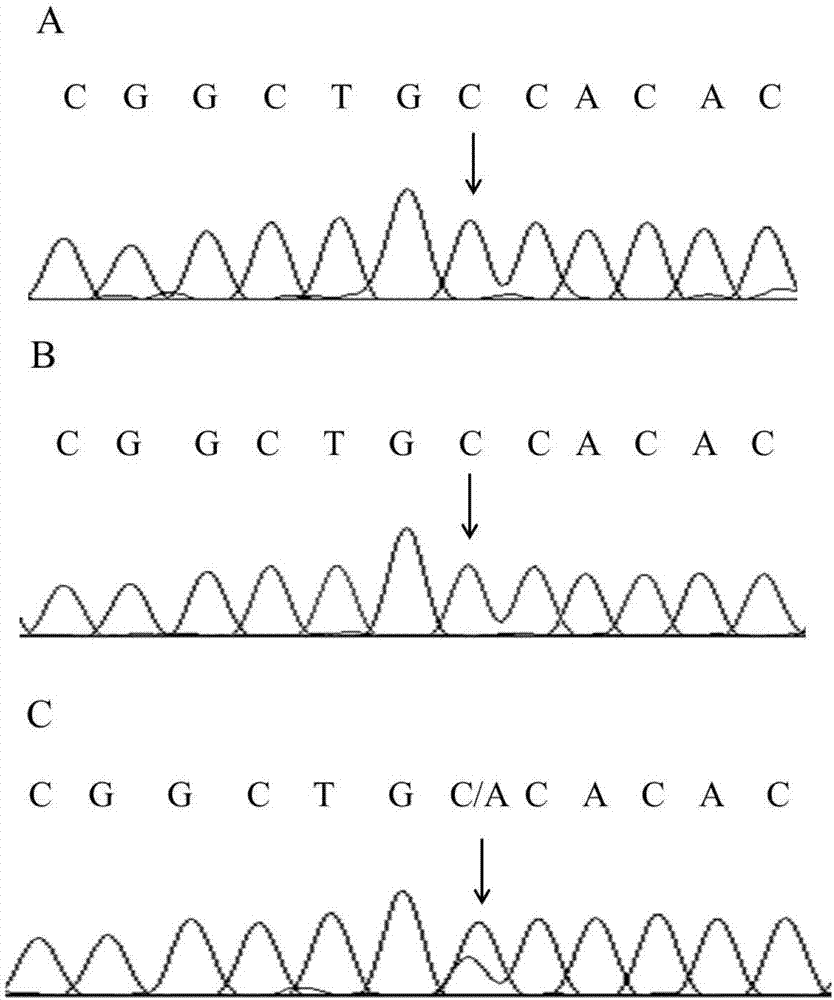
:甲状腺功能减退症(甲减)是常见的甲状腺疾病之一,是由各种原因导致的甲状腺激素合成和分泌减少或组织利用不足而引起的全身性低代谢综合征,依据病变发生部位可分为原发性、中枢性和甲状腺激素抵抗综合征(resistancetothyroidhormones,rth),其中原发性甲减占90%以上。原发性甲减依据发病原因可分为自身免疫性、手术后或131i治疗后、药物性和特发性甲减,依据甲状腺功能减退程度可分为临床和亚临床甲减。不同地域的甲减患病率有所差异。国外报告的临床甲减患病率为0.8%~1.0%,发病率为3.5/1000。在美国,临床甲减患病率为0.3%,亚临床甲减患病率为4.3%。我国学者报告的临床甲减患病率为1.0%,发病率为2.9/1000。甲减的成人患病率较高,女性患病率较男性高,老年人以及某些种族和区域的患病率也较高。甲减的主要发病原因包括:①自身免疫功能损伤可导致自身免疫性甲状腺炎,包括桥本、萎缩性和产后甲状腺炎等。②因甲状腺手术、131i治疗等而引起的甲状腺损伤。③碘缺乏或过量。生活环境中碘缺乏是世界范围内常见的甲减发病原因,而碘过量也可引起潜在甲状腺疾病患者发生甲减,且可诱发和加重自身免疫性甲状腺炎。④某些类别的药物如咪唑类、硫脲类和锂类药物等亦可引起甲减。中枢性甲减的主要发病原因有垂体瘤或颅咽管瘤等鞍区肿瘤、席汉综合征、垂体炎、头颅或颅底放疗和中、重度颅脑外伤等。早期患者的症状一般较隐匿,病情轻的可没有特异症状,而以基础代谢率降低和交感神经兴奋性下降为主要表现,典型患者则有畏寒、乏力、手足肿胀感、嗜睡、记忆力减退、少汗、关节疼痛、体重增加、便秘、女性月经紊乱或月经过多、不孕等表现。现在常用的甲减的诊断的方法包括:(1)病史详细询问病史有助于甲减的诊断,如甲状腺手术史、甲状腺功能亢进症131i治疗史、graves病、桥本甲状腺炎及家族史等。(2)临床指标检测tsh水平升高、ft4水平降低,诊断为原发性临床甲减;仅tsh水平升高、而ft4水平正常,考虑为亚临床甲减。现有技术中的诊断方法不能精确的诊断甲减,只能提出患病的可能性,因此寻找一种准确度高、灵敏性高、特异性高的诊断方法是亟待解决的问题。技术实现要素:为了解决现有技术中存在的缺陷,本发明提供了一种能够在甲状腺功能减退早期即可准确诊断疾病发生与否的诊断标志物及其应用。根据本发明的一个方面,本发明提供了一种用于诊断甲状腺功能减退的snp位点,所述snp位点包括rs13306186、和/或rs200842352。即可以通过单独检测rs13306186或rs200842352,或联合检测rs13306186和rs200842352两个snp位点来诊断甲状腺功能减退。进一步,所述snp位点还可包括rs118109635。即可以通过联合检测rs13306186和rs118109635两个snp位点;rs200842352和rs118109635两个snp位点;rs200842352、rs13306186、和rs118109635三个snp位点。根据本发明的又一个方面,本发明提供了一种前面所述的snp位点基因型的检测试剂。优选地,所述试剂包括针对前面所述的snp位点的特异性扩增引物。进一步,所述试剂还包括dntps、taq酶、mg2+和pcr反应缓冲液等pcr扩增反应中常规试剂。根据本发明的又一个方面,本发明提供了前面所述的试剂在制备甲状腺功能减退风险预测产品、诊断产品、预后评估产品中的应用。进一步,所述风险预测产品通过检测样本中前面所述的snp位点的基因型来诊断受试者患有甲状腺功能减退的风险;所述诊断产品通过检测样本中前面所述的snp位点的基因型来诊断受试者是否患有甲状腺功能减退;所述预后评估产品通过检测样本中前面所述的snp位点的基因型来评估甲状腺功能减退患者的预后。进一步,所述风险预测产品包括诊断试剂盒、芯片、或者试纸;所述诊断产品包括诊断试剂盒、芯片、或者试纸;所述预后评估产品包括诊断试剂盒、芯片、或者试纸。具体地,所述风险预测产品包括前面所述的试剂;所述诊断产品包括前面所述的试剂;所述预后评估产品包括前面所述的试剂。根据本发明的又一个方面,本发明提供了一种甲状腺功能减退风险预测产品、诊断产品、预后评估产品,所述风险预测产品包括前面所述的试剂;所述诊断产品包括前面所述的试剂;所述预后评估产品包括前面所述的试剂。术语解释引物如本文所用,术语“引物”指的是能与模板互补配对,在dna聚合酶的作用合成与模板互补的dna链的寡聚核苷酸的总称。引物可以是天然的rna、dna,也可以是任何形式的天然核苷酸,引物甚至可以是非天然的核苷酸如lna或zna等。引物“大致上”(或“基本上”)与模板上一条链上的一个特殊的序列互补。引物必须与模板上的一条链充分互补才能开始延伸,但引物的序列不必与模板的序列完全互补。比如,在一个3’端与模板互补的引物的5’端加上一段与模板不互补的序列,这样的引物仍大致上与模板互补。只要有足够长的引物能与模板充分的结合,非完全互补的引物也可以与模板形成引物-模板复合物,从而进行扩增。文库及其制备如本文所用,术语“文库”是指对基因组的目的片段进行打断,获得一组具有一定大小的dna片段混合物。文库的制备方法为本领域技术人员所熟知,包括(但不局限于)步骤:1.提供一待检测样本,所述样品含有经打断的、源自基因组dna的双链核酸片段,并且所述核酸片段具有平末端;2.在双链核酸片段的末端添加接头连接序列;通过所述接头连接序列,在所述双链核酸片段的两端添加接头,其中所述接头具有引物结合区以及连接互补区,所述的连接互补区与所述的接头连接序列互补;两侧3’端和5’端的接头的引物结合区序列不同。3.对上一步骤获得的带有接头的dna双链核酸片段,用第一引物和第二引物进行扩增,从而获得pcr扩增产物的混合物,其中所述引物具有对应于所述接头的引物结合区的接头结合区,并且位于接头结合区外侧的测序探针结合区。还可以对打断产物、末端修复产物、接头产物和富集产物进行纯化。纯化条件及参数为本领域技术人员所熟知,对反应的条件进行一定的变化或优化也在本领域技术人员能力范围之内。捕获如本文所用,术语“捕获”,指的是探针对文库中外显子区域的dna片段进行特异性选择和结合的过程。dna分子正常情况下是双链,因此捕获之前,dna分子必须变为单链,一般是通过加热使其变性而达到解链目的,解链的dna分子被迅速冷却,即保持单链状态。文库变性后在杂交平台与芯片进行捕获杂交。含有外显子区域的dna片段与固定在芯片上的探针之间在严格的条件下进行分子杂交。较佳地,芯片上探针分子的浓度要远远高于靶分子浓度。待杂交完毕后,通过变性等方法收集捕获的序列并纯化,得到来自捕获后的序列混合物。本领域技术人员可以通过通用的方法进行外显子捕获和目的片段的洗脱和纯化,也可以应用市售(如:德国qiagen公司的minelutepcrpurificationkit)试剂盒进行上述过程。在一个优选例中,对待检测的dna文库的pcr扩增产物的混合物进行单链化,并用封闭分子封闭所述扩增产物中对应于第一引物和第二引物的区域,从而获得两端被封闭的单链扩增产物的混合物;用核酸芯片从所述的经封闭的单链扩增产物的混合物中,捕获疾病相关的核酸分子;对经捕获的核酸分子,用第三引物和第四引物进行扩增,从而获得第二pcr扩增产物的混合物,其中第三引物和第四引物分别特异性结合于所述的第一引物和第二引物;对上一步骤获得的第二pcr扩增产物的混合物进行测序,从而获得样本中疾病相关核酸分子的核苷酸序列信息。高通量测序基因组的“高通量测序”使得人类能够尽早地发现与疾病相关基因的异常变化,有助于对个体疾病的诊断和治疗进行深入的研究。本领域技术人员通常可以采用三种第二代测序平台进行高通量测序:454flx(roche公司)、solexagenomeanalyzer(illumina公司)和appliedbiosystems公司的solid等。这些平台共同的特点是极高的测序通量,相对于传统测序的96道毛细管测序,高通量测序一次实验可以读取40万到400万条序列,根据平台的不同,读取长度从25bp到450bp不等,因此不同的测序平台在一次实验中,可以读取1g到14g不等的碱基数。solexa高通量测序包括dna簇形成和上机测序两个步骤:pcr扩增产物的混合物与固相载体上固定的测序探针进行杂交,并进行固相桥式pcr扩增,形成测序簇;对所述测序簇用“边合成-边测序法”进行测序,从而得到样本中疾病相关核酸分子的核苷酸序列。dna簇的形成是使用表面连有一层单链引物(primer)的测序芯片(flowcell),单链状态的dna片段通过接头序列与芯片表面的引物通过碱基互补配对的原理被固定在芯片的表面,通过扩增反应,固定的单链dna变为双链dna,双链再次变性成为单链,其一端锚定在测序芯片上,另一端随机和附近的另一个引物互补从而被锚定,形成“桥”;在测序芯片上同时有上千万个dna单分子发生以上的反应;形成的单链桥,以周围的引物为扩增引物,在扩增芯片的表面再次扩增,形成双链,双链经变性成单链,再次成为桥,称为下一轮扩增的模板继续扩增;反复进行了30轮扩增后,每个单分子得到1000倍扩增,称为单克隆的dna簇。dna簇在solexa测序仪上进行边合成边测序,测序反应中,四种碱基分别标记不同的荧光,每个碱基末端被保护碱基封闭,单次反应只能加入一个碱基,经过扫描,读取该次反应的颜色后,该保护集团被除去,下一个反应可以继续进行,如此反复,即得到碱基的精确序列。在solexa多重测序(multiplexedsequencing)过程中会使用index(标签)来区分样品,并在常规测序完成后,针对index部分额外进行7个循环的测序,通过index的识别,可以在1条测序甬道中区分12种不同的样品。本发明的优点和有益效果:与现有技术相比,本发明具有的有益效果为:本发明提供了能够诊断甲状腺功能减退的snp;通过对本发明提供的标志物snp进行基因分型(genotyping),即可检测出个体是否有患病的风险或者检测出个体是否患病或者可评价患病个体预后的好坏。本发明的诊断snp的检测可达到早预测、早诊断、早干预、早治疗的目的;同时,本发明提供标志物snp还可用于诊断试剂盒的开发,并能够应用于临床研究、分析及诊断等诸多用途。附图说明图1显示甲状腺功能减退家系遗传图谱;图2利用sanger测序检测rs200842352位点基因型的结果图,其中,a:家系中非患病个体;b:正常人;c:家系中甲状腺功能减退患者;图3利用sanger测序检测rs118109635位点基因型的结果图,其中,a:家系中非患病个体;b:正常人;c:家系中甲状腺功能减退患者;图4利用sanger测序检测rs13306186位点基因型的结果图,其中,a:家系中非患病个体;b:正常人;c:家系中甲状腺功能减退患者。具体实施方案下面结合具体实施例,进一步阐述本发明。应理解,这些实施例仅用于说明本发明而不用于限制本发明的范围。下列实施例中未注明具体条件的实验方法,通常按照常规条件如sambrook等人,分子克隆:实验室手册(newyork:coldspringharborlaboratorypress,1989)中所述的条件,或按照制造厂商所建议的条件。实施例1样本获取发明人发现了一个四代的甲状腺功能减退(简称甲减)家系,该显性甲减家系部分成员的临床信息见表1。该家系中四代人中都有甲减患者,推测该疾病为显性遗传;另外,患者中有女性,也有男性,因此推测该疾病为常染色体遗传,与性别无关。图1显示了显性甲减家系图谱,其中,●或■表示患病个体。诊断标准:可参照《中国甲状腺疾病诊治指南》2007版:(1)临床表现:病情轻的早期病人可以没有特异症状。典型病人畏寒、乏力、手足肿胀感、嗜睡、记忆力减退、少汗、关节疼痛、体重增加、便秘。(2)体格检查:典型病人可有表情呆滞、反应迟钝、声音嘶哑、听力障碍,面色苍白、颜面和(或)眼睑水肿、唇厚舌大常有齿痕,皮肤干燥、粗糙、脱皮屑、皮肤温度低、水肿、手脚掌皮肤可呈姜黄色,毛发稀疏干燥,跟键反射时间延长,脉率缓慢。少数病例出现胫前粘液性水肿,重症病人可以发生粘液性水肿昏迷。(3)激素水平:血清tsh和总t4(t4)、游离t4(ft4)作为诊断甲减的第一线指标。临床甲减血清tsh增高,t4、ft4降低,或伴有t3降低。亚临床甲减仅有tsh增高,t4和ft4正常,或伴有t3正常或轻度增高。表1甲状腺功能减退家系部分成员的临床信息编号采用i(第一代)、ii(第二代)、iii(第三代)和iv(第四代)进行。家系中确诊的3例患者(ii:3、iii:1、iv:1)挑选用于测序,从其他表型正常的家庭成员中优先挑选与iv:1亲缘关系最近的2例(iii:2父亲和iii3:3小姨),以便于有效的过滤与疾病无关的变异位点。实施例2外显子测序1、仪器设备如表2所示。表2仪器设备2、试剂耗材agilentsureselecthumanallexonkit(agilent)、agilentdna1000kit(agilent)、1.5ml离心管(eppendorf)、0.2ml离心管(eppendorf)、枪头(axygen)、96孔板(axygen)、bigdyev3.1(thermo)、无水乙醇、pop7胶(thermo)、毛细管电泳buffer(thermo)、sequencestandard(3500)(thermo)、血液基因组dna提取试剂盒(tiangen)、d2000dnamarker(tiangen)、琼脂糖(sunshinebio)、eb(amresco)。3、试剂配方3.1tbe电泳液5×tbe电泳液按照表3配制。表35×tbe电泳液配方试剂体积tris54g硼酸7.5gedta(ph8.0,0.5mol/l)20mlddh2o900ml3.20.5×tbe电泳液按照表4配制。表40.5×tbe电泳液配方试剂体积5×tbe100mlddh2o900ml3.31×磷酸缓冲液(pbs)按照表5配制。表5pbs配方试剂体积nacl18gkcl0.2gnahpo4.12h2o1.56gkh2po40.2gddh2o1l4、实验步骤在家系中选取确诊的3例患者(ii:3、iii:1、iv:1)作为研究样本,挑选iii:2父亲和iii:3小姨作为正常样本对照,采集每位研究对象的外周血5ml作为研究样品。根据世界医学会《赫尔辛基宣言》的要求,所有被采血的家系成员均签署了患者知情同意书。4.1样本dna提取采用omegablooddnamidikit全血dna提取试剂盒从外周血样品中提取dna,提取步骤如下:(1)取2ml全血样本,加入150μlobprotease,2.1mlbufferbl和20μlrnasea,最大速度漩涡1分钟,彻底混匀;(2)65℃水浴15-20分钟,并在水浴过程中漩涡5次;(3)加入2.2ml无水乙醇,最大速度漩涡30秒,彻底混匀;(4)将3.5ml裂解液移入带过滤柱的15ml离心管,4000转离心5分钟,取出过滤柱,倒掉过滤液体,放回过滤柱;(5)将第3步剩余裂解液加入带过滤柱的15ml离心管,4000转离心5分钟,取出过滤柱,倒掉过滤液体,放回过滤柱;(6)加入3mlhbbuffer,洗涤过滤柱,4000转离心5分钟,取出过滤柱,倒掉过滤液体,放回过滤柱;(7)加入3mldnawashbuffer,4000转离心5分钟,取出过滤柱,倒掉过滤液体,放回过滤柱;(8)再次加入3mldnawashbuffer,4000转离心5分钟,取出过滤柱,倒掉过滤液体,放回过滤柱;(9)4000转离心15分钟,甩干过滤柱;(10)将过滤柱移至新的15ml离心管,加入500μl70℃的elutionbuffer,室温静置5分钟,4000转离心5分钟,收集含有dna的过滤液;(11)再次将过滤柱移至新的15ml离心管,加入500μl70℃的elutionbuffer,室温静置5分钟,4000转离心5分钟,收集含有dna的过滤液;(12)利用分光光度计测量dna的浓度及纯度,所得的每个标本基因组dna的od260/od280均位于1.7-2.0之间,浓度不少于200ng/μl,总量不少于30μg。4.2外显子测序(1)取2μgdna,在适当体系中以bioruptor做机械打断,使片段主带在200bp附近,切胶回收150-250bp片段;(2)对dna片段做末端修复和3’末端加a;(3)连接测序接头,连接产物纯化后进行pcr扩增,扩增产物纯化为预文库;(4)取一定量预文库以agilentcapturekit中的探针做杂交捕获,杂交产物经洗脱回收后做pcr扩增,产物回收即为终文库,琼脂糖凝胶电泳跑小样确认;(5)对文库进行质控,对合格的外显子序列进行高通量测序,得到初始数据。(6)hiseq4000测序仪测序。4.3数据分析质控:用seqprep和sickle对原始测序数据进行质控,去除接头,去除低质量碱基;对原始数据和质控数据都进行相关统计。比对:用bwa将质控后的数据比对到参考基因组,然后用samtools对比对结果进行排序,再用picard标记重复reads,最后利用重复标记过的比对结果进行覆盖度、测序深度和外显子区域捕获率的统计。4.3.1变异检测(1)突变预测:用picard将比对结果中的pcr重复序列去掉后,通过gatk软件对比对结果进行indel附近重比对,碱基重校正,最后通过unifiedgenotyper模块结合agilentv5utr芯片位置信息预测snv和indel;(2)突变筛选:首先通过预测的覆盖度支持数进行筛选,然后过滤掉dbsnp138,1000genome数据库中的高频位点。3.3.2预测疾病相关变异(1)根据家系信息,通过患者个体和正常个体的比较,筛选只在患者个体中存在并不存在于正常个体中的位点,这些位点是在患者中存在的,位点不考虑基因组位置。(2)使用oncotatorv1.5.3.0,annovar,sift和polyphen工具对筛选的位点进行注释,注释内容包括基因名称、功能结果、polyphen-2预测、以及该疾病特异的相关注释。4.4结果最终得到5个可能具有致病意义的基因突变。其中三个基因突变位点分别是rs200842352、rs13306186、rs118109635,在甲减家系患者个体中rs200842352位点的基因型是ca,在甲减家系正常人体中rs200842352位点的基因型是cc;在甲减家系患者个体中rs13306186位点的基因型是cg,在甲减家系正常人体中rs13306186位点的基因型是cc;在甲减家系患者个体中rs118109635位点的基因型是ct,在甲减家系正常人体中rs118109635位点的基因型是cc。实施例3sanger测序验证由于外显子组测序存在一定程度的假阳性,因此我们进一步利用sanger测序法,对rs200842352、rs13306186、rs118109635进行验证。分别对实施例1中的5名患者、8名家系内正常人和100名家系外正常人进行rs200842352、rs13306186、rs118109635位点基因型检测。具体方法步骤如下:(1)dna提取按照实施例1的方法提外周血白细胞中的基因组dna。(2)引物设计引物设计参考人类基因组序列数据库hg19/build36.3。针对rs200842352位点的引物序列如下所示:5’-atggtacttggccttgggtg-3’(seqidno.1)5’-cagtgtagcacagggcagg-3’(seqidno.2);针对rs13306186位点的引物序列如下所示:5’-ctcacaggggaggagagtga-3’(seqidno.3)5’-cctctccctcctcagttcca-3’(seqidno.4);针对rs118109635位点的引物序列如下所示:上游引物:5’-ccaatcccactggtccctatt-3’(seqidno.5),下游引物:5’-tgcctggtttgatgacctcag-3’(seqidno.6)。(3)pcr扩增反应体系:在冰上融化模板dna、引物以及extenderpcr-to-gelmastermix;按照表6中的反应体系进行pcr并保持反应体系在冰上。表6反应体系反应条件:将反应体系放入pcr仪,执行以下反应程序:95℃5min→(95℃30sec,67℃30sec-0.5℃/循环,72℃1min)x14循环→(95℃30sec,57℃30sec,72℃1min)x30循环→72℃7min→4℃forever。(4)琼脂糖凝胶电泳检测量取适量1×tbe缓冲液并称取一定量琼脂粉溶于其中制成1%-2%的琼脂糖凝胶,在微波炉上加热溶化,待温度降至60℃-70℃左右加入荧光染料,温度降至40℃-50℃左右将琼脂粉溶液倒入插有梳子的凝胶槽中冷却,待凝胶完全凝固备用。将凝胶置于水平电泳槽中,取少量pcr产物上样电泳,将电泳好的样品置于凝胶成像系统中进行检测和分析。(5)将检测合格的pcr产物用酶解法进行纯化。根据核酸外切酶i(exoi),碱性磷酸酶(aip)的作用浓度,加入到pcr反应产物中,37℃消化15min,85℃使酶失活15min。纯化体系如表7所示。表7纯化体系试剂体积pcr产物5μlexoi0.5μl碱性磷酸酶1μl(6)纯化后的pcr产物的bigdye反应bigdye反应体系:见表8。表8bigdye反应体系试剂体积纯化并稀释好的pcr产物1μlprimer(1μm)1μlbigdye(2.5×)8μl总体积10μlpcr循环条件:一般测序:96℃1min→(96℃10sec→50℃5sec→60℃4min)x25循环→4℃保温(7)bigdye反应产物纯化:1)每管加入2.5μl125mmedta(ph=8),加到管底;2)加入30μl100%酒精,封严,震荡4次,室温放置15min;20℃最大转速离心45min,马上倒置96孔板,倒置最小转速离心10s;3)加入60μl70%酒精,最大转速4℃离心15min,马上倒置96孔板,最小转速离心1min;4)70%酒精重复洗涤1次或2次;5)让残余的酒精在室温挥发干,加入10μlhi-di甲酰胺,95℃变性4min,迅速置冰上4min,上样。(8)测序将纯化后的bigdye反应产物进行dna测序。(9)结果sanger测序结果显示,5个患者的rs200842352位点的基因型是ca,rs13306186位点的基因型是cg,rs118109635位点的基因型是ct,而8个非患病个体和100个无血缘关系的正常对照的rs200842352位点的基因型是cc,rs13306186位点的基因型是cc,rs118109635位点的基因型是cc。图2a显示检测家系中非患病个体rs200842352位点的基因型是cc,图2b显示正常人rs200842352位点的基因型是cc,图3c显示家系中患病个体rs200842352位点的基因型是ca;图3a显示检测家系中非患病个体rs118109635位点的基因型是cc,图3b显示正常人rs118109635位点的基因型是cc,图3c显示家系中患病个体rs118109635位点的基因型是ct;图4a显示检测家系中非患病个体rs13306186位点的基因型是cc,图4b显示正常人rs13306186位点的基因型是cc,图4c显示家系中患病个体rs13306186位点的基因型是cg。实施例4甲减诊断试剂盒1、试剂盒组成:引物:如实施例4所示taq酶缓冲液dntp从待检测的生物体样本中提取和纯化基因材料(dna样本)2、使用方法:(1)基因组dna提取:使用美国promega公司的wizardgenomicdna提取试剂盒提取外周血液样本基因组dna。(2)先采用上述pcr引物、taq酶、样本基因组dna、缓冲液、dntp等进行pcr扩增反应;(3)对pcr扩增产物进行纯化;(4)对纯化的pcr产物进行bigdye反应;(5)对biydye反应产物纯化;(6)对biydye反应产物测序,测序序列与正常序列相比较。此外应理解,在阅读了本发明的上述讲授内容之后,本领域技术人员可以对本发明作各种改动或修改,这些等价形式同样落于本申请所附权利要求书所限定的范围。序列表<110>济南市中心医院<120>诊断甲状腺功能减退的snp及其应用<160>6<170>siposequencelisting1.0<210>1<211>20<212>dna<213>人工序列(artificialsequence)<400>1atggtacttggccttgggtg20<210>2<211>19<212>dna<213>人工序列(artificialsequence)<400>2cagtgtagcacagggcagg19<210>3<211>20<212>dna<213>人工序列(artificialsequence)<400>3ctcacaggggaggagagtga20<210>4<211>20<212>dna<213>人工序列(artificialsequence)<400>4cctctccctcctcagttcca20<210>5<211>21<212>dna<213>人工序列(artificialsequence)<400>5ccaatcccactggtccctatt21<210>6<211>21<212>dna<213>人工序列(artificialsequence)<400>6tgcctggtttgatgacctcag21当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1