一种用于PPD辅助诊断的WISP3基因突变及其应用的制作方法
本发明涉及生物医学
技术领域:
,具体涉及一种用于ppd辅助诊断的wisp3基因突变及其应用。
背景技术:
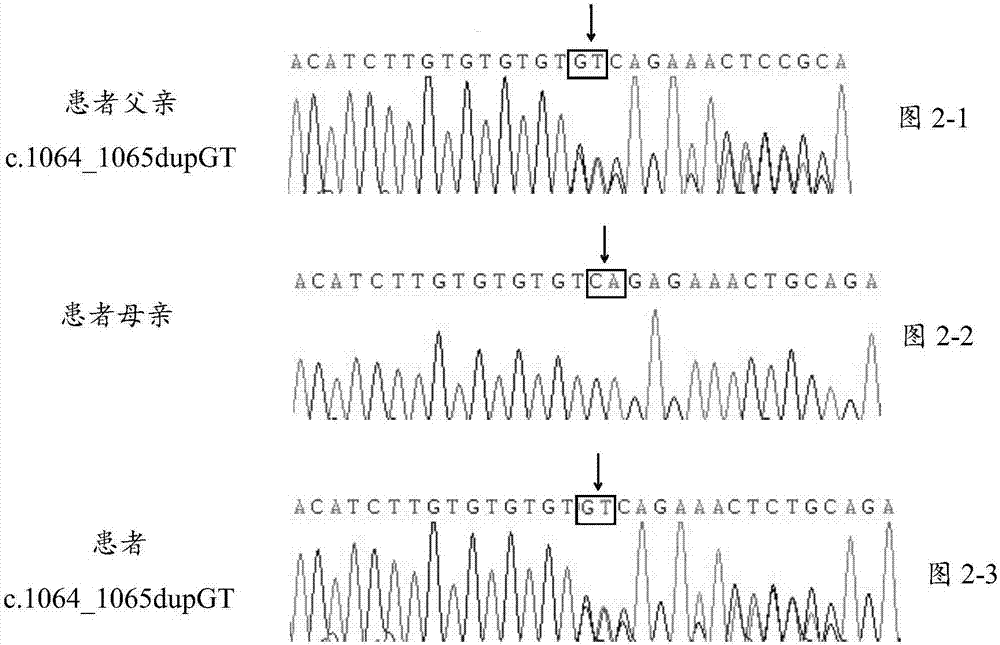
:进行性假性类风湿性发育不良症(ppd)是一种罕见的、由于wnt1诱导的信号肽通路蛋白3基因突变导致的常染色体隐性遗传性软骨发育不良疾病,英国联邦国家报道的发病率约为1/100万,国内病例报道极少。发病年龄多为1~10岁,其中77%为3~5岁。ppd患儿临床症状主要为大小关节疼痛、肿胀、畸形、运动受限,临床上常误诊为幼年型类风湿性关节炎、粘多糖病等。全身骨骼(包括脊柱)的影像学检查对诊断十分重要,表现为普遍性扁平椎并椎体终板不规则、骨骺增大、继发性退行性变和关节周围骨质疏松。外周大小关节均可受累,依次累及双手小关节、髋、膝、踝、腕、肩等,早发骨关节炎改变是致残的主要原因,38%的患者脊柱受累可出现短躯干畸形。本病临床症状与类风湿关节炎相似,但不同的是无滑膜炎和其他炎性改变、x线无破坏性改变。从目前对ppd疾病的认识来看,ppd不影响患者的寿命,除骨关节炎及脊柱外,无其他重要脏器的受累。但由于进行性关节退变和脊柱畸形,患者预后不良。目前对于ppd尚无有效的治疗药物,主要是采用对症治疗,合理地使用非淄体抗炎药或止痛药,给予软骨保护剂和补钙治疗。由于ppd多累及外周关节,导致外周关节活动受限及严重畸形,所以早期干预将有利于保持关节功能。wnt1诱导的信号肽通路蛋白3基因(wisp3)是cnn家族成员之一,含有5个外显子,编码354个氨基酸,可编码多种细胞外基质蛋白,参与细胞增殖分化与凋亡的调控,与软骨形成、成骨作用相关。携带wisp3功能性突变的个体极有可能发展为ppd患者。针对突变携带者采取一系列的预防措施,例如较早的进入ppd筛查,并提高筛查频率,做好早期干预和治疗。目前,在对ppd进行分子生物学研究的过程中发现了一些与其相关wisp3基因的突变位点,但是尚未发现足够量的突变“热点”,若能筛选出ppd相关的突变位点作为生物标志物,并研制相应的诊断试剂盒,对我国ppd筛查和早期诊断必将是一次有力的推动。技术实现要素:本发明的目的是提供一种用于ppd辅助诊断的wisp3基因的新突变。本发明的第二个目的是提供所述wisp3基因突变在制备ppd检测、治疗或预后产品中的应用。本发明的第三个目的是提供一种用于检测wisp3基因突变的特异性引物。本发明的第四个目的是提供一种ppd辅助诊断的试剂盒。发明人通过分离和研究ppd患者及其父母外周血dna中的位点突变,寻找与ppd高度相关的高特异性和敏感性的突变位点,并研制出可便于临床应用的ppd辅助诊断试剂盒,为ppd的筛查和诊断提供数据支持。本发明的目的是通过下列技术方案实现的:本发明首先提供了一种用于ppd辅助诊断的wisp3基因突变,所述突变包括wisp3基因的两个位点突变,分别为nm_198239.1:c.643+2t>c和nm_198239.1:c.1064_1065dupgt:p.gln356valfster33。进一步地,本发明提供了所述wisp3基因突变在制备ppd检测、治疗或预后产品中的应用。优选的,所述产品包括试剂盒或试剂。进一步地,本发明提供了一种用于检测wisp3基因突变的特异性引物,所述引物为检测wisp3基因的两个位点突变的引物,其核苷酸序列如seqidno:1~seqidno:4所示。优选的,扩增所述wisp3基因突变的特异性引物可以是按照primerpremier5.0引物设计软件或ncbi数据库提供的在线引物设计软件设计的引物,也可以是公司设计合成的引物。在一优选实施例中本发明选用如seqidno:1~4所示引物是由上海生工设计合成的2对引物。本发明选用的引物对特异性强,扩增效果好。进一步地,本发明还提供了一种用于检测所述wisp3基因突变的检测方法,所述方法包括sanger测序、高通量测序、基因芯片或taqmanpcr法。更进一步地,本发明提供了一种ppd辅助诊断的试剂盒,所述试剂盒包括检测wisp3基因的两个位点突变的试剂,所述突变分别为nm_198239.1:c.643+2t>c和nm_198239.1:c.1064_1065dupgt。优选的,所述试剂包括用于扩增所述剪接突变和移码突变位点的引物,或是包括扩增所述剪接突变和移码突变位点的引物和限制性内切酶。优选的,所述引物的核苷酸序列如seqidno:1~seqidno:4所示。优选的,所述试剂还包括dntps、taq酶、mg2+和pcr反应缓冲液。本发明有益效果:本发明研究了wisp3基因的两个突变位点在ppd辅助诊断中的应用前景,阐述wisp3基因的的两个突变位点对于ppd进展的影响,揭示其诊断价值。因此,本发明通过wisp3基因的两个位点突变辅助诊断ppd,为临床医生快速准确掌握患者病情,为临床治疗效果评价奠定基础,并为发现具有潜在治疗价值的新型小分子药物靶标提供帮助。附图说明图1为wisp3:nm_198239.1:c.643+2t>c位点的测序图;图2为wisp3:nm_198239.1:c.1064_1065dupgt位点的测序图。具体实施方式以下实施例用于说明本发明,但不用来限制本发明的范围。若未特别指明,实施例中所用的技术手段为本领域技术人员所熟知的常规手段。本发明的技术方案具体包括:采集ppd家系患者的血液样本,系统收集临床资料;利用外显子测序,找出与ppd相关的突变位点;对筛选出的阳性关联突变位点,进一步采用sanger测序进行位点验证;根据上述与ppd相关的突变位点开发辅助诊断试剂盒。具体来说研究的实验方法主要包括以下几个部分:1.研究样本的选择2016年12月在北京协和医院就诊ppd的1例患者,男17岁,有典型的临床表现,经x线检查确诊。其父母无病,为对照组。取得受试者知情同意采集研究对象的血液样本,编号后置-80℃低温冰箱保存。2.酚-氯仿法提取外周血基因组dna,按常规方法操作。通常能得到20-50ng/μldna,纯度(紫外2600d:2800d)在1.6-2.0。3.全外显子组测序检测(1)取受试者全基因组dna样本;(2)全外显子测序(南京世和基因生物技术有限公司);(3)检测并比较各基因型在ppd患者与其父母对照中的分布差异。4.sanger测序进行验证(1)取受试者dna样本;(2)设计特异性扩增引物;(3)进行pcr反应,回收产物进行测序;(4)比较ppd患者与其父母对照中不同基因型的分布差异。5.诊断试剂盒制备方法根据全外显子测序和sanger测序检测后确定与ppd相关的基因突变,作为ppd诊断的指标并利用其开发辅助诊断ppd的试剂盒。所述突变包括wisp3基因的两个位点突变,分别为nm_198239.1:c.643+2t>c和nm_198239.1:c.1064_1065dupgt:p.gln356valfster33。诊断试剂盒还包括检测wisp3基因突变的特异性引物,以及taq酶、dntps等试剂。6.临床应用例利用本发明人制备的ppd辅助诊断试剂盒对25例ppd患者进行检测并与实际临床检测结果相比较以确定ppd辅助诊断试剂盒的检测率,为临床医生快速准确掌握患者的疾病状态和病情严重程度,及时采取更具个性化的防治方案提供支持。实施例1全外显子组测序1、样本收集2016年12月在北京协和医院就诊ppd的1例患者,男17岁,有典型的临床表现,经x线检查确诊患病;其父母经检测均没有患病。取得其家系受试者知情同意采集研究对象的血液样本,并经本医院伦理委员会通过。编号后置-80℃低温冰箱保存。2、外周血dna的提取和纯化(1)向储存于2ml冻存管中的外周血加入溶血试剂(即裂解液,40份量配置方法如下:蔗糖219.72g、氯化镁2.02g和曲拉通x-100(amresco0694)20ml混合后,用trishcl溶液定容至2000ml,下同),颠倒混匀后完全转入。(2)去除红细胞:用溶血试剂将5ml离心管补至4ml,颠倒混匀,4000rpm离心10分钟,弃上清。向沉淀中加入4ml溶血试剂,再次颠倒混匀清洗一次,4000rpm离心10分钟,弃上清。(3)抽提dna:向沉淀中加1ml抽提液(每300ml中含有122.5ml0.2m氯化钠,14.4ml0.5m乙二胺四乙酸,15ml10%sds(10gsds加水溶解,最后定容到100ml),148.1ml双蒸水,下同)和8μl蛋白酶k,振荡器上充分振荡混匀,37℃水浴过夜。(4)去除蛋白质:加1ml饱和酚充分混匀(手轻摇15分钟),4000rpm离心10分钟,取上清转入新的5ml离心管中。在上清液中加入等体积氯仿与异戊醇混合液(氯仿:异戊醇=24:1,v/v,下同),充分混匀后(手摇15分钟),4000rpm离心10分钟,取上清(分入两个1.5ml的离心管)。(5)dna沉淀:在上清液中加入3m的醋酸钠60μl,再加入与上清液等体积的冰无水乙醇,上下轻摇,可见白色絮状沉淀物,再以12000rpm离心10min。(6)dna洗涤:在沉淀中加入冰无水乙醇1ml,12000rpm离心10min,弃上清后真空抽干或置于清洁干燥环境中蒸干。(7)测量浓度:通常能得到20-50ng/μldna,纯度(紫外2600d:2800d)在1.8-2.0。3、测序(1)文库构建南京世和基因生物技术有限公司采用agilent的液相芯片捕获系统,对人的全外显子区域dna进行高效富集,然后在illuminahiseq平台上进行高通量、高深度测序。建库和捕获实验采用agilentsureselecthumanallexonv5试剂盒,严格使用说明书推荐的试剂和耗材,并参照最新的经过优化的实验流程进行操作。实验基本流程:将基因组dna经covaris破碎仪随机打断成长度为200-300bp左右的片段,经末端修复和加a尾后在片段两端分别连接上接头制备dna文库。带有特异index的文库pooling后与多达543,872个生物素标记的探针进行液相杂交,再使用带链霉素的磁珠将20,965个基因的334,378个外显子捕获下来,经pcr线性扩增后进行文库质检,合格即可进行上机测序。(2)库检文库构建完成后,先使用qubit2.0进行初步定量,稀释文库至1ng/μl,随后使用agilent2100对文库的insertsize进行检测,insertsize符合预期后,使用q-pcr方法对文库的有效浓度进行准确定量(文库有效浓度>2nm),以保证文库质量。(3)上机测序库检合格,根据文库的有效浓度及数据产出需求进行illuminahiseq平台测序。4、数据分析与处理全外显子测序产出的大量数据经初步质量控制后,利用soapaligner等软件进行数据评估以确保数据的可信度,主要包括数据量、重复率、捕获效率、测序深度及覆盖率等指标,继而与人类基因组dna进行对比。生物信息学分析主要针对与人类基因组对比后获得的各类变异,主要包括snp和indels。针对性的分析主要突变对蛋白结构及功能影响的注释,常用到的软件包括sift、polyphen2和mutationtaster。5、分析结果经过数据筛选、深度加工和生物信息学序列比对,最终分析发现患病者wisp3基因具有两个新突变位点,具体情况见表1,其中,nm_198239.1:c.643+2t>c杂合突变为剪接体突变;wisp3基因另一种杂合突变nm_198239.1:c.1064_1065dupgtfster33为移码突变。患者父亲的wisp3基因发生了nm_198239.1:c.1064_1065dupgtfster33的杂合突变,未发生nm_198239.1:c.643+2t>c杂合突变;患者的母亲的wisp3基因发生了nm_198239.1:c.643+2t>c杂合突变,未发生nm_198239.1:c.1064_1065dupgtfster33杂合突变。由此可以确定上述wisp3基因的两个杂合突变为复合杂合突变。患者为这两个杂合突变同时发生时致病,父母只是其中一个杂合突变的携带者,为正常人。表1wisp3基因突变检测结果实施例2sanger测序进行突变位点的验证1、采集实施例1中家系中3个样本的血样,提取dna样本同实施例1;2、pcr扩增pcr引物设计:引物由上海生工设计合成,共设计2对引物,如表2所示。表2引物序列pcr反应体系如表3所示,25μl体系的配制:表3反应体系组分加入量模板1μl正向引物0.5μl反向引物0.5μldntp10mm0.5μltaqbuffer2.5μltaq酶5u/μl0.2μl水19.8μlpcr扩增程序如表4所示。表4反应体系3、测序pcr扩增结束后,取5μl扩增产物,1%琼脂糖凝胶电泳,电泳30min,染色20min,然后将凝胶块置于凝胶成像仪中观察,根据比对marker的片段大小情况,初步判断扩增片段是否正确。进而对符合要求的扩增产物进行纯化,对纯化后的产物进行双向测序:采用abi公司bigdye3.1sequencingkit试剂盒,并按试剂盒要求进行操作;用abi公司3730型测序仪进行测序。4、结果分析测序结果用chromas序列分析软件,将测序结果与标准序列进行比对,并结合父本和母本的序列,寻找突变位点,通过分析突变位点处碱基的类型,得到位点的基因型。结果如图1和图2所示:患者wisp3(nm_198239.1)基因发生了两个突变,在wisp3基因cdna第643位置为内含子与外显子拼接区的最后一个碱基,在基因组dna上,该位置向后推进2个碱基的内含子643+2位置上的t突变成c,这种拼接区的突变为剪接突变,容易造成转录后rna剪切的错误,从而导致蛋白质的改变;另一种是在第1064_1065位出现重复gt,从而导致wisp3蛋白第356号氨基酸位置上谷氨酰胺变成了缬氨酸,并造成结构移码突变,两个突变均为杂合突变。患者的母亲的wisp3基因只发生了nm_198239.1:c.643+2t>c杂合突变;患者父亲的wisp3基因只发生了nm_198239.1:c.1064_1065dupgtfster33的杂合突变。sanger测序结果与全外显子测序结果相符合。附图中箭头和方框所标位置为突变位点。根据测序图查看ppd患者及其父母的wisp3基因突变位点是否有变化。如图1-1中所示,测序图中该位点为单峰t,峰的颜色浅,位点未发生突变;如图1-2和1-3中所示,该位点为双峰重叠,同时含有c和t,峰的颜色深,位点发生了杂合突变。从而进一步确认所述两个突变位点可同时用于进行性假性类风湿性发育不良症的检测、治疗、诊断、预后评估等辅助诊断。实施例3基因突变检测试剂盒的制作突变位点试剂盒的制作和操作流程是基于sanger测序扫描检测分型技术。试剂盒含有实施例2中扩增wisp3基因两个突变位点的特异性引物,该试剂盒还可以包括pcr反应常用的试剂,如taq酶、dntp混合液、mgcl2溶液、去离子水等;这些常用试剂都是本领域技术人员熟知的,另外还可以含有标准品和/或对照品(如确定基因型的标准品和空白对照等)。此试剂盒的价值在于只需要外周血而不需要其它组织样品,通过最精简和特异的引物对检测突变位点,再通过突变位点谱辅助判断ppd,不仅稳定,检测方便,且精确,大大提高疾病诊断的敏感性和特异性,因此将此试剂盒投入实践,可以帮助指导诊断和更有效的个体化治疗。实施例4ppd辅助诊断试剂盒的验证1、病例选取25例临床确诊为的ppd患者,取样来源于2016年5月到2017年3月期间在北京协和医院骨科就诊的的病人。采集所有研究对象的血液样本,编号后置-80℃低温冰箱保存。本研究的所有临床样本,均对患者进行知情告知并经本医院伦理委员会通过。2、方法提取样本dna,使用实施例3中ppd辅助诊断试剂盒检测血液样本中wisp3基因的c.643+2t>c和c.1064_1065dupgt:p.gln356valfster33的两个突变位点是否同时发生突变,如同时发生突变确定为患有ppd。3、结果结果显示,25例ppd患者的血液样本中有9例患者样本中wisp3基因的c.643+2t>c和c.1064_1065dupgt:p.gln356valfster33的两个突变位点发生突变;有0例患者血液样本中单独出现c.643+2t>c位点突变;有0患者样本中单独出现c.1064_1065dupgt:p.gln356valfster33突变;16例患者两个位点均未发生突变。本发明制备的试剂盒检测率为36%。据此推断,本ppd的诊断试剂盒可以为临床提供诊断线索。虽然,上文中已经用一般性说明及具体实施方案对本发明作了详尽的描述,但在本发明基础上,可以对之作一些修改或改进,这对本领域技术人员而言是显而易见的。因此,在不偏离本发明精神的基础上所做的这些修改或改进,均属于本发明要求保护的范围。序列表<110>中国医学科学院北京协和医院<120>一种用于ppd辅助诊断的wisp3基因突变及其应用<130>p17007<160>4<170>patentinversion3.5<210>1<211>25<212>dna<213>人工序列<400>1ggttgagagctatacttcatacagg25<210>2<211>23<212>dna<213>人工序列<400>2ctctgaccaccaatcaacaagta23<210>3<211>23<212>dna<213>人工序列<400>3ggtaaagagagtgctggaaatca23<210>4<211>25<212>dna<213>人工序列<400>4atgccttaaatgtagtgatctgaga25当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1