一种酶交联水凝胶的制备方法及其应用与流程
本发明属于水凝胶技术领域,尤其涉及一种酶交联水凝胶的制备方法及其应用。
背景技术:
可注射性水凝胶基于的支架材料包括天然高分子材料和合成高分子材料,如胶原、壳聚糖海藻酸、透明质酸及聚乙二醇(peo)、聚乳酸(pla)等。其在原位“溶胶-凝胶”转变成型的方式一般有温敏交联、化学交联(michal加成交联、自由基交联、离子交联、光交联等)以及酶交联等。
温敏性交联的水凝胶主要是通过温度的改变发生“溶胶-凝胶”的转变,分为降温型转变和升温型转变。虽然其转变过程中不需添加其他添加剂,但是其转变方式需依赖一定的温度。化学交联是将带有光敏性或不饱和官能团的前驱物在离子、光照或交联因子的作用下发生自由基聚合或氧化还原反应进而发生交联反应。虽然其交联速度相对较快,但是该凝胶方式可能会引起水凝胶体系的ph值的变化,并伴随着副产物的毒性问题。其中光交联中的uv光引发聚合方式可能会损伤组织,且uv光的透过率有限,不适用于较深组织的修复。
技术实现要素:
针对现有技术中的上述问题,本发明的主要目的在于提供一种酶交联水凝胶的制备方法,得到了一种温和的酶促交联自聚合水凝胶,具有优异生物相容性,克服了现有水凝胶中化学交联因子残留于体系或光交联引起的毒副作用等缺点。
为了达到上述目的,本发明采用如下技术方案:一种酶交联水凝胶的制备方法,所述方法包括如下步骤:将cs-c(儿茶酚改性的壳聚糖)分别溶于0.06wt%的h2o2溶液及0.004wt%的hrp酶溶液(辣根过氧化物酶)中,得到1.5-1.8wt%的cs-c的h2o2溶液和cs-c的hrp酶溶液;分别将cs-c的h2o2溶液和cs-c的hrp酶溶液加入到y型注射器中进行混合注射,在凝胶模具中形成凝胶。
作为进一步的优选,所述凝胶模具为底部锯掉的ep管,形成凝胶的时间为150s。
作为进一步的优选,所述cs-c的制备方法包括:
1)将cs(壳聚糖)溶解于酸液中,搅拌得到cs溶液;调节所述cs溶液至ph=5.0后,再将cha(3,4-二羟苯基丙酸)加入到所述cs溶液中,cha和cs的摩尔比为0.8~1,搅拌至澄清,得到溶液a;
2)将edc(1-(3-二甲氨基丙基)-3-乙基碳二亚胺盐酸盐)溶解于第一溶剂中,得到溶液,将所述溶液逐滴加入到溶液a中,搅拌,使其充分混合;edc和cha的摩尔比为1-2,偶联反应12-24h,并保持ph=5,温度37℃;反应结束后,透析除去反应物质及副产物,冻干得到cs-c(儿茶酚改性接枝的壳聚糖)。
作为进一步的优选,所述步骤1)中,所述酸液为ph=1~2的hcl溶液,所述搅拌时间为4-6h。
作为进一步的优选,所述步骤2)中,所述第一溶剂为乙醇。
作为进一步的优选,所述步骤2)中,控制滴加的速率为以1滴/秒。
作为进一步的优选,所述步骤2)中,所述透析包括:依次置于含有1wt%的nacl、ph=5.0的hcl溶液和去离子水中透析。
本发明的另一目的还在于提供了一种酶交联水凝胶的应用,所述水凝胶可负载人诱导多能干细胞。
作为进一步的优选,所述水凝胶负载人诱导多能干细胞的方法包括:将15-18mg的cs-c分别溶于1ml0.06wt%的h2o2溶液及1ml0.004wt%的hrp酶溶液中,得到cs-c的h2o2溶液和cs-c的hrp酶溶液;将所述cs-c的h2o2溶液和cs-c的hrp酶溶液预混,得到预混液;在预混液未完全凝胶之前,加入0.2~0.3mlipsc(4×106个/ml)的细胞悬液到所述预混液中,轻柔混合均匀后,在37℃,5%co2培养箱中培养3天。
本发明的有益效果是:本发明水凝胶制备方法将cs-c分别溶于h2o2溶液及hrp酶溶液中,为辣根过氧化物酶催化交联,该交联方式克服了常用化学交联因子残留于体系或光交联引起的毒副作用的缺点;继而将cs-c的h2o2溶液和cs-c的hrp酶溶液分别加入到y型注射器中进行混合注射,在凝胶模具中形成凝胶;使用y型注射器一方面提高了操作的简便性;另一方面能够实现凝胶前躯体溶液的充分混合。另外,本发明首次引入种子细胞诱导多功能干细胞(ipsc),提供了体外立体构建ipsc增殖培养水凝胶的载体,该凝胶载体具有良好的生物相容性。
附图说明
图1为儿茶酚改性的壳聚糖cs-c的结构式。
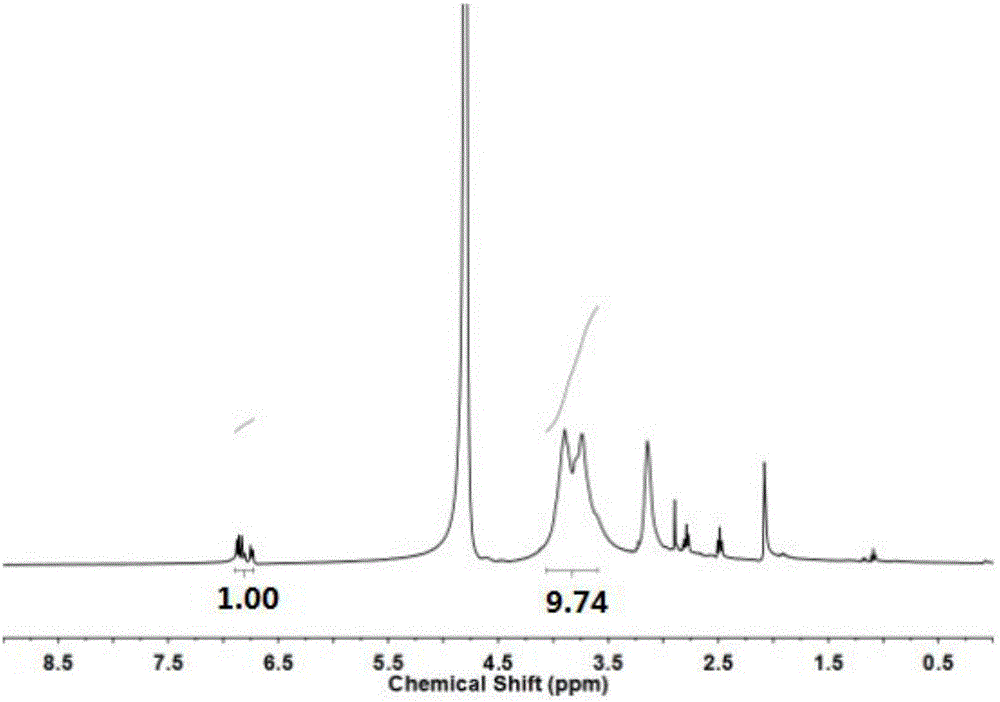
图2为儿茶酚改性的壳聚糖(cs-c)的h1nmr示意图。
图3为本发明实施例酶交联水凝胶的制备流程示意图。
图4为本发明实施例得到的cs-c的hrp/h2o2水溶液以及酶交联水凝胶的样本示意图。
图5a-5b为本发明实施例酶交联水凝胶的扫描电镜示意图。
图6为humanipsc细胞(人诱导多能干细胞)在凝胶上增殖3天后的扫描电镜图。
图7a-7b为humanipsc细胞在凝胶上增殖3天后的蔡司显微镜图。
具体实施方式
本发明通过提供一种酶交联水凝胶的制备方法及其应用,克服了现有水凝胶中化学交联因子残留于体系或光交联引起的毒副作用等缺点。
为了克服上述缺陷,本发明实施例的主要思路是:
本发明实施例酶交联水凝胶的制备方法,所述方法包括如下步骤:将cs-c(儿茶酚改性的壳聚糖)分别溶于0.06wt%的h2o2溶液及0.004wt%的hrp酶溶液(辣根过氧化物酶)中,得到1.5-1.8wt%的cs-c的h2o2溶液和cs-c的hrp酶溶液;分别将cs-c的h2o2溶液和cs-c的hrp酶溶液加入到y型注射器中进行混合注射,在凝胶模具中形成凝胶。
本发明所用的cs-c(儿茶酚改性的壳聚糖)可选择现有市售产品或现有常规方法制备而得,也可采用下述本发明实施例中的方法制备。另外,所配制h2o2溶液和hrp酶溶液的水溶液均经过高温高压灭菌处理。
针对传统的可注射性水凝胶“溶胶-凝胶”转变基于的交联方式存在温度依赖性、潜在副作用、交联局限性等难点,本发明通过辣根过氧化物酶(hrp)、h2o2催化作用于儿茶酚改性的壳聚糖大分子,形成原位交联的可注射水凝胶。另外,本发明方法提供了一种具有优异生物相容性的可注射型酶交联水凝胶,能够应用于三维细胞培养和组织工程中。
为了让本发明之上述和其它目的、特征、和优点能更明显易懂,下文通过实施例具体阐述本发明所述之酶交联水凝胶的制备方法及其应用。
实施例1:
第一步:儿茶酚改性的壳聚糖(cs-c)的制备
1)在常温下,将壳聚糖(cs)溶解于0.05mol/l的hcl溶液中,室温25℃磁力搅拌4h得到1wt%的cs溶液;将配置好的0.1mol/lnaoh溶液缓慢调节其ph=5.0后,再将3,4-二羟苯基丙酸(cha)加入cs溶液中,3,4-二羟苯基丙酸和壳聚糖的摩尔比为0.8~1。搅拌至澄清,得到溶液a;
2)在常温下,将(1-(3-二甲氨基丙基)-3-乙基碳二亚胺盐酸盐)(edc)溶解于50ml乙醇,逐滴加入到溶液a中,控制滴加速率,以1滴/秒的速度逐滴滴加至烧瓶中,并用磁力搅拌器搅拌,使其充分溶解。edc和cha的摩尔比为1,偶联反应12h,并保持ph=5,温度37℃。反应结束后,依次置于含有nacl(1wt%)的ph=5.0的hcl溶液和去离子水中透析除去反应物质及副产物,冻干得到儿茶酚改性接枝的壳聚糖(cs-c)。cs-c的产率均大于60%,接枝率约为17%。图1为儿茶酚改性的壳聚糖cs-c的结构式,图2为儿茶酚改性的壳聚糖(cs-c)的h1nmr示意图。
第二步:cs-c酶响应水凝胶的制备
分别称取3.5mgcs-c,溶于0.2ml0.06wt%的h2o2溶液及0.2ml0.004wt%的hrp酶溶液(所配制h2o2溶液和hrp酶溶液的水溶液均经过高温高压灭菌处理)。分别将cs-c的h2o2溶液和cs-c的hrp酶溶液加入到1ml的y型注射器中进行混合注射,凝胶模具为低部锯掉的5mlep管,同时用秒表记录其凝胶时间(以倒置ep管时,溶液不向下流出为凝胶标准)凝胶时间为:150s,制备得到了可注射型酶交联3d水凝胶。图3为本发明实施例酶交联水凝胶的制备流程示意图。图4为本发明实施例得到的cs-c的hrp/h2o2水溶液以及酶交联水凝胶的样本示意图。图5a-5b为本发明实施例制备的酶交联水凝胶的扫描电镜示意图。
实施例2:
第一步:儿茶酚改性的壳聚糖(cs-c)的制备
1)在常温下,将壳聚糖(cs)溶解于0.05mol/l的hcl溶液中,室温25℃磁力搅拌4h得到1wt%的cs溶液;将配置好的0.1mol/lnaoh溶液缓慢调节其ph=5.0后,再将3,4-二羟苯基丙酸(cha)加入cs溶液中,3,4-二羟苯基丙酸和壳聚糖的摩尔比为0.8~1。搅拌至澄清,得到溶液a;
2)在常温下,将(1-(3-二甲氨基丙基)-3-乙基碳二亚胺盐酸盐)(edc)溶解于50ml乙醇,逐滴加入到溶液a中,控制滴加速率,以1滴/秒的速度逐滴滴加至烧瓶中,并用磁力搅拌器搅拌,使其充分溶解。edc和cha的摩尔比为1,偶联反应12h,并保持ph=5,温度37℃。反应结束后,依次置于含有nacl(1wt%)的ph=5.0的hcl溶液和去离子水中透析除去反应物质及副产物,冻干得到儿茶酚改性接枝的壳聚糖(cs-c)。cs-c的产率均大于60%,接枝率约为17%。
第二步:cs-c酶响应水凝胶负载人诱导多能干细胞(humanipsc)
分别称取17.5mgcs-c,溶于1ml0.06wt%的h2o2溶液及1ml0.004wt%的hrp酶溶液(配溶液所用的di-water均经过高温高压灭菌处理)。首先将两种溶液预混后,在其未完全凝胶之前,加入0.25mlipsc的细胞悬液到凝胶中,轻柔混合均匀后,然后将该复合支架转移至6孔培养板中,在37℃,5%co2培养箱中培养3天。
图6为humanipsc细胞(人诱导多能干细胞)在凝胶上增殖3天后的扫描电镜图。图7a-7b为humanipsc细胞在凝胶上增殖3天后的蔡司显微镜图。本实施例2制备得到了ipsc的3d水凝胶载体。该凝胶载体具有良好的生物相容性,人诱导多能干细胞活性先增加后不变(经mtt验证)。细胞在凝胶化和混合过程中有部分死亡,凝胶中的细胞呈“团状”或铺展的细胞层。
上述本申请实施例中的技术方案,至少具有如下的技术效果或优点:本发明水凝胶制备方法将cs-c分别溶于h2o2溶液及hrp酶溶液中,为辣根过氧化物酶催化交联,该交联方式克服了常用化学交联因子残留于体系或光交联引起的毒副作用的缺点;继而将cs-c的h2o2溶液和cs-c的hrp酶溶液分别加入到y型注射器中进行混合注射,在凝胶模具中形成凝胶;使用y型注射器一方面提高了操作的简便性;另一方面能够实现凝胶前躯体溶液的充分混合。另外,本发明首次引入种子细胞诱导多功能干细胞(ipsc),提供了体外立体构建ipsc增殖培养水凝胶的载体,该凝胶载体具有良好的生物相容性。
尽管已描述了本发明的优选实施例,但本领域内的技术人员一旦得知了基本创造性概念,则可对这些实施例作出另外的变更和修改。所以,所附权利要求意欲解释为包括优选实施例以及落入本发明范围的所有变更和修改。显然,本领域的技术人员可以对本发明进行各种改动和变型而不脱离本发明的精神和范围。这样,倘若本发明的这些修改和变型属于本发明权利要求及其等同技术的范围之内,则本发明也意图包含这些改动和变型在内。
- 还没有人留言评论。精彩留言会获得点赞!