三多巴胺基化合物与聚合物及其制备方法与应用与流程
本发明属于高分子化学表面改性技术领域,具体涉及三多巴胺端基三聚合物尾链的聚合物与其化合物及其制备方法和应用于基材表面改性。
背景技术:
由蛋白质、细菌、细胞等生命有机体内物质在基材表面的聚集而导致的生物污染问题会严重导致基材功能减退,影响人体健康和增加成本,因此材料是否具有阻抗生命物质吸附的性能对其能否得到广泛应用是至关重要的。
目前,广泛应用的抗生物污染策略是通过基材表面改性构筑聚合物亲水性表面,利用聚合物对表面改性通常有两种方法:即1)将已有高分子接枝于表面上(grafting-to);2)在表面原位生长高分子链(grafting-from)。前者方法简单,但表面改性效率低且不稳定;后者改性效果好,但过程复杂、条件苛刻,适用基材表面少。因此,利用仿贻贝黏附辅助的“graftingto”法在基材表面制备高分子刷具有重要应用前景,如gao,c.;li,g.;xue,h.;yang,w.;zhang,f.;jiang,s.functionalizableandultra-lowfoulingzwitterionicsurfacesviaadhesivemusselmimeticlinkages.biomaterials2010,31(7):1486-92.和brault,n.d.;gao,c.;xue,h.;piliarik,m.;homola,j.;jiang,s.;yu,q.ultra-lowfoulingandfunctionalizablezwitterioniccoatingsgraftedontosio2viaabiomimeticadhesivegroupforsensinganddetectionincomplexmedia.biosensorsandbioelectronics2010,25(10):2276-2282.等利用含多巴胺端基的两性离子聚合物聚甲基丙烯酸羧基甜菜碱(pcbma),通过“graftingto”的方法将其接枝到基材表面,结果显示,这种基材具有较高的接枝密度和抗蛋白质吸附的能力,但效率低且保持材料长期稳定较困难。
技术实现要素:
本发明合成了如下结构
的三多巴胺端基三聚合物尾链的聚合物(dopa)3-(polymer)3,可将其应用于制备长期稳定的分子刷,用于基材表面的改性,以达到抗生物污染的目的。
该聚合物的三多巴胺端基结构可有效解决利用“graftingto”的方法在基材表面接枝高分子效率低且不稳定的问题,通过设计或改变聚合物单体可以获得具有不同性质的新型聚合物。
聚合物尾链polymer选自聚甲基丙烯酸n,n-二甲氨基乙酯pdmaema、聚甲基丙烯酸磺酸甜菜碱psbma、聚n-异丙基丙烯酰胺pnipam的一种或多种,其中聚合物尾链polymer的聚合度为20~150的整数。(dopa)3-polymern中的n表示每根聚合物尾链的聚合度,如(dopa)3-polymer40表示聚合度为40。
本发明还提供上述三多巴胺端基三聚合物尾链的聚合物的合成方法。
聚合物合成方法采用atrp法,具体步骤如下:
该聚合反应体系由引发剂(dopa)3-br、混合溶剂(水与极性有机溶剂)、单体、配体、cubr/cubr2组成。其中单体与引发剂摩尔比为3~60,配体与引发剂摩尔比在8~9,cubr与引发剂摩尔比3~4,cubr2与引发剂摩尔比在0~0.5,混合溶剂:极性有机溶剂与h2o体积比在3~4。反应在惰性气体氛围下进行,反应时间10~20h,反应温度15~30℃,反应结束后通入空气或用液氮淬灭,最后除去液体,收集沉淀,透析,冷冻干燥得到白色固体粉末。
将上述白色粉末与正丁基氟化铵反应,以脱除叔丁基二甲基硅烷基保护基团,反应在惰性气体氛围中进行,反应温度为20~30℃,反应时间10~20h。混合物离心洗涤,真空干燥得到聚合物。
单体选自甲基丙烯酸磺基甜菜碱、甲基丙烯酸n,n-二甲氨基乙酯、n-异丙基丙烯酰胺;配体选自2-2'-联吡啶(bpy)、n,n,n',n,'n”-五甲基二亚乙基三胺(pmdeta)、二亚乙基三胺(deta);极性有机溶剂选自n,n-二甲基甲酰胺(dmf)、四氢呋喃(thf)、甲醇(methanol);惰性气体可以是氮气、氩气。
本发明还提供了化合物(dopa)3-br及其制备方法。
化合物(dopa)3-br可以用作制备聚合物(dopa)3-(polymer)3的引发剂。
化合物(dopa)3-br结构如下:
化合物(dopa)3-br的制备方法,是将结构式如下的前驱物
和三(2-氨基乙基)胺末端的氨基相连,具体步骤:
1)在惰性气体保护下,将三(2-氨基乙基)胺加入含有过量前驱物的溶液中。0~5℃下,将三乙胺加入混合溶液中。持续反应10~20h,停止反应。得到含有化合物(dopa)3-br的混合液。
2)蒸干溶剂,滴入盐酸溶液。萃取,真空除去溶剂,得到含有化合物(dopa)3-br的粗产品。
3)粗产品通过柱层析法分离(梯度洗脱,二氯甲烷/甲醇体积比为15~30),最后收集得到化合物(dopa)3-br的白色粉末。
前驱物通过文献zhang,a.f.,elal.angewchemintedit2004,43(39):5185-5188;li,g.,etal.biomaterials2008,29(35):4592-4597;maier,g.p.,science2015,349(6248):628-631.的方法制得。
聚合物在基材表面改性中的应用,具体过程:聚合物溶于ph=7.5~10的tris(三羟甲基氨基甲烷)-hcl水溶液中,聚合物浓度为0.5~5mg/ml,取清洗干净的基材浸入溶液,搅拌或振荡10min~24h,使聚合物自黏附在基材表面。取出基材,交替用磷酸缓冲盐溶液pbs和超纯水冲洗,以除去表面没有固定黏附的自由聚合物,冷冻干燥或者用惰性气体吹干。相应基片的对照样品则为相同条件下将聚合物溶液改为超纯水,其他步骤均相同。
将表面改性后的基材进行稳定性测试:浸泡在pbs缓冲溶液中,在不同时间段(5~30天)取出相应硅片,测试浸泡过后的基材表面抗蛋白质吸附的性能,实验证明改性基板表面能够稳定存在于pbs缓冲液中至少30天且仍具有抗蛋白吸附性。
基材可以是常见材料,如硅片、不锈钢、云母片、聚偏氟乙烯pvdf。
本发明的优点:1)设计三多巴胺端基结构的化合物为引发剂,使利用“graftingto”的方法在基材表面高效、稳定的接枝高分子成为可能;2)通过改变聚合反应单体,可制备如环境响应性、抗生物污染等不同功能性的新型聚合物刷。
附图说明
图1是三多巴胺端基三聚合物尾链的聚合物的合成路线图示。
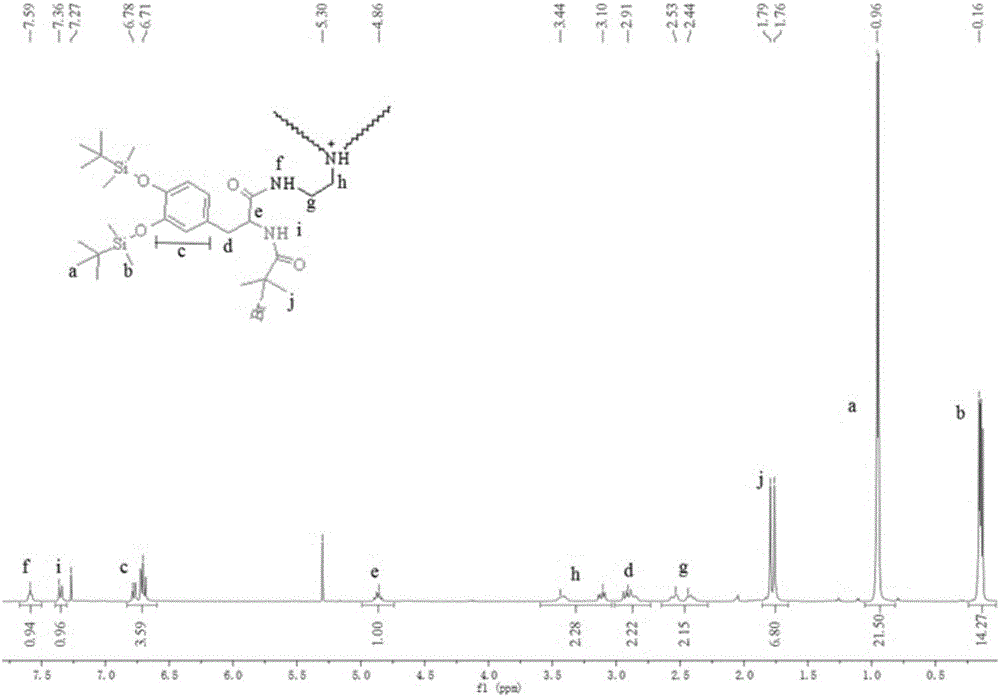
图2是三多巴胺端基结构的化合物(dopa)3-br的1h-nmr图谱(cdcl3,400mhz,298k)。
图3是三多巴胺端基结构的化合物(dopa)3-br的13cnmr图谱(cdcl3,100mhz,298k)
图4是三多巴胺端基结构的化合物(dopa)3-br的质谱图。
图5是三多巴胺端基三聚甲基丙烯酸n,n-二甲氨基乙酯尾链的聚合物(dopa3-pdmaema)的1h-nmr图谱(溶剂d2o)。
图6是三多巴胺端基三聚甲基丙烯酸磺基甜菜碱尾链的聚合物(dopa3-psbma)的1h-nmr图谱(溶剂d2o)。
图7是三多巴胺端基三聚n-异丙基丙烯酰胺尾链的聚合物(dopa3-pnipam)的1h-nmr图谱(溶剂d2o)
图8是异硫氰酸荧光素(fitc)标记的牛血清白蛋白(bsa)培养改性硅板30天后,激光共聚焦显微镜(lscm)测得硅片表面抗蛋白吸附性能对比图(具体:激发光为488nm和发射光为520nm的波长下,检测的吸附情况,a为未改性硅片,b1、b2分别为dopa-psbma40、dopa3-psbma40改性硅片;c1、c2分别为dopa-psbma70、dopa3-psbma70改性硅片,d1、d2分别为dopa-psbma100、dopa3-psbma100改性硅片)
具体实施方式
制备三多巴胺端基三聚合物尾链包括两个步骤,在此基础上可以构建三多巴胺端基三聚甲基丙烯酸磺酸甜菜碱尾链的抗生物污染表面:
1)由三(2-氨基乙基)胺连接的三多巴胺端基的原子转移自由基引发剂——化合物(dopa)3-br的合成,通过1h-nmr,13cnmr和质谱确定其结构;
2)三多巴胺端基三聚合物尾链的新型聚合物的合成,通过1h-nmr和gpc确定结构和分子量;
3)构建三多巴胺端基三聚甲基丙烯酸磺酸甜菜碱尾链的新型聚合物改性的基材表面:本发明中的待改性基材表面的清洁处理的方法和原理相似,本领域普通技术人员仅需根据基材的不同,选用合适清洁处理方法。将清洗后的基材浸入浓度为0.5~5mg/ml的三多巴胺端基三聚甲基丙烯酸磺酸甜菜碱尾链的聚合物的tris-hcl缓冲溶液(浓度8~12mm,ph=7.5~10)中,再放入0~40℃的恒温振荡器中培养10min~24h。培养后的硅片先后用pbs缓冲液和超纯水清洗以除去表面没有固定粘附的自由聚合物,清洗完毕后冷冻干燥或用n2吹干。利用激光共聚焦显微镜(lscm)测得三多巴胺端基三聚甲基丙烯酸磺基甜菜碱尾链改性前后硅片在异硫氰酸荧光素标记牛血清白蛋白(fitc-bsa)溶液中培养5~30天后表面的抗蛋白吸附性能。以下结合具体实施方式对本发明进行详细描述。
实施例1
三多巴胺端基的原子转移自由基引发剂——化合物(dopa)3-br的前驱物的合成:
根据文献zhang,a.f.;elal.angewchemintedit2004,43(39):5185-5188;li,g.;etal.biomaterials2008,29(35):4592-4597;maier,g.p.;science2015,349(6248):628-631.方法制备。在n2氛围下,将2.072g(18mmol)n-羟基丁二酰亚胺加入2.556g(15mmol)2-溴异丁酸的15ml二氯甲烷溶液中,搅拌十分钟后,在冰水浴下,加入3.866g(18.75mmol)二环己基碳二亚胺。反应混合物在冰水浴下搅拌反应一个小时后,再在室温下继续反应十六个小时。真空抽滤除去固体,再用20ml二氯甲烷淋洗固体,滤液用旋转蒸发仪蒸发浓缩。最后,粗产品用硅胶柱分离纯化(梯度洗脱,石油醚/乙酸乙酯体积比例从5/1到5/2),纯化后得3.58g白色晶体,即为合成路线中的化合物1;
将6.81g(44.73mmol))叔丁基二甲基氯硅烷加入史莱克瓶中,抽充气循环三次后,再把30ml乙腈用注射器加入瓶中,搅拌使叔丁基二甲基氯硅烷溶解。在n2保护下,迅速的将3g(14.19mmol)左旋多巴加入混合溶液中。搅拌均匀后,在冰水浴下,将6.826ml(44.73mmol)1,8-二氮杂二环十一碳-7-烯逐滴加入混合溶液中。反应混合物在冰水浴中反应六个小时后,再在室温下继续反应十六个小时。在后处理之前,停止搅拌,将史莱克瓶放入-27℃的冰箱中保持一个小时。取出后,真空抽滤除去滤液,白色固体再用200ml冷的氯仿淋洗,收集固体并干燥。干燥后的固体用甲醇溶解,用柱层析法分离(甲醇为洗脱液),最后收集到2.580g白色粉末产物,即为合成路线中的化合物2;
在室温n2保护下,将2.32g(5.46mmol)化合物2加入1.348g(5.46mmol)化合物1的6mln,n-二甲基甲酰胺溶液中。在冰水浴下,将0.96ml(5.46mmol)n,n-二异丙基乙胺用注射器逐滴加入混合液中。在冰水浴下反应一个小时,再在室温下反应十五个小时。停止搅拌,为除去n,n-二异丙基乙胺和n,n-二甲基甲酰胺,把混合液滴入50ml质量分数为3%的盐酸溶液中,然后用乙酸乙酯萃取三次(3×40ml),合并有机相,再用去离子水洗涤三次(3×40ml),最后用无水硫酸镁干燥。混合液用旋转蒸发仪浓缩,再用柱层析法分离提纯(先用0.5%乙酸的二氯甲烷混合液酸化柱子,再用10/1的二氯甲烷/甲醇混合液进行洗脱),收集到3.028g泡沫状淡黄色黏稠物,即为合成路线中的化合物3;
在n2保护下,把2.072g(18mmol)n-羟基丁二酰亚胺加入盛有3.028g(5.269mmol)化合物3和10ml二氯甲烷的史莱克瓶中。冰水浴中搅拌十分钟后,在n2保护下,加入1.358g(6.58mmol)二环己基碳二亚胺。冰水浴下反应一小时后,再在室温反应十六个小时。终止反应,真空抽滤去除固体,再用20ml二氯甲烷淋洗液体,收集滤液并用旋转蒸发仪浓缩。粗产品过硅胶柱分离提纯(梯度洗脱,石油醚/乙酸乙酯体积比例从5/1到5/2),最后得2.823g泡沫状透明黏稠物,即三多巴胺端基的原子转移自由基引发剂((dopa)3-br)的前驱物化合物;
实施例2
三多巴胺端基的原子转移自由基引发剂((dopa)3-br)的合成:
在n2保护下,将136μl(0.863mmol)三(2-氨基乙基)胺迅速加入含有过量2.8227g(4.315mmol)前驱化合物③的6ml二氯甲烷溶液中。在冰水浴下,将606μl(4.315mmol)三乙胺用注射器加入溶液中。冰水浴下反应一小时后,再在室温下持续反应十六个小时,停止反应。蒸干二氯甲烷,加入10ml乙酸乙酯,再滴入50ml盐酸溶液(质量分数0.6%)。溶液用乙酸乙酸溶液分三次萃取(3×40ml),合并有机相,用无水硫酸镁干燥过滤,再用旋转蒸发仪除去溶剂进行浓缩。粗产品用中性氧化铝柱分离提纯(梯度洗脱,先用纯二氯甲烷洗脱,再用二氯甲烷/甲醇体积比为20/1的洗脱液洗脱),最后收集到0.862g三多巴胺端基的引发剂((dopa)3-br)的白色粉末。
实施例3
三多巴胺端基三聚甲基丙烯酸n,n-二甲氨基乙酯(dopa3-pdmaema)的合成:
将引发剂(43.14mg,0.0238mmol),溴化亚铜(11.3mg,0.0786mmol),溴化铜(2.8mg,0.0125mmol)和2,2'-联吡啶(31.3mg,0.2mmol)加入史莱克瓶中,抽真空—充氮气循环三次后,使史莱克瓶中保持n2氛围。然后把经过除氧处理的n,n-二甲基甲酰胺(4ml)用注射器加入反应瓶中。搅拌十分钟后,将经过除氧处理的甲基丙烯酸n,n-二甲氨基乙酯单体(0.337g,2.2mmol)和n,n-二甲基甲酰胺(体积6ml)混合溶液用注射器注入史莱克瓶中,然后在20℃的恒温下反应十个小时。反应在液氮中淬灭,随后解冻。最后除去液体,收集沉淀并溶于去离子水中,透析三天,冷冻干燥得到固体粉末。
白色粉末高分子需要脱除叔丁基二甲基硅烷基保护基团,高分子中保护基与正丁基氟化铵以2/5的比例反应。把高分子粉末加入史莱克瓶中,抽真空—充氮气循环三次后,用注射器把四氢呋喃加入史莱克瓶中,搅拌十分钟后,加入正丁基氟化铵,室温反应二十小时。混合物用四氢呋喃离心洗涤三次,室温真空干燥得粉末状固体。
实施例4
三多巴胺端基三聚磺基甜菜碱尾链的聚合物(dopa3-psbma)的合成:
将引发剂(43.14mg,0.0238mmol),溴化亚铜(11.3mg,0.0786mmol),溴化铜(2.8mg,0.0125mmol)和2,2'-联吡啶(31.3mg,0.2mmol)加入史莱克瓶中,抽真空—充氮气循环三次后,使史莱克瓶中保持n2氛围。然后把经过除氧处理的n,n-二甲基甲酰胺(4ml)用注射器加入反应瓶中。搅拌十分钟后,将经过除氧处理的甲基丙烯酸单体(1.397g,5mmol)和水/dmf(体积比3ml/6.5ml)混合溶液用注射器注入史莱克瓶中,然后在20℃的恒温下反应十五个小时。反应在液氮中淬灭,随后解冻。最后除去液体,收集沉淀并溶于去离子水中,透析三天,冷冻干燥得到白色固体粉末。脱除叔丁基二甲基硅烷基保护基团同上。
实施例5
三多巴胺端基三聚n-异丙基丙烯酰胺尾链的聚合物(dopa3-pnipam)的合成:
将引发剂(43.14mg,0.0238mmol),溴化亚铜(11.3mg,0.0786mmol),溴化铜(2.8mg,0.0125mmol)和2,2’-联吡啶(31.3mg,0.2mmol)加入史莱克瓶中,抽真空—充氮气循环三次后,使史莱克瓶中保持n2氛围。然后把经过除氧处理的n,n-二甲基甲酰胺(4.5ml)用注射器加入反应瓶中。搅拌十分钟后,将经过除氧处理的n-异丙基丙烯酰胺单体(1.211g,10.71mmol)和水/dmf(体积比3ml/5ml)混合溶液用注射器注入史莱克瓶中,然后在20℃的恒温下反应十八个小时。反应在液氮中淬灭,随后解冻。最后除去液体,收集沉淀并溶于去离子水中,在透析袋中透析三天,再冷冻干燥得到固体粉末。脱除叔丁基二甲基硅烷基保护基团的步骤同上。
实施例6
硅片的清洗:首先用适量的超纯水清洗硅片,每次超声处理10min,为防止在超声中破坏硅片,将超声的功率调到40hz,重复超声处理三次。再用紫外灯清洗仪处理一小时,然后用超纯水冲洗三次,之后在氮气氛围下吹干,放置无尘烘箱中干燥。
实施例7
不锈钢的清洗:首先用适量的超纯水超声清洗不锈钢10min,超声功率40hz,然后依次换用丙酮,乙醇,超纯水重复清洗各一次。在氮气氛围下吹干,放置无尘烘箱中干燥备用。
实施例8
聚偏氟乙烯膜(pvdf)的清洗:用超纯水和乙醇交替超声清洗三次,每次10min,功率40hz。
实施例9
三多巴胺端基三聚磺基甜菜碱尾链的聚合物(dopa3-psbma70)对硅片表面的改性:上述清洗后的硅片浸入2mg/ml的dopa3-psbma70的tris缓冲溶液(浓度10mm,ph=8.5)中,再放入25℃的恒温振荡器中培养6h。培养后的硅片用pbs缓冲液(10mm,ph=7.4)清洗3次,紧接着用水清洗3次,清洗完毕用n2吹干。
实施例10
三多巴胺端基三聚甲基丙烯酸n,n-二甲氨基乙酯(dopa3-pdmaema40)对不锈钢板表面的改性:上述清洗后的不锈钢浸入2mg/ml的dopa3-pdmaema40的tris缓冲溶液(浓度10mm,ph=8.5)中,再放入25℃的恒温振荡器中培养5h。培养后的不锈钢用pbs缓冲液(10mm,ph=7.4)清洗3次,紧接着用水清洗3次,清洗完毕用n2吹干。
实施例11
三多巴胺端基三聚n-异丙基丙烯酰胺尾链的聚合物(dopa3-pnipam100)对聚偏氟乙烯膜表面的改性:上述清洗后的聚偏氟乙烯膜浸入2mg/ml的dopa3-pnipam100的tris缓冲溶液(浓度10mm,ph=8.5)中,再放入25℃的恒温振荡器中培养12h。培养后的不锈钢用pbs缓冲液(10mm,ph=7.4)清洗3次,紧接着用水清洗3次,清洗完毕用n2吹干。
实施例12
三多巴胺端基三聚磺基甜菜碱尾链的聚合物(dopa3-psbma)改性硅片表面的抗蛋白性能评价:
利用激光共聚焦显微镜(lscm)测试异硫氰酸荧光素标记牛血清白蛋白(fitc-bsa)的吸附情况:将上述样品板放入24孔细胞培养板中,在样品孔中分别加入0.5ml的fitc-bsa/pbs溶液(浓度为0.25mg/ml),用铝箔纸包裹孔板以避光,然后将24孔细胞培养板放在37℃恒温振荡器中缓慢振荡培养2h。培养结束后,用pbs缓冲液样品清洗五次(每次1ml的pbs,每次清洗5min),再用水清洗一次,最后用n2吹干。处理后的样片用激光共聚焦显微镜(lscm)在激发光为488nm和发射光为520nm的波长下,检测fitc-bsa在基板表面的吸附情况。
实施例13
三多巴胺端基三聚磺基甜菜碱尾链的聚合物(dopa3-psbma70)改性硅片表面的长期稳定性评价:
将改性后的基板放入24孔细胞培养板中,然后在每个样品孔中分别加入2ml的pbs缓冲溶液(浓度10mm,ph=7.4),室温条件下放置30天后,取出样片于新的24孔细胞培养板中,再向相应样品孔板中加入0.5ml的异硫氰酸荧光素标记牛血清白蛋白的磷酸盐(fitc-bsa/pbs)溶液(浓度为0.25mg/ml),用铝箔纸将孔板包裹避光,并放在37℃恒温振荡器中缓慢振荡培养2h。培养结束后,用pbs缓冲液样品清洗五次(每次1ml的pbs,每次清洗5min),再用水清洗一次,最后用n2吹干。处理后的样片用激光共聚焦显微镜(lscm)在激发光为488nm和发射光为520nm的波长下,检测fitc-bsa在基板表面的吸附情况。
- 还没有人留言评论。精彩留言会获得点赞!