OLED中间体2-溴芘的合成法的制作方法
本发明涉及有机物合成方法,尤其涉及一种高纯度的oled中间体2-溴芘的合成及精制方法。
背景技术:
2-溴芘是oled材料行业重要的中间体,其应用比较广泛,由于其合成方法和提纯方法比较复杂,所以市面上的高纯度的2-溴芘价格都比较昂贵。
现有技术通常采用芘氢化、溴化、芳构化三步反应合成2-溴芘:
该方法存在每步反应所得产物的收率非常低(收率≤20%)的问题,很难获取2-溴芘纯品,且成本高,不利于工业化生产。
技术实现要素:
本发明要解决的技术问题是提供一种易于操作的高纯度oled中间体2-溴芘的合成法,采用本发明的方法,能获得纯度≥99.5%的2-溴芘。
为解决上述技术问题,本发明提出一种oled中间体2-溴芘的合成法,包括以下步骤:
1)、2-溴芘粗品的合成:
于浓度为1.5~2g/10ml的硫酸溶液中加入1-氨基-2-溴芘,搅拌(搅拌时间约为30±5分钟)直至1-氨基-2-溴芘完全溶解;将所得溶液降温至0~5℃后(此时会有固体析出),滴加亚硝酸钠水溶液(滴加过程中控制体系温度不超过5℃),滴加完毕后(此时反应体系变澄清),于0~5℃保温搅拌30±5分钟,获得重氮盐溶液;
所述1-氨基-2-溴芘:硫酸(h2so4)=1:1.25~2的摩尔比;
所述1-氨基-2-溴芘:亚硝酸钠=1:1~1.5的摩尔比;
将重氮盐溶液滴加到降温至0~5℃的次亚磷酸水溶液中(约1小时滴完),于0~5℃反应30±5min(从而实现充分反应),过滤,干燥所得滤饼,得到2-溴芘粗品;
所述1-氨基-2-溴芘:次亚磷酸=1:3.5~4.5(最佳为1:4)摩尔比;
2)、2-溴芘的精制:
在步骤1)所得2-溴芘粗品中加入1.5~2.5质量倍的乙酸乙酯,升温至回流,再降温至20±2℃从而实现结晶,将所得的结晶干燥(80℃干燥至恒重),即得到2-溴芘纯品(纯度≥99.5%)。
作为本发明oled中间体2-溴芘的合成法的改进:
所述亚硝酸钠水溶液的浓度为2~4g/10ml。
作为本发明oled中间体2-溴芘的合成法的改进:
所述次亚磷酸水溶液的浓度为2~3.5g/10ml。
作为本发明oled中间体2-溴芘的合成法的改进:
所述1-氨基-2-溴芘的制备方法为包括以下步骤:
①、在1-氨基芘中加入作为溶剂的dmf(n,n-二甲基甲酰胺),均匀搅拌后(搅拌时间为5~15分钟),降温至0~5℃,再加入溴化试剂(分批加入溴化试剂,从而确保体系温度不超过5℃),然后于0~5℃保温反应30±5min(从而实现充分反应);
所述1-氨基芘:溴化试剂中的溴原子=1:0.8~1.2(最佳为1:1)的摩尔比
注:可采用hplc监控上述溴化反应;
②、向步骤①所得物中加入水,此时析出固体,将所析出的固体干燥(60℃干燥至恒重),得1-氨基-2-溴芘(黄色的固体)。
作为本发明oled中间体2-溴芘的合成法的改进:
所述步骤①,每1mol的1-氨基芘配用1000±200ml的dmf;
所述步骤②,水的体积用量为步骤①中dmf体积用量的0.8~1.2体积倍。
作为本发明oled中间体2-溴芘的合成法的改进:
所述步骤①中,溴化试剂为溴素、nbs或二溴海因。
在本发明中,首先采用价格较低的1-氨基芘为反应原料,溴化获得1-氨基-2-溴芘;选用溴化试剂为:溴素,nbs(n-溴代琥珀酰亚胺),二溴海因等。其反应方程式为:
之后采用1-氨基-2-溴芘为原料,采用重氮化脱氨法,获取2-溴芘粗品,其反应方程如下:
上述重氮化脱氨法的具体步骤如下:
首先令1-氨基-2-溴芘和亚硝酸钠在酸性体系中形成重氮盐,然后用次亚磷酸还原该重氮盐,即可得到2-溴芘粗品,该2-溴芘粗品用乙酸乙酯重结晶后获得纯度高的2-溴芘成品。
针对现有技术,本发明的技术优势是:
1、本发明利用1-氨基-2-溴芘制备2-溴芘,收率高(收率≥80%),另外其精制方法可以得到高纯度(纯度≥99.5%)的2-溴芘。
2、本发明利用1-氨基芘和溴化试剂反应制备1-氨基-2-溴芘,副产物少,收率高(收率≥95%),易于操作,同时对环境的污染少,节约了企业的生产成本。
附图说明
下面结合附图对本发明的具体实施方式作进一步详细说明。
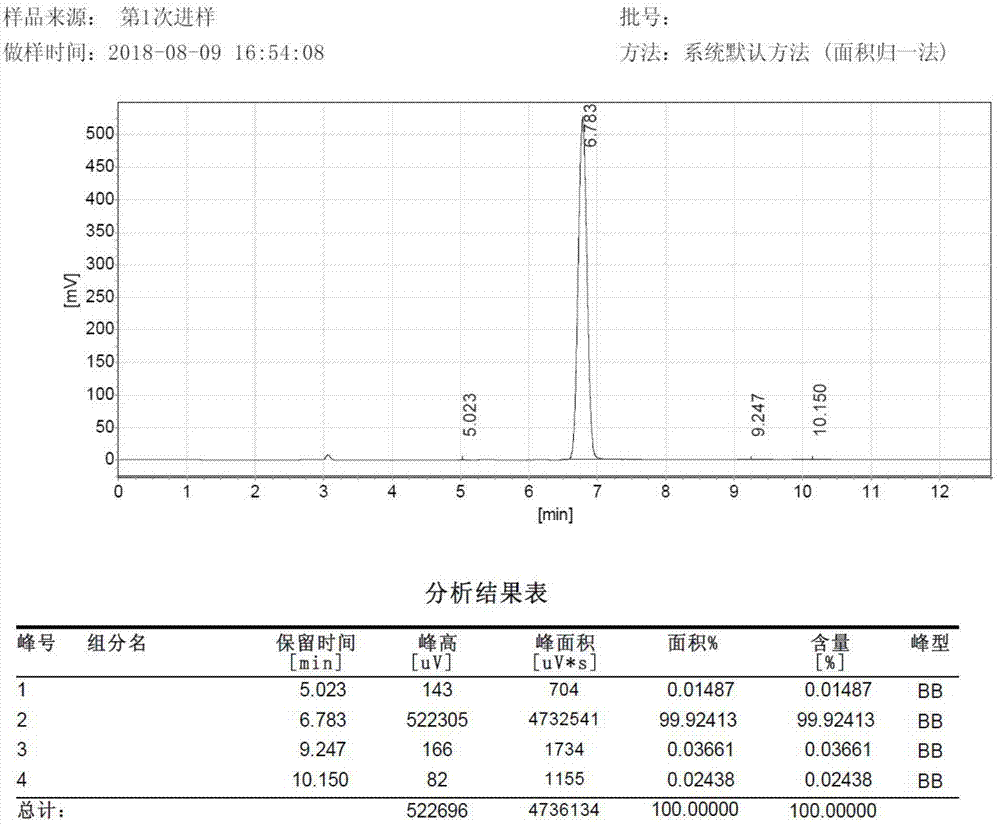
图1为实施例4制备的高纯度的2-溴芘的hplc图谱(highperformanceliquidchromatography,高效液相色谱法,又称“高压液相色谱”)示意图。
具体实施方式
下面结合具体实施例对本发明进行进一步描述,但本发明的保护范围并不仅限于此:
实施例1、1-氨基-2-溴芘的合成(采用1-氨基芘和二溴海因在溶剂中反应合成1-氨基-2-溴芘),依次进行以下步骤:
1.1、在2000ml反应瓶中加入217g1-氨基芘(1mol)和dmf(n,n-二甲基甲酰胺)1000ml,搅拌5分钟,降温至0-5℃,再分次加入(分5次,在60分钟内完成加入)142.8g二溴海因(0.5mol),使用水浴控制反应瓶内液体的温度控制在不超过5℃,加完后于5℃进行保温反应约30分钟,采用hplc监控,此时已反应结束。
1.2、向反应瓶内的液体中加入1000ml水,此时会有大量固体析出,搅拌至不再析出固体后(约5分钟后)后过滤、所得滤饼干燥(于60℃干燥至恒重),得到黄色的固体1-氨基-2-溴芘283g。收率:95.5%。
实施例2、1-氨基-2-溴芘的合成(采用1-氨基芘和nbs在溶剂中反应合成1-氨基-2-溴芘):
将实施例1步骤1.1中的二溴海因142.8g改为nbs178g(1mol),其他不变;其余等同于实施例1;最终得到黄色的固体1-氨基-2-溴芘282g。收率95.27%。
实施例3、1-氨基-2-溴芘的合成(采用1-氨基芘和溴素在溶剂中反应合成1-氨基-2-溴芘):
将实施例1步骤1.1中的二溴海因142.8g改为溴素80g(0.5mol),其他不变;其余等同于实施例1;最终得到黄色的固体1-氨基-2-溴芘284g。收率95.9%。
实施例4、2-溴芘的合成,依次进行以下步骤:
1)、2-溴芘合成:
1.1)、在1000ml反应瓶中加入硫酸溶液(含硫酸1mol),再加入148g1-氨基-2-溴芘(0.5mol,实施例1制备所得),搅拌30分钟使其全部溶解,将溶液降温至0-5℃,此时会有固体析出,随后滴加(滴加过程中控制体系温度不超过5℃)亚硝酸钠水溶液(含亚硝酸钠0.5mol),控制反应温度在0-5℃,滴完后,反应体系会变澄清,控制温度于0-5℃搅拌30分钟,获得重氮盐溶液备用。
本实施例采用浓度为2g/10ml的硫酸溶液(含硫酸1mol),浓度为3.5g/10ml的亚硝酸钠水溶液(含亚硝酸钠0.5mol)。
即,1-氨基-2-溴芘:硫酸(h2so4)=1:2的摩尔比;
1-氨基-2-溴芘:亚硝酸钠=1:1的摩尔比。
注:上述重氮化反应中,硫酸和亚硝酸钠反应,生成亚硝酸,亚硝酸与1-氨基-2-溴芘中的nh2反应,生成重氮盐。
1.2)、将步骤1.1)制备所得的重氮盐溶液缓慢滴加到机械搅拌下降温至0-5℃的次亚磷酸水溶液中(约1小时滴完),滴加过程中会有大量的气体放出。滴加完成后于0-5℃进行保温反应约30分钟,采用hplc监控,此时已反应结束;过滤,干燥所得滤饼(于60℃干燥至恒重),得到2-溴芘粗品130g。
本实施例中采用浓度为2.5g/10ml的次亚磷酸水溶液(含次亚磷酸2mol);
即,1-氨基-2-溴芘:次亚磷酸=1:4摩尔比。
2)、2-溴芘精制:将步骤1)所得130g的2-溴芘粗品,加入到500ml三口瓶中,再加入2倍重量的乙酸乙酯,升温至回流,再降温至20±2℃从而实现结晶,最后将混合液过滤、所得结晶体干燥(80℃干燥至恒重),即得到2-溴芘纯品(纯度99.9%),重量115g,收率88.5%,其hplc图谱如图1所示。
对比例1、将实施例4步骤1.1)中所采用的“硫酸溶液”改成“盐酸溶液”,盐酸溶液的浓度3.6g/10ml,酸的有效摩尔量保持不变,即为2mol。其余等同于实施例4。
得到2-溴芘(纯度55.7%),收率32%。
注:盐酸溶液无法将1-氨基-2-溴芘充分溶解,故所得2-溴芘的纯度与收率远不如本发明。
最后,还需要注意的是,以上列举的仅是本发明的若干个具体实施例。显然,本发明不限于以上实施例,还可以有许多变形。本领域的技术人员能从本发明公开的内容直接导出或联想到的所有变形,均应认为是本发明的保护范围。
- 还没有人留言评论。精彩留言会获得点赞!
- 一种丙辛吲哚盐酸盐药物中间体丙辛吲哚的合成方法与制造工艺
- 一种吲哚洛尔药物中间体(一)‑4‑(2‑羟基‑3‑异丙氨基丙氧)吲哚的合成方法与制造工艺
- 依替米贝的中间体及其合成方法与依替米贝的合成方法与制造工艺
- 一种白消安药物中间体1,4‑双甲基磺酸丁二酯的合成方法与制造工艺
- 一种塞利洛尔药物中间体3‑(4‑乙氧基苯基)‑1,1‑二乙基脲的合成方法与制造工艺
- 一种羟基保泰松药物中间体4‑羟基偶氮苯的合成方法与制造工艺
- 一种甲氧卡那霉素药物中间体γ‑氨基‑α‑羟基丁酸的合成方法与制造工艺
- 一种非那西丁药物中间体对硝基苯乙醚的合成方法与制造工艺
- 一种间尼索地平药物中间体乙酰乙酸异丁酯的合成方法与制造工艺
- 一种甲氧苄啶药物中间体3,4,5—三甲氧基苯甲酸甲酯的合成方法与制造工艺