一种新型小分子芳香性化合物salaciacochineA及其制备方法和应用与流程
本发明属于植物有效成分提取技术领域,具体涉及一种新型小分子芳香性化合物salaciacochinea及其制备方法和应用。
背景技术
五层龙属植物中柳叶五层龙茎叶的乙醇提取物具有较好的α-葡萄糖苷酶抑制活性。柳叶五层龙(salaciacochinchinensislour)为灌木,高达2米,主要产于云南西双版纳,越南、柬埔寨也有分布。该属植物的化学成分主要包括木栓烷型三萜、降碳醌甲基型五环三萜、羽扇豆烷型五环三萜、齐墩果烷型五环三萜等三萜类化合物和四环三萜、降倍半萜、黄酮以及锍盐等类型的化合物。生物活性研究显示其中的部分化合物有细胞保护作用及α-葡萄糖苷酶抑制等活性。
迄今为止未见关于柳叶五层龙的化学成分报道,为了从中寻找高效低毒的降糖活性成分,目前,缺乏一种活性好的新型小分子芳香性化合物salaciacochinea及其制备方法和应用。
技术实现要素:
本发明的第一目的是提供一种活性好的新型小分子芳香性化合物salaciacochinea;第二目的在于提供所述的新型小分子芳香性化合物salaciacochinea的制备方法;第三目的在于提供所述新型小分子芳香性化合物salaciacochinea在制备α-葡萄糖苷酶抑制剂类降糖药物中的应用。
为了解决现有技术的问题,本发明提出了如下技术方案:本发明的一种新型小分子芳香性化合物salaciacochinea,所述的新型小分子芳香性化合物的结构式如式(i)所示:
进一步地,所述的新型小分子芳香性化合物的分子式为c14h22o8,该化合物命名为salaciacochinea。
本发明的一种所述的新型小分子芳香性化合物salaciacochinea的制备方法,包括如下步骤:所述的新型小分子芳香性化合物salaciacochinea以干燥的五层龙属植物全草为原料,经粉碎提取、有机溶剂萃取、硅胶柱层析、hplc分离获得,具体步骤为:
a、粉碎提取:将干燥的五层龙属植物茎叶粗粉碎到20~40目,用有机溶剂在85~90℃下回流提取2~4次,每次30~60分钟,提取液合并;提取液过滤,减压浓缩提取液至1/4~1/2体积时,静置,滤除沉淀物,浓缩成浸膏a;
b、有机溶剂萃取:浸膏a中加入重量比1~2倍量的水,用与水等体积的有机溶剂萃取3~5次,合并有机溶剂萃取相,减压浓缩成浸膏b;
c、硅胶柱层析:将浸膏b用重量比1.5~3倍量的甲醇溶解,然后用浸膏重0.8~1.2倍的80~100目硅胶拌样,然后上硅胶柱层析,装柱硅胶为160~200目,用量为浸膏b重量6~8倍量;用体积比为1:0~0:1的混合有机溶剂梯度洗脱,收集梯度洗脱液、浓缩,经tlc检测,合并相同的部分;
d、反相柱层析:将以9:1配比的有机溶剂进行洗脱得到的洗脱液上反相柱层析,反相柱是用反相材料c-18装柱;用体积含量为20~100%的甲醇水溶液进行梯度洗脱,收集各部分洗脱液并浓缩,经tlc检测,合并相同的部分;
e、hplc分离:将d步骤中以体积含量30~50%甲醇水溶液洗脱得到的洗脱液经高效液相色谱hplc分离纯化,制得所述的新型小分子芳香性化合物;
f、e步骤所述的高效液相色谱分离纯化是以18%的甲醇为流动相,流速2~3ml/min,10×250mm(5μm)的agilentzorbaxc18制备色谱柱为固定相,紫外检测器检测波长为254nm,每次进样50~100μl,收集8.5~10.5min的色谱峰,多次累加后蒸干,制得所述的新型小分子芳香性化合物salaciacochinea。
进一步地,在a步骤中,所述的有机溶剂为70~90%的乙醇或70~90%甲醇。
进一步地,在b步骤中,所述的有机溶剂为乙酸乙酯或正丁醇。
更进一步地,在c步骤中,所述的混合有机溶剂为氯仿-甲醇或乙酸乙酯-甲醇。
进一步地,在c步骤中,所述的混合有机溶剂的体积配比为1:0、20:1、9:1、8:2、3:2、1:1。
本发明的一种新型小分子芳香性化合物salaciacochinea在制备α-葡萄糖苷酶抑制剂类降糖药物制剂中的应用。
本发明新型小分子芳香性化合物salaciacochinea是首次被分离出来的,通过核磁共振、质谱及高分辨质谱等确定其结构,并表征其具体结构为:
该化合物为小分子芳香性成分化合物中,较为少见的含有丙三醇部分结构。
本发明在生物活性指导下对前期筛选有良好α-葡萄糖苷酶抑制作用的s.cochinchinensis进行了活性成分研究,从中分离得到一个新型小分子芳香性化合物salaciacochinea,该化合物具有显著的α-葡萄糖苷酶抑制活性,可作为α-葡萄糖苷酶抑制剂类降糖药物的先导化合物。
有益效果:本发明的新型小分子芳香性化合物salaciacochinea能通过本发明的方法分离出来。以salaciacochinea为原料,阿卡波糖为阳性对照,经α-葡萄糖苷酶抑制活性筛选实验,结果显示salaciacochinea抑制α-葡萄糖苷酶活性显著,ic50值为0.59μm。本发明化合物为不常见的分子内含有丙三醇结构片段的小分子芳香性成分,且活性好,可作为α-葡萄糖苷酶抑制剂类降糖药物的先导性化合物,有良好的应用前景。
附图说明
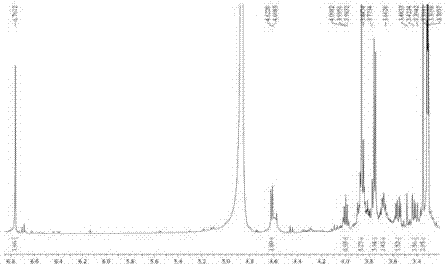
图1为本发明的化合物salaciacochinea的核磁共振氢谱(1hnmr);
图2为本发明的化合物salaciacochinea的核磁共振碳谱(13cnmr);
图3为本发明的化合物salaciacochinea的高分辨质谱。
具体实施方式
下面结合附图对本发明作进一步的说明,但不以任何方式对本发明加以限制,基于本发明教导所作的任何变换或改进,均落入本发明的保护范围。
本发明的一种新型小分子芳香性化合物salaciacochinea,所述的新型小分子芳香性化合物的结构式如式(i)所示:
所述的新型小分子芳香性化合物的分子式为c14h22o8,该化合物命名为salaciacochinea。
本发明的一种所述的新型小分子芳香性化合物salaciacochinea的制备方法,包括如下步骤:所述的新型小分子芳香性化合物salaciacochinea以干燥的五层龙属植物全草为原料,经粉碎提取、有机溶剂萃取、硅胶柱层析、hplc分离获得,具体步骤为:
a、粉碎提取:将干燥的五层龙属植物茎叶粗粉碎到20~40目,用有机溶剂在85~90℃下回流提取2~4次,每次30~60分钟,提取液合并;提取液过滤,减压浓缩提取液至1/4~1/2体积时,静置,滤除沉淀物,浓缩成浸膏a;所述的有机溶剂为70~90%的乙醇或70~90%甲醇。
b、有机溶剂萃取:浸膏a中加入重量比1~2倍量的水,用与水等体积的有机溶剂萃取3~5次,合并有机溶剂萃取相,减压浓缩成浸膏b;所述的有机溶剂为乙酸乙酯或正丁醇。
c、硅胶柱层析:将浸膏b用重量比1.5~3倍量的甲醇溶解,然后用浸膏重0.8~1.2倍的80~100目硅胶拌样,然后上硅胶柱层析,装柱硅胶为160~200目,用量为浸膏b重量6~8倍量;用体积比为1:0~0:1的混合有机溶剂梯度洗脱,收集梯度洗脱液、浓缩,经tlc检测,合并相同的部分;所述的混合有机溶剂为氯仿-甲醇或乙酸乙酯-甲醇。所述的混合有机溶剂的体积配比为1:0、20:1、9:1、8:2、3:2、1:1。
d、反相柱层析:将以9:1配比的有机溶剂进行洗脱得到的洗脱液上反相柱层析,反相柱是用反相材料c-18装柱;用体积含量为20~100%的甲醇水溶液进行梯度洗脱,收集各部分洗脱液并浓缩,经tlc检测,合并相同的部分;
e、hplc分离:将d步骤中以体积含量30~50%甲醇水溶液洗脱得到的洗脱液经高效液相色谱hplc分离纯化,制得所述的新型小分子芳香性化合物;
f、e步骤所述的高效液相色谱分离纯化是以18%的甲醇为流动相,流速2~3ml/min,10×250mm(5μm)的agilentzorbaxc18制备色谱柱为固定相,紫外检测器检测波长为254nm,每次进样50~100μl,收集8.5~10.5min的色谱峰,多次累加后蒸干,制得所述的新型小分子芳香性化合物salaciacochinea。
本发明的一种新型小分子芳香性化合物salaciacochinea在制备α-葡萄糖苷酶抑制剂类降糖药物制剂中的应用。
本发明新型小分子芳香性化合物salaciacochinea是首次被分离出来的,通过核磁共振、质谱及高分辨质谱等确定其结构,并表征其具体结构为:
本发明所述的五层龙属植物不受地区和品种限制,均可以实现本发明。
实施例1
取干燥的五层龙属植物茎叶10.0kg,粗粉碎至40目,用90%的乙醇在85-90℃下回流提取4次,每次60min,提取液合并;提取液过滤,减压浓缩至体积的1/4;静置,滤除沉淀物,浓缩成1780g浸膏a;在浸膏a中加入1780g水,用与水等体积的正丁醇萃取4次,合并萃取相,减压浓缩成250g浸膏b;用7倍量200目硅胶(1750g)装柱,在浸膏b中加入2倍量的甲醇(500g)溶解,然后加入1.2倍量90目硅胶(300g)拌样,室温挥干后上柱;用体积比分别为1:0、20:1、9:1、8:2、3:2、1:1的氯仿-甲醇混合有机溶剂梯度洗脱,收集梯度洗脱液、浓缩,经tlc监测,合并相同的部分,得到6个部分,体积比9:1的氯仿-甲醇混合有机溶剂的洗脱液c为13.6g;用反相材料c-18装柱,洗脱液c部分13.6g上反相柱,以体积含量为20~100%的甲醇水溶液进行梯度洗脱,收集各部分洗脱液并浓缩,经tlc监测,合并相同的部分;取以体积含量30~50%甲醇水溶液洗脱得到的洗脱液,再以10%的甲醇为流动相,流速2ml/min,10×250mm(5μm)的agilentzorbaxc18制备色谱柱为固定相,紫外检测器检测波长为254nm,每次进样50μl,收集10.5min的色谱峰,多次累加后蒸干,即得所述的新型小分子芳香性化合物salaciacochinea。
实施例2
取干燥的五层龙属植物茎叶8kg,粗粉碎至20目,用70%的乙醇在85-90℃下回流提取2次,每次50min,提取液合并;提取液过滤,减压浓缩至体积的1/3;静置,滤除沉淀物,浓缩成1420g浸膏a;在浸膏a中加入1420g的水,用与水等体积的正丁醇萃取3次,合并萃取相,减压浓缩成200g浸膏b;用8倍量160目硅胶(1600g)装柱,在浸膏b中加入3倍量的甲醇(600g)溶解,然后加入0.8倍量80目硅胶160g拌样,室温挥干后上柱;用体积比分别为1:0、20:1、9:1、8:2、3:2、1:1的乙酸乙酯-甲醇混合有机溶剂梯度洗脱,收集梯度洗脱液、浓缩,经tlc监测,合并相同的部分;体积比9:1的乙酸乙酯-甲醇混合有机溶剂的洗脱液c为10.5g;用反相材料c-18装柱,洗脱液c部分上反相柱,以体积含量为20~100%的甲醇水溶液进行梯度洗脱,收集各部分洗脱液并浓缩,经tlc监测,合并相同的部分;取以体积含量30~50%甲醇水溶液洗脱得到的洗脱液,再以18%的甲醇为流动相,流速2ml/min,10×250mm(5μm)的agilentzorbaxc18制备色谱柱为固定相,紫外检测器检测波长为254nm,每次进样70μl,收集10.5min的色谱峰,多次累加后蒸干得新型小分子芳香性化合物salaciacochinea。
实施例3
取干燥的五层龙属植物茎叶6kg,粗粉碎至30目,用70%的甲醇在85-90℃下回流提取3次,每次30min,提取液合并;提取液过滤,减压浓缩至体积的1/2;静置,滤除沉淀物,浓缩成1068g浸膏a;在浸膏a中加入2倍量的水(2136g),用与水等体积的正丁醇萃取4次,合并萃取相,减压浓缩成150g260g浸膏b;用8倍量200目硅胶1200g装柱,在浸膏b中加入2倍量的甲醇(300g)溶解,然后加入100目硅胶150g拌样,室温挥干后上柱;用体积比分别为1:0、20:1、9:1、8:2、3:2、1:1的氯仿-甲醇混合有机溶剂梯度洗脱,收集梯度洗脱液、浓缩,经tlc监测,合并相同的部分;体积比9:1的乙酸乙酯-甲醇混合有机溶剂的洗脱液c为8.2g。用反相材料c-18装柱,洗脱液c部分上反相柱,以体积含量为20~100%的甲醇水溶液进行梯度洗脱,收集各部分洗脱液并浓缩,经tlc监测,合并相同的部分;取以体积含量30~50%的甲醇-水溶液洗脱得到的洗脱液,再以18%的甲醇为流动相,流速2ml/min,10×250mm(5μm)的agilentzorbaxc18制备色谱柱为固定相,紫外检测器检测波长为254nm,每次进样80μl,收集10.0min的色谱峰,多次累加后蒸干即得新型小分子芳香性化合物salaciacochinea。
实施例4
取干燥的五层龙属植物茎叶5kg,粗粉碎至20目,用90%的甲醇在85-90℃下回流提取4次,每次35min,提取液合并;提取液过滤,减压浓缩至体积的1/2;静置,滤除沉淀物,浓缩成880g浸膏a;在浸膏a中加入2倍量的水1600g,用与水等体积的正丁醇萃取5次,合并萃取相,减压浓缩成130g浸膏b;用7倍量200目硅胶910g装柱,在浸膏b中加入3倍量的甲醇390g溶解,然后加入0.8倍量100目硅胶104g拌样,室温挥干后上柱;用体积比分别为1:0、20:1、10:1、8:2、3:2、1:1的氯仿-甲醇混合有机溶剂梯度洗脱,收集梯度洗脱液、浓缩,经tlc监测,合并相同的部分;体积比9:1的氯仿-甲醇混合有机溶剂的洗脱液c为7.2g。用反相材料c-18装柱,洗脱液c部分上反相柱,以体积含量为20~100%的甲醇水溶液进行梯度洗脱,收集各部分洗脱液并浓缩,经tlc监测,合并相同的部分;取以体积含量30~50%甲醇水溶液洗脱得到的洗脱液,再以18%的甲醇为流动相,流速3ml/min,10×250mm(5μm)的agilentzorbaxc18制备色谱柱为固定相,紫外检测器检测波长为254nm,每次进样100μl,收集8.5min的色谱峰,多次累加后蒸干得新型小分子芳香性化合物salaciacochinea。
实施例5
取实施例1制备的化合物salaciacochinea,为白色无定型粉末;测定方法为:用核磁共振,结合其它波谱技术鉴定结构。
(1)紫外光谱(溶剂为甲醇),λmax(logε):258(2.20)nm;
(2)红外光谱(溴化钾压片)νmax3446,1598,1502,1446,1158cm–1;
(3)esi-ms(+):m/z341[m+na]+.hresims(+)显示本发明化合物准分子离子峰m/z341.1207[m+na]+(c14h22o8na+,计算值为341.1212)。1hnmr(cdcl3,400mhz)和13cnmr(cdcl3,100mhz)数据,见表1。化合物salaciacochinea的1h(400mhz)和13cnmr(100mhz)数据(溶剂为cdcl3),化学位移δ(ppm),偶合常数j(hz)如表1所示:
表1
实施例6
取实施例2制备的化合物salaciacochinea分别按实施例5中的方法进行结构测定,结果为:其结构同实施例5,分子式为c14h22o8。
实施例7
取实施例3制备的化合物salaciacochinea分别按实施例5中的方法进行结构测定,结果为:其结构同实施例5,分子式为c14h22o8。。
实施例8
取实施例4制备的化合物salaciacochinea分别按实施例5中的方法进行结构测定,结果为:其结构同实施例5,分子式为c14h22o8。
试验1
取实施例1~4所制备的任一salaciacochinea进行α-葡萄糖苷酶抑制活性检测试验,试验情况如下:
1、α-葡萄糖苷酶抑制活性实验
α-葡萄糖苷酶抑制剂是一类以延缓肠道碳水化合物吸收而达到治疗糖尿病的口服降糖药物。作用机制:竞争性抑制位于小肠的各种α-葡萄糖苷酶,使淀粉类分解为葡萄糖的速度减慢,从而减缓肠道内葡萄糖的吸收,降低餐后高血糖。
α-葡萄糖苷酶抑制活性筛选的原理:对-硝基苯酚-α-d-葡萄糖苷(pnpg)作反应底物;该底物是无色的。经α-葡萄糖苷酶水解后可以释放出对-硝基苯酚(pnp),pnp在碱性条件下是黄色的,其在405nm处有最大吸收,因此可以通过测定405nm处的吸光度反应出pnp的浓度(吸光度与pnp浓度成正比关系)。吸光度越小,说明pnp的浓度越小,即酶被抑制的程度越大。
1.1实验试剂
α-glucosidase(α-葡萄糖苷酶)、4-硝基苯-α-d-吡喃葡萄糖苷(4-nitrphtnylα-d-glucopyranoside,pnpg)、阿卡波糖(acarbose)购自sigma,试剂无水na2co3、kh2po4,na2hpo4为分析纯,水为实验室自制超纯水。实验样品salaciacochinosidea为自制。
1.1.1试剂配制
(1)ph值6.8的0.1mol/l磷酸缓冲液
分别配制0.1mol/lna2hpo4和kh2po4(13.6g配成1l),用这两种溶液混匀互调ph值至6.8即得0.1mol/l磷酸缓冲液
(2)用ph值6.8的0.1mol/l磷酸缓冲液配制0.26u/ml的α-glucosidase
(3)底物(pnpg)用ph值6.8的0.1mol/l磷酸缓冲液配制成浓度为5mmol/l(1.505mg/ml)
(4)反应终止液:0.2mol/lna2co3。
(5)阳性药的配制:精密称取阿波卡糖样品,以磷酸缓冲液为溶剂溶解,配成10mg/ml的浓度。
1.1.2实验方法
(1)各浓度药液按每孔50μl加入酶标板,每浓度设三复孔。另设一药物对照孔、空白反应孔及空白对照孔。然后向药物反应孔和空白反应孔加入50μl0.26u/ml的-葡萄糖苷酶,其他组加50μl磷酸缓冲液,经此步骤后,各孔的组成为:
药物反应孔:50μl药液+50μl酶
药物对照孔:50μl药液+50μl磷酸缓冲液
空白反应孔:50μl磷酸缓冲液+50μl酶
空白对照孔:50μl磷酸缓冲液+50μl磷酸缓冲液
上述反应体系在微型振荡器上震荡30秒,置于恒温37℃水浴中孵育10min。
(2)每孔加100μl底物(5mmol/l的pnpg,15mg配成10ml)后,在微型振荡器上震荡30s,在恒温水浴锅中37℃孵育20min。
(3)每孔加入100μl0.2mol/lna2co3终止反应(1.06g配成50ml)。在酶标仪405nm处测定od值。
(4)计算公式:抑制率(%)=[1-(药物反应孔od值-药物对照孔od值)/(空白反应od值-空白对照od值)]×100
每个样品活性测试三次,活性结果去平均值,并计算相对标准偏差。通过相对标准偏差来反应实验的重复性和精密度,偏差越小,说明实验重复性和精确度越好。
2.实验结果
salaciacochinea降糖活性的实验结果如表2所示:
表2
本实验采用目前糖尿病治疗一线用药阿卡波糖(acarbose)为阳性对照,实验结果为3次独立试验的平均值。研究结果显示:salaciacochinea对α-葡萄糖苷酶有显著抑制作用,其ic50值为0.59μm,阳性对照阿卡波糖(acarbose)对α-葡萄糖苷酶的抑制活性ic50值为0.13μm,表明本发明所述的化合物salaciacochinea抑制α-葡萄糖苷酶活性与一线用药阿卡波糖(acarbose)相当,是具有较好的抑制α-葡萄糖苷酶活性天然小分子,因此可以作为潜在的治疗糖尿病活性先导化合物。
以上显示和描述了本发明的基本原理、主要特征和本发明的优点。本行业的技术人员应该了解,本发明不受上述实施例的限制,上述实施例和说明书中描述的只是说明本发明的原理,在不脱离本发明精神和范围的前提下,本发明还会有各种变化和改进,本发明要求保护范围由所附的权利要求书、说明书及其等效物界定。
- 还没有人留言评论。精彩留言会获得点赞!