一种DNA片段分选\文库纯化用的磁珠及其分选方法与流程
本发明属于基因测序领域,具体涉及一种dna片段分选\文库纯化用的磁珠及其分选方法。
背景技术:
现有技术当中,目前市面上分选磁珠种类多样,价格昂贵,市售分选磁珠的每400ml报价接近2万,而且批次的问题会导致同样的分选浓度片段分选范围会有些许差异。
对于企业来说,磁珠过高的价格会导致企业生产成本的增加,因此继续一种更为便宜的分选、纯化手动来节约成本。
技术实现要素:
为了克服现有技术存在的上述缺陷,本发明的目的之一在于提供一种dna片段分选\文库纯化用的磁珠,能够以更便宜的方法来进行dna片段的分选,比如片段范围在100bp到1000bp;用本发明的方法可以将片段范围控制在460bp左右。另外一种是多样性建库过程中,扩增产物中会存在引物二聚体,用本发明的方法能够去掉引物二聚体并纯化多样性文库。
本发明的目的之二在于一种dna片段分选\文库纯化用的磁珠分选方法。
为了实现本发明的目的之一,所采用的技术方案是:
一种dna片段分选\文库纯化用的磁珠,所述的分选磁珠,按重量份计,包括如下组成部分:
孔径1μm的含羧基官能团的裸磁珠38-42份;
磁珠分选母液350-370份;
其中,所述的磁珠分选母液中包含浓度为190-210mg/mlpeg8000和浓度为3.3-3.5m/l的nacl。
其中,所述的磁珠为南京盘古有限公司g12311号裸磁珠。
为了实现本发明的目的之二,所采用的技术方案是:
一种dna片段分选\文库纯化用的磁珠分选方法,包括如下步骤:
1.使用所述的分选磁珠提取目标基因组dna;
2.将步骤(1)所得基因组dna随机片段化;
3.选取步骤(2)片段化dna90-100份加入pcr管,再加入所述的分选磁珠46-48份,用移液枪充分吹打混匀,室温放置3-8min;
4.将步骤(3)pcr管置于磁力架上,静置3-8min;
5.将步骤(4)pcr管中上清转移至新的pcr管中,并在此加入所述的分选磁珠11-13份,室温放置3-8min;
6.将步骤(4)pcr管置于磁力架上,静置3-8min;
7.将步骤(6)pcr管中上清弃掉,加入190-210份的75-85%浓度的乙醇,室温孵育25-35秒,弃掉废液;
8.重复步骤(7)一次,室温干燥3-5min;
9.在步骤(8)pcr管中加入30-34份10mmph8.0的tris-hc缓冲溶液,用移液枪充分吹打混匀,室温静置1-3min;转移29-31份洗脱后的dna到新的管中;
10.转移步骤(9)pcr管中29-31份洗脱后的dna到新的pcr管中;
11.对步骤(10)中29-31份的洗脱产物进行接头连接,pcr扩增,获得扩增后文库;
12.在步骤(11)pcr管中加入79-81份所述的分选磁珠,用移液枪充分吹打混匀,室温放置3-8min;
13.将步骤(12)pcr管置于磁力架上,静置3-8min;
14.将步骤(13)pcr管中上清弃掉,加入190-210份的75-85%浓度的乙醇,25-35秒,弃掉废液;
15.重复步骤(14)一次,室温干燥3-5min;
16.在步骤(15)pcr管中加入31-33份10mmph8.0tris-hc缓冲溶液,用移液枪充分吹打混匀,室温静置1-3min;转移29-31份洗脱后的dna到新的管中待上机。
本发明的有益效果在于:
大大节约了磁珠的使用成本,本发明所使用的分选用磁珠,每400ml报价约4-5千人民币。
附图说明
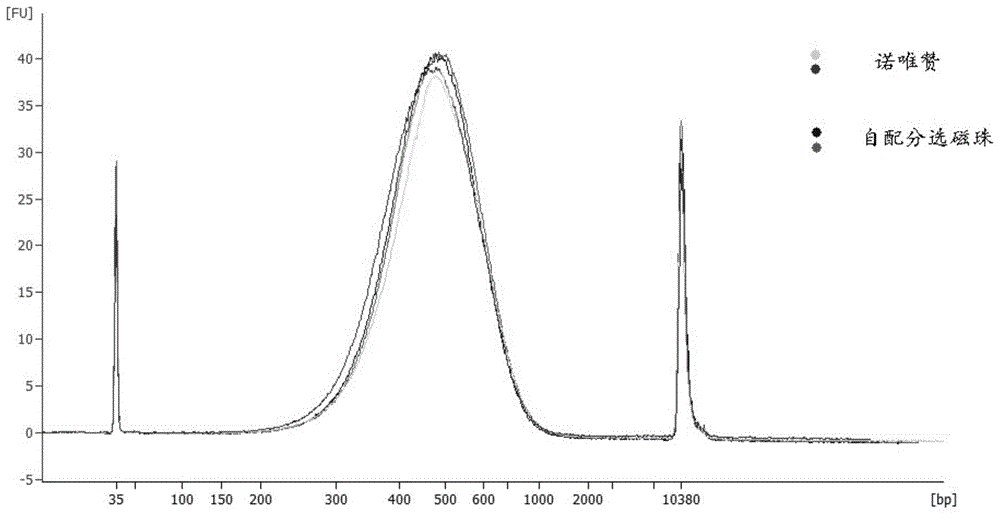
图1为诺唯赞和本发明的分选纯化磁珠片段分选检测结果示意图。
具体实施方式
以下通过实施例进一步对本发明进行说明:
实施例1
本发明的羧基磁珠选购于南京盘古有限公司:货号为g12311孔径1μm。(也可采购其他同类含羧基基团的磁珠)
磁珠分选母液配置:peg8000200mg/mlnacl3.5m/l
本发明解决的技术问题是针对二代测序文库构建过程中片段分选以及文库纯化过程中所用磁珠价格昂贵的缺陷。
为解决上述技术问题,本发明采取的技术方案之一为:采购廉价裸磁珠,配置适用于生产的自配dna分选纯化磁珠。所述方法包括下列步骤:
(1)磁珠分选母液配置:peg8000200mg/mlnacl3.4m/l;
(2)从南京盘古有限公司购置货号为g12311孔径1μm的含羧基官能团的裸磁珠;
(3)取步骤(1)中溶液360ml,步骤(2)中磁珠溶液40ml,混合,最终配置成‘自配分选纯化磁珠’;
(4)提取目标基因组dna;
(5)将步骤(4)所得基因组dna随机片段化;
(6)此步开始进行dna片段分选,选取步骤(5)片段化dna100μl加入pcr管,再加入步骤(3)‘自配分选纯化磁珠’48μl,用移液枪充分吹打混匀,室温放置5min;
(7)将步骤(6)pcr管置于磁力架上,静置5min;
(8)将步骤(7)pcr管中上清转移至新的pcr管中,并在此加入步骤(3)溶液12μl,室温放置5min;
(9)将步骤(8)pcr管置于磁力架上,静置5min;
(10)将步骤(9)pcr管中上清弃掉,加入200μl的80%乙醇,室温孵育30s,弃掉废液;
(11)重复步骤(10)一次,室温干燥3-5min;
(12)在步骤(11)pcr管中加入32μl10mmph8.0tris-hc冲溶液,用枪充分吹打混匀,室温静置2min;转移30μl洗脱后的dna到新的管中。
(13)转移步骤(12)pcr管中30μl洗脱后的dna到新的pcr管中;
(14)对步骤(13)中30μl洗脱产物进行接头连接,pcr扩增,获得扩增后文库。
(15)在步骤(14)pcr管中加入80μl步骤(3)‘自配分选纯化磁珠’,用移液枪充分吹打混匀,室温放置5min;
(16)将步骤(15)pcr管置于磁力架上,静置5min;
(17)将步骤(16)pcr管中上清弃掉,加入200μl的80%乙醇,室温孵育30s,弃掉废液;
(18)重复步骤(17)一次,室温干燥3-5min;
(19)在步骤(18)pcr管中加入32μl10mmph8.0tris-hc冲溶液,用枪充分吹打混匀,室温静置2min;转移30μl洗脱后的dna到新的管中。
步骤(14)中接头连接,pcr扩增可以参考目前常用的二代测序建库试剂盒。有illumina公司自产的,也有国内全式金,诺唯赞等公司开发的dna建库试剂盒。
步骤(4)为提取目标基因组dna。所述目标基因组dna提取的方法为常规提取方法。较佳地为利用各种市售试剂盒或其他常规技术提取目标基因组dna。所述目标基因组dna较佳地是动物基因组dna、植物基因组dna或微生物基因组dna;所述目标基因组dna包括具有参考基因组序列的基因组dna,或者不具有参考基因组序列的基因组dna。
步骤(4)中所述基因组是本领域常规概念,是指物种的基因组序列被全基因组测序。具有参考基因组序列的物种基因组dna是指该物种已经被全基因测序;不具有参考基因组序列的基因组dna是指该物种没有被全基因测序。
分选片段范围比较
为了评估所配分选磁珠片段分选能力以及分选片段范围,我们选取了目前市面上比较常用的诺唯赞分选纯化磁珠进行了比较,两种磁珠起始投入量为500ng,片段范围100bp~3000bp,按照诺唯赞分选纯化磁珠文库分选比例(55-15)与自配分选比例(48-12)进行比较,从结果中我们可以看出,两种试剂盒在分选片段大小以及浓度上上并无太大差异,也证明了我们的自配分选纯化磁珠在dna片段分选中的效果见图1。图1为诺唯赞和自配分选纯化磁珠片段分选检测结果。
扩增文库纯化后浓度比较
通过在50μl扩增文库中按照1:0.8的比列添加自配磁珠和诺唯赞分选纯化磁珠,发现两者在浓度变化上并无明显变化,并且文库浓度和产量完全符合二代测序上机,结果见表1,而诺唯赞的磁珠每400ml报价接近2万,本发明的分选磁珠成本才每400ml报价约4-5千人民币,且也能达到与价格高的市售产品一样的效果。
表1
- 还没有人留言评论。精彩留言会获得点赞!