外泌体miRNA在制备肝癌诊断产品中的应用的制作方法
本发明属于生物医学领域,涉及癌症的诊断产品,具体涉及一种外泌体mirna在制备肝癌诊断产品中的应用,所述外泌体mirna为血液外泌体mir-1283。
背景技术:
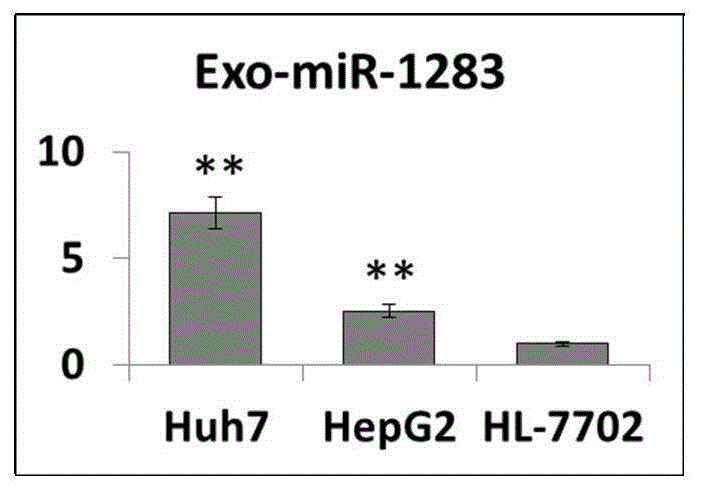
:肝癌是人类常见的恶性肿瘤之一,其死亡率一直高居不下,在所有肿瘤致死原因中位居第三。而主要原因是:第一,基数庞大,全球范围内每年新增50万~100万病例,约有70万人死于肝癌,其5年死亡率更是超过90%。而全球肝癌病例中有半数以上在中国,因此肝癌在我国具有高发性及高危性。肝癌病人治疗后的复发率高,据统计术后5年复发率高达60-70%。而其中侵袭性(浸润-转移)作为恶性肿瘤的主要特点之一,是导致肝癌复发转移甚至患者死亡的重要原因。若能在肿瘤未转移或仅微量转移时就具有有效的临床预警指标,则可为高转移风险患者的早期干预提供依据,进而改善其预后。我们在前期研究中证实pnc(perinucleolarcompartment)作为一种特殊的细胞核结构与肿瘤细胞的转移特性密切相关,因此可作为肿瘤转移预测和预后判断的有效指标。但是pnc作为一个细胞核内结构,其检测需依赖于组织活检。若能以外周血特定指标体现pnc比例,则可为肝癌患者转移风险的预警和预后评估提供有效且便捷的无创诊断标志物。近来,外泌体(exosome)在肿瘤临床诊断中的作用备受关注。exosome是由多种活细胞分泌的囊泡小体,其中含有蛋白质和rna等多种组分。这种机体内普遍存在的纳米级被膜结构能够参与细胞间的物质交换和信息交流,在多种生理和病理过程中发挥重要作用。外泌体在外周血、尿液、唾液、腹水、羊水等体液中具有很高的丰度,因而有望作为循环生物标志物而实现非侵入性的疾病诊断。技术实现要素:本发明的目的在于提供一种外泌体mirna在制备肝癌诊断产品中的应用,所述外泌体mirna为血液外泌体mir-1283,所述血液外泌体mir-1283的序列如seqidno.1所示。本发明的另一个目的是提供所述外泌体mirna(血液外泌体mir-1283)在制备肝癌转移风险预警和预后评估产品中的应用。所述产品为检测exo-mir-1283的试剂,所述检测exo-mir-1283的试剂包括任何可用于检测exo-mir-1283存在与否或表达高低的方法中所使用的试剂。所述检测exo-mir-1283存在与否或表达高低的方法可采用而不局限于:相对定量rt-pcr、绝对定量pcr、数字pcr。进一步,检测exo-mir-1283的试剂包括mir-1283的逆转录引物、pcr检测上下游引物。逆转录引物序列如seqidno.2所示。mir-362的pcr检测上游引物序列如seqidno.3所示,mir-362的pcr检测下游引物序列如seqidno.4所示。本发明的再一个目的是提供一种外泌体mirna在制备肝癌转移风险预警和预后评估的诊断产品。所述诊断产品包括检测exo-mir-1283的试剂盒。所述检测exo-mir-1283存在与否或表达高低的方法可采用而不局限于:相对定量rt-pcr、绝对定量pcr、数字pcr。所述检测exo-mir-1283的试剂盒包括mir-1283的引物。进一步,所述试剂盒还包括分离外泌体所用的试剂、裂解外泌体所用的试剂。所述分离外泌体所用的试剂包括任何能够分离外泌体的方法中使用的试剂。分离外泌体的方法包括但不局限于超速离心法、沉淀法、分子排阻层析、亲和分离法、免疫磁珠法、超滤法等。本发明用于肝癌转移风险预警和预后评估的外泌体来自体液,所述体液包括血液、尿液、唾液、腹水、脑脊液等。优选地,本发明的用于肝癌诊断的外泌体来自血液。本发明的诊断产品进行肝癌转移风险预警和预后评估的步骤包括:(1)从体液中分离外泌体;(2)检测exo-mir-1283表达水平;(3)根据exo-mir-1283表达信息帮助肝癌转移风险预警及预后评估。本发明的第四个目的是提供一种外泌体mirna在肝癌pnc比例分析的无创诊断产品中的应用。所述诊断产品包括检测exo-mir-1283的试剂。所述检测exo-mir-1283存在与否或表达高低的方法可采用而不局限于:相对定量rt-pcr、绝对定量pcr、数字pcr。所述检测exo-mir-1283的试剂包括mir-1283的引物。进一步,所述试剂盒还包括分离外泌体所用的试剂、裂解外泌体所用的试剂。所述分离外泌体所用的试剂包括任何能够分离外泌体的方法中使用的试剂。分离外泌体的方法包括但不局限于超速离心法、沉淀法、分子排阻层析、亲和分离法、免疫磁珠法、超滤法等。本发明用于肝癌pnc比例分析的外泌体来自体液,所述体液包括血液、尿液、唾液、腹水、脑脊液等。优选地,本发明的用于肝癌诊断的外泌体来自血液。本发明的诊断产品进行肝癌pnc比例分析的步骤包括:(1)从体液中分离外泌体;(2)检测exo-mir-1283表达水平;(3)根据exo-mir-1283表达信息反映肝癌组织pnc比例。我们采用肝癌细胞株建立小鼠肝癌转移模型,发现转移灶肝癌细胞的pnc比例远远高于原位灶细胞。分离转移灶和原位灶肝癌组织并行细胞培养,然后对两种细胞培养上清的外泌体mirna组分进行芯片分析,发现外泌体mir-1283(exo-mir-1283)在高pnc比例(转移灶)的肝癌细胞中显著升高。提示exo-mir-1283有望作为一种pnc相关的新型标志物而用于肝癌转移预警,并用于相关诊断产品的制备。本发明的优点和有益效果如下:(1)血液exo-mir-1283是一种新型生物标志物,区别于传统生物标志物,不仅稳定、微创、易于检测,且定量精确,将大大提高疾病诊断的敏感性和特异性,该生物标志物的开发有助于肝癌的诊断及转移风险预警,并为其他肿瘤类似生物标志物的研制提供借鉴。(2)通过血液exo-mir-1283的含量来判断肝癌预后的方法,可为临床医生快速准确掌握患者病情、及时采取更具个性化的防治方案提供依据。通过血液exo-mir-1283可反映肝癌pnc比例,可为基于pnc的肝癌转移预警及预后评估提供便捷的无创诊断方式。附图说明图1:肝癌细胞株huh7、hepg2和正常肝细胞株hl-7702的exo-mir-1283水平分析。**p<0.01。图2:原位癌肝癌患者,门静脉侵犯肝癌患者及健康对照者的血清exo-mir-1283水平分析。hc代表健康对照,hcc代表原位癌肝癌患者,hcc-m代表有门静脉侵犯或淋巴结转移的肝癌患者。a:各组患者与hc相比有统计学差异;b:hcc-m与hcc相比有统计学差异。具体实施方式下面结合附图和具体实施例进一步说明本发明,本发明的实施例仅用于解释本发明,并不意味着限制本发明的保护范围。下述实施例中所使用的实验方法如无特殊说明,均为常规方法。下述实施例中所用的材料、试剂等,如无特殊说明,均可从商业途径得到。实施例1外泌体的制备肝癌细胞株huh7和hepg2,以及正常肝细胞系hl-7702,常规培养至40%左右密度时,pbs洗涤2遍后换用添加无外泌体血清的培养体系进行培养。48小时后收集细胞上清,采用超速离心法进行外泌体的分离制备。先4℃,300g离心10分钟;取上清后再次离心(4℃,2000g,10分钟);再次取上清进行离心(4℃,10,000g,30分钟)。弃沉淀,上清于100,000g离心70分钟;收集沉淀用pbs重悬后,再次离心(100,000g,70分钟),所得沉淀即为细胞外泌体。收集患者或体检者的抗凝及非抗凝血,于4℃,2000rpm离心10分钟,分别分离血浆和血清,取1ml血浆或血清采用wako公司的magcapturetmexosome分离试剂盒,基于磁珠和磷脂酰丝氨酸(ps)亲和法进行血液外泌体的分离。也可采用超速离心法、peg沉淀法、分子排阻层析、免疫磁珠法、超滤法等进行外泌体的分离。实施例2外泌体的鉴定通过nta法(nanoparticletrackinganalysis:纳米颗粒跟踪分析法)分析细胞上清及血浆或血清外泌体的粒径,细胞上清外泌体粒径范围在40-150nm,血浆或血清外泌体的粒径范围在35-135nm。并采用westernblot或磁珠法(流式细胞术)检测其表面的外泌体标志物。westernblot检测显示分离的huh7细胞和肝癌患者血浆及血清外泌体均表达cd63、cd9和cd81。实施例3外泌体mir-1283表达水平的分析收集huh7、hepg2和hl-7702细胞的外泌体,或者肝癌患者及健康对照者血清外泌体。分别用200μl的pbs重悬后置于冰上,加入thermofisher公司200μl的2xdenaturingsolution混匀,再加入25fmol的外参cel-mir-39。然后采用thermofisher公司的mirvanamirna抽提试剂盒进行血清外泌体mirna的分离制备。接着使用mirna逆转录试剂盒,采用mir-1283的逆转录引物(seqidno.2:cagcataggtcacgcttatggagcctgggacgtgacctatgctgagaaag)进行逆转录,反应程序为:42℃15分钟,85℃5秒。再用mir-1283的pcr检测引物对进行其进行荧光定量pcr检测,pcr体系为:2×sybrgreenmix-10μl;mir-1283上游引物(seqidno.3:gccgggtctacaaaggaaagcg)5μm-0.8μl;mir-1283下游通用引物(seqidno.4:gtcacgcttatggagcctgg)5μm-0.8μl;模板-2ul;dd水-补至20μl。pcr条件为:95℃预变性10min,然后95℃5s,60℃30s,72℃30s,40个循环。使用cel-mir-39作为外参,采用相对定量2-δδct分析法,以及非参数检验比较各细胞株间和患者间的exo-mir-1283表达差异。如图1所示,肝癌细胞株的exo-mir-1283水平显著高于正常肝细胞株。如图2所示,肝癌患者的exo-mir-1283水平显著高于健康对照,并且有门静脉侵犯或淋巴结转移的肝癌患者其exo-mir-1283水平亦显著高于原位癌患者。实施例4细胞pnc比例与exo-mir-1283表达水平的相关性huh7、hepg2和hl-7702细胞爬片、固定后,采用ptb鼠单克隆抗体进行细胞pnc结构的免疫荧光染色。结果显示三株细胞的pnc比例分别为78.03%±2.96%、3.27%±0.88%、1.01%±0.45%。huh7细胞的pnc比例最高,对应其exo-mir-1283表达水平最高;hl-7702细胞的pnc比例最低,对应其exo-mir-1283表达水平最低(表1)。实施例5肿瘤细胞转移性与exo-mir-1283表达水平的相关性分别用划痕实验和transwell实验检测huh7、hepg2和hl-7702细胞的迁移能力和侵袭能力。划痕实验显示,三株细胞在48小时的划痕间距对比初始间距的比值分别为41.93%±3.66%,56.07%±3.04%和81.21%±4.01%。transwell实验显示,36小时后穿过matrigel基质胶的细胞数分别为32.31±2.88,19.55±3.51和3.84±1.74。表明huh7细胞的迁移和侵袭能力最强,其次为hepg2细胞,hl-7702细胞的迁移和侵袭能力最弱。huh7、hepg2和hl-7702细胞的迁移和侵袭能力与其pnc比例相关(表1),亦与其exo-mir-1283表达水平相关。表1细胞pnc比例与其迁移和侵袭能力相关细胞株huh7hepg2hl-7702ppnc比例(%)78.03±2.963.27±0.881.01±0.45<0.001划痕间距比(%)41.93±3.6656.07±3.0481.21±4.01<0.001侵袭细胞数32.31±2.8819.55±3.513.84±1.74<0.001exo-mir-12837.13±0.752.55±0.311.0±0.12<0.01上述实施例的说明只是用于理解本发明的方法及其核心思想。应当指出,对于本领域的普通技术人员来说,在不脱离本发明原理的前提下,还可以对本发明进行若干改进和修饰,这些改进和修饰也将落入本发明权利要求的保护范围内。序列表<110>浙江大学<120>外泌体mirna在制备肝癌诊断产品中的应用<160>4<170>siposequencelisting1.0<210>1<211>22<212>rna<213>mir-1283<400>1ucuacaaaggaaagcgcuuucu22<210>2<211>50<212>dna<213>mir-1283逆转录引物(人工序列unknow)<400>2cagcataggtcacgcttatggagcctgggacgtgacctatgctgagaaag50<210>3<211>22<212>dna<213>mir-1283上游引物(人工序列unknow)<400>3gccgggtctacaaaggaaagcg22<210>4<211>20<212>dna<213>mir-1283下游引物(人工序列unknow)<400>4gtcacgcttatggagcctgg20当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1