一种性腺组织中特异高表达基因增加雄鱼繁殖力的方法与流程
本发明属于基因表达技术领域,尤其涉及一种性腺组织中特异高表达基因增加雄鱼繁殖力的方法。
背景技术:
目前,最接近的现有技术:一种鱼类繁殖能力大小直接决定了其应用推广的程度。目前大规模商品化养殖的四大家鱼,之所以能够全国大规模推广养殖,主要原因之一是能够实现大规模人工繁殖,获得大量的苗种。但是,对于黄鳝、石斑鱼等一些名特优鱼类,推广养殖的最大瓶颈就是繁殖能力较差,不能获得大量的苗种,也使得这些鱼类价格常年居高不下。因此,提高鱼类的繁殖力,对于一些鱼类的进一步推广具有非常重要的意义。对于雄性明显少于雌性的鱼类,例如青鲫及雌雄同体的石斑鱼等,提高雄性个体繁殖力,可以一定程度上缓解雄性个体稀少的问题,有利于进一步促进其推广养殖。目前,解决一些鱼类繁殖力弱的问题大多采用调控影响鱼类性腺发育的外部生态条件,如营养、水温、光照、水流及溶氧等,这些操作一定程度上增加了鱼类的繁殖力,但是由于影响因素太多,操作复杂,增加了养殖成本,且对于室外养殖可重复性较小。另外,近年来,“借腹怀胎”为鱼类生殖相关研究中的热点,但是,目前该技术仍处于理论阶段,尚没有推广使用。在此背景下,通过转基因的方法增加雄鱼生殖力,通过建立家系,可以使生殖力增强的性状代代相传,可以做到一蹴而就。
鱼类是人类赖以生存优质蛋白的重要来源之一,是最后的野生食物源。鱼类中含有人体必需的8种氨基酸,不饱和脂肪酸等,营养价值丰富,而且几乎不存在人鱼共患的疾病,因此备受青睐。渔业的可持续发展已经成为当今世界各国关注的主题。这种情况下,水产养殖被认为是满足人类不断增长的对水产动物蛋白需求的唯一途径。具有优良性状的养殖鱼类新品种是未来水产养殖可持续发展的关键之一。人工选育、引种和杂交育种是获得具有优良性状的养殖鱼类新品种的传统方法,但是传统育种方法超长的育种年限极大的限制了鱼类育种业的发展。转基因技术可在短时间内即可获得具有优良性状的新品种。
相比于哺乳动物,鱼类具有体外受精,体外发育,怀卵量大,且易于转基因操作,胚胎经转基因操作后不需要放回母体培育等优势,这些优势使转基因技术能够迅速应用于鱼类育种。转基因技术应用于鱼类育种的首次探索开始于20世纪80年代,朱作言等利用小鼠金属硫基因启动子成功驱动人的生长激素基因在鲫鱼中表达,培育出世界上第一批快速生长的转基因鱼。之后,转基因技术应用于鱼类育种中并迅速展开,经过30多年的发展,目前通过转基因操作获得具有生长速度快、饵料利用率高、抗病抗逆强等优良性状的转基因鱼类近40种,而且几乎包括世界上所有的重要养殖鱼类。
一个新的鱼类品种的大规模推广养殖的前提是能够进行人工繁殖,获得大量苗种。但是,目前一些鱼类雌雄比例严重失调,雄鱼个体非常少,如石斑鱼、青鲫等,这些鱼类虽然具有诸多优良性状,但是由于缺少雄性个体,其繁殖规模受到严重限制,阻止了其进一步推广养殖。但是,目前仍然没有针对增加雄鱼生殖能力的转基因研究。目前关于转基因鱼的研究主要对象为产量较大的鱼类,如四大家鱼及鲤鱼等,目的是提高这些鱼类的生长速度、抗病、抗寒能力等。但是对这些鱼类而言,生殖能力很强,不需要增加繁殖能力。但是,目前我国渔业发展的重点是经济效益好的特种水产鱼类,特种水产鱼类种类繁多,其中一些鱼类推广养殖的瓶颈问题,就是繁殖力差,因此,今后渔业的发展方向要求研究增加鱼类繁殖力的技术。
综上所述,现有技术存在的问题是:
(1)目前一些鱼类雌雄比例严重失调,雄鱼个体非常少;缺少雄性个体,其繁殖规模受到严重限制,阻止了其进一步推广养殖。
(2)目前没有针对增加雄鱼生殖能力的转基因研究。
解决上述技术问题的难度:
1寻找具有增强鱼类繁殖力的靶基因。我们研究发现tesk1基因过表达能够增强雄性鱼类生殖力。
2如何使靶基因在性腺组织特异表达?我们选择在性腺组织特异表达kop启动子及能够将mrna定位于性腺组织特异表达的nanos3’utr,使得靶基因tesk1在性腺组织特异表达。
解决上述技术问题的意义:
提高鱼类的繁殖力,对于一些雄性明显少于雌性的鱼类的进一步推广具有非常重要的意义。例如青鲫及雌雄同体的石斑鱼等,对于这些鱼类,提高雄性个体繁殖力,可以一定程度上缓解雄性个体稀少的问题,有利于进一步促进其推广养殖。
技术实现要素:
针对现有技术存在的问题,本发明提供了一种性腺组织中特异高表达基因增加雄鱼繁殖力的方法。
本发明是这样实现的,一种性腺组织中特异高表达基因增加雄鱼繁殖力的方法,所述性腺组织中特异高表达基因增加雄鱼繁殖力的方法包括以下步骤:
第一步,提取性腺组织rna-反转录为cdna,以cdna为模板,以tesk1-f/tesk1-r为引物,以高保真酶pfu进行pcr扩增,tesk1基因的克隆;
第二步,所用载体为含有kop启动子和nanos3’utr的质粒载体,kop启动子和nanos3’utr能将目的基因在生殖细胞中特异表达,通过ncoi和bseai酶切,将tesk1基因插入kop启动子和nanos3’utr之间,形成转基因载体;
第三步,显微注射获得转基因鱼。
进一步,所述第一步的引物为:
tesk1-f5’-cacccatgggttgcgttaaagtgacccgct-3’;
tesk1-r5’-ttctccggagagatgtcgcagtggtcgtc-3’。
进一步,所述第二步的转基因载体,含有主要的元件为tol2-kop-tesk1-nanos3’utr-tol2。
进一步,所述第三步的显微注射获得转基因鱼方法包括:
(1)在显微注射前,进行所述转基因载体处理,其包括去毒性处理和防串联处理;
(2)体外合成tol2转座酶mrna;
(3)对斑马鱼胚胎显微注射所述转基因载体处理后的质粒dna和所述tol2转座酶mrna;
(4)将显微注射后的斑马鱼胚胎作为p0代,所述p0代养殖性成熟后,通过与野生斑马雌鱼测交得到后代f1代,将所述f1代阳性个体饲养至性成熟后采用自交获得纯合f2代。
进一步,所述体外合成tol2转座酶mrna方法包括:
首先,将带有转座酶基因的396载体,用notⅰ限制性内切酶线性化,然后用sp6体外转录试剂盒进行体外转录;
其次,进行dna模板的去除及反应终止;
最后,纯化。
综上所述,本发明的优点及积极效果为:目前,解决一些鱼类繁殖力弱的问题大多采用调控影响鱼类性腺发育的外部生态条件,如营养、水温、光照、水流及溶氧等,这些操作一定程度上增加了鱼类的繁殖力,但是由于影响因素太多,操作复杂,增加了养殖成本,且对于室外养殖可重复性较小。本发明针对增加雄性鱼类生殖能力,以斑马鱼为对象,在雄鱼性腺组织中特异高表达tesk1基因,发现可以显著性增加雄鱼的性腺指数,增加其产精量,实现了提高雄性斑马鱼生殖能力的目的,并有望推广至经济鱼类。
附图说明
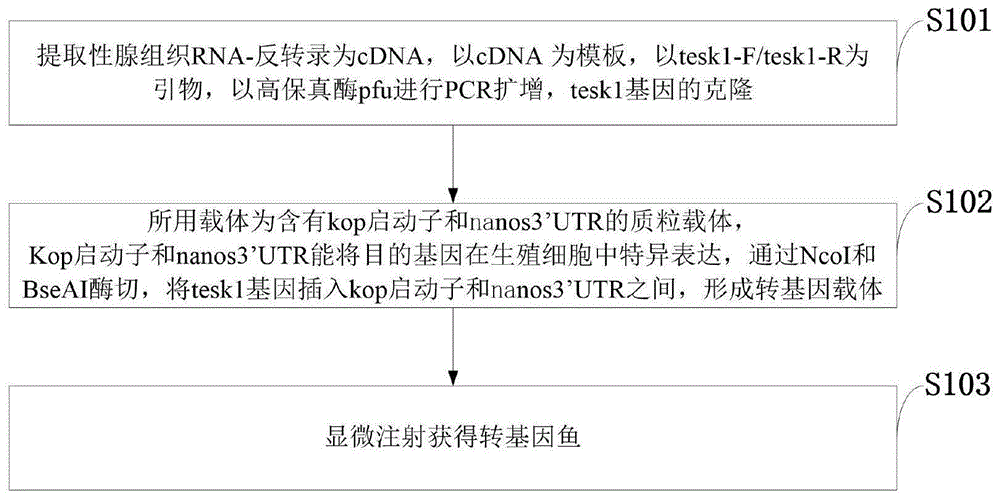
图1是本发明实施例提供的性腺组织中特异高表达基因增加雄鱼繁殖力的方法流程图。
图2是本发明实施例提供的转基因载体示意图。
图3是本发明实施例提供的斑马鱼不同组织中tesk1基因的表达示意图。
图4是本发明实施例提供的转tesk1基因雄性斑马鱼性腺指数显著增加示意图。
图5是本发明实施例提供的转tesk1基因雄性斑马鱼和野生斑马鱼性腺组织切片观察示意图;
图中:(a)转tesk1基因雄性斑马鱼;(b)野生对照。
具体实施方式
为了使本发明的目的、技术方案及优点更加清楚明白,以下结合实施例,对本发明进行进一步详细说明。应当理解,此处所描述的具体实施例仅仅用以解释本发明,并不用于限定本发明。
针对现有技术存在的问题,本发明提供了一种性腺组织中特异高表达基因增加雄鱼繁殖力的方法,下面结合附图对本发明作详细的描述。
如图1所示,本发明实施例提供的性腺组织中特异高表达基因增加雄鱼繁殖力的方法包括以下步骤:
s101:提取性腺组织rna-反转录为cdna,以cdna为模板,以tesk1-f/tesk1-r为引物,以高保真酶pfu进行pcr扩增,tesk1基因的克隆;
s102:所用载体为含有kop启动子和nanos3’utr的质粒载体,kop启动子和nanos3’utr能将目的基因在生殖细胞中特异表达,通过ncoi和bseai酶切,将tesk1基因插入kop启动子和nanos3’utr之间,形成转基因载体;
s103:显微注射获得转基因鱼。
下面结合实验对本发明的技术方案作进一步的描述。
一、实验步骤:
1、tesk1基因的克隆(ncbi序列号xm_678756.5)
提取性腺组织rna-反转录为cdna,以cdna为模板,以tesk1-f/tesk1-r为引物,以高保真酶pfu进行pcr扩增,产物总长2034bp;
seqidno:1
tesk1-f5’-cacccatgggttgcgttaaagtgacccgct-3’(下划线为ncoi及其保护碱基);
seqidno:2;
tesk1-r5’-ttctccggagagatgtcgcagtggtcgtc-3’(下划线为bseai及其保护碱基)。
2、所用载体为含有kop启动子和nanos3’utr的质粒载体,kop启动子和nanos3’utr能将目的基因在生殖细胞中特异表达,通过ncoi和bseai酶切,将tesk1基因插入kop启动子和nanos3’utr之间,形成转基因载体,含有主要的元件为tol2-kop-tesk1-nanos3’utr-tol2,如图2所示:
3、显微注射获得转基因鱼,如下:
(1)在显微注射前,进行所述转基因载体处理,其包括去毒性处理和防串联处理;
(2)体外合成tol2转座酶mrna,具体方法如下:
首先,将带有转座酶基因的396载体,用notⅰ限制性内切酶线性化,然后用sp6体外转录试剂盒进行体外转录;
其次,进行dna模板的去除及反应终止;
最后,纯化;
(3)对斑马鱼胚胎显微注射所述转基因载体处理后的质粒dna和所述tol2转座酶mrna;
(4)将显微注射后的斑马鱼胚胎作为p0代,所述p0代养殖性成熟后,通过与野生斑马雌鱼测交得到后代f1代,将所述f1代阳性个体饲养至性成熟后采用自交获得纯合f2代。
二、结果:
1、tesk1基因在斑马鱼不同组织中的表达情况
斑马鱼不同组织中tesk1基因的表达,如图3所示;
主要方法:提取斑马鱼不同组织总rna,反转录为cdna,以此为模板,利用引物:rt-tesk1-f:5’-gctgccattggttgcttatt-3’;
rt-tesk1-r:5’-gtggactttgaaacggcaat-3’;
退火温度60度,长度154bp,所用试剂为takara(sybr)
以odc为参照基因的实时荧光定量pcr
引物用primerpremier5软件设计或(5’-3’):
rt-odc-f:5’-acactatgacggcttgcaccg-3’
rt-odc-r:5’-cccactgactgcacgatctgg-3’
反应体系如下:(模板为cdna原液稀释5倍)
反应条件如下:95℃,3min;(94℃,15s;60℃,15s;72℃,45s;40个循环)。
2、p0代转基因斑马鱼性腺指数
如图4所示,性腺指数测定:待阳性斑马鱼性成熟后,解剖取其性腺组织,称重,性腺重与体重之比即为性腺指数(野生和转基因各检测了10条斑马鱼)。
3、转tesk1基因雄性斑马鱼和野生斑马鱼性腺组织切片观察,如图5所示;从图5可以看出转tesk1基因雄性斑马鱼性腺组织中小叶腔显著增大,有大量成熟的精子存在于小叶腔中,而野生斑马鱼小叶腔较小,其中只有较少的精子。
操作方法如下:取斑马鱼性腺组织于4%pfa溶液中4℃固定过夜,然后将性腺组织埋入1.5%琼脂中,在以下溶液中进行脱水,透化,透蜡。具体步骤如下:50%乙醇6~8h、75%乙醇6~8h、85%乙醇3~5h、95%乙醇1~2h、95%乙醇1~2h、100%乙醇ⅰ1h、100%乙醇ⅱ1h、100%乙醇/二甲苯40min、二甲苯40min、二甲苯30min、二甲苯/石蜡30min、石蜡(60℃)1h、石蜡(60℃)1h。
经过上述处理过的组织,要进行石蜡包埋,待石蜡凝固后就可以进行石蜡切片,厚度6-8um。切片用苏木精-伊红(hematoxylinandeosin,he)染色,染色步骤如下:
(1)二甲苯侵两次,每次15min。
(2)无水乙醇侵两次,每次5min。
(3)80%乙醇,5min。
(4)蒸馏水,5min。
(5)pbs洗3次,每次5min。
(6)苏木精染色8-10min。
(7)流水洗去苏木精后,1%盐酸乙醇溶液侵5-10s。
(8)流水沾洗后,用蒸馏水洗5s。
(9)0.5%伊红染色5min。
(10)80%乙醇沾洗1-2s,95%乙醇沾洗两次,每次5s。
(11)无水乙醇两次,每次5min。
(12)石碳酸二甲苯,5min。
(13)二甲苯3次,每次2min。
(13)将二甲苯拭去,马上用树脂进行封片处理,待树脂风干后,即可显微镜下观察。
以上所述仅为本发明的较佳实施例而已,并不用以限制本发明,凡在本发明的精神和原则之内所作的任何修改、等同替换和改进等,均应包含在本发明的保护范围之内。
序列表
<110>湖南文理学院
<120>一种性腺组织中特异高表达基因增加雄鱼繁殖力的方法
<160>2
<170>siposequencelisting1.0
<210>1
<211>30
<212>dna
<213>人工序列(artificialsequence)
<400>1
cacccatgggttgcgttaaagtgacccgct30
<210>2
<211>29
<212>dna
<213>人工序列(artificialsequence)
<400>2
ttctccggagagatgtcgcagtggtcgtc29
- 还没有人留言评论。精彩留言会获得点赞!
- 一种经腺病毒基因修饰的肿瘤特异性细胞毒性t淋巴细胞的培养方法
- CRISPR-Cas9特异性敲除猪SLA-1基因的方法及用于特异性靶向SLA-1基因的sgRNA的制作方法
- 一种特异性靶向QKI基因的sgRNA及其应用
- 一种泰国库蠓的特异基因及其分子鉴定方法
- 一种美丽库蠓特异基因及其分子鉴定方法
- 一种特异于禽类原始生殖细胞的基因转移系统及方法
- CRISPR-Cas9特异性敲除猪SALL1基因的方法及用于特异性靶向SALL1基因的sgRNA的制作方法
- CRISPR-Cas9特异性敲除猪CMAH基因的方法及用于特异性靶向CMAH基因的sgRNA的制作方法
- CRISPR-Cas9特异性敲除猪SLA-2基因的方法及用于特异性靶向SLA-2基因的sgRNA的制作方法
- 一种安宁铗蠓的特异基因及其分子鉴定方法