一种柱芳烃与冠醚类杂化大环的缩合物作为胶粘剂的应用的制作方法
本发明属于有机合成技术领域,具体涉及一种柱芳烃与冠醚类杂化大环的缩合物作为胶粘剂的应用。
背景技术:
胶粘剂是一种能将两种材料的表面粘合在一起,并能防止脱落的一类材料,多为高分子化合物和各类辅助材料组成。随着超分子胶粘剂的发展,出现了一批具有可逆特性的胶粘剂,该超分子胶粘剂由于具有动态非共价键,能够多次重复使用。传统胶粘剂或者含二羟基苯丙氨酸(dopa)的仿生胶粘剂虽然能够牢牢粘附各种表面,可是要想将粘在一起的表面分开且不破坏被粘接的部分,比较困难。虽然已经报道的超分子胶粘剂已经能够轻松实现不损伤粘附表面而分离被粘接的部分,但能够应用在极端环境下(如南极北极极低温度甚至液氮(-196℃))的超分子胶粘剂少之又少。这是因为大多数超分子胶粘剂属于温敏性材料,随着温度的升高或者降低其粘性会大大降低甚至失效。尤其是极低温度下,尚没有成功粘附的报道。
技术实现要素:
为了解决现有技术中存在的缺陷,本发明的目的是在于提供了一种柱芳烃与冠醚类化合物的缩合物作为胶粘剂的应用,不仅可以在日常环境下粘附玻璃、金属、大理石等一系列材质,而且也可以粘附耐超低温金属材料,能够在-196℃~60℃温度范围内使用,即使由极低温度(液氮,-196℃)环境中取出依然能够保持其较强的粘附性能。
为了实现上述技术目的,本发明采用如下技术方案:
一种柱芳烃与冠醚类杂化大环的缩合物作为胶粘剂的应用,所述柱芳烃与冠醚类杂化大环的缩合物的结构式如式i所示:
式i中,x为o,s或nh,rn为选自以下取代基中的一种:
其中,a′和a″中的一个为h,另一个为卤素、no2、nh2、oh或och3;或a′和a″均为h;
n为1、2、3、4、5或6。
作为优选,式i中,x为o,rn为选自以下取代基中的一种:
其中,a′和a″中的一个为h,另一个为卤素、no2、nh2、oh或och3;或a′和a″均为h;
n为1、2、3、4、5或6。
作为优选,式i中,x为o,rn为选自以下取代基中的一种:
其中,a′和a″均为h;n为2、3、4或5。
作为优选,当rn为
作为优选,当rn为
本发明的式i化合物能够通过加适量的水或者通过加热的方法,形成超分子聚合物。本发明的化合物具有可逆的粘附性能,由于超分子聚合物的非共价键易受温度影响通过加热的方法破坏非共价键使其脱粘附,待冷却后非共价键重新恢复其超分子聚合物粘附性能随之恢复,从而实现可逆粘附。此外,本发明的式i化合物能够在-196℃~60℃温度范围内使用。
本发明的式i化合物作为胶粘剂时,可根据具体式i化合物的性质选择加入水或者通过加热的方法来黏附材料,当采用加水的方式时,其水量一般占式i化合物的质量的十分之一;而当采用加热的方式时,其加热熔融的温度可根据实际使用的式i化合物的熔点进行设置,一般加热温度高于熔点10℃左右即可。
本发明所述的柱芳烃与冠醚类杂化大环的缩合物式i,通过常规的缩合反应即可获得,其反应路线如下:
与现有技术相比,本发明的优势和有益效果:
(1)本发明通过柱芳烃与冠醚类杂化大环经缩合反应得到的式i化合物作为胶粘剂使用时,不需要添加各种辅助物质,只需要加入水或者仅需要加热即可实现粘附。
(2)本发明通过柱芳烃与冠醚类杂化大环经缩合反应得到的式i化合物作为胶粘剂使用时,粘附过程简单,无需有机溶剂参与,避免了因溶剂的存在,而使被粘物变形、错位和收缩等弊病。
(3)本发明通过柱芳烃与冠醚类杂化大环经缩合反应得到的式i化合物作为胶粘剂使用时,硬化速度快,可用于玻璃、金属、纸张、木头、大理石、瓷砖等材料的快速粘合。
(4)本发明通过柱芳烃与冠醚类杂化大环经缩合反应得到的式i化合物作为胶粘剂使用时,具有耐超低温性质,能够在-196℃~60℃温度范围内使用,并且可重复利用,粘附能力不变化,是一类绿色环保可循环利用的新型胶粘剂。
附图说明
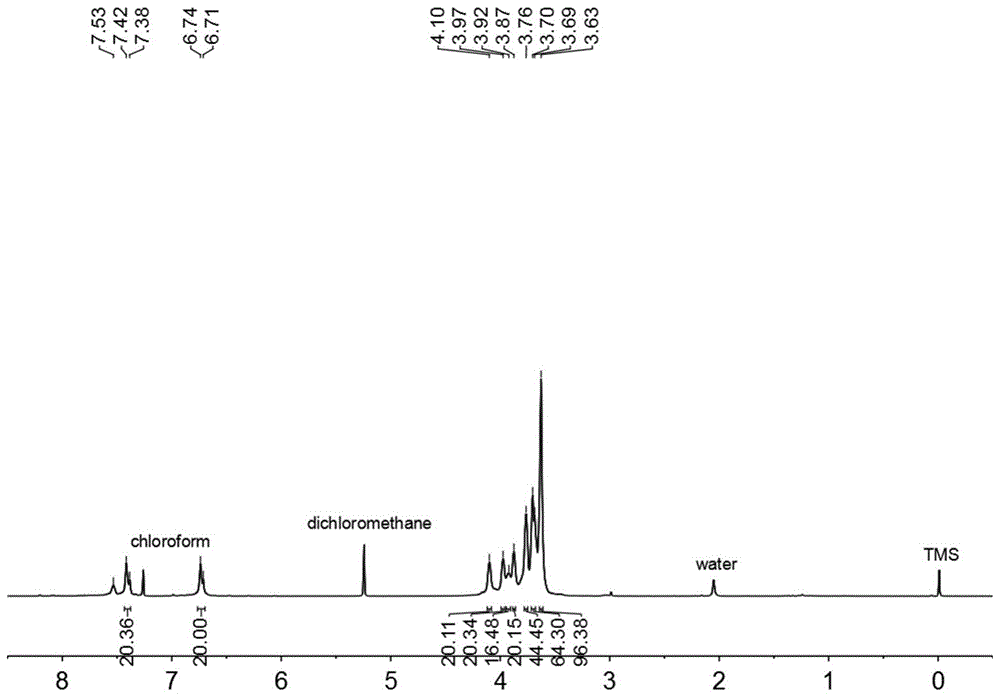
图1为本发明实施例1制得的样品的核磁氢谱图;
图2为本发明实施例1制得的样品的核磁碳谱图;
图3为本发明实施例2制得的样品的核磁氢谱图;
图4为本发明实施例2制得的样品的核磁碳谱图;
图5为本发明的样品1由-196℃至环境温度变化下的粘附状态实物图。
具体实施方式
下面结合具体实施例,进一步阐述本发明。值得说明,这些实施例仅用于说明本发明,而不用于限定本发明的保护范围。在实际应用中技术人员根据本发明做出的改进和调整,仍属于本发明的保护范围。
实施例1
本实施例提供的化合物,分子结构式如下所示:
在100毫升的圆底烧瓶中,投入2.36克苯并21-冠-7-羧酸,0.52克十胺柱[5]芳烃和1.44克4-二甲氨基吡啶,用50毫升二氯甲烷溶解,冰浴搅拌十分钟后加入4.54克1-(3-二甲氨基丙基)-3-乙基碳二亚胺盐酸盐,室温反应6天。加入2毫升10%盐酸搅拌5分钟后分液,下层有机层水洗旋干得粗产物,粗产物再通过硅胶柱分离纯化,得到1.28克产物,产率为45%。
氢谱、碳谱数据分别如下:
1hnmr(400mhz,cdcl3,roomtemperature)δ7.40(d,j=16.0hz,20h),6.73(d,j=12.0hz,20h),4.10(s,20h),3.97(s,20h),3.92(s,16h),3.87(s,20h),3.76(s,46h),3.70-3.69(m,64h),3.63(s,96h);熔点:69.4-71.1℃。
13cnmr(101mhz,cdcl3,roomtemperature)δ167.61,151.46,149.93,148.44,128.49,127.21,120.58,115.58,112.96,112.66,71.20,71.04,70.94,70.88,70.49,69.58,69.55,69.12,69.06,66.92,39.92.hrmsc245h340o90n10na2+2:cal.2455.1093,found2455.0857,error9.6ppm.
实施例2
本实施例提供的化合物,分子结构式如下所示:
在100毫升的圆底烧瓶中,投入2.59克双苯并24-冠-8-羧酸,0.48克十胺柱[5]芳烃和1.32克4-二甲氨基吡啶,用50毫升二氯甲烷溶解,冰浴搅拌十分钟后加入4.17克1-(3-二甲氨基丙基)-3-乙基碳二亚胺盐酸盐,室温反应6天。待反应结束后,加入2毫升10%盐酸搅拌5分钟后分液,下层有机层水洗旋干得粗产物,粗产物再通过硅胶柱分离纯化,得到1.72克产物,产率为55%。
氢谱、碳谱数据分别如下:
1hnmr(400mhz,cdcl3,roomtemperature)δ7.43(s,16h),6.85(s,40h),6.71(s,6h),6.67(d,j=8.0hz,8h),4.14–4.09(m,44h),4.04(s,20h),3.97(s,20h),3.90(s,20h),3.83(s,62h),3.75–3.73(m,104h),3.63(s,10h).熔点:89.2-91.0℃。
13cnmr(101mhz,cdcl3,roomtemperature)δ167.6,151.46,149.93,148.44,128.49,127.21,120.58,115.58,112.96,112.66,71.20,71.04,70.94,70.88,70.49,69.55,69.21,69.06,69.92,39.92.
拉伸性能测试:
采用样品1、样品2和市售pva胶粘剂均匀涂布于材料的粘附表面后,使用微机控制电子万能材料试验机(hy-0580,上海衡翼精密仪器有限公司)进行拉力测试。
样品1:取实施例1的化合物,加入其质量十分之一的水即得胶状物样品1。
样品2:取实施例2的化合物,于100℃的条件下加热熔融,即得胶状物样品2。
(1)分别将相同量的样品1、样品2和市售pva胶粘剂均匀涂布于玻璃表面进行粘接,再于室温下进行粘附强度测试,其结果如表1所示:
表1不同样品对玻璃的拉伸试验测试结果
(2)分别将样品1均匀涂布于不同材料表面进行粘接,再于不同温度下进行粘附强度测试,其结果如表2所示:
表2样品1对不同材料于不同温度下的拉伸试验测试结果
(3)分别将样品2均匀涂布于不同材料表面进行粘接,再于不同温度下进行粘附强度测试,其结果如表3所示:
表3样品2对不同材料于不同温度下的拉伸试验测试结果
(4)如图5所示,将样品1均匀涂布于铁片上,另一块铁片置于上方,使用市售夹子将两块粘附的铁片夹住,保持10分钟,即可制备好可悬挂重物的材料。将粘附好的铁片一端悬挂在支撑物上,另一端悬挂重物,并置于容器内。接着快速注入液氮使液面完全淹没铁片,经一段时间的冷冻,由样品1粘附的铁片依然没有分离或错位。将装有液氮的容器取走后,样品1粘附的铁片自然缓慢地恢复至室温,其粘附效果不变。
- 还没有人留言评论。精彩留言会获得点赞!