微流控纸芯片及应用其的检测系统的制作方法
本发明属于移动医疗检测领域,尤其涉及一种微流控纸芯片及应用其的检测系统。
背景技术:
卵巢是女性的生殖器官,卵细胞在卵巢内生成、发育,并由卵巢内卵泡分泌排出,卵子如进入输卵管并遇到精子即受精成为孕卵(受精卵)。卵巢还具有内分泌功能,其合成分泌的性激素控制着人体骨骼、免疫、生殖、神经等九大系统的400多个部位,维持这些器官的青春和活力。如果卵巢功能异常会引起多种疾病,比如卵巢功能衰退会造成生育困难甚至不孕不育,还会对人体的生理心理健康带来负面影响。卵巢功能监测在卵巢疾病诊断、治疗效果评估、备孕指导及女性生理健康等具有非常重要的意义。以不孕症为例,who推测不孕不育症将成为21世纪仅次于肿瘤和心脑血管病的第三大疾病。发达国家约有5%-8%的夫妇受到不孕症的影响,发展中国家一些地区不孕症的患病率高达30%,我国目前约有4000万不孕症患者,且每年以数十万的速度递增。对不孕症进行诊断、治疗及治疗效果评估都需要对卵巢功能进行动态监测。
对卵巢功能进行监测的手段很多,最常见的最适宜的是通过体内性激素的水平评估卵巢功能。性激素是人体重要的内分泌物质,既可以调节卵巢功能,也是卵巢功能检测的生化指标,可以通过检测性激素量化水平检测女性卵巢功能和诊断卵巢相关的疾病。常用的性激素六项即卵泡生成激素(fsh)、黄体生成激素(lh)、雌二醇(e2)、孕酮(p)、睾酮(t)、催乳激素(prl)。在性激素六项中,fsh主要功能是促进卵巢的卵泡发育和成熟;lh主要是促使排卵,在fsh的协同作用下,形成黄体并分泌孕激素;雌二醇e2主要功能是促使子宫内膜转变为增殖期和促进女性第二性征的发育。这三项联合检测基本可以满足临床医生和科研人员对卵巢功能监测的需求。
lh、fsh和e2等性激素在人体血液中含量极低,需要较高的检测灵敏度,目前检测主要采用免疫方法,如免疫胶体金试条、免疫生化检测仪等方法。其中胶体金试条基于免疫层析方法,结构简单,操作方便,价格低,但是采用显色方法,为定性或半定量检测,灵敏度不高,无法满足定量检测需求。免疫生化检测仪可以实现多参数同时检测,检测灵敏度高,但是检测周期长,需样量大(采用静脉采血3-4ml),且免疫分析仪多为大型仪器,适于医院的检验科或中心实验室,难以满足家庭、个人对lh、fsh和e2等快速检测的需求。
技术实现要素:
鉴于现有方案存在的问题,为了克服上述现有技术方案的不足,本发明提出了微流控纸芯片及应用其的检测系统。
根据本发明的一个方面,提供一种微流控纸芯片,用于检测性激素含量,沿层叠方向依次包括:加样过滤层,用于引入待测液体,并过滤截留液体中的细胞;第一移动隔离层;辅助电极层;工作电极层;第二移动隔离层;以及吸水层,用于保障待测液体流通穿过辅助电极层和工作电极层并收集多余液体,其中:辅助电极层和工作电极层构成检测区域层,包括电化学检测电路,通过电化学方式检测待测液体中性激素含量;第一和第二移动隔离层用于待测液体进入检测区层完全反应后隔绝检测区域层与其他层之间的液体流动。
根据本发明的一个方面,提供一种检测系统,包括:微流控纸芯片;电化学控制模块,用于向微流控纸芯片输入检测信号;顶部开口的盒体,容置电化学模块和所述微流控纸芯片;以及检测装置,用于封闭所述盒体的顶部开口,并控制所述电化学控制模块输出检测信号,以及检测所述微流控纸芯片发出的光信号,分析待测液体性激素的含量。
从上述技术方案可以看出,本发明具有以下有益效果:
将纳米材料与技术和直接免疫电化学发光检测方法相结合,建立了只需一步反应的直接免疫电化学发光检测方法,简化了操作,提高了检测速度;
在工作电极层设置工作电极和差分电极检测时,采用分时复用的方式,按次序分别扫描各个电极,首先对差分电极进行扫描,记录得到的信号,然后依次扫描3个工作电极,对获得的信号进行差分,获得检测信号,减小干扰,提高检测一致性和准确度;
设置移动隔离层,避免检测时非检测层液体的干扰,检测结果精确。
附图说明
图1为本发明一实施例中微流控纸芯片的爆炸图;
图2为图1中辅助电极层的结构示意图;
图3为图1中工作电极层的结构示意图;
图4为图1中的工作电极制备的流程示意图;
图5为图1中第一移动隔离层的结构示意图;
图6为图1中第二移动隔离层的结构示意图;
图7为图1中加样过滤层的结构示意图;
图8为图1中吸水层的结构示意图;
图9为图1中覆盖层的结构示意图;
图10为本发明另一实施例检测系统的结构示意图;
图11为图10中检测系统的检测原理示意图。
具体实施方式
本发明某些实施例于后方将参照所附附图做更全面性地描述,其中一些但并非全部的实施例将被示出。实际上,本发明的各种实施例可以许多不同形式实现,而不应被解释为限于此数所阐述的实施例;相对地,提供这些实施例使得本发明满足适用的法律要求。
在本说明书中,下述用于描述本发明原理的各种实施例只是说明,不应该以任何方式解释为限制发明的范围。参照附图的下述描述用于帮助全面理解由权利要求及其等同物限定的本发明的示例性实施例。下述描述包括多种具体细节来帮助理解,但这些细节应认为仅仅是示例性的。因此,本领域普通技术人员应认识到,在不悖离本发明的范围和精神的情况下,可以对本文中描述的实施例进行多种改变和修改。此外,为了清楚和简洁起见,省略了公知功能和结构的描述。此外,贯穿附图,相同附图标记用于相似功能和操作。
为使本发明的目的、技术方案和优点更加清楚明白,以下结合具体实施例,并参照附图,对本发明进一步详细说明。
本发明一实施例提供一种微流控纸芯片,用于检测性激素含量,图1为本发明一实施例中微流控纸芯片100的爆炸图,如图1所示,微流控纸芯片100沿层叠方向依次包括:覆盖层10、加样过滤层20、第一移动隔离层30、辅助电极层40、工作电极层50、第二移动隔离层60、吸水层70。其中加样过滤层20,用于引入待测液体,并过滤截留液体中的细胞;吸水层70用于保障待测液体流通穿过辅助电极层和工作电极层并收集多余液体。辅助电极层40和工作电极层50构成检测区域层,包括电化学检测电路,通过电化学方式检测待测液体中性激素含量;第一移动隔离层30和第二移动隔离层20用于待测液体进入检测区层完全反应后隔绝检测区域层与其他层之间的液体流动。
以下详细介绍该实施例中微流控纸芯片各层的具体结构及作用。图2和图3分别为图1中辅助电极层40、工作电极层50的结构示意图。
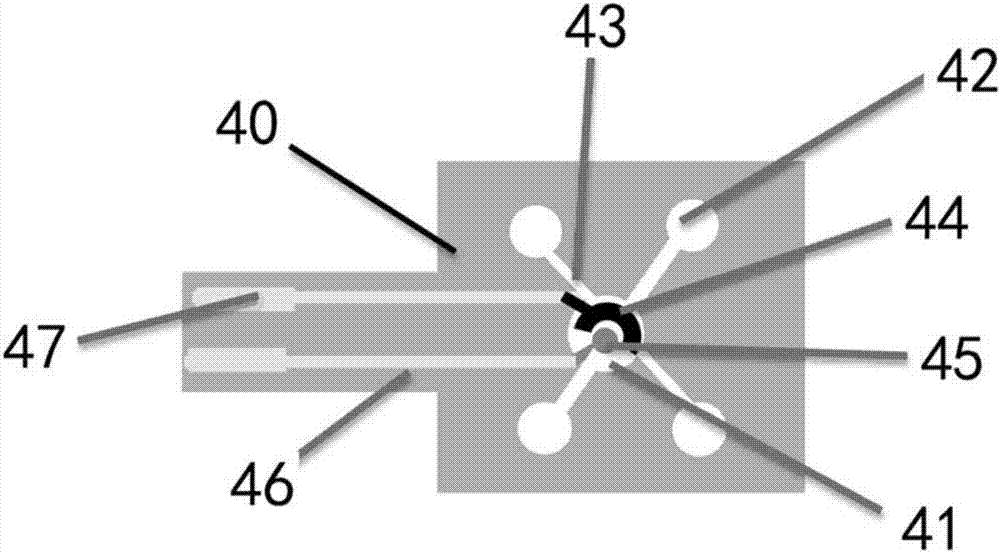
如图2所示,辅助电极层40可以采用whatman1号滤纸作为基底材料,在基底材料上设置第一中心分流区41及位于第一中心分流区周围均匀排布的n个第一通孔42(n可以为大于等于2的正整数,本实施例中n=4),第一中心分流区41与每一第一通孔42通过连接通路43连接,可以将流入到中心分流区41的待测液体传输至每一第一通孔42。中心分流区41上设置有参比电极44和对电极45,分别通过导线46连接至辅助电极层的两输出电极47上;可以通过丝印方式在中心分流区41上丝印对电极45(碳浆)和参比电极44(ag/agcl),对电极45和参比电极44与介绍的工作电极层50的工作电极形成三电极体系。
如图3所示,工作电极层50以采用whatman1号滤纸作为基底材料,在基底材料上设置n个第一亲水区51,其与n个第一通孔42一一正对设置,一第一亲水区上设置不固定抗体的差分电极52,其他第一亲水区上设置固定抗体的工作电极53,差分电极52和工作电极53分别通过导线54连接至工作电极层的n个输入电极55上。在第一亲水区51设置差分电极52和工作电极53时首先在第一亲水区51上丝印碳浆,形成基础电极,之后在其上制备差分电极52和工作电极53。
图4为工作电极制备的流程示意图,工作电极53制备采用以下流程,如图4所示:
1)取haucl4水溶液,调节ph至7.2,加热煮沸,在快速搅拌的情况下加入柠檬酸钠溶液,保持沸腾30分钟,可以得到纳米金溶液,4℃存储备用。在快速搅拌的情况下,在ru(bpy)3cl2加入溶液中加入纳米金溶液,ru(bpy)32+与表面带负电的金纳米粒子结合形成ru(bpy)32+/纳米金复合物。
2)向氧化石墨烯(go)中加入聚乙酰亚胺(pei),在回流作用下,135度加热3小时,经过清洗和离心分离后,得到还原氧化石墨烯(rgo)。硫堇分子(thi)通过π-π堆积作用吸附到还原氧化石墨烯的表面,而ru(bpy)32+/纳米金复合物粒子通过与还原氧化石墨烯上的胺基反应而固定从而形成复合物。
3)基础电极经表面处理后,然后在基础电极上滴加ru(bpy)32+/金纳米/硫堇/石墨烯复合物形成纳米复合膜。
4)在纳米复合膜上滴加抗体,通过纳米金与蛋白质的氨基作用,将抗体固定在工作电极上。
5)为降低非特异性吸附,最后用牛血清白蛋白封闭多余的活性位点。
差分电极52与工作电极53的区别仅仅在于工作电极53固定抗体,而差分电极52不固定抗体,即差分电极52的制备的流程与工作电极53的制备流程基本一致,仅仅去除步骤4)。
工作电极层差分电极52与工作电极53分别和辅助工作电极中的对电极45和参比电极44构成三电极体系,检测时,采用分时复用的方式,按次序分别扫描各个差分电极及工作电极。首先对差分电极进行扫描,记录得到的差分光信号,然后依次扫描3个工作电极,对获得的光信号与差分光信号进行差分,分别获得对应每一工作电极的检测信号,这可以减小干扰,提高一致性。
不同工作电极53上可以固定不同性激素抗体,例如三个工作电极53分别对应固定lh、fsh和e2性激素的抗体,每一工作电极扫描时检测对应性激素的含量。
图5为图1中第一移动隔离层的结构示意图,如图5所示,第一移动隔离层30同样可以采用whatman1号滤纸作为基底材料,包括第一固定部分31和可相对于第一固定部分31移动的第一移动部分32,第一固定部分31上设置有n个与第一通孔42一一正对设置的第二通孔311,第一移动部分32上设置有与第一中心分流区41对应设置的第二中心分流区321,第一固定部分31粘结至固定至辅助电极层40,第一移动部分32可以相对于第一固定部分31在流通位置和隔离位置之间移动。当第一移动部分32相对于第一固定部分31位于流通位置时,如图5中(a)所示,第二中心分流区321与第一中心分流区41正对设置,保证待测液体的流路畅通,当第一移动部分32相对于第一固定部分31位于隔离位置时,如图5中(b)所示,第二中心分流区321与第一中心分流区41错位设置,隔断流路。
图6为图1中第二移动隔离层的结构示意图,如图6所示,第二移动隔离层60同样可以采用whatman1号滤纸作为基底材料,包括第二固定部分61和可相对于第二固定部分61移动的第二移动部分62,第二移动部分62上设置有n个与第一亲水区51一一对应设置的第二亲水区621,第一固定部分61粘结至固定至工作电极层50,第一移动部分62可以相对于第一固定部分61在流通位置和隔离位置之间移动。当第二移动部分62相对于第二固定部分61位于流通位置时,如图6中(a)所示,第二亲水区621与第一亲水区51正对设置,保证待测液体的流路畅通,当第二移动部分62相对于第二固定部分61位于隔离位置时,如图6中(b)所示,第二亲水区621与第一亲水区51错位设置。
图7为图1中加样过滤层的结构示意图,如图7所示,加样过滤层20采用whatman公司的plasmaseparation膜lf1(为一种滤纸)作为基材,这种膜可以有效地截流血液中的红细胞白细胞,减小血液对检测的干扰,包括第三中心分流区21及位于第三中心分流区21周围均匀排布的n个第三通孔22,其中第三中心分流区21与第一中心分流区41正对设置,n个第三通孔22分别与n个第二通孔42一一正对设置,加样过滤层20还包括与第三中心分流区21联通的加样口23,采用毛细作用将待测液体引入第三中心分流区21。可以采用以下流程制备:
1)采用截图机将滤纸裁成a4大小;
2)采用喷蜡打印机对滤纸进行喷蜡打印喷蜡区,第三中心分流区和加样口不喷蜡。3)采用精确数控加热仪器加热处理打印好的滤纸,使蜡融化形成喷蜡区、第三中心分流区和加样口。
3)进行裁剪,获得多个加样过滤层。
在其实施例中加样过滤层20可以采用常规材料作为基底材料,仅在第三中心分流区21上设置过滤膜,用于过滤截留液体中的细胞。
图8为图1中吸水层的结构示意图,如图8所示,吸水层70位于微流控纸芯片100最下层,采用吸水材料制成,包括n个与第一亲水区51一一正对设置的第三亲水区71以及吸水区72,所述吸水区72与每个第三亲水区71相连通,吸水区72可以通过中央汇集区73与各第三亲水区72相连通。主要作用作为待测液收集槽,为液体流动提供动力,并容置多余的待测液。
图9为图1中覆盖层的结构示意图,如图9所示,覆盖层10包括n个与第三通孔21一一正对设置的第四通孔11,即第四通孔11位置与加样过滤层20的第三通孔21、第一移动隔离层30的第二通孔311、辅助电极层40的第一通孔42及工作电极层40的差分电极和工作电极对准,作用是防止工作电极的发光被遮挡。覆盖膜10可以选用的单面胶材料,具有粘接作用和疏水特性,可以粘结至加样过滤层20,防止待测液体散溢及避免加样过滤层被外界污染。
在本实施例中,待测液体从加样过滤膜20的加样口23流到第三中心分流区21,经由第一移动隔离层30的第二中心分流区321,流至辅助电极层40的第一中心分流区41,然后通过连接通路43经由第一通孔42分别流向工作电极层50的3个工作电极53和1个差分电极。液体中的待测物和工作电极53上固定的抗体反应,当抗原和抗体结合后会改变电极表面空间位阻,抑制电子转移,降低电化学反应信号,造成发光光强的降低,通过检测光强的变化可以得到待测物的浓度。
本发明另一实施例提供一种检测系统1000,图10为本发明另一实施例检测系统的结构示意图。如图10所示,检测系统1000,包括:微流控纸芯片100;电化学控制模块200、顶部开口的盒体300以及检测装置400.其中,电化学控制模块200,用于向微流控纸芯片输入检测信号;顶部开口的盒体300,容置电化学模块和所述微流控纸芯片;检测装置400,用于封闭所述盒体的顶部开口,并控制所述电化学控制模块输出检测信号,以及检测所述微流控纸芯片发出的光信号,分析待测液体性激素的含量。
具体地,顶部开口的盒体300可选用壳式手机接口,检测装置400可以采用智能手机,壳式手机接口可以采用3d打印机制备,保证接口与手机紧密相连防止外界光的干扰以及作为载体固定电化学控制模块200和微流控纸芯片100。智能手机的摄像头可用于检测微流控纸芯片发出的光信号,且智能手机具控制和计算功能,用于提供控制信号,并根据摄像头检测到的光信号分析出测量结果。
图11为图10中检测系统的检测原理示意图,如图11所示,电化学控制模块200包括蓝牙通信模块201、中央控制器202、电信号输出模块203和电极接口204,蓝牙通信模块201主要实现电化学控制模块201和智能手机的无线通信,从智能手机获得控制信号,并将状态信息回传手机;中央控制器202进行信号处理和行为控制;电信号输出模块203根据要求输出指定的用于激发电化学物质发光的电信号,通过电极接口204与微流控纸芯片100相连。电信号输出模块203包括多个工作电极通路(本实例中为三个)、一个差分电极通路和一对复用的对电极和参比电极通路。三个工作电极通路分别与微流控纸芯片100不同的工作电极相连,在不同时间段激发不同的通路,保证待测通路的电极受激发发光,而其他通路不发光,这样就可以避免不同通路的交叉干扰。本检测系统分利用智能手机的拍照和运算功能实现电化学发光检测。通过蓝牙发送信号控制电化学控制模块的电信号输出,通过自带的光学传感器例如摄像头进行光信号检测,并通过计算分析获得待测物的浓度。
需要说明的是,在附图或说明书正文中,未绘示或描述的实现方式,均为所属技术领域中普通技术人员所知的形式,并未进行详细说明。此外,上述对各元件和方法的定义并不仅限于实施例中提到的各种具体结构、形状或方式,本领域普通技术人员可对其进行简单地更改或替换。
以上所述的具体实施例,对本发明的目的、技术方案和有益效果进行了进一步详细说明,应理解的是,以上所述仅为本发明的具体实施例而已,并不用于限制本发明,凡在本发明的精神和原则之内,所做的任何修改、等同替换、改进等,均应包含在本发明的保护范围之内。
- 还没有人留言评论。精彩留言会获得点赞!