一种应用于工业级电流密度下海水电解制氢的阳极催化电极及其制备方法与应用
1.本发明属于纳米材料制备和清洁能源领域,具体涉及一种应用于工业级电流密度下海水电解制氢的阳极催化电极及其制备方法与应用。
背景技术:
2.公开该背景技术部分的信息仅仅旨在增加对本发明的总体背景的理解,而不必然被视为承认或以任何形式暗示该信息构成已经成为本领域一般技术人员所公知的现有技术。
3.氢(h2)作为一种可持续和安全能源,具有142.351mj kg-1
的能量密度且不排放任何污染,对于解决当前紧迫的环境危机和化石能源供应不足至关重要。电解水制氢在处理效率、可再生能源兼容性和生产高纯氢气的碳中和方面优于传统的石油化工技术,因此电解水制氢成为未来一种有吸引力的可再生能源存储解决方案。电解水制氢除了阴极析氢半反应(her),还必须包括阳极半反应,一般为析氧反应(oer)。然而由于其缓慢的、多步骤的质子耦合电子转移过程,极大地阻碍了电解水产氢的整体效率,因此,开发高活性和稳定的oer催化电极是电解水产氢的关键。
4.电解水制氢的另一个重大问题是自然界淡水资源缺乏,使用淡水作为电解水产氢的电解液将对重要的水资源带来沉重的压力。海洋占据了地球96.5%的水储备,提供了无限的氢资源,而不会对全球淡水资源造成严重影响,是未来电解水制氢的有前景的电解液。然而,海水中多种金属离子的干扰,导致海水电解制氢oer电催化剂的活性和稳定性都不理想,一直不能满足工业化的需求。特别是天然海水中存在的氯阴离子(cl-,约0.5m),会在阳极导致析氯副反应(cler),与oer竞争。虽然oer具有热力学优势,但其复杂的四电子转移反应比只有两个电子的cler反应动力学更为迟缓。在碱性条件下(ph》7.5),cl-与oh-进一步反应生成次氯酸盐(cl-+2oh-→
clo-+h2o+2e-),保持了与oer的最大热力学电位差(约480mv),为oer提供了一个方便的选择性电位差窗口。综上所述,碱性条件有利于海水的选择性氧化,oer催化剂如果在480mv过电位之前实现工业级高电流密度输出就可以避免次氯酸盐的形成。此外,氯化物腐蚀和不溶性沉淀物或微生物的中毒也会损害电极材料的稳定性和使用寿命,这对电极材料的结构稳定性和耐腐蚀性提出了更高的要求。然而,到目前为止,要减小极化过电位,需要在远低于工业标准的电流密度(500-1000ma cm-2
)下进行电解(《200ma cm-2
)。因此,为满足工业级应用,开发能够在超低电位下(低于480mv)驱动大电流密度(500-1000ma cm-2
)并保持良好稳定性的oer电催化剂非常有必要和具有挑战性。
技术实现要素:
5.为了解决现有技术的不足,本发明的目的是提供一种应用于工业级电流密度下海水电解制氢的阳极催化电极及其制备方法与应用,本发明提供的阳极催化电极在安培级电流密度下持续稳定的产氢而不受cl-氧化等副反应的影响。
6.为了实现上述目的,本发明的技术方案为:
7.第一方面,提供了一种应用于工业级电流密度下海水电解制氢的阳极催化电极,其特征在于,所述阳极催化电极以金属泡沫作为三维载体,三维载体表面原位生长有钴掺杂的硫化镍阵列,在列阵表面覆盖一层含空位的高活性硫保护层。
8.第二方面,提供了上述应用于工业级电流密度下海水电解制氢的阳极催化电极的制备方法,包括以下步骤:
9.步骤1:称取钴盐、镍盐和尿素溶于去离子水中形成溶液;
10.步骤2:将金属泡沫置于步骤1的溶液中,密闭反应,得到钴掺杂的氢氧化镍前驱体;
11.步骤3:将步骤2得到的前驱体加入含有硫盐的水溶液中,密闭反应,得到钴掺杂的硫化镍前驱体;
12.步骤4:将步骤3得到的前驱体加入双氧水溶液中,反应即得。
13.本发明的应用于工业级电流密度下海水电解制氢的阳极催化电极,在安培级电流密度下持续稳定的产氢而不受cl-氧化等副反应的影响,因而第三方面,提供了上述应用于工业级电流密度下海水电解制氢的阳极催化电极在海水电解制氢中的应用。
14.本发明的有益效果为:
15.(1)本发明的阳极催化电极的合成均在较低温度下进行,易于操作和批量制备;且该方法适用于不同三维基底,是一种普适的硫化物材料阵列的合成方法,适合大规模的工业化生产。
16.(2)本发明所制备的阳极催化电极具有多级孔纳米通道,可以快速促进物质的转移和运输;同时原位生长的纳米阵列有助于提高材料催化过程的稳定性和电子的快速传输;阳极催化电极材料表面轻松形成的阴离子硫空位可调节活性位点的电子结构,从而提高表面高度不协调的钴原子的本征电催化析氧活性;表面硫保护层可以抑制氯离子在材料表面析出,使得阳极催化电极在模拟海水中表现出优异的稳定性。综上,本发明的阳极催化电极具有高的本征催化活性、高暴露的活性位点、快速的质子和气体传质速率和抑制氯离子在表面的吸附。
17.(3)本发明所制备的阳极催化电极在析氯电位(480mv)之前就展现了优异的工业级电流密度,避免了析氯副反应,解决了高电流密度产生氯气副产物等问题,可实现工业化海水电解产氢。
附图说明
18.构成本发明的一部分的说明书附图用来提供对本发明的进一步理解,本发明的示意性实施例及其说明用于解释本发明,并不构成对本发明的不当限定。
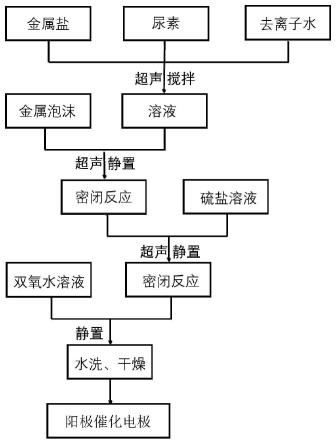
19.图1是本发明钴掺杂硫化镍阵列制备的合成路线示意图;
20.图2是本发明实施例1所制备的钴掺杂硫化镍(conis-60)阵列的场发射扫描电镜图;
21.图3是本发明实施例2所制备的钴掺杂硫化镍(conis-30)阵列的场发射扫描电镜图;
22.图4是本发明实施例3所制备的钴掺杂硫化镍(conis-90)阵列的场发射扫描电镜
图;
23.图5是本发明对比例1所制备的钴掺杂硫化镍(conis)阵列的场发射扫描电镜图;
24.图6是本发明实施例1所制备的钴掺杂硫化镍(conis-60)阵列的x射线衍射图;
25.图7是本发明实施例1所制备的钴掺杂硫化镍(conis-60)阵列、对比例1所制备的钴掺杂硫化镍(conis)阵列、以及商用的ruo2、nf在1m koh电解液中氧析出反应的线性扫描伏安曲线;
26.图8是本发明实施例1所制备的钴掺杂硫化镍(conis-60)阵列、对比例1所制备的钴掺杂硫化镍(conis)阵列、实施例2所制备的钴掺杂硫化镍(conis-30)阵列和实施例3所制备的钴掺杂硫化镍(conis-90)阵列在1mkoh电解液中氧析出反应的线性扫描伏安曲线;
27.图9是商用的nf、ruo2、conis、conis-60在1m koh电解液中氧析出反应的tafel曲线;
28.图10是本发明实施例1所制备的钴掺杂硫化镍(conis-60)阵列、对比例1所制备的钴掺杂硫化镍(conis)阵列、实施例2所制备的钴掺杂硫化镍(conis-30)阵列和实施例3所制备的钴掺杂硫化镍(conis-90)阵列在1mkoh电解液中氧析出反应的tafel曲线;
29.图11是本发明实施例1所制备的钴掺杂硫化镍(conis-60)阵列、对比例1所制备的钴掺杂硫化镍(conis)阵列、以及商用的ruo2、nf在1m koh+0.5m nacl(模拟海水)电解液中氧析出反应的线性扫描伏安曲线;
30.图12是本发明实施例1所制备的钴掺杂硫化镍(conis-60)阵列、对比例1所制备的钴掺杂硫化镍(conis)阵列、实施例2所制备的钴掺杂硫化镍(conis-30)阵列和实施例3所制备的钴掺杂硫化镍(conis-90)阵列在1mkoh+0.5m nacl(模拟海水)电解液中氧析出反应的线性扫描伏安曲线;
31.图13是本发明实施例1所制备的钴掺杂硫化镍(conis-60)阵列、对比例1所制备的钴掺杂硫化镍(conis)阵列、以及商用的ruo2、nf在1m koh+0.5m nacl(模拟海水)电解液中氧析出反应的tafel曲线;
32.图14是本发明实施例1所制备的钴掺杂硫化镍(conis-60)阵列、对比例1所制备的钴掺杂硫化镍(conis)阵列、实施例2所制备的钴掺杂硫化镍(conis-30)阵列和实施例3所制备的钴掺杂硫化镍(conis-90)阵列在1mkoh+0.5m nacl(模拟海水)电解液中氧析出反应的tafel曲线;
33.图15是本发明实施例1所制备的钴掺杂硫化镍(conis-60)阵列、对比例1所制备的钴掺杂硫化镍(conis)阵列、以及商用的ruo2、nf在1m koh+海水(碱性海水)电解液中氧析出反应的线性扫描伏安曲线;
34.图16是本发明实施例1所制备的钴掺杂硫化镍(conis-60)阵列、对比例1所制备的钴掺杂硫化镍(conis)阵列、实施例2所制备的钴掺杂硫化镍(conis-30)阵列和实施例3所制备的钴掺杂硫化镍(conis-90)阵列在1mkoh+海水(碱性海水)电解液中氧析出反应的线性扫描伏安曲线;
35.图17是本发明实施例1所制备的钴掺杂硫化镍(conis-60)阵列、对比例1所制备的钴掺杂硫化镍(conis)阵列、以及商用的ruo2、nf在1m koh+海水(碱性海水)电解液中氧析出反应的tafel曲线;
36.图18是本发明实施例1所制备的钴掺杂硫化镍(conis-60)阵列、对比例1所制备的
钴掺杂硫化镍(conis)阵列、实施例2所制备的钴掺杂硫化镍(conis-30)阵列和实施例3所制备的钴掺杂硫化镍(conis-90)阵列在1mkoh+海水(碱性海水)电解液中氧析出反应的tafel曲线;
37.图19是本发明实施例1所制备的钴掺杂硫化镍(conis-60)阵列在1m koh,1m koh+0.5m nacl(模拟海水)和1m koh+海水(碱性海水)电解液中氧析出反应的线性扫描伏安曲线;
38.图20是本发明实施例1所制备的钴掺杂硫化镍(conis-60)阵列在1m koh,1m koh+0.5m nacl(模拟海水)和1m koh+海水(碱性海水)电解液中氧析出反应的tafel曲线;
39.图21是本发明实施例1所制备的钴掺杂硫化镍(conis-60)阵列在1m koh+海水(碱性海水)电解液中氧析出反应电流密度随时间变化的稳定性曲线。
具体实施方式
40.鉴于目前为满足工业级应用,开发能够在超低电位下(低于480mv)驱动大电流密度(500-1000ma cm-2
)并保持良好稳定性的oer电催化剂非常有必要,本发明提出了应用于工业级电流密度下海水电解制氢的阳极催化电极及其制备方法与应用。
41.本发明的一种典型实施方式,提供了一种应用于工业级电流密度下海水电解制氢的阳极催化电极,所述阳极催化电极以金属泡沫作为三维载体,三维载体表面原位生长有钴掺杂的硫化镍阵列,在列阵表面覆盖一层含空位的高活性硫保护层。
42.该实施方式的一些实施例中,所述金属泡沫包括泡沫镍、泡沫铜、泡沫镍铁、泡沫钴。
43.该实施方式的一些实施例中,钴掺杂的硫化镍列阵和含空位的高活性硫保护层中,钴的含量为0%-10%,镍的含量为40%-50%,硫的含量为30%-50%,空位的含量占硫含量的0%-10%,摩尔比。
44.本发明的另一种典型实施方式,提供了上述应用于工业级电流密度下海水电解制氢的阳极催化电极的制备方法,包括以下步骤:
45.步骤1:称取钴盐、镍盐和尿素溶于去离子水中形成溶液;
46.步骤2:将金属泡沫置于步骤1的溶液中,密闭反应,得到钴掺杂的氢氧化镍前驱体;
47.步骤3:将步骤2得到的前驱体加入含有硫盐的水溶液中,密闭反应,得到钴掺杂的硫化镍前驱体;
48.步骤4:将步骤3得到的前驱体加入双氧水溶液中,反应即得。
49.该实施方式的一些实施例中,钴盐、镍盐选自任一种可溶性金属盐。
50.其中,钴盐:镍盐的摩尔比为1:1-50;
51.该实施方式的一些实施例中,步骤1的溶液中,金属盐的总摩尔浓度为50-200mm。
52.其中,尿素与金属盐的摩尔比为1:1-10。
53.该实施方式的一些实施例中,步骤2中,反应温度为100-200℃,反应时间为2-72h。
54.该实施方式的一些实施例中,步骤3中,反应温度为100
ꢀ‑
200℃,反应时间为2-72h。
55.该实施方式的一些实施例中,所述硫盐包括硫化钠、硫代乙酰胺、硫脲、硫粉。
56.该实施方式的一些实施例中,含有硫盐的水溶液中硫盐的摩尔浓度为0.2-1m。
57.该实施方式的一些实施例中,所述双氧水溶液浓度为3%-30%,体积百分数。
58.该实施方式的一些实施例中,步骤4中反应温度为0-60℃,优选为25℃;反应时间为10s-20min。
59.该实施方式的一些实施例中,步骤4中,反应结束后,用去离子水冲洗,得到具有表面空位的钴掺杂的硫化镍电极。
60.本发明的第三种典型实施方式,提供上述应用于工业级电流密度下海水电解制氢的阳极催化电极在海水电解制氢中的应用。
61.该实施方式的一些实施例中,所述应用为阳极催化电极作为电催化海水电解产氢装置的阳极。
62.为了使得本领域技术人员能够更加清楚地了解本发明的技术方案,以下将结合具体的实施例详细说明本发明的技术方案。
63.实施例1:应用于工业级电流密度下海水电解制氢的阳极催化电极的制备方法
64.步骤一:将按照化学计量比称取的硝酸镍、硝酸钴和尿素加入40ml去离子水中,搅拌均匀形成混合溶液;混合溶液中硝酸镍浓度为150mm,硝酸钴浓度为10mm,尿素浓度为900mm;
65.步骤二:将3*3cm2的泡沫金属置于步骤一所配置的溶液中,在120℃下的密闭容器中反应6h;
66.步骤三:将步骤二得到的金属泡沫加入40ml浓度为625mm的硫化钠水溶液中,在120℃下的密闭容器中反应8h;
67.步骤四:将步骤三得到的金属泡沫在25℃加入至20ml浓度为30%的双氧水溶液中,静置反应60s后用去离子水冲洗,得到conis-60阳极催化电极。
68.所得conis-60阳极催化电极的场发射扫描电镜图如图2所示,表明催化电极的形貌为纳米片阵列包裹的有序纳米棒排列形成的多级阵列结构。多级阵列结构有助于电荷的转移和气体的扩散,同时二维纳米片可以暴露更多的活性面积。纳米片和纳米棒之间强的粘附有助于催化剂活性的提高和稳定性的增强。
69.x射线衍射图如图6所示,具有良好的结晶性,与pdf卡片比较证明其单一ni3s2相。
70.在1m koh电解液中氧析出线性扫描伏安曲线如图7所示,在500和1000ma cm-2
的过电位分别为308mv和336mv,比商业ruo2分别低238mv和333mv。在1m koh电解液中氧析出tafel曲线如图9所示,conis-60的tafel斜率仅为113mv dec-1
,远低于商业ruo2(208mv dec-1
)。
71.在1m koh+0.5m nacl(模拟海水)电解液中氧析出线性扫描伏安曲线如图11所示,在500和1000ma cm-2
的过电位分别为285mv和316mv,比商业ruo2分别低311mv和398mv。在1m koh+0.5m nacl(模拟海水)电解液中氧析出tafel曲线如图13所示,conis-60的tafel斜率仅为108mv dec-1
,远低于商业ruo2(225mv dec-1
)。
72.在1m koh+海水(碱性海水)电解液中氧析出线性扫描伏安曲线如图15所示,在500和1000ma cm-2
的过电位分别为334mv和373mv,而商业ruo2在过电位为700mv依旧没有达到500ma cm-2
。在1m koh+海水(碱性海水)电解液中氧析出tafel曲线如图17所示,conis-60的tafel斜率仅为120mv dec-1
,远低于商业ruo2(310mv dec-1
),表明conis-60具有优异的析氧
动力学。
73.进一步,综合比较conis-60在1m koh,1m koh+0.5m nacl(模拟海水)和1m koh+海水(碱性海水)中的析氧性能。如图19所示,conis-60在1m koh+0.5m nacl(模拟海水)的性能优于1m koh,进一步优于1mkoh+海水(碱性海水)中的性能。但是,总体上三者差别不大,说明conis-60可以抗cl-等干扰。如图20所示,tafel斜率在1m koh,1m koh+0.5m nacl(模拟海水)和1m koh+海水(碱性海水)中分别为113mv dec-1
,108mv dec-1
和120mv dec-1
,具有较小的动力学差异。在1m koh+海水(碱性海水)中运行100h后没有明显的电流密度降低,表明conis-60具有优异的海水电解析氧稳定性。
74.实施例2:应用于工业级电流密度下海水电解制氢的阳极催化电极的制备方法
75.步骤一:将按照化学计量比称取的硝酸镍、硝酸钴和尿素加入40ml去离子水中,搅拌均匀形成混合溶液;混合溶液中硝酸镍浓度为150mm,硝酸钴浓度为10mm,尿素浓度为900mm;
76.步骤二:将3*3cm2的泡沫金属置于步骤一所配置的溶液中,在120℃下的密闭容器中反应6h;
77.步骤三:将步骤二得到的金属泡沫加入40ml浓度为625mm的硫化钠水溶液中,在120℃下的密闭容器中反应8h;
78.步骤四:将步骤三得到的金属泡沫在25℃加入至20ml浓度为30%的双氧水溶液中,静置反应30s后用去离子水冲洗,得到conis-30阳极催化电极。
79.所得conis-30阳极催化电极的场发射扫描电镜图如图3所示,表明催化电极的形貌为纳米片阵列包裹的有序纳米棒排列形成的多级阵列结构。
80.在1m koh电解液中氧析出线性扫描伏安曲线如图8所示,在500和1000macm-2
的过电位分别为372mv和454mv。在1m koh电解液中氧析出tafel曲线如图10所示,conis-30的tafel斜率为132mv dec-1
,低于商业ruo2(208mv dec-1
)。
81.在1m koh+0.5m nacl(模拟海水)电解液中氧析出线性扫描伏安曲线如图12所示,在500和1000macm-2
的过电位分别为325mv和359mv。在1mkoh+0.5m nacl(模拟海水)电解液中氧析出tafel曲线如图14所示,conis-30的tafel斜率仅为114mv dec-1
,远低于商业ruo2(225mv dec-1
)。
82.在1m koh+海水(碱性海水)电解液中氧析出线性扫描伏安曲线如图16所示,在500和1000ma cm-2
的过电位分别为408mv和503mv。在1m koh+海水(碱性海水)电解液中氧析出tafel曲线如图18所示,conis-30的tafel斜率仅为151mv dec-1
。
83.实施例3:应用于工业级电流密度下海水电解制氢的阳极催化电极的制备方法
84.步骤一:将按照化学计量比称取的硝酸镍、硝酸钴和尿素加入40ml去离子水中,搅拌均匀形成混合溶液;混合溶液中硝酸镍浓度为150mm,硝酸钴浓度为10mm,尿素浓度为900mm;
85.步骤二:将3*3cm2的泡沫金属置于步骤一所配置的溶液中,在120℃下的密闭容器中反应6h;
86.步骤三:将步骤二得到的金属泡沫加入40ml浓度为625mm的硫化钠水溶液中,在120℃下的密闭容器中反应8h;
87.步骤四:将步骤三得到的金属泡沫在25℃加入至20ml浓度为30%的双氧水溶液
中,静置反应90s后用去离子水冲洗,得到conis-90阳极催化电极。
88.所得conis-90阳极催化电极的场发射扫描电镜图如图4所示,表明催化电极的形貌为团聚的纳米颗粒。
89.在1m koh电解液中氧析出线性扫描伏安曲线如图8所示,在500和1000ma cm-2
的过电位分别为365mv和441mv。在1m koh电解液中氧析出tafel曲线如图10所示,conis-90的tafel斜率为132mv dec-1
,低于商业ruo2(208mv dec-1
)。
90.在1m koh+0.5m nacl(模拟海水)电解液中氧析出线性扫描伏安曲线如图12所示,在500和1000ma cm-2
的过电位分别为327mv和361mv。在1mkoh+0.5m nacl(模拟海水)电解液中氧析出tafel曲线如图14所示,conis-90的tafel斜率仅为113mv dec-1
,远低于商业ruo2(225mv dec-1
)。
91.在1m koh+海水(碱性海水)电解液中氧析出线性扫描伏安曲线如图16所示,在500和1000macm-2
的过电位分别为399mv和508mv。在1m koh+海水(碱性海水)电解液中氧析出tafel曲线如图18所示,conis-90的tafel斜率仅为152mv dec-1
。
92.对比例1:一种阳极催化电极的制备方法
93.步骤一:将按照化学计量比称取的硝酸镍、硝酸钴和尿素加入40ml去离子水中,搅拌均匀形成混合溶液;混合溶液中硝酸镍浓度为150mm,硝酸钴浓度为10mm,尿素浓度为900mm;
94.步骤二:将3*3cm2的泡沫金属置于步骤一所配置的溶液中,在120℃下的密闭容器中反应6h;
95.步骤三:将步骤二得到的金属泡沫加入40ml浓度为625mm的硫化钠水溶液中,在120℃下的密闭容器中反应8h,得到conis阳极催化电极。
96.所得conis阳极催化电极的场发射扫描电镜图如图5所示,表明催化电极的形貌为有序纳米棒排列形成的阵列结构。
97.在1m koh电解液中氧析出线性扫描伏安曲线如图8所示,在500和1000macm-2
的过电位分别为394mv和498mv。在1m koh电解液中氧析出tafel曲线如图10所示,conis的tafel斜率为183mv dec-1
,低于商业ruo2(208mv dec-1
)。
98.在1m koh+0.5m nacl(模拟海水)电解液中氧析出线性扫描伏安曲线如图12所示,在500和1000macm-2
的过电位分别为353mv和420mv。在1mkoh+0.5m nacl(模拟海水)电解液中氧析出tafel曲线如图14所示,conis的tafel斜率仅为141mv dec-1
,远低于商业ruo2(225mv dec-1
)。
99.在1m koh+海水(碱性海水)电解液中氧析出线性扫描伏安曲线如图16所示,在500和1000macm-2
的过电位分别为405mv和505mv。在1m koh+海水(碱性海水)电解液中氧析出tafel曲线如图18所示,conis的tafel斜率为185mv dec-1
。
100.以上所述仅为本发明的优选实施例而已,并不用于限制本发明,对于本领域的技术人员来说,本发明可以有各种更改和变化。凡在本发明的精神和原则之内,所作的任何修改、等同替换、改进等,均应包含在本发明的保护范围之内。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1