一种枳壳药材指纹图谱的检测方法及标准指纹图谱与流程
本发明属于药物分析
技术领域:
,特别涉及一种枳壳药材指纹图谱及其建立方法。具体地,本发明涉及一种枳壳药材的高效液相色谱(HPLC)切换波长法指纹图谱及其建立方法,以及枳壳的标准指纹图谱。本发明还涉及一种枳壳药材质量优劣的鉴别方法。
背景技术:
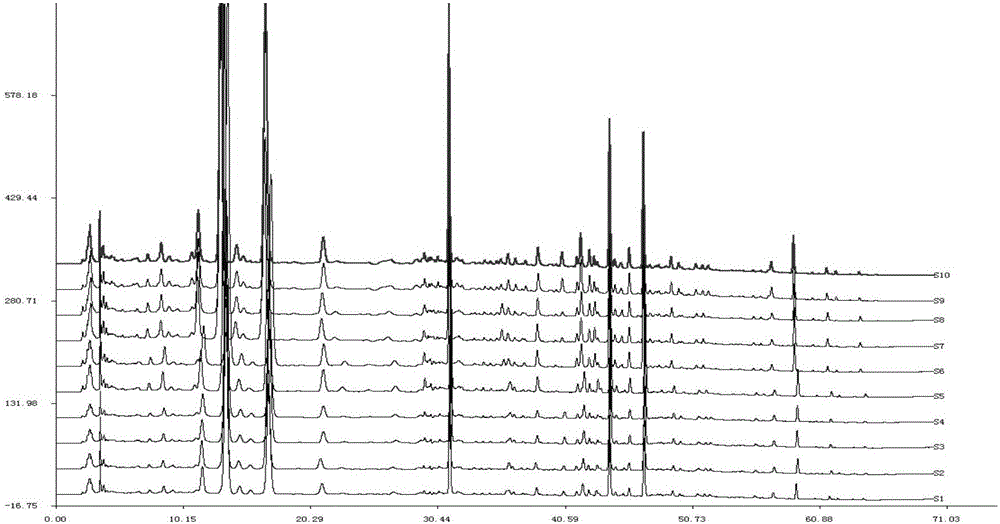
:枳壳为芸香科柑橘属植物酸橙CitrusaurantiumL及其栽培变种的干燥未成熟果实。《中国药典》2015年版收载的栽培变种为黄皮酸橙(Citrusaurantium‘Huangpi’)、塘橙(Citmsaurantium‘Tangcheng’)、朱栾(Citrusaurantium‘Chuluan’)、代代花(Citrusaurantium‘Daidai’)的干燥未成熟果实,枳壳为7月果皮尚绿时采收,是常用中药材。枳壳味苦、辛、酸,温,归脾、胃经,具有行气宽中、消食、化痰等功能,用于胸脘满闷胀痛、食积不化、痰饮、胃下垂、脱肛、子宫脱垂。枳壳药材来源于酸橙和甜橙,由于各产地的地理环境、气候、土壤等生长条件不同以及采收后加工炮制方法不同,使枳实药材在化学成分组成及含量上差异很大,因而直接影响到药材质量。2015版药典规定,以柚皮苷、新橙皮苷作为枳壳质量控制的指标(国家药典委员会编,中华人民共和国药典2015年版,北京:中国医药工业出版社,2015,一部:246),采用两个指标成分进行中药质量控制的方法不能全面反映中药内在化学成分的种类和数量,存在一定局限性,不能全面控制药材质量。枳壳中的主要活性成分为挥发油、黄酮类化合物和少量生物碱类化合物,其药理作用应该是多种成分综合作用的结果。因此仅以单一成分或几个主要有效成分来控制和评价枳壳的质量是不全面的。而指纹图谱作为一种综合的、可量化的评价中药质量的检测手段,恰好适用于对中药多成分的质量评价。针对枳壳的研究主要涉及栽培技术与提取分离技术,质量检测方法公开较少,如中国专利201410837547.7(公开号CN104587014A)涉及的质量检测方法主要是对枳壳提取物进行总黄酮检测,不是对枳壳药材进行检测,也没有对质量进行全面控制,仅测定了总黄酮总类成分。《海峡药学》2003年第6期《绿衣枳壳指纹图谱的研究》记载了一种应用气相色谱(GC)测定绿衣枳壳中挥发油指纹图谱的方法;《中国药学杂志》2005年第11期《中药积壳HPLC指纹图谱分析及化学模式识别分类研究》记载了应用高效液相(HPLC)测定枳壳的指纹图谱方法,但仅有8个共有峰且仅指认柚皮苷、橙皮苷、新橙皮苷等三个指标成分;《中草药》2009年第3期《不同栽培品种枳壳HPLC指纹图谱研究》记载了测定枳壳的HPLC指纹图谱方法,但仅采用单一波长,没有对共有峰进行指标成分指认;《中国中药杂志》2008年第20期《不同产地和品种枳壳药材的毛细管电泳指纹图谱研究》记载了应用毛细管电泳测定枳壳的指纹图谱方法;《中国现代中药》2009年第12期《麸炒积壳HPLC指纹图谱的研究》记载了应用高效液相色谱测定枳壳炮制品的指纹图谱方法,但仅采用单一波长测定,仅鉴定了柚皮苷、新橙皮苷、橙皮苷3个特征峰;《中国现代应用药学》2015年第4期《市售枳壳饮片的质量调查与指纹图谱研究》记载了应用高效液相色谱测定枳壳饮片的指纹图谱方法,采用单一波长仅有5个共有峰且仅指认芸香柚皮苷、柚皮苷、橙皮苷、新橙皮苷等四个指标成分。现有技术中,鉴定的指标成分少,不能全面反映药材的质量优劣,保证用药的疗效,因此,建立枳壳药材的指纹图谱检测方法及标准指纹图谱方法具有非常重要的意义。技术实现要素:本发明所要解决的技术问题是提供一种枳壳指纹图谱的测定方法,该方法在控制枳壳的质量,有效的指导临床和生产中使用、保证用药的有效、安全和可靠具有积极作用。建立的方法和枳壳药材HPLC标准指纹图谱能够用于鉴定或者鉴别枳壳药材质量真伪优劣,具有较高的可信度和极高的灵敏度。由此提供了下述发明:本发明的一种枳壳药材指纹图谱的检测方法,包括以下步骤:(1)供试品溶液的制备:取枳壳药材粗粉,精密称定,加入甲醇,超声或回流提取,提取液以微孔膜过滤,取续滤液,即得供试品溶液;(2)对照品溶液的制备:分别取芸香柚皮苷对照品、柚皮苷对照品、橙皮苷对照品、新橙皮苷对照品、柠檬苦素对照品、川陈皮素对照品、诺米林对照品、橘红素对照品,精密称定,分别加入甲醇制成对照品溶液;(3)高效液相色谱检测:分别精密吸取供试品溶液和对照品溶液,注入高效液相色谱仪测定,即得枳壳指纹图谱;其中,色谱条件为:采用十八烷基硅烷键合硅胶为填料的色谱柱,4.6×250mm,5μm;柱温:20~40℃;检测波长为280nm、215nm,切换时间为0min、24.01min;进样量为10μl;流速:1.0ml/min;分析时间为70min;流动相为流动相A为乙腈,流动相B为0.1%磷酸溶液;采用梯度洗脱方式:0min→25min→25.01min→35min→60min→70min,乙腈20%→24%→30%→40%→95%→100%。所述步骤(1)的枳壳粗粉与甲醇的比例为0.2g:50ml。所述步骤(1)的超声或回流提取时间为1小时。所述步骤(2)中的对照品溶液具体为:每1ml各含芸香柚皮苷70ng、柚皮苷80ng、橙皮苷40ng、新橙皮苷80ng、柠檬苦素70ng、川陈皮素80ng、诺米林70ng、橘红素60ng的混合溶液。枳壳指纹图谱中12个色谱峰被确定为共有峰,通过与对照品保留时间的比较,确定峰1为芸香柚皮苷,峰2为柚皮苷,峰3为橙皮苷,峰4为新橙皮苷,峰8为柠檬苦素,峰9为川陈皮素,峰10为诺米林,峰11为橘红素,所述指纹图谱的12个共有指纹峰的相对保留时间范围及相对标准偏差如下:1号峰:0.680~0.692,RSD为0.68%;2号峰:0.789~0.804,RSD为0.92%;3号峰:0.862~0.877,RSD为0.75%;4号峰:1,RSD为0%;5号峰:1.277~1.296,RSD为0.51%;6号峰:1.893~1.924,RSD为0.74%;7号峰:2.322~2.345,RSD为0.65%;8号峰:2.530~2.547,RSD为1.02%;9号峰:2.670~2.696,RSD为0.84%;10号峰:2.765~2.828,RSD为0.34%;11号峰:2.834~2.854,RSD为0.59%;12号峰:3.560~3.571,RSD为0.64%。本发明与现有技术相比,具有以下有益效果:(1)本发明建立的切换波长指纹图谱能够较单波长指纹图谱更全面的反应中药的物质信息,克服了枳壳质量检测方法所检测的有效成分单一,不能全面反应枳壳质量的缺陷。通过波长的转换,增强了指纹峰的可视化比较,指认了8个指标成分,更有效的表征了枳壳的质量信息,更有利于增强对药材的质量监控;(2)本发明获得的标准指纹图谱比较指纹图谱中共有峰的有无,能有效地监控枳壳药材的质量,完善了枳壳药材的质量评价体系,为枳壳药材质量的全面、有效控制提供了理论和实践基础;(3)本发明方法适用于枳壳药材真伪和品质的鉴别,有利于指导投料、规范生产操作,真正确保临床用药的安全、有效、可控;(4)本发明方法操作简便、稳定、重复性好,结论客观、准确。附图说明图1为枳壳药材标准指纹图谱,其中峰1为芸香柚皮苷,峰2为柚皮苷,峰3为橙皮苷,峰4为新橙皮苷,峰8为柠檬苦素,峰9为川陈皮素,峰10为诺米林,峰11为橘红素。图2为10个批次枳壳药材指纹图谱。图3为8个对照品混合溶液图谱。图4为实施例2中检测到的两批质量有问题的药材与标准指纹图谱对比图。具体实施方式下面结合具体实施例,进一步阐述本发明。应理解,这些实施例仅用于说明本发明而不用于限制本发明的范围。此外应理解,在阅读了本发明讲授的内容之后,本领域技术人员可以对本发明作各种改动或修改,这些等价形式同样落于本申请所附权利要求书所限定的范围。本发明药材、对照品来源如下:新橙皮苷对照品(中国食品药品检定研究院、111857-201102);橙皮苷对照品(中国食品药品检定研究院、110738-201337);柚皮苷对照品(中国食品药品检定研究院、110721-201316);柠檬苦素对照品(中国食品药品检定研究院、110800-201400);诺米林对照品(湖北拓楚慷元医药化工有限公司、1163770-201137);川陈皮素对照品(上海纯优生物科技有限公司、487013-201393);橘红素对照品(研域化学试剂有限公司、481538-2015422);芸香柚皮苷对照(南京景竹生物科技有限公司)。10批次采自不同产区的枳壳药材中包括湖南沅江、湖南汉寿、四川遂宁、浙江金华、浙江兰溪、江西新干、江西上高、江西新余;各枳壳药材供试样品来源等基本信息如表1。样品来源样1沅江杨梅山样2沅江赤山样3沅江三眼塘样4汉寿白鹭桥样5四川遂宁样6浙江金华样7浙江兰溪样8江西新干样9江西上高样10江西新余实施例1:枳壳切换波长指纹图谱的建立和验证。1.1仪器与试药:安捷伦1260高效液相色谱仪,含在线真空脱气机器(G-1311C)、二元泵(G-1311C)、标准自动进样器(G-1329B)、智能化柱温箱(G-1316A)、DAD检测器(G-1314B)、Agilent1260Infinity色谱工作站(美国安捷伦科技有限公司);SB-5200D超声波清洗仪(宁波新芝生物科技股份有限公司);FAZ004B分析天平(上海佑科);BT125D电子天平(赛多利斯科学仪器(北京)有限公司)。1.2色谱条件的选择。(1)流动相的选择选择乙腈-0.01%磷酸溶液、乙腈-0.1%磷酸溶液、乙腈-4%磷酸溶液、乙腈-0.01%甲酸溶液、乙腈-0.1%甲酸溶液、、乙腈-4%甲酸溶液、乙腈-0.01%冰醋酸溶液、乙腈-0.1%冰醋酸溶液、、乙腈-4%冰醋酸溶液、等为流动相进行试验,结果表明,上述各溶液为流动相时,色谱峰的峰形均较理想,各峰分离较完全,其中乙腈-0.1%磷酸溶液为流动相时效果最好,故选用乙腈-0.1%磷酸溶液作为最佳流动相。由于样品中成分复杂,在恒流条件下,样品中的各个成分分离度差,较难体现指纹图谱的整体特性;流动相以如下梯度运行,样品中各组分均有较好的分离,基线平稳,故选用该梯度为最佳洗脱梯度,见表2。表2梯度运行表。时间(min)乙腈(%)0.1%磷酸溶液(%)0~2520~2480~7625.01~3530~4070~6035~6040~9560~560~7095~1005~0(2)检测波长的选择通过对供试品进行全波长测定比较,当程序切换波长的程序为0~24min选择300nm波长,24.01~70min选择215nm波长时,极大的增强了指纹峰的可视化,使样品特征峰最丰富。(3)色谱柱的选择通过比较AgilentZORBAXXDB-C18(5μm,4.6×250mm),ThermoSyncronis-C18(5μm,4.6×250mm),Unitary-C18,(5µm,4.6mm×250mm),迪马Diamonsil-C18(5μm,4.6×250mm)4种不同型号规格的色谱柱,结果表明,以上4种品牌的色谱柱均可达到保留时间适中,峰数目较多,分离度好的较理想的色谱效果。(4)柱温的选择考察了不同柱温20℃、25℃、30℃、35℃、40℃时对同一样品的分离效果。结果表明,不同温度对色谱峰的分离影响较小,以20℃~40℃时分离效果都较理想。(5)不同流速的选择在其他色谱条件相同的情况下,分别考察流速为0.8ml/min、1.0ml/min、1.2ml/min对同一样品色谱峰分离的影响。结果表明,当流速为1.0ml/min时,色谱峰保留时间适中,分离度最好,重复性最好。1.3对照品溶液的制备分别精密称取芸香柚皮苷对照品、柚皮苷对照品、橙皮苷对照品、新橙皮苷对照品、柠檬苦素对照品、川陈皮素对照品、诺米林对照品、橘红素对照品,置于容量瓶中,加甲醇溶解并稀释制成每1ml含40ug、70ug、40ug、80ug、40ug、40ug、40ug、80ug的混合溶液,即得对照品溶液。1.4供试品溶液的制备分别取枳壳药材粗粉0.2g,精密称定,置具塞锥形瓶中,精密甲醇50ml,密塞,称定重量,回流提取1h,放冷,再称定重量,用甲醇补足减失的重量,摇匀,滤过,取续滤液,作为供试品溶液。1.5测定法分别精密吸取供试品溶液和对照品溶液10μl,注入高效液相色谱仪,测定。1.6分析时间的确定在上述色谱条件下进样考察120分钟,结果表明,在70分钟内,样品中所有峰均可被完全洗脱出,故分析时间确定为70分钟。1.7枳壳方法学考察。(1)稳定性试验分别取枳壳同一供试品溶液,在上述液相色谱条件下,分别在0、2、4、6、12、24小时进行检测,每次进样10μl,考察主要色谱峰的相对保留时间和相对峰面积的一致性。结果枳壳主要色谱峰的相对保留时间和相对峰面积的RSD<3%,表明供试品溶液24小时内较稳定。(2)精密度试验取同一份枳壳供试品溶液,在上述液相色谱条件下,重复进样6次,每次进样10μl,考察主要色谱峰的相对保留时间和相对峰面积的一致性。结果枳壳主要色谱峰的相对保留时间和相对峰面积的RSD<3%,表明仪器精密度良好。(3)重复性试验取枳壳同一批样品,按供试品制备方法制备6份供试品溶液,在上述液相色谱条件下,进样分析,考察主要色谱峰的相对保留时间和相对峰面积的一致性。结果枳壳主要色谱峰的相对保留时间和相对峰面积的RSD<3%,表明该方法重复性好。1.8枳壳准指纹图谱的制定按拟定的方法制备10批次枳壳药材供试品,依法测定,记录色谱图;用中药色谱指纹图谱相似度评价系统以十批成品指纹图谱为基础获得标准指纹图谱。见图1、2。通过软件匹配,确定12个共有峰,与对照品溶液比较,其中1号峰为芸香柚皮苷,2号峰为柚皮苷,3号峰为橙皮苷,4号峰为新橙皮苷、8号峰为柠檬苦素,9号峰为川陈皮素、10号峰为诺米林、11号峰为橘红素,本发明的标准指纹图谱中包含了枳实中已知的多个化合物,具有高度的可靠性,见附图3。1.9枳壳药材相似度评价以中药色谱指纹图谱相似度评价软件生成的枳壳标准指纹图谱为参照,计算相似度,10批枳壳药材的相似度大于0.90,相似度较好,因此确定为与标准指纹图谱比较,枳壳药材的限度标准定为相似度应大于0.90。结果见表3。表310批枳壳药材HPLC指纹图谱相似度评价结果表。S1S2S3S4S5S6S7S8S9S10对照图谱S11.0000.9190.9590.9150.9040.9610.9880.9580.9650.9060.997S20.9191.0000.9050.9830.9090.9730.9010.9220.9410.9620.939S30.9590.9051.0000.9000.9340.9040.9370.9030.9090.9150.956S40.9150.9830.9001.0000.9230.9730.9060.9560.9050.9530.932S50.9040.9090.9340.9231.0000.9760.9790.9340.9520.9200.905S60.9610.9730.9040.9730.9761.0000.9150.9600.9770.9510.972S70.9880.9010.9370.9060.9790.9151.0000.9900.9800.9470.979S80.9580.9220.9030.9560.9340.9600.9901.0000.9670.9110.945S90.9650.9410.9090.9050.9520.9770.9800.9671.0000.9080.948S100.9060.9620.9150.9530.9200.9510.9470.9110.9081.0000.927对照图谱0.9970.9390.9560.9320.9050.9720.9790.9450.9480.9271.000实施例2:标准指纹图谱在鉴别枳壳药材中的用途。1.1仪器与试药:安捷伦1260高效液相色谱仪,含在线真空脱气机器(G-1311C)、二元泵(G-1311C)、标准自动进样器(G-1329B)、智能化柱温箱(G-1316A)、DAD检测器(G-1314B)、Agilent1260Infinity色谱工作站(美国安捷伦科技有限公司);SB-5200D超声波清洗仪(宁波新芝生物科技股份有限公司);FAZ004B分析天平(上海佑科);BT125D电子天平(赛多利斯科学仪器(北京)有限公司)。1.2枳壳药材HPLC指纹图谱的测定。(1)供试品溶液的制备分别取枳壳药材粗粉0.2g,精密称定,置具塞锥形瓶中,精密甲醇50ml,密塞,称定重量,超声提取1h,放冷,再称定重量,用甲醇补足减失的重量,摇匀,滤过,取续滤液,作为供试品溶液。(2)色谱条件分析:色谱柱为Unitary-C18,(5µm,4.6mm×250mm);柱温:30℃;检测波长为280nm、215nm,切换时间为0min、24.01min;进样量为10μl;流速:1.0ml/min;分析时间为70min;流动相为流动相A为乙腈,流动相B为0.1%磷酸溶液;采用梯度洗脱方式:0min→25min→25.01min→35min→60min→70min,乙腈20%→24%→30%→40%→95%→100%。(3)测定结果分析测定了多批随机购买的枳壳药材,检测到其中2批与枳壳标准指纹图谱比对有明显的共有峰缺失(如附图4,其中3号峰、4号峰、5号峰、9号峰、11号峰缺失)。另外,采用国家药监局颁布的指纹图谱相似度评价软件的相似度评价。结果表明这两批药材与标准指纹图谱的相似度在0.2以下。因此,可以判断该批次枳壳药材质量不合格。根据根据实施例1与对照品溶液比对的色谱峰定性鉴别结果,其中3号峰、4号峰、9号峰、11号峰分别为橙皮苷、新橙皮苷、川陈皮素、橘红素,这些指标成分是枳壳中非常重要的活性成分,这从另一个方面验证了上述“该批次枳壳药材质量不合格”的结论是正确的。因此,通过构建HPLC指纹图谱及分析,可以有效评价枳壳药材的质量状况,达到监控枳壳药材的质量及鉴别真伪的目的。当前第1页1 2 3
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1