一种有机合成色素含量检测方法与流程
本发明涉及质量控制技术领域,特别涉及一种有机合成色素含量检测方法。
背景技术:
合成色素即人工合成的色素,其优点很多,如色泽鲜艳,着色力强,色调多样,可改善商品外观并吸引消费者购买,因此被广泛应用于食品领域。中国允许在食品中添加的合成色素共计28种,合成色素的分类包括有机合成色素、无机合成色素、天然等同合成色素等。其中,有机合成色素通常包括:苋菜红、胭脂红、柠檬黄、新红、赤藓红、诱惑红、日落黄、亮蓝和靛蓝(在食品工业中,靛蓝以其磺酸钠盐或其铝化的形式等用作食用色素)及其铝色淀,喹啉黄。铝色淀是合成色素和铝离子的络合物,具有更好的光稳定性,颜色更持久,是食品工业常用的添加剂之一。
虽然合成色素具有诸多优点,但它具有毒性。这些毒性源于合成色素中的砷、铅、铜、苯酚、苯胺、乙醚、氯化物和硫酸盐,它们对人体均可造成不同程度的危害。合成色素进入人体后会大量消耗体内解毒物质,干扰人体正常代谢功能并直接作用于靶器官,主要毒性表现在不耐受、致癌和儿童多动症。国家标准gb2760-2014《食品添加剂使用标准》对于合成色素及其铝色淀的使用都有严格的规定:靛蓝及其铝色淀的最大使用量为0.3g/kg,诱惑红及其铝色淀的最大使用量为0.5g/kg。然而在利欲驱使下,不法分子突破允许使用品种、范围和数量,滥用、重剂量使用合成色素,使食品安全面临挑战。为了避免食品中合成色素的过量使用,对合成色素的检测显得非常重要。
目前食品中合成色素的检验方法主要有高效液相色谱法、离子色谱法、高效液相-质谱联用法、毛细管电泳色谱法和薄层色谱法等。由于诱惑红铝色淀和靛蓝二磺酸钠铝色淀既不溶于水也不溶于有机溶剂,难以从样品中提取诱惑红和靛蓝二磺酸钠,从而造成含量测定难度很大。因此,目前已有报道 方法均不能测定食品中靛蓝二磺酸钠铝色淀和诱惑红铝色淀。
技术实现要素:
有鉴于此,本发明提供了一种有机合成色素含量检测方法。通过对诱惑红和靛蓝二磺酸钠的含量测定方法进行线性、精密度、重复性、稳定性、空白、检出限、定量限、回收率试验,均符合gb/t27404-2008《实验室质量控制规范》的要求,证明含量测定方法科学有效,能对样品中诱惑红和靛蓝二磺酸钠含量起到质量控制的目的。
为了实现上述发明目的,本发明提供以下技术方案:
本发明提供了一种有机合成色素含量检测方法,包括:
步骤1:将样品与碱液混合,调节ph值至7,获得供试液;
步骤2:采用高效液相色谱法检测供试液,根据标准品含量检测结果,获得有机合成色素的含量;高效液相色谱法的色谱条件为:
流动相:流动相a为乙酸铵,流动相b为乙腈;
洗脱程序:梯度洗脱;
色谱柱:c18色谱柱;
有机合成色素为诱惑红和/或靛蓝二磺酸钠。
本发明建立了反相高效液相色谱法可准确测定如紫色薄膜衣片剂等样品中铝色淀的靛蓝二磺酸钠和诱惑红,为包含这两种色素的产品的质量标准提供依据。
在本发明提供的一些实施例中,标准品为诱惑红和/或靛蓝二磺酸钠。
在本发明提供的一些实施例中,碱液为氢氧化钠溶液。
作为优选,氢氧化钠溶液的浓度为0.1~0.5mol/l。
优选地,氢氧化钠溶液的浓度为0.5mol/l。
作为优选,混合的时间为10~20min。
优选地,混合的时间为15min。
在本发明提供的一些实施例中,以g/ml计,样品与碱液的用量比为(1~3):10。
为了防止靛蓝二磺酸钠在碱性环境下降解,在本发明中,供试液制备过程中还包括加入抗坏血酸的步骤。在本发明提供的一些实施例中,将样品与碱液混合具体为:将样品、抗坏血酸与碱液混合。
作为优选,样品与抗坏血酸的质量比为(1~3):(0.015~0.1)。
在本发明提供的一些实施例中,调节ph值采用的试剂为盐酸溶液。
在本发明提供的一些实施例中,盐酸溶液的浓度为0.1~0.5mol/l。
在本发明提供的一些实施例中,盐酸溶液的浓度为0.5mol/l。
作为优选,梯度洗脱的程序如下:
作为优选,乙酸铵的浓度为30~100mmol/l。
在本发明提供的一些实施例中,乙酸铵的浓度为50mmol/l。
作为优选,流动相的流速为0.5~1.0ml/min。
在本发明提供的一些实施例中,流动相的流速为1.0ml/min。
作为优选,色谱柱的柱温为30~40℃。
在本发明提供的一些实施例中,色谱柱的柱温为40℃。
作为优选,c18色谱柱为phenomenexgemini-nxc18色谱柱、phenomenexsynergihydro-rp色谱柱、agilentzorbaxsb-c18色谱柱、inertsilods-sp色谱柱。
在本发明提供的一些实施例中,c18色谱柱的规格为250×4.6mm,5μm。
作为优选,诱惑红的检测波长为500nm,靛蓝二磺酸钠的检测波长为600nm。
作为优选,进样量为5~20μl。
在本发明提供的一些实施例中,进样量为20μl。
本发明提供了一种有机合成色素含量检测方法,该检测方法包括:将样品与碱液混合,调节ph值至7,获得供试液;采用高效液相色谱法检测供试液,根据标准品含量检测结果,获得有机合成色素的含量;高效液相色谱法的色 谱条件为:流动相:流动相a为乙酸铵,流动相b为乙腈;洗脱程序:梯度洗脱;色谱柱:c18色谱柱;有机合成色素为诱惑红和/或靛蓝二磺酸钠。本发明具有如下优势:
本发明检测方法在线性、精密度、重复性、稳定性、空白、检出限、定量限、回收率方面均符合gb/t27404-2008《实验室质量控制规范》的要求,证明含量测定方法科学有效,能对片剂中诱惑红和靛蓝二磺酸钠含量起到质量控制的目的。结果具体为:
线性评价:诱惑红的相关系数r为1.00000,靛蓝二磺酸钠的相关系数r为1.00000,所以用该方法测定诱惑红在浓度为0.00100225mg/ml至0.0150338mg/ml之间呈现良好的线性,靛蓝二磺酸钠在浓度为0.00016366mg/ml至0.0024549mg/ml之间呈现良好的线性;
精密度:诱惑红和靛蓝二磺酸钠重复测定6次峰面积的rsd(%)分别为0.1%、0.7%,表明该方法有较好的精密度;
重复性:6份样品诱惑红含量的rsd(%)为2.3%,靛蓝二磺酸钠含量的rsd(%)为2.8%,表明该方法有较好的重复性;
稳定性:诱惑红和靛蓝二磺酸钠对照品溶液分别在室温下放置0h、1h、2h、4h、8h、12h后,rsd(%)分别为0.3%、3.4%,表明诱惑红和靛蓝二磺酸钠对照品溶液在室温下12小时内的稳定性良好;
空白试验:空白溶液在诱惑红和靛蓝二磺酸钠的出峰时间处均无吸收峰,表明空白对测定结果基本无干扰;
检出限:当信噪比(s/n)为3时,诱惑红检出限为0.0025056μg/ml,靛蓝二磺酸钠检出限为0.0040915μg/ml;得到方法的诱惑红检出限为0.0392mg/kg,靛蓝二磺酸钠检出限为0.0639mg/kg;
定量限:当信噪比(s/n)为10时,诱惑红定量限为0.010023μg/ml,靛蓝二磺酸钠定量限为0.016366μg/ml;得到方法的诱惑红定量限为0.1566mg/kg,靛蓝二磺酸钠定量限为0.2557mg/kg;
回收率:诱惑红平均回收率为:98.0%,相对标准偏差(rsd)为3.9%,靛蓝二磺酸钠平均回收率为:95.4%,相对标准偏差(rsd)为3.8%。
附图说明
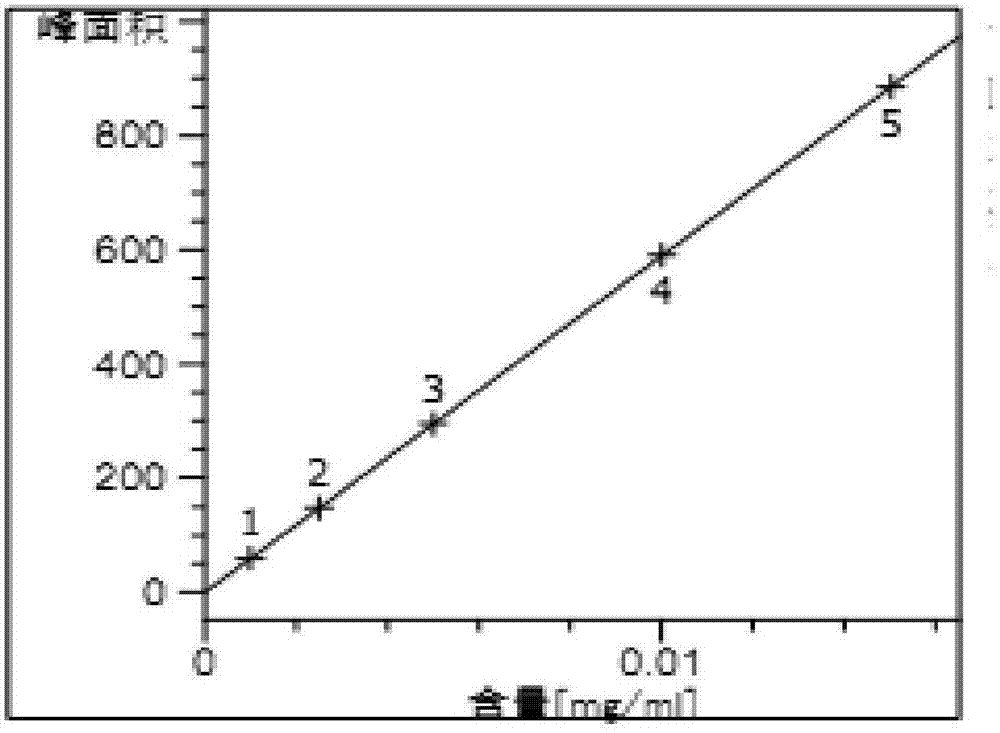
图1示靛蓝二磺酸钠的标准工作曲线;
图2示诱惑红的标准工作曲线;
图3~图8分别示重复1~6测定的靛蓝二磺酸钠和诱惑红含量色谱图,显示本检测方法具有良好的精密度;
图9~图14分别示6份样品中靛蓝二磺酸钠和诱惑红含量色谱图,显示本检测方法具有良好的重复性;
图15~图20分别示样品在室温下放置0h、1h、2h、4h、8h、12h后靛蓝二磺酸钠和诱惑红含量色谱图,显示本检测方法具有良好的稳定性;
图21示空白溶液中靛蓝二磺酸钠和诱惑红含量色谱图;
图22示对照品溶液中靛蓝二磺酸钠和诱惑红含量色谱图;
图23示诱惑红的检出限色谱图;
图24示靛蓝二磺酸钠的检出限色谱图;
图25示诱惑红的定量限色谱图;
图26示靛蓝二磺酸钠的定量限色谱图;
图27~35分别示9份样品中靛蓝二磺酸钠和诱惑红的回收率色谱图。
具体实施方式
本发明公开了一种有机合成色素含量检测方法,本领域技术人员可以借鉴本文内容,适当改进工艺参数实现。特别需要指出的是,所有类似的替换和改动对本领域技术人员来说是显而易见的,它们都被视为包括在本发明。本发明的方法及应用已经通过较佳实施例进行了描述,相关人员明显能在不脱离本发明内容、精神和范围内对本文所述的方法和应用进行改动或适当变更与组合,来实现和应用本发明技术。
本发明提供的诱惑红和/或靛蓝二磺酸钠含量检测方法中所用试剂、仪器均可由市场购得。
下面结合实施例,进一步阐述本发明:
实施例1
1原理:试样中的诱惑红和靛蓝二磺酸钠,用氢氧化钠溶液提取,盐酸溶液中和后,用高效液相色谱c18柱将诱惑红和靛蓝二磺酸钠分离,经二极管阵列检测器检测,并用外标法定量。
2仪器:安捷伦1260高效液相色谱仪(配二极管阵列检测器),或其它配二极管阵列检测器的高效液相色谱仪。
3试剂试药:氢氧化钠(ar,即分析纯);浓盐酸(ar);乙酸铵(色谱纯);乙腈(色谱纯);一级用水。
诱惑红,对照品来源:中国食品药品检定研究院,批号:510003-201301,纯度:86.7%;
靛蓝二磺酸钠,对照品来源:sigma,批号:bcbd1142v,纯度:98.0%。
4分析步骤:
4.1色谱条件:
流动相:a:50mmol/l的乙酸铵溶液,b:乙腈,梯度洗脱;
流速:1.0ml/min;
波长:诱惑红(500nm)、靛蓝二磺酸钠(600nm);
柱温:40℃;
进样量:20μl;
色谱柱:phenomenexgemini-nx,c18,250×4.6mm,5μm。
4.2对照储备液的配制:
精密称取诱惑红对照品5.7mg,置于50ml棕色容量瓶中,加入水溶解并定容至刻度,摇匀,即得储备液。储备液放在4℃的冰箱中储存备用。
精密称取靛蓝二磺酸钠对照品8.3mg,置于50ml棕色容量瓶中,加入水溶解并定容至刻度,摇匀,即得储备液。储备液放在4℃的冰箱中储存备用。
4.3标准工作曲线绘制:
分别精密移取诱惑红储备液100μl、250μl、500μl、1000μl、1500μl,靛蓝二磺酸钠储备液10μl、25μl、50μl、100μl、150μl于10ml容量瓶中,用水定容至刻度,摇匀,即得工作标准液。
4.4试样制备:
精密称取多种维生素矿物质片的样品两片(约1.6g,理论含量:诱惑红0.05g/kg,靛蓝二磺酸钠0.01g/kg),置于50ml离心管中,加入20mg抗坏血酸,加入0.5mol/l的氢氧化钠溶液10ml浸泡,2分钟震荡一次,15min后样片包衣变白,捞出残片弃去,用0.5mol/l的盐酸溶液调节ph值至7(以ph试纸检测),用水定容至25ml,摇匀,8000r/min离心3min,经0.45μm的水相滤膜过滤,即得供试液。
4.5结果计算:
x=c×v/m×k
式中:x—样品诱惑红(靛蓝二磺酸钠)的含量,g/kg;
m—样品的质量,g;
k—单位转换系数(k=1);
v—样品的稀释倍数,ml;
c—样品溶液中诱惑红(靛蓝二磺酸钠)的浓度,mg/ml。
5方法学验证:
5.1线性范围确认:
5.1.1试验数据:(色谱图见图1、2)
表1诱惑红的线性关系试验数据
表2靛蓝二磺酸钠的线性关系试验数据
5.1.2标准工作曲线图:
以浓度为横坐标,峰面积为纵坐标,绘制标准工作曲线,靛蓝二磺酸钠和诱惑红的标准工作曲线分别如图1、2所示。
5.1.3线性试验结论:
线性评价:诱惑红的相关系数r为1.00000,靛蓝二磺酸钠的相关系数r为1.00000,所以用该方法测定诱惑红在浓度为0.00100225mg/ml至0.0150338mg/ml之间呈现良好的线性,靛蓝二磺酸钠在浓度为0.00016366mg/ml至0.0024549mg/ml之间呈现良好的线性,符合gb/t27404-2008《实验室质量控制规范》的要求【gb/t27404-2008要求相关系数r≥0.99】。
5.2精密度试验
5.2.1试验方法:
将诱惑红和靛蓝二磺酸钠的对照品溶液按4.1色谱条件重复测定6次,计算其峰面积rsd(%)。
5.2.2试验数据:(色谱图见附图3~8)
表3诱惑红的精密度试验数据
表4靛蓝二磺酸钠的精密度试验数据
5.2.3试验结论:
诱惑红和靛蓝二磺酸钠重复测定6次峰面积的rsd(%)分别为0.1%、0.7%,表明该方法有较好的精密度。
5.3重复性试验:
5.3.1试验方法:
称取6份样品,按4.4试样制备方法处理样品,检测样品含量,计算其rsd(%)。
5.3.2试验数据:(色谱图见附图9~14)
表5诱惑红的重复性试验数据
表6靛蓝二磺酸钠的重复性试验数据
5.3.3试验结论:
6份样品诱惑红含量的rsd(%)为2.3%,靛蓝二磺酸钠含量的rsd(%)为2.8%,表明该方法有较好的重复性,符合gb/t27404-2008《实验室质量控制规范》的要求【gb/t27404-2008要求rsd(%)≤5.3%】。
5.4稳定性试验
5.4.1试验方法:
将诱惑红和靛蓝二磺酸钠对照品溶液分别在室温下放置0h、1h、2h、4h、8h、12h后,按4.1色谱条件测定峰面积,计算其rsd(%)。
5.4.2试验数据:(色谱图见附图15~20)
表7诱惑红的稳定性试验数据
表8靛蓝二磺酸钠的稳定性试验数据
5.4.3试验结论:
诱惑红和靛蓝二磺酸钠对照品溶液分别在室温下放置0h、1h、2h、4h、8h、12h后,rsd(%)分别为0.3%、3.4%,表明诱惑红和靛蓝二磺酸钠对照品溶液在室温下12小时内的稳定性良好。
5.5空白试验
5.5.1试验方法:
不称取样品,按4.4试样制备方法处理空白溶液,按4.1色谱条件测定空白溶液,与诱惑红和靛蓝二磺酸钠对照品溶液的出峰时间对比。
5.5.2试验结果:
试验结果见图21、22。
5.5.3试验结论:
空白溶液在诱惑红和靛蓝二磺酸钠的出峰时间处均无吸收峰,表明空白对测定结果基本无干扰。
5.6检出限与定量限试验
分析方法的定量限和检出限由信噪比(s/n)计算。
当信噪比(s/n)为3时,诱惑红检出限为0.0025056μg/ml,靛蓝二磺酸钠检出限为0.0040915μg/ml;得到方法的诱惑红检出限为0.0392mg/kg,靛蓝二磺酸钠检出限为0.0639mg/kg(见图23、24)。
当信噪比(s/n)为10时,诱惑红定量限为0.010023μg/ml,靛蓝二磺酸钠定量限为0.016366μg/ml;得到方法的诱惑红定量限为0.1566mg/kg,靛蓝二磺酸钠定量限为0.2557mg/kg(见图25、26)。
5.7回收率试验:
5.7.1试验方法:
加标:精密称取约1.6g样品9份(已知诱惑红含量:0.0553g/kg,靛蓝二磺酸钠含量:0.0111g/kg),置于50ml离心管中,分成3组,每组3份,各组分别精密加入诱惑红的对照品储备液300μl、800μl、1200μl,靛蓝二磺酸钠的对照品储备液30μl、70μl、120μl。按4.4试样制备方法处理样品。
5.7.2试验数据如下:(色谱图见附图27~35)
表9诱惑红的回收率试验数据
表10靛蓝二磺酸钠的回收率试验数据
测得加入量=加标样品测得量-样品测得量
回收率(%)=测得加入量/理论加入量
5.7.3试验结论:
诱惑红平均回收率为:98.0%,相对标准偏差(rsd)为3.9%,靛蓝二磺酸钠平均回收率为:95.4%,相对标准偏差(rsd)为3.8%,符合gb/t27404-2008《实验室质量控制规范》的要求【gb/t27404-2008要求回收率为90—110%】。
6结论:
通过对诱惑红和靛蓝二磺酸钠的含量测定方法进行线性、精密度、重复性、稳定性、空白、检出限、定量限、回收率试验,均符合gb/t27404-2008《实验室质量控制规范》的要求,证明含量测定方法科学有效,能对片剂中诱惑红和靛蓝二磺酸钠含量起到质量控制的目的。
实施例2
1分析步骤:
1.1色谱条件:
流动相:a:30mmol/l的乙酸铵溶液,b:乙腈,梯度洗脱;
流速:0.8ml/min;
波长:诱惑红(500nm)、靛蓝二磺酸钠(600nm);
柱温:30℃;
进样量:5μl;
色谱柱:phenomenexgemini-nx,c18,250×4.6mm,5μm。
1.2对照储备液的配制:
精密称取诱惑红对照品5.7mg,置于50ml棕色容量瓶中,加入水溶解并定容至刻度,摇匀,即得储备液。储备液放在4℃的冰箱中储存备用。
精密称取靛蓝二磺酸钠对照品8.3mg,置于50ml棕色容量瓶中,加入水溶解并定容至刻度,摇匀,即得储备液。储备液放在4℃的冰箱中储存备用。
1.3标准工作曲线绘制:
分别精密移取诱惑红储备液100μl、250μl、500μl、1000μl、1500μl,靛蓝二磺酸钠储备液10μl、25μl、50μl、100μl、150μl于10ml容量瓶中,用水定容至刻度,摇匀,即得工作标准液。
1.4试样制备:
精密称取胆碱片的样品两片(约1.75g,理论含量:诱惑红0.05g/kg,靛蓝二磺酸钠0.01g/kg),置于50ml离心管中,加入100mg抗坏血酸,加入0.1mol/l的氢氧化钠溶液10ml浸泡,2分钟震荡一次,20min后样片包衣变白,捞出残片弃去,用0.1mol/l的盐酸溶液调节ph值至7(以ph试纸检测),用水定容至25ml,摇匀,8000r/min离心3min,经0.45μm的水相滤膜过滤,即得供试液。
1.5结果计算:
x=c×v/m×k
式中:x—样品诱惑红(靛蓝二磺酸钠)的含量,g/kg;
m—样品的质量,g;
k—单位转换系数(k=1);
v—样品的稀释倍数,ml;
c—样品溶液中诱惑红(靛蓝二磺酸钠)的浓度,mg/ml。
2方法学验证:
采用上述方法进行线性、精密度、重复性、稳定性、空白、检出限、定量限、回收率试验,试验结果与实施例1的试验结果相近,均符合gb/t27404-2008《实验室质量控制规范》的要求,证明含量测定方法科学有 效,能对片剂中诱惑红和靛蓝二磺酸钠含量起到质量控制的目的。
实施例3
1分析步骤:
1.1色谱条件:
流动相:a:100mmol/l的乙酸铵溶液,b:乙腈,梯度洗脱;
流速:0.5ml/min;
波长:诱惑红(500nm)、靛蓝二磺酸钠(600nm);
柱温:35℃;
进样量:10μl;
色谱柱:phenomenexgemini-nx,c18,250×4.6mm,5μm。
1.2对照储备液的配制:
精密称取诱惑红对照品5.7mg,置于50ml棕色容量瓶中,加入水溶解并定容至刻度,摇匀,即得储备液。储备液放在4℃的冰箱中储存备用。
精密称取靛蓝二磺酸钠对照品8.3mg,置于50ml棕色容量瓶中,加入水溶解并定容至刻度,摇匀,即得储备液。储备液放在4℃的冰箱中储存备用。
1.3标准工作曲线绘制:
分别精密移取诱惑红储备液100μl、250μl、500μl、1000μl、1500μl,靛蓝二磺酸钠储备液10μl、25μl、50μl、100μl、150μl于10ml容量瓶中,用水定容至刻度,摇匀,即得工作标准液。
1.4试样制备:
精密称取叶酸片的样品四片((约2.0g,理论含量:诱惑红0.01g/kg,靛蓝二磺酸钠0.0005g/kg),置于50ml离心管中,加入15mg抗坏血酸,加入0.3mol/l的氢氧化钠溶液10ml浸泡,2分钟震荡一次,10min后样片包衣变白,捞出残片弃去,用0.3mol/l的盐酸溶液调节ph值至7(以ph试纸检测),用水定容至25ml,摇匀,8000r/min离心3min,经0.45μm的水相滤膜过滤,即得供试液。
1.5结果计算:
x=c×v/m×k
式中:x—样品诱惑红(靛蓝二磺酸钠)的含量,g/kg;
m—样品的质量,g;
k—单位转换系数(k=1);
v—样品的稀释倍数,ml;
c—样品溶液中诱惑红(靛蓝二磺酸钠)的浓度,mg/ml。
2方法学验证:
采用上述方法进行线性、精密度、重复性、稳定性、空白、检出限、定量限、回收率试验,试验结果与实施例1的试验结果相近,均符合gb/t27404-2008《实验室质量控制规范》的要求,证明含量测定方法科学有效,能对片剂中诱惑红和靛蓝二磺酸钠含量起到质量控制的目的。
以上所述仅是本发明的优选实施方式,应当指出,对于本技术领域的普通技术人员来说,在不脱离本发明原理的前提下,还可以做出若干改进和润饰,这些改进和润饰也应视为本发明的保护范围。
- 还没有人留言评论。精彩留言会获得点赞!