一种液相淌度分离装置及与液相色谱和质谱联用的接口的制作方法
本实用新型涉及质谱领域,具体地说,涉及一种液相淌度分离装置及与液相色谱和质谱联用的接口。
背景技术:
质谱分析法(mass spectrometry)是将样品按不同质荷比(m/z)进行分离检测,实现成分和结构鉴别的一种分析方法。质谱技术因其具有的高特异性和灵敏度,在生物分析领域中的重要地位日益凸显。
质谱分析的基本原理,是使样品中各组分在离子源中发生电离,生成不同质荷比的离子,以离子束的形式进入质量分析器。对于液体样品的检测,最常用的离子源是电喷雾离子源。当使用电喷雾方法检测混合样品时,待测组分之间、待测组分与杂质之间会产生离子化竞争,使得低丰度、离子化效率低的组分不易被检出。
技术实现要素:
为了克服上述技术问题,本实用新型提供了一种液相淌度分离装置以及与液相色谱和质谱联用的接口,实现了复杂样品体系的组分分离,提升了分离效果。
为了实现上述目的,本实用新型提供了一种液相淌度分离装置,包括:
分离毛细管,所述分离毛细管一端为电喷雾尖端,另一端为缓冲液注入端;
注射泵,所述注射泵连接所述缓冲液注入端;
进样针,所述进样针在靠近所述注射泵的位置连接所述分离毛细管;
分离电极,所述分离电极连接所述注射泵,或在靠近所述注射泵的位置连接所述分离毛细管;
接地电极,所述接地电极在靠近所述电喷雾尖端的位置连接所述分离毛细管。
在一种可选的实施方式中,所述液相淌度分离装置还包括:
第一多通阀,所述注射泵、进样针通过所述第一多通阀连接所述分离毛细管;
第二多通阀,所述接地电极通过所述第二多通阀连接所述分离毛细管。
在一种可选的实施方式中,所述分离电极通过所述第一多通阀连接所述分离电极。
在一种可选的实施方式中,所述液相淌度分离装置还包括:
辅助毛细管,所述辅助毛细管通过所述第二多通阀连接所述分离毛细管,为所述分离毛细管导入辅助缓冲液,或导出废液。
本实用新型还提供了一种与液相色谱和质谱联用的接口,包括:
如前任意一项所述的液相淌度分离装置;
液相色谱设备,所述液相色谱设备的出样端连接所述液相淌度分离装置的进样针。
本实用新型实施例所述的液相淌度分离装置以及与液相色谱和质谱联用的接口,该液相淌度分离装置包括分离毛细管、注射泵、进样针、分离电极和接地电极,其中分离毛细管一端为电喷雾尖端,另一端为缓冲液注入端;注射泵连接所述缓冲液注入端;进样针在靠近所述注射泵的位置连接所述分离毛细管;分离电极在靠近所述注射泵的位置连接所述分离毛细管;接地电极在靠近所述电喷雾尖端的位置连接所述分离毛细管。本实用新型方案使用注射泵注入缓冲液对分离毛细管中的样品进行冲洗,同时施加分离电场,使得样品中的各组分在分离毛细管中充分分离,提升了分离效果,并且分离速度较快,同时产品结构简单,操作方便。
附图说明
图1为液相淌度原理示意图;
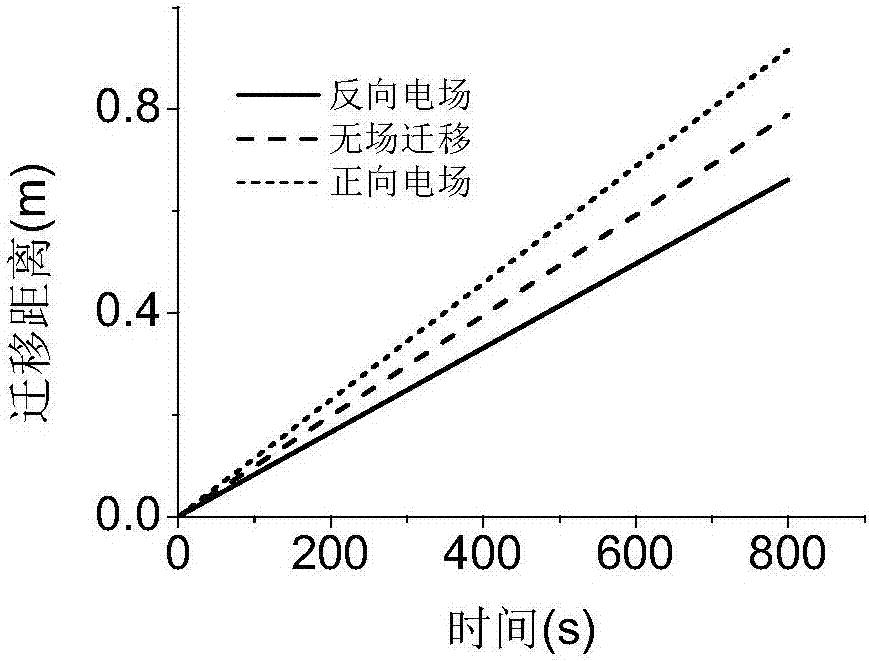
图2-1至图2-2为离子在不同电场作用下的理论运动轨迹和色谱图;
图3为本实用新型实施例提供的一种液相淌度分离装置的结构图;
图4-1至图4-4为本实用新型实施例提供的另外四种液相淌度分离装置的结构图;
图5为本实用新型实施例提供的一种液相淌度分离装置的控制方法流程图;
图6-1和图6-2为本实用新型实施例中施加不同压力时,样品迁移时间的比对图;
图7-1和图7-2为本实用新型实施例中施加不同分离电压时,样品迁移时间的比对图;
图8-1和图8-2为本实用新型实施例中分离毛细管的长度不同时,样品迁移时间的比对图;
图9-1和图9-2为本实用新型实施例中缓冲液的粘度系数不同时,样品迁移时间的比对图;
图10为本实用新型实施例中样品带电荷数不同时,样品迁移时间的比对图;
图11为本实用新型实施例中样品几何尺寸不同时,样品迁移时间的比对图;
图12-1和图12-2为采用本实用新型实施例对多种混合样品进行分离的效果图。
具体实施方式
下面参考附图来说明本实用新型的实施例。在本实用新型的一个附图或一种实施方式中描述的元素和特征可以与一个或更多个其他附图或实施方式中示出的元素和特征相结合。应当注意,为了清楚的目的,附图和说明中省略了与本实用新型无关的、本领域普通技术人员已知的部件或处理的表示和描述。
下面结合附图对本实用新型做进一步描述。
本实用新型实施例提出了一种液相淌度理论,并在该理论基础上提供了一种液相淌度分离装置及其控制方法。液相淌度是指在气相离子迁移谱的基础之上结合差速运动进行分离,在本实用新型实施例中,随载流运动的混合样品在电场作用下实现差速运动。以带正电的物质为例,反向电场会延缓带正电物质的迁移。基于本实用新型实施例,还可将液相淌度运用于色谱分离后的进一步分离分析,色谱主要是依据物质的极性进行分离,而液相淌度分离装置可根据物质带电性质的不同来进行再次分离。
其原理如图1所示,混合多种组分的样品注入分离通道后,注入缓冲液,缓冲液作为载流承载样品向前移动,此时施加分离电压,由于不同组分的离子带电性质以及等效半径不同,导致速度不同,实现分离。
分离通道中的混合样品,在平流不可压缩的载流牵引下,可做匀速运动,各组分平衡时速度与载流速度vcarrier一致。如果混合样品可解离成为离子,通过施加反向电场使之受到与载流运动方向相反电场力作用FE,由此与载流产生相对运动,此过程导致组分受到应力Ff,FE和Ff分别由以下公式得出:
FE=qE
Ff=6πηrv
其中E为分离电场强度、q为离子带电量、η为缓冲液的粘度系数、r为离子的等效半径、v为离子相对于载流的速度。当FE与Ff相等时,离子与载流相对速度v恒定,此时离子表观速度vE为:
vE=vcarrier+v
表观速度与离子带电性质与等效半径r相关,不同离子具有不同的表观速度,在通过一段长度为L分离通道后,所用时间t不同,即实现分离。
则离子表观位移S可表示为微分方程:
其中,U为分离电压。
通过数值方法求解微分方程,可获得不同离子迁移L距离所用时间。
如图2-1和图2-2示出了离子在不同电场作用下的理论运动轨迹和色谱图。选取的计算条件为:分离通道长60cm,通道内径75μm,电势为±10kV,压力为30mbar,黏度系数为0.89mPa·S,样品相对分子量为433,带1个正电荷,样品等效半径为1nm。图2-1为离子在+10kV、0V、-10kV作用下的运动轨迹,正向电场会使离子更早出峰,而反向电压会使离子出峰延后。如果继续升高反向电场,甚至会使离子无法出峰。图2-2为理论的色谱图,正向电场出峰时间最短,负向电场出峰时间最长。
本实用新型实施例提供了一种液相淌度分离装置,如图3所示,包括分离毛细管1,注射泵2,进样针3,分离电极4和接地电极5。
分离毛细管1一端为电喷雾尖端11,另一端为缓冲液注入端12。注射泵2连接分离毛细管1的缓冲液注入端12。进样针3在靠近注射泵2的位置连接至分离毛细管1。分离电极4连接至注射泵,或者在靠近注射泵2的位置连接至分离毛细管1。接地电极5在靠近电喷雾尖端11的位置连接分离毛细管1。
开启注射泵2,使注射泵2以预设的恒定压力向分离毛细管1注入缓冲液。经过预定时间段后,关闭注射泵2。此后进样针3向分离毛细管1进样。停止进样针3的进样后,再次开启注射泵2,向分离毛细管1注入缓冲液,并通过分离电极4施加分离电压,在电喷雾尖端11施加喷雾电压。
本实用新型实施例所述的液相淌度分离装置,使用注射泵注入缓冲液对分离毛细管中的样品进行冲洗,同时施加分离电场,使得样品中的各组分在分离毛细管中充分分离,提升了分离效果,并且分离速度较快,同时产品结构简单,操作方便。
进一步的,本实用新型实施例提供的液相淌度分离装置还包括:第一多通阀和第二多通阀。注射泵、进样针通过第一多通阀连接分离毛细管。接地电极通过第二多通阀连接分离毛细管。
本实用新型实施例提供的液相淌度分离装置的一种具体实施方式如图4-1所示。第一多通阀和第二多通阀具体为三通阀6和三通阀7。
注射泵2、分离毛细管1的缓冲液注入端12、进样针3分别连接三通阀6的三个端口61、62、63,通过此种连接,注射泵2、进样针3通过三通阀6分别向分离毛细管1注入缓冲液和样品。分离电极4可设置在注射泵2与三通阀6之间。从三通阀6伸出的分离毛细管1进入三通阀7的第一个端口71,电喷雾尖端11从三通阀7的第二个端口72伸出。接地电极5连接三通阀7的第三个端口73。
本实用新型实施例提供的液相淌度分离装置的一种具体实施方式如图4-2所示。第一多通阀和第二多通阀分别具体为四通阀9和三通阀10。
注射泵2、分离毛细管1的缓冲液注入端12、进样针3、分离电极4分别连接四通阀9的四个端口91、92、93、94,通过此种连接,注射泵2、进样针3分别通过四通阀9向分离毛细管1注入缓冲液和样品,分离电极4向缓冲液和样品的混合液提供分离电压。从四通阀9伸出的分离毛细管1进入三通阀10的第一个端口101,电喷雾尖端11从三通阀10的第二个端口102伸出。接地电极5连接三通阀10的第三个端口103。
本实用新型实施例提供的液相淌度分离装置的一种具体实施方式如图4-3所示。第一多通阀和第二多通阀分别具体为四通阀13和四通阀14。图4-3中还包括辅助毛细管15。
注射泵2、分离毛细管1的缓冲液注入端12、进样针3、分离电极4分别连接四通阀13的四个端口131、132、133、134,通过此种连接,注射泵2、进样针3分别通过四通阀13向分离毛细管1注入缓冲液和样品,分离电极4向缓冲液和样品的混合液提供分离电压。从四通阀13伸出的分离毛细管1进入四通阀14的第一个端口141,电喷雾尖端11从四通阀14的第二个端口142伸出。接地电极5连接四通阀14的第三个端口143,辅助毛细管15连接四通阀14的第四个端口144。辅助毛细管15可以用于向分离毛细管1中提供辅助离子化的喷雾缓冲液,也可以用于从分离毛细管1中吸收废液。
本实用新型实施例提供的液相淌度分离装置的一种具体实施方式如图4-4所示。第一多通阀和第二多通阀分别具体为三通阀16和四通阀17。图4-4中还包括辅助毛细管15。
注射泵2、分离毛细管1的缓冲液注入端12、进样针3分别连接三通阀16的三个端口161、162、163,通过此种连接,注射泵2、进样针3分别通过三通阀16向分离毛细管1注入缓冲液和样品。分离电极4可设置在注射泵2与三通阀16之间。从三通阀16伸出的分离毛细管1进入四通阀17的第一个端口171,电喷雾尖端11从四通阀17的第二个端口172伸出。接地电极5连接四通阀17的第三个端口173,辅助毛细管15连接四通阀17的第四个端口174。辅助毛细管15可以用于向分离毛细管1中提供辅助离子化的喷雾缓冲液,也可以用于从分离毛细管1中吸收废液。
在图4-1至图4-4中,电喷雾尖端11可连接质谱入口8。在分离电极4施加分离电压+/-HV2的同时,在电喷雾尖端11处施加喷雾电压-HV1。
在该液相淌度分离装置中,尽量使分离毛细管保持直线状。为此需要选择合适的三通阀和四通阀,使得分离毛细管能够直线贯穿三通阀和四通阀。
在本实用新型实施例的另一种实现方式中,还可在分离毛细管处开一个检测窗口,通过光学检测方法来辅助检测样品分离过程。
本实用新型实施例的的另一种实现方式中,还可通过改变缓冲液体系实现多模式分离,如在缓冲液添加与质谱兼容的表面活性剂形成胶束,可用于中性物质的分离及用于改善带电物质的分离。
本实用新型实施例还提供了一种与液相色谱和质谱联用(LC-MS)的接口,包括如前所述的液相淌度分离装置,以及液相色谱设备。其中,液相色谱设备的出样端连接所述液相淌度分离装置的进样端。液相色谱设备基于样品极性进行样品分离,极性相似的产品流入进样针,通过液相淌度分离装置进行再次分离。
本实用新型实施例还提供了一种液相淌度分离装置的控制方法,如图5所示,该方法包括:
501、开启注射泵,使注射泵以预设的冲洗压力向分离毛细管注入缓冲液。
分离毛细管可采用多种内、外径参数,喷雾尖端的内径范围为3μm~50μm。缓冲液可以为甲醇水溶液(含0.1%甲酸(w/w)),或者乙酸铵溶液、甲酸铵溶液。
502、经过第一时间段后,关闭注射泵。
该预定时间段为4分钟-6分钟,具体操作中,可以为5分钟。
503、进样针以预设的进样压力向分离毛细管进样。
504、经过第二时间段后,停止进样针的进样,再次开启注射泵,以预设的分离压力向分离毛细管注入缓冲液,并通过分离电极施加分离电压,在电喷雾尖端施加喷雾电压。
分离压力的持续时间范围为0.1-60分钟,具体为按出峰时间而定。
冲洗压力为1-1000mbar,进样压力为10-100mbar,分离压力为1-200mbar,第一时间段为4-6分钟,所述第二时间段为1-10秒。
实际应用中,冲洗压力具体可为900mbar,进样压力具体为50mbar,分离压力具体为30mbar,第一时间段具体为5分钟,第二时间段具体为5秒。
分离电压的输出范围0~+/-30kV。
当再次开启注射泵注入缓冲液后,进样的样品在缓冲液的承载下在分离毛细管中向电喷雾尖端移动,此时通过分离电极提供分离电压,使得分离毛细管内的样品中的混合组分分离。
注射泵向分离毛细管注入缓冲液,这种流动式操作便于实现分离毛细管的微型化,减小设备体积,操作方便。且流动操作过程中封闭的毛细管道避免了液体的蒸发,提供了待测溶液流动通过的可精确重复的通道并提供了安全有利的环境。
可选的,还可以通过辅助毛细管向分离毛细管中提供辅助离子化的喷雾缓冲液,还可以通过辅助毛细管从分离毛细管中吸收废液。喷雾缓冲液可以为甲醇或乙腈溶液。
本实用新型实施例提供的液相淌度分离装置的控制方法,使用注射泵注入缓冲液对分离毛细管中的样品进行冲洗,同时施加分离电场,使得样品中的各组分在分离毛细管中充分分离,提升了分离效果,并且分离速度较快,同时产品结构简单,操作方便。
根据前文描述,表观速度vE与分离电场强度E、离子带电量q、粘度系数η、离子的等效半径r等参数有关,这些参数的变化会对离子迁移时间造成影响。下面通过实施例1至实施例7,进行具体分析。
实施例1
本实施例分别通过仿真理论计算和实验测试两方面分析压力对样品迁移时间的影响。
仿真参数设定为:毛细管管长60cm,管内径75μm,反向分离电压为-10kV或不施加分离电压,黏度系数为0.89mPa·S,样品相对分子量为1048,带2个正电荷,样品等效半径为1.2nm。分离通道两端的分离压力分别为10mbar、15mbar、20mbar、30mbar、40mbar、50mbar。仿真结果如图6-1所示。可见在施加了反向分离电压的情况下随着分离通道两端压力的提高,物质迁移时间缩短,并且从10mbar至15mbar时迁移时间陡然变短,从15mbar至50mbar过程中,迁移时间缓慢变短。与不施加电场的迁移结果对比可知,压力越小,物质的迁移时间受到电场的作用越大。
实验条件:样品为1mg/mL的血管紧张素II,缓冲液为20%甲醇水溶液(含0.1%甲酸(w/w)),毛细管管长40cm,管内径75μm。操作方式为:用50mbar的进样压力进样5s,在分离通道两端仅施加分离压力,不施加电压,分离气压分别为10mbar、30mbar、50mbar、100mbar。实验结果如图6-2所示。可见随着气压升高,样品随缓冲液受到的推力越大,运动速度越快,所以样品迁移时间变短。此外,气压越高,样品峰高变低,脱尾愈发严重。
进样压力和分离压力可以由同一个气压装置提供。进样还可以通过电压或虹吸方式实现。
实施例2
本实施例分别通过仿真理论计算和实验测试两方面分析分离电压对样品迁移时间的影响。
仿真参数设定为:毛细管管长60cm,管内径75μm,泵入缓冲液的分离压力为30mbar,黏度系数为0.89mPa·S,样品相对分子量为1048,带2个正电荷,样品等效半径为1.2nm。反向分离电压分别为0V、-100V、-200V、-500V、-1kV、-2kV、-5kV、-10kV、-15kV、-20kV、-25kV、-30kV。结果如图7-1所示,可见随着分离电压提高,物质迁移时间逐渐延长。
实验条件:使用上述实施例1的实验条件,具体为:样品为1mg/mL的血管紧张素II,缓冲液为20%甲醇水溶液(含0.1%甲酸),毛细管管长60cm,管内径75μm,并选取50mbar的分离压力泵入缓冲液,并在分离通道两端引入分离电压。分离电压分别施加+10kV、-1kV、-3kV、-5kV、-10kV的电压,并与不施加分离电压的实验结果进行比对。实验结果如图7-2所示。+10kV缩短了样品的迁移时间使得样品更早出峰。当施加与气压反向的电压,随着电压的升高,样品的迁移时间延长,同时样品峰的峰宽不断变宽,峰高变低。
实施例3
本实施例分别通过仿真理论计算和实验测试两方面分析分离毛细管长度对样品迁移时间的影响。
仿真参数设定为:管内径75μm,反向分离场强为-300V/cm,泵入缓冲液的分离压力为30mbar,黏度系数为0.89mPa·S,样品相对分子量为1048,带2个正电荷,样品等效半径为1.2nm。毛细管管长分别为20cm、40cm、60cm、80cm、100cm。仿真结果如图8-1所示。可见在分离场强不变的情况下,随着毛细管管长的增加,物质迁移时间先缓慢增加,之后快速增加。
实验条件:样品为终浓度1mg/mL的血管紧张素II和1mg/mL缓激肽混合溶液,缓冲液为20%甲醇水溶液(含0.1%甲酸(w/w)),毛细管管内径75μm。操作方式为:进样为用50mbar的进样压力进样5s,在分离通道两端施加50mbar的分离压力和-410V/cm的场强,毛细管管长分别为20cm、40cm、60cm,实验结果如图8-2所示。可见随着管长的增加,样品迁移时间越长,组分之间的分离度越大,同时峰宽增加。图中物质1为血管紧张素II,物质2为缓激肽。
实施例4
本实施例分别通过仿真理论计算和实验测试两方面分析缓冲液的粘度系数η对样品迁移时间的影响。
仿真参数设定为:毛细管管长60cm,管内径75μm,反向分离电压为-10kV,泵入缓冲液的进样压力为30mbar,样品相对分子量为1048,带2个正电荷,样品等效半径为1.2nm。缓冲液分别为25摄氏度条件下的水(η=0.89mPa·S)、10%甲醇(η=1.18mPa·S)、20%甲醇(η=1.40mPa·S)、30%甲醇(η=1.56mPa·S)、40%或50%甲醇(η=1.62mPa·S)、60%甲醇(η=1.54mPa·S)、70%甲醇(η=1.36mPa·S)、80%甲醇(η=1.12mPa·S)、90%甲醇(η=0.84mPa·S)、100%甲醇(η=0.56mPa·S)。仿真结果如图9-1所示。可见随着水溶液中甲醇含量的提高,物质迁移时间先延长后缩短。
实验条件:样品为终浓度1mg/mL的血管紧张素II和1mg/mL缓激肽混合溶液,毛细管管长40cm,管内径75μm。操作方式为:进样为用50mbar的进样压力进样5s,在分离通道两端施加50mbar的分离压力和-20kV的电压,缓冲液分别为水、20%甲醇、50%甲醇、80%甲醇(含0.1%甲酸(w/w)),实验结果如图9-2所示。可见随着缓冲液水溶液中甲醇含量的增加,样品迁移时间先增加后降低,当甲醇含量很高时,对峰形影响很大。图中物质1为血管紧张素II,物质2为缓激肽。
实施例5
本实施例通过仿真理论计算,分析样品带电性质对样品迁移时间的影响。
仿真参数设定为:毛细管管长60cm,管内径75μm,反向分离电压为-10kV,泵入缓冲液的进样压力为30mbar,黏度系数为0.89mPa·S。样品相对分子量为8600,样品等效半径为1.2nm,分别带4、5、6、9、10、11、12个正电荷。仿真结果如图10所示。可见随着离子带电量的增加,物质迁移时间延长。物质在不同pH下解离不同,即所带电荷数不同,出峰时间会发生变化。
实施例6
本实施例通过仿真理论计算,分析样品的几何尺寸对样品迁移时间的影响。
仿真参数设定为:毛细管管长60cm,管内径75μm,反向分离电压为-10kV,泵入缓冲液的进样压力为30mbar,黏度系数为0.89mPa·S。样品相对分子量为8600,样品等效半径r0分别为2.243nm与2.207nm,带7个正电荷。仿真结果如图11所示。可见随着样品等效半径的变大,物质迁移时间会缩短,样品会提前出峰。
实施例7
本实施例分别通过仿真理论计算和实验测试两方面分析多种混合样品的分离效果。
仿真实验选取了血管紧张素I(+3)、血管紧张素II(+2)、缓激肽(+1)、泛素(+9)这4种物质进行混合物分离仿真。选取的仿真条件为:毛细管管长40cm,管内径75μm,电势为-2kV,泵入缓冲液的进样压力为10mbar,黏度系数为0.89mPa·S。仿真结果如图12-1所示,4种物质之间实现分离。
实验条件:样品为终浓度1mg/mL的血管紧张素II和1mg/mL缓激肽混合溶液,缓冲液为20%甲醇水溶液(含0.1%甲酸(w/w)),毛细管管长40cm,管内径75μm。操作方式为:进样为用50mbar的进样压力进样5s,在分离通道两端施加50mbar的分离压力和-20kV的电压,实验结果如图12-2所示,图中物质1为血管紧张素II,物质2为缓激肽。可见两种肽段间实现分离且分离效果良好。在此条件下进行了5次重复实验,重现性良好。
本实用新型实施例提供了液相淌度分离装置和控制方法以及与液相色谱和质谱联用的接口,该液相淌度分离装置包括分离毛细管、注射泵、进样针、分离电极和接地电极,其中分离毛细管一端为电喷雾尖端,另一端为缓冲液注入端;注射泵连接缓冲液注入端;进样针在靠近注射泵的位置连接分离毛细管;分离电极在靠近注射泵的位置连接分离毛细管;接地电极在靠近电喷雾尖端的位置连接分离毛细管。本实用新型实施例方案使用注射泵注入缓冲液对分离毛细管中的样品进行冲洗,同时施加分离电场,使得样品中的各组分在分离毛细管中充分分离,提升了分离效果,并且分离速度较快,同时产品结构简单,操作方便。
虽然已经详细说明了本实用新型及其优点,但是应当理解在不超出由所附的权利要求所限定的本实用新型的精神和范围的情况下可以进行各种改变、替代和变换。而且,本申请的范围不仅限于说明书所描述的过程、设备、手段、方法和步骤的具体实施例。本领域内的普通技术人员从本实用新型的公开内容将容易理解,根据本实用新型可以使用执行与在此所述的相应实施例基本相同的功能或者获得与其基本相同的结果的、现有和将来要被开发的过程、设备、手段、方法或者步骤。因此,所附的权利要求旨在在它们的范围内包括这样的过程、设备、手段、方法或者步骤。
- 还没有人留言评论。精彩留言会获得点赞!