直肠肿瘤标志物及其应用、试剂盒的制作方法
本发明属于生物医药技术领域,具体涉及一种直肠肿瘤标志物及其应用、试剂盒。
背景技术:
细胞自噬(autophagy)是多细胞生物的一种“自食”现象,细胞通过包裹胞浆内容物将其运送到溶酶体系降解以循环使用降解产物供正常活动之需,该现象具有进化保守性。自噬是机体重要的防御和保护机制,在许多生理和病理过程中扮演着复杂而多效的角色。在细胞生存受到威胁时,如缺氧或营养缺失,自噬可通过溶酶体降解生存非紧急的蛋白和细胞器等,循环使用新陈代谢营养原料以促进细胞存活;自噬还可以降解和消除有毒性倾向的陈旧蛋白以及蛋白聚集体,形成保护机制以抵抗神经退行性病变;此外,自噬亦能吞噬入侵的细菌和病毒,将其锁定在自噬体内,最终运送到溶酶体消除以起到免疫防御的作用。自噬作用的紊乱会引起许多病理反应,肿瘤即是其功能紊乱的结果之一。
自噬需要多个信号通路和酶复合物的协同作用,beclin1(bcl2-bindingmyosin-likeprotein1)为自噬分子机制的核心成分,是beclin1-vps34复合体中的骨架蛋白。vps34是哺乳动物iii型磷脂酰肌醇3激酶(pi3k),它特异性地磷酸酯化肌糖环三位的磷脂酸肌醇并将其转化为磷脂酸肌醇3磷酸酯(pi3ps)。vps34胞质激酶活性的激活是自噬启动机制中的关键步骤,因为自噬过程的标志成员-用来包裹胞浆内容物的双膜自噬体-的形成需要大量由vps34产生的pi3ps。beclin1与vps34紧密结合,为自噬调节因子提供相互作用的平台,因此它在自噬调控中扮演着独特的角色。就目前所知,多个自噬调节因子均通过与beclin1相互作用而形成功能独特的beclin1-vps34次级复合体以调节vps34的活性,从而发挥各自对自噬过程的调节作用。beclin1-vps34复合体活性的调节除了通过与自噬调控因子的结合来实现以外,还可以通过beclin1磷酸化实现,从而改变自噬强度。beclin1可在某些部位被磷酸化,从而影响beclin1-vps34复合体的形成,继而敏锐而准确地针对细胞内诸多影响因素产生应答。
直肠肿瘤是由直肠组织细胞发生恶变而形成的从齿状线至乙状结肠交界处之间的肿瘤,其位置深入盆腔,手术后复发率高。其成因未明,目前认为的高危因素涉及营养不均衡,即动物脂肪和蛋白质摄入过高而食物纤维摄入不足。直肠肿瘤的发病率逐年增加,仅次于肺癌及胃癌,未来或可超过肺癌及胃癌,跃居第一,因此直肠肿瘤的诊断及治疗是当今世界极为重要的研究课题。当前直肠肿瘤通行的诊断流程所涉及的特异性生物标志物有癌胚抗原(cea)和糖链抗原19-9(ca19-9)两种,前者用于诊断和检测,后者用于预后评估,两者须联合应用,但失误率依然存在,需要更多检测手段以佐证,如影像学和内窥镜检查,而这些检查手段均有各自的缺点,如耗时、有创伤性、价格昂贵等,对病人构成身体、精神加经济等多重分担。尤其值得注意的是,直肠肿瘤中的中下段肿瘤因接近于肛管括约肌,导致术后保留肛门成为一个难题,这也使得直肠肿瘤成为手术方法上争议最大的一种疾病,临床医师采取的策略通常是“先保命,再保肛”。但由于人工肛门通过腹壁结肠造瘘而成,患者必须永久性地于腹壁位置排便,因心理及社会原因,由此带来极大的精神痛苦,严重影响患者的生活质量和生命尊严,以至于很多患者宁肯选择死亡也不愿接受腹壁人造肛门。
直肠肿瘤的防治难点包括:1)早期诊断,由于患者病情的个体性,用于早期筛查的生物标志物的选取颇为困难,使得多数病人查出时已是中晚期;2)保肛,手术治疗能否保住肛门,成为患者的主要关注点;3)耐药性,化疗药物由于分子靶标特异性差,使得耐药性和药物副作用明显。因此寻找个性化靶标对于直肠肿瘤的防治非常关键。
技术实现要素:
本发明的目的在于克服现有技术的上述不足,提供一种直肠肿瘤标志物及其应用、试剂盒,旨在解决现有直肠肿瘤的特异性生物标志物有限及直肠肿瘤防治困难的技术问题。
为实现上述发明目的,本发明采用的技术方案如下:
一方面,本发明提供一种直肠肿瘤标志物,所述直肠肿瘤标志物为beclin1蛋白。
另一方面,本发明提供一种用于检测上述beclin1蛋白的表达水平和/或磷酸化水平的试剂在制备用于检测和/或诊断直肠肿瘤或用于对直肠肿瘤患者的治疗和/或预后评价的试剂盒中的应用。
最后,本发明还提供一种检测和/或诊断直肠肿瘤或对肠肿瘤患者的治疗和/或预后评价的试剂盒,所述试剂盒包括检测上述beclin1蛋白的表达水平和/或磷酸化水平的试剂。
本发明提供的直肠肿瘤标志物为beclin1蛋白,该beclin1蛋白的表达水平和/或磷酸化水平与直肠肿瘤具有相关性。我们从细胞自噬角度出发,以该通路中的骨架蛋白beclin1为研究对象,首次对直肠肿瘤临床样本中的beclin1水平及磷酸化水平表征。beclin1的状态可以分为自噬促进型和自噬抑制型,自噬的状态可以分为肿瘤细胞有益型和肿瘤细胞有害型。肿瘤处于不同分期(形成与发展,转移与浸润,以及放化疗)时,自噬处于不同的状态中,因此可以通过监测beclin1的状态(蛋白总水平与磷酸化修饰水平)来调整肿瘤患者的治疗方案,如对于自噬促进-肿瘤细胞有益型(处于肿瘤生长过程中)和自噬抑制-肿瘤细胞有害型(处于有效治疗过程中)患者,应该选择自噬抑制型化疗药物;对于自噬促进-肿瘤细胞有害型(处于有效治疗过程中)和自噬抑制-肿瘤细胞有益型(处于肿瘤生长过程中)患者,应该选择自噬促进型化疗药物。因此,beclin1的状态可以用作直肠肿瘤的早期诊断、以及治疗效果跟踪以及预后评价提供参考。
本发明提供在一种用于检测上述beclin1蛋白的表达水平和/或磷酸化水平的试剂在制备用于检测和/或诊断直肠肿瘤或对直肠肿瘤患者的治疗和/或预后评价的试剂盒中的应用,该应用体现在产品上为一种检测和/或诊断直肠肿瘤或对肠肿瘤患者的治疗和/或预后评价的试剂盒。通过收集临床直肠肿瘤组织样本,研究病患个性化表达beclin1的情况,在beclin1磷酸化的个体化与肿瘤个体化之间建立可供临床参考的联系,为临床诊断和治疗提供帮助。该试剂盒可对直肠肿瘤临床样本中的beclin1蛋白水平以及beclin1磷酸化水平两个层次的检测,考察beclin1表达与修饰个性化与直肠肿瘤表征个性化之间的关系,通过联合评估,可以作为直肠肿瘤早期检测和/或诊断的参考,以及直肠肿瘤患者的用药监测、耐药性预测的参考。
附图说明
图1为本发明实施例1中利用恒温量热滴定法测定体外蛋白beclin1_wt、beclin1_229e233e与atg14l相互作用结果数据图;
图2为本发明实施例2中beclin1磷酸化条件测试的免疫印迹分析结果图;
图3为本发明实施例3中临床直肠肿瘤lc3-i/ii及beclin1/beclin1磷酸化表达水平的免疫印记分析结果图;
图4为本发明实施例4中直肠肿瘤临床样本中不同组织部位beclin1表达水平的免疫组化分析结果图;
图5为本发明实施例5中经抗直肠肿瘤药物处理后的hela细胞中lc3-i/ii及p62表达水平的免疫印记分析结果图。
具体实施方式
为了使本发明要解决的技术问题、技术方案及有益效果更加清楚明白,以下结合实施例,对本发明进行进一步详细说明。应当理解,此处所描述的具体实施例仅仅用以解释本发明,并不用于限定本发明。
一方面,本发明实施例提供了一种直肠肿瘤标志物,该直肠肿瘤标志物为beclin1蛋白。该beclin1蛋白的表达水平和/或磷酸化水平与直肠肿瘤具有相关性。通过研究,自噬状态的个性化与直肠肿瘤的个性化一一对应,提出beclin1表达及修饰化状态,可从分子水平上判断直肠肿瘤病人的个体特征,为直肠肿瘤个性化治疗提供理论依据。
本发明一实施例中,用beclin1突变蛋白模拟beclin1磷酸化与自噬活化因子atg14l之间的结合力。完整的beclin1一共有三个功能区(bh3区、ccd区、ecd区),本发明实施例以人源beclin1的部分氨基酸序列,即bh3区和ccd区的序列(编号为102-268的氨基酸序列)作为野生型beclin1蛋白(简称beclin1_wt),将该野生型beclin1蛋白中的两个酪氨酸(氨基酸编号分别229和233)同时突变为谷氨酸形成突变体(简称beclin1_229e233e,e为谷氨酸,glutamicacid,三字母简写为glu,单字母简写为e,谷氨酸酸性氨基酸,可从电荷上模拟磷酸化后的原子微环境),即该突变体长度为起始氨基酸编号102,终止氨基酸编号268,一共167个氨基酸,再引入连接表达载体的4个氨基酸(即最开始的4个氨基酸“gpgs”),因此一共171个氨基酸组成本发明的beclin1突变蛋白,该beclin1突变蛋白的氨基酸序列为seqidno:1:gpgseasdggtmenlsrrlkvtgdlfdimsgqtdvdhplceectdtlldqldtqlnvtenecqnykrcleileqmneddseqlqmelkelaleeerliqeledveknrkivaenlekvqaeaerldqeeaqeqreesefkrqqlelddelksvenqmryaqtqldklkktn。
因自噬的启动需要经历三个步骤:第一步,beclin1_wt-beclin1_wt同源二聚体解离,变为belcin1_wt单体;第二步,beclin1_wt单体与atg14l形成beclin1_wt-atg14l异源二聚体;第三步,beclin1_wt-atg14l异源二聚体作为结合平台,募集相应活化因子,启动自噬。基于这种蛋白相互作用的分子机制,在已解析的beclin1_wt-beclin1_wt同源二聚体三维结构的基础上,通过基因突变手段,设计了人源beclin1_229e233e突变,旨在模拟beclin1229、233两个位点的酪氨酸磷酸化。结果显示,229、233两个位点的酪氨酸被磷酸化后,将下调beclin1_wt与atg14l之间的相互作用,进一步暗示其产生自噬抑制作用。
另一方面,本发明实施例提供一种用于检测上述beclin1蛋白的表达水平和/或磷酸化水平的试剂在制备用于检测和/或诊断直肠肿瘤或用于对直肠肿瘤患者的治疗和/或预后评价的试剂盒中的应用。本发明实施例以beclin1蛋白总水平及beclin1磷酸化水平作为检测指标应用于直肠肿瘤早期诊断与研究,以制备检测和/或诊断直肠肿瘤或对直肠肿瘤患者的治疗和/或预后评价的试剂盒。
优选地,beclin1蛋白的磷酸化水平为beclin1蛋白的229位点和233位点的酪氨酸磷酸化水平。在本发明一实施例中,对beclin1磷酸化的条件测试,表明229、233这两个位点或为egfr的主要底物位点,证明其担任重要的由结构修饰引起功能改变的角色。
优选地,检测beclin1蛋白的表达水平的试剂包括抗beclin1蛋白抗体或荧光探针修饰的beclin1蛋白抗体,检测述beclin1蛋白的磷酸化水平的试剂包括抗磷酸化酪氨酸抗体。在本发明一实施例中,用抗beclin1抗体对临床直肠癌癌组织及癌旁组织进行免疫组化实验分析;在本发明另一实施例中,用抗beclin1抗体和抗磷酸化酪氨酸抗体对临床直肠肿瘤beclin1/beclin1磷酸化表达水平的免疫印记分析。
优选地,检测所述的beclin1蛋白的表达水平和/或磷酸化水平的方法为免疫学方法。在本发明实施例中,免疫学方法包括免疫印迹法、免疫组化法和免疫共沉淀法。
优选地,对直肠肿瘤患者的治疗和/或预后评价的试剂盒可与抗直肠肿瘤药物联合用药。抗直肠肿瘤药物包括卡培他滨、伊立替康、奥沙利铂、氟尿嘧啶和亚叶酸钙中的至少一种。在本发明一实施例中,通过对临床抗直肠肿瘤药物自噬能力分类,“奥沙利铂+氟尿嘧啶+亚叶酸钙”联用有自噬促进作用;而卡培他滨和伊立替康未有自噬促进作用,该试剂盒通过beclin1蛋白的表达水平和/或磷酸化水平,获得相关信息作为直肠肿瘤用药监测、耐药性预测的参考。
最后,本发明实施例提供一种检测和/或诊断直肠肿瘤或对肠肿瘤患者的治疗和/或预后评价的试剂盒,该试剂盒包括上述beclin1蛋白的表达水平和/或磷酸化水平的试剂。具体地,beclin1蛋白的磷酸化水平是指beclin1蛋白的229位点和233位点的酪氨酸磷酸化水平,这两个位点或为egfr的主要底物位点。具体地,检测beclin1蛋白的表达水平的试剂包括抗beclin1蛋白抗体或荧光探针修饰的beclin1蛋白抗体,检测beclin1蛋白的磷酸化水平的试剂包括抗磷酸化酪氨酸抗体。
本发明先后进行过多次试验,现举一部分试验结果作为参考对发明进行进一步详细描述,下面结合具体实施例进行详细说明。
实施例1beclin1磷酸化的作用模拟
恒温量热滴定法测定体外蛋白beclin1_wt、beclin1_229e233e与自噬调节因子atg14l相互作用,用beclin1突变蛋白模拟beclin1磷酸化与自噬活化因子atg14l之间的结合力。具体过程如下:
先在大肠杆菌中实现人源beclin1_wt、beclin1_229e233e、atg14l蛋白的可溶表达,并分离纯化得到足量的目的蛋白;beclin1_wt、beclin1_229e233e及atg14l均被透析至缓冲液(含有50mmtris,150mmnacl;ph8.0)中;在等温量热滴定仪的滴定注射器分别上样40μl的beclin1_wt(浓度12mg/ml)和40μl的beclin1_229e233e(浓度12mg/ml),并在等温量热滴定仪之样品池上样220μl的atg14l(浓度500μg/ml),利用等温量热滴定仪itc200(microcal)分别测定自噬骨架蛋白beclin1_wt与atg14l、beclin1_229e233e与atg14l之间的相互作用所引起的热转化;每次测定具有10-40次进样,每两次进样之间平衡180秒,其数据用origin7.0采集和分析。
通过测定结合常数并进行定量计算,结果如图1所示:从图中数据可知,较之野生型beclin1_wt与atg14l之间的相互作用(图1a为恒温量热滴定测定beclin1_wt与atg14l相互作用),突变型beclin1_229e233e与atg14l之间的相互作用(图1b为恒温量热滴定测定beclin1_229e233e与atg14l相互作用)减弱,暗示229、233两个位点的酪氨酸被磷酸化后,将下调beclin1_wt与atg14l之间的相互作用,进一步说明其产生自噬抑制作用。
实施例2beclin1磷酸化的条件测试
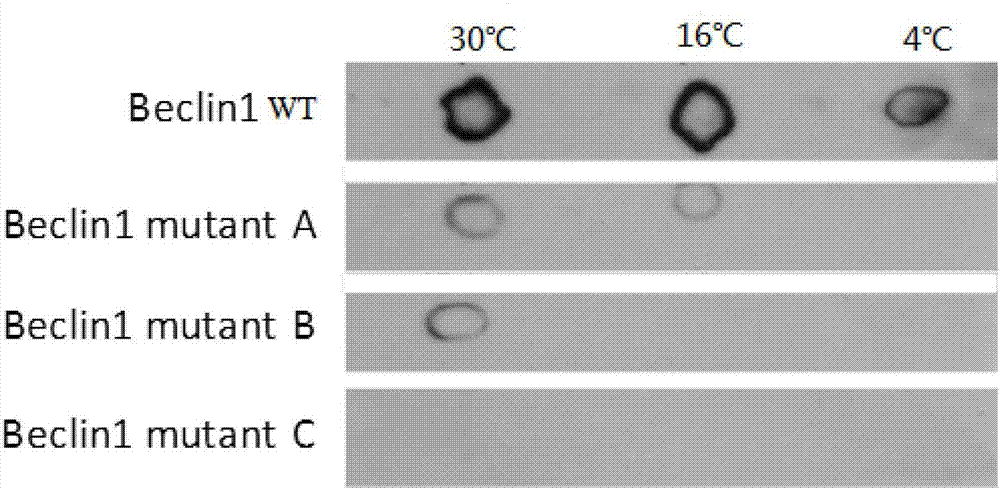
利用大肠杆菌对beclin1野生型(beclin1_wt)及突变型(针对229、233酪氨酸位点进行突变)进行异源表达,分离纯化,测试磷酸化条件。在egf、egfr的作用下,beclin1_wt及三种突变(beclin1mutanta:beclin1_229e,只对229酪氨酸位点进行突变;beclin1mutantb:beclin1_233e,只对233酪氨酸位点进行突变;beclin1mutantc:beclin1_229e223e,针对229和233两个酪氨酸位点进行突变),分别在4℃、16℃、30℃下进行磷酸化测试,采用免疫印迹法(westernblot)进行表征,其中,一抗为抗磷酸化酪氨酸抗体。
实验结果如图2所示:beclin1_wt的酪氨酸可以被egfr磷酸化,且受温度的影响较小;而beclin1_229e和beclin1_233e则明显信号减弱,这表明229、233这两个位点为egfr的底物,而且其敏感性受温度影响明显;而beclin1_229e233e没有检测到信号,表明229、233这两个位点或为egfr的主要底物位点。此试验结果说明,该两个位点担任重要的由结构修饰引起功能改变的角色。
实施例3临床直肠肿瘤lc3-i/ii、beclin1总水平和磷酸化水平分析
获取五份直肠肿瘤临床样本(iii期,手术所获样本,编号a、b、c、d、e),用免疫印迹法(westernblot)对五份样本中lc3-i/ii及beclin1总水平进行表征:即先从石蜡组织中提取对应的目的蛋白,并用对应的抗体直接检测;同时,也对五份样本中的beclin1磷酸化水平进行表征:即先用抗beclin1抗体进行免疫共沉淀后,再用抗磷酸化酪氨酸抗体检测。
检测结果如图3的所示:结果表明,直肠肿瘤晚期自噬水平与beclin1的总水平之间无明显关联。结合该五份样本的临床化疗实情,化疗药物影响了beclin1的磷酸化调控通路,如化疗靶向联用中的西妥昔单抗与帕尼单抗为靶向egfr的抗体,其对egfr酪氨酸激酶活性的抑制作用使得beclin1磷酸化水平下调,从而解除自噬抑制,所以结果显示:beclin1磷酸化(图中的p-beclin1)水平越低,lc3-ii条带强度增加。然而自噬增强对于抗直肠肿瘤治疗是利是弊有待商榷,我们发现图3中的样本d的临床评价不及样本c,这提示beclin1磷酸化水平可以作为用药监测的参考。因此,beclin1表达水平及其与p-beclin1的比值联合评估,可以作为用药监测、耐药性预测的参考。
实施例4临床直肠肿瘤不同组织中beclin1表达水平分析
选取20例临床直肠癌病人的组织样本(iii期,手术所获样本),并用抗beclin1抗体对每个直肠癌病人的直肠癌癌组织及癌旁组织进行免疫组化实验分析。
其结果如图4所示:从图可知,beclin1在直肠癌癌细胞中的表达水平(图4b:癌组织免疫组化结果)明显高于直肠癌癌旁组织的表达水平(图4a:癌旁组织免疫组化结果),这说明从正常细胞向直肠肿瘤发展的过程中,beclin1的表达水平升高。因此,beclin1的表达水平可以作为直肠肿瘤早期诊断的参考。
实施例5临床抗直肠肿瘤药物自噬能力分类
用免疫印记分析法分析抗直肠肿瘤药物处理后的hela细胞中lc3-i/ii及p62的表达水平,根据lc3-ii的转化率以及p62的移除率分类直肠肿瘤药物的自噬能力。具体过程如下:
先将hela细胞分四组进行培养,每组转染lc3及p62进入hela细胞后进行过量表达;其中三组分别用三类直肠肿瘤化疗的常规药物(druga:卡培他滨;drugb:伊立替康;drugc:“奥沙利铂+氟尿嘧啶+亚叶酸钙”联用)处理hela细胞,另外一组做空白对照(control);对四组hela细胞于37℃培养箱中孵育24小时,并将hela细胞用pbs清洗,lysisbuffer裂解,最后提取细胞蛋白。将提取的细胞蛋白经过煮沸变性后,利用免疫印迹实验进行目标蛋白表征:即表征lc3-ii的转化率以及p62的移除率。
最终结果如图5所示:实验结果表明,“奥沙利铂+氟尿嘧啶+亚叶酸钙”联用组(drugc)相对未用抗直肠肿瘤药物处理组(control),其lc3-ii的转化率显著提高,同时p62蛋白移除率(降解速率)提高,即表明drugc有自噬促进作用;而在卡培他滨组(druga)和伊立替康组(drugb)中,lc3-ii的转化率以及p62的移除率未见明显变化,即druga和drugb未有自噬促进作用,显影后扫描定量分析,drugc的lc3-ii转化率为druga和drugb的两倍。同过对直肠肿瘤药物进行以自噬能力为标准的分类,将对临床直肠肿瘤患者治疗提供指导。
以上所述仅为本发明的较佳实施例而已,并不用以限制本发明,凡在本发明的精神和原则之内所作的任何修改、等同替换和改进等,均应包含在本发明的保护范围之内。
sequencelisting
<110>深圳人仁生物医药科技有限公司
<120>直肠肿瘤标志物及其应用、试剂盒
<160>1
<170>patentinversion3.5
<210>1
<211>171
<212>prt
<213>人工序列
<400>1
glyproglyserglualaseraspglyglythrmetgluasnleuser
151015
argargleulysvalthrglyaspleupheaspilemetserglygln
202530
thraspvalasphisproleucysgluglucysthraspthrleuleu
354045
aspglnleuaspthrglnleuasnvalthrgluasnglucysglnasn
505560
tyrlysargcysleugluileleugluglnmetasngluaspaspser
65707580
gluglnleuglnmetgluleulysgluleualaleugluglugluarg
859095
leuileglngluleugluaspvalglulysasnarglysilevalala
100105110
gluasnleuglulysvalglnalaglualagluargleuaspglnglu
115120125
glualaglngluglnarggluglusergluphelysargglnglnleu
130135140
gluleuaspaspgluleulysservalgluasnglnmetargtyrala
145150155160
glnthrglnleuasplysleulyslysthrasn
165170
- 还没有人留言评论。精彩留言会获得点赞!
- 普适型用于同时检测多种肿瘤标志物的微流控芯片装置的制造方法
- 男性适用的典型肿瘤标志物联合检测用微流控芯片装置的制造方法
- 女性适用的典型肿瘤标志物联合检测用微流控芯片装置的制造方法
- 一种检测口腔癌的标志物及其试剂盒的制造方法与工艺
- microRNA 标志物组及其在制备检测胃癌淋巴结转移试剂盒中的应用的制造方法与工艺
- 基于弹性蛋白酶荧光底物检测乳腺癌肿瘤标志物CA153的酶联免疫试剂盒制备方法与制造工艺
- 检测和评价力量训练效果的miRNA标志物或其组合及其应用的制造方法与工艺
- 一种最优超平面的构建方法、动态优化系统和构建装置与制造工艺
- 癌症标志物及癌症的判定方法与制造工艺
- 检测尿液中单羟酚类代谢物的试剂盒及其制备方法与制造工艺