一种亚铁离子的检测方法与流程
本发明涉及一种亚铁离子的检测方法,具体涉及一种以碳量子点-二氧化锰复合材料作为荧光探针检测亚铁离子的方法。
背景技术:
铁元素在自然界中很常见,也是水环境中最活泼的元素之一。此外,铁广泛存在于人体和动植物体及食品药品中,是人体不可缺少的微量元素,对人体起着至关重要的作用,比如铁参与氧气运输、参与很多辅酶形成、维持造血功能、增强免疫功能等但过量摄入对人体有毒,产生潜在危害。建立快速、准确的方法测定环境水样中铁的含量具有重要的意义。
目前测铁的方法主要有三类。第一,电感耦合等离子体发射光谱,即icp-aes,此方法检测限低,精度高,但此法测试费昂贵且只能测总铁离子。第二,原子吸收,此法和icp-aes有着同样的缺点,并且样品前处理比较繁琐。第三,分光光度法。
技术实现要素:
本发明提供了一种亚铁离子的检测方法,其以碳量子点-二氧化锰复合材料作为荧光探针实现对亚铁离子的高灵敏性定量检测。
本发明采取的技术方案为:
一种亚铁离子的检测方法,所述检测方法以碳量子点-二氧化锰复合材料作为荧光探针来检测亚铁离子。
所述检测方法包括以下步骤:
(1)制备碳量子点-二氧化锰复合材料;
(2)将步骤(1)得到的碳量子点-二氧化锰复合材料稀释10倍,然后加入不同浓度的亚铁离子,调节体系的ph为4.4~5.5,并测试体系的其荧光光谱;
(3)在直角坐标系中,以荧光回升强度δf对加入的亚铁离子浓度作图,并进行曲线拟合,得到线性方程,根据线性方程即可计算出任意荧光回升强度下所对应的fe2+的浓度,其中δf=f–f0,f0为不加fe2+体系在450nm波长处的荧光强度,f为加入fe2+体系在450nm波长处的荧光强度。
所述线性方程为δf=-20.5+228.7[fe2+],其线性相关系数r2为0.996,检测限为0.17μm;且在0~3.5μm范围内具有很好的线性关系。
所述步骤(2)中,亚铁离子的终浓度依次为0、0.15μm、0.3μm、0.75μm、1.0μm、1.25μm、1.5μm、1.75μm、2.0μm、2.25μm、2.5μm、3.0μm、3.5μm。
进一步地,所述步骤(2)中,调节体系的ph为4.8。
所述碳量子点-二氧化锰复合材料的制备方法包括以下步骤:
(1-1)制备碳量子点:将柠檬酸和乙二胺溶解于去离子水中,采用水热法制备得到棕黑色的产物,将产物装入透析袋中,放入蒸馏水中渗析后得到碳量子点溶液;
(1-2)制备二氧化锰纳米片溶液:将过氧化氢和五水合四甲基氢氧化铵混合完全后快速将其加入到四水合二氯化锰溶液中,搅拌反应8h,依次用乙醇、去离子水洗涤产物;将洗涤后的产物分散于去离子水中,制得浓度为220μm二氧化锰纳米片溶液;
(1-3)将步骤(1-1)得到的碳量子点溶液按体积比1:1加入到步骤(1-2)得到的二氧化锰纳米片溶液中,即可制得碳量子点-二氧化锰复合材料。
所述步骤(1-1)中,柠檬酸:乙二胺:去离子水=1.05g:335μl:10ml;水热反应的温度为200℃,时间为5h。
所述步骤(1-1)中,所述透析袋的截留分子量为3000da;蒸馏水的体积为150~200ml,渗析时间为4~5小时。
所述步骤(1-2)具体包括:将2ml质量浓度为30%的h2o2加入到12ml浓度为1mol/l的五水合四甲基氢氧化铵中,混合完全后快速将其加入到10ml浓度为0.3mol/l的四水合二氯化锰溶液中,溶液迅速变为深棕色,持续搅拌8h,依次用95%的乙醇、去离子水洗涤产物,过滤,将产物分散在去离子水中,制得浓度为220μm的二氧化锰溶液。
所述检测方法可排除其他金属离子的干扰,。所述其他金属离子为co2+、ni2+、zn2+、na+、cu2+、mg2+、ca2+、cd2+、k+和al3+。
本发明公开的亚铁离子的检测方法以柠檬酸为碳源采用水热法制备具有很强荧光的碳量子点,利用碳量子点(cds)的荧光“猝灭-回升”机理构建了一种快速检测fe2+的方法。首先,以柠檬酸为碳源采用水热法制备cds,然后将cds加入到二氧化锰(mno2)纳米薄片中,通过内滤光效应猝灭cds的荧光,形成cds-mno2探针。当向上述探针中加入fe2+,由于mno2会与fe2+发生氧化还原反应从而使mno2纳米薄片溶解,生成mn2+离子,从而使cds的荧光恢复,且在一定条件下荧光增强程度与fe2+离子浓度成正比。
本发明借助于mno2纳米片能使cds的荧光发生猝灭。而fe2+可与mno2纳米片发生氧化还原反应,从而使mno2纳米薄片溶解,生成mn2+离子,导致cds的荧光回升。所述检测方法的检测限低至0.17μm,对fe2+具有很好的选择性,可排除其他金属离子的干扰。
与现有技术相比,本发明公开的亚铁离子的检测方法具有简单、实用、可靠等优点,可以广泛应用于实际,其检测方法为以后研究发明高灵敏低成本的检测fe2+探针提供了一种新的思路。
附图说明
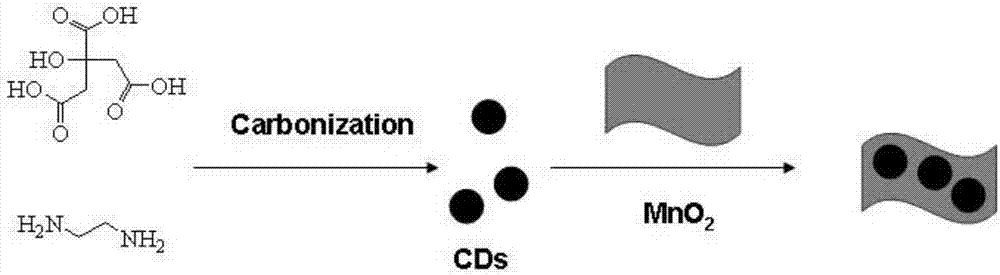
图1为碳量子点-二氧化锰复合材料的合成示意图;
图2为cds(a)、mno2纳米片(b)、碳量子点-二氧化锰复合材料(c)的透射电镜图;
图3为cds-mno2体系中加入不同浓度的fe2+(自上而下fe2+的浓度为:0~3.5μm)的荧光光谱图;
图4为荧光回升强度δf与fe2+浓度的线性关系图;
图5为cds-mno2体系对亚铁离子的选择性实验图;
图6为mno2纳米片的浓度对cds-mno2体系检测fe2+的影响;
图7为体系ph对cds-mno2体系检测fe2+的影响。
具体实施方式
实施例1
一种亚铁离子的检测方法,包括以下步骤:
(1)制备碳量子点-二氧化锰复合材料,其合成示意图如图1所示;
(1-1)称取1.05g柠檬酸、335μl乙二胺溶解于10ml去离子水中,充分搅拌使其完全溶解然后,将溶液转移到容积为30ml的聚四氟乙烯-高压反应釜,200℃加热5h,待反应结束后,自然冷却到室温,得到棕黑色的产物,将产物装入截留分子量为3000da透析袋中密封,再放入到150ml~200ml的去离子水中渗析4~5小时,收集渗析液,即可得到cds溶液,放入冰箱中冷藏备用。其透射电镜图如图2a所示,从图中可以看出cds粒径在2~4nm之间,且分散性较好;
(1-2)将2ml质量浓度为30%的h2o2加入到12ml浓度为1mol/l的五水合四甲基氢氧化铵中,混合完全后快速将其加入到10ml浓度为0.3mol/l的四水合二氯化锰溶液中,溶液迅速变为深棕色,持续搅拌8h,依次用95%的乙醇、去离子水洗涤产物,过滤得到黑色固体产物,再将其分散在去离子水中,利用超声分散得到分散均匀的二氧化锰纳米片溶液,其浓度为220μm。其透射电镜图如图2b所示,从图中可以看出mno2纳米片非常纯净、形态较好、分散均匀;
(1-3)将步骤(1-1)得到的碳量子点溶液按体积比1:1加入到步骤(1-2)得到的二氧化锰纳米片溶液中,搅拌混合均匀后,即可制得碳量子点-二氧化锰复合材料。其透射电镜图如图2c所示,从图中可以看出cds已经附着在mno2纳米片表面,表明碳量子点-二氧化锰(cds-mno2)复合材料的荧光探针已经合成。
(2)将步骤(1)得到的碳量子点-二氧化锰复合材料稀释10倍,此时溶液中二氧化锰纳米片的浓度为11μm,然后加入不同浓度的亚铁离子,以pbs缓冲溶液调节体系的ph为4.8,亚铁离子的终浓度依次为:0、0.15μm、0.3μm、0.75μm、1.0μm、1.25μm、1.5μm、1.75μm、2.0μm、2.25μm、2.5μm、3.0μm、3.5μm,并测试体系的其荧光光谱,得到的荧光光谱图如图3所示,从图中可以看到,随着fe2+浓度的逐渐增大,体系的荧光强度逐渐增强。
(3)在直角坐标系中,以荧光回升强度δf对加入的亚铁离子浓度作图,并进行曲线拟合,如图4所示,从图中可以看出,在0~3.5μm范围内δf与[fe2+]呈现出良好的线性关系,得到线性方程δf=-20.5+228.7[fe2+],其线性相关系数r2为0.996,检测限为0.17μm,根据线性方程即可计算出任意荧光回升强度下所对应的fe2+的浓度,其中δf=f–f0,f0为不加fe2+体系在450nm波长处的荧光强度,f为加入fe2+体系在450nm波长处的荧光强度。
实施例2
选择性实验
向实施例1中的步骤(1)得到的碳量子点-二氧化锰复合材料中加入相同浓度的co2+、ni2+、zn2+、na+、cu2+、mg2+、ca2+、cd2+、k+和al3+,测其荧光强度,并以δf为纵坐标,离子种类为横坐标作柱状图,之后再分别向包含这些离子的体系中加入fe2+,测其荧光强度,并以δf为纵坐标,离子种类为横坐标作柱状图,此试验中,其他金属离子(co2+、ni2+、zn2+、na+、cu2+、mg2+、ca2+、cd2+、k+和al3+)的终浓度为2.0μmol/l,fe2+的终浓度为2.0μmol/l,其他实验条件同实施例1。
结果如图5所示,从图中可以看出,当往cds-mno2体系中加入相同浓度的其他金属离子时,其他金属离子对cds-mno2体系的荧光强度的回升基本无影响。但是,当继续向体系中加入fe2+时,体系的荧光强度回升。结果证明cds-mno2体系作为荧光传感器在检测fe2+具有非常好的选择性和专一性,因此,此方法可以用来定量检测溶液中fe2+的含量。
实施例3
mno2纳米片的浓度对fe2+检测的影响
向含有不同mno2纳米片浓度的cds-mno2复合材料中,加入终浓度为1μm的fe2+,其他实验条件同实施例1,测其荧光强度,并以δf为纵坐标,mno2纳米片的终浓度为横坐标作曲线图,如图6所示,从图中可以看出,mno2纳米片浓度很低时cds的荧光回升较低;然而当mno2纳米片浓度太高时会抑制cds的荧光回升,因为溶液中的fe2+可以与游离的mno2纳米片发生反应,从而阻碍了cds与mno2纳米片相结合。基于以上两个因素,mno2纳米片的最佳浓度为11μm。
实施例4
体系ph对fe2+检测的影响
向不同ph值的cds-mno2复合材料的荧光探针体系中,再加入终浓度为1μm的fe2+,其他实验条件同实施例1,测其荧光强度,并以δf为纵坐标,体系ph为横坐标作曲线图,如图7所示,从图中可以看出,当ph值在3.5~4.8的范围内,体系的δf值逐渐增大,在ph=4.8时到达峰的最高点。这是因为当ph值较低时cds的荧光强度会减弱进而影响检测效果。当ph大于4.8时,δf会减小。这可能是由于随着ph的增大,fe2+会发生水解。
上述参照实施例对一种亚铁离子的检测方法进行的详细描述,是说明性的而不是限定性的,可按照所限定范围列举出若干个实施例,因此在不脱离本发明总体构思下的变化和修改,应属本发明的保护范围之内。
- 还没有人留言评论。精彩留言会获得点赞!