一种无适配体纳米金水溶胶可视化检测三聚氰胺的方法与流程
本发明涉及一种三聚氰胺的检测方法,具体涉及一种成本低、无适配体纳米金水溶胶可视化检测三聚氰胺的方法,涉及三聚氰胺检测技术领域。
技术背景
三聚氰胺(melamine)是一种白色无臭的含氮杂环化合物,分子式为c3n3(nh2)3,被广泛应用在塑料,肥料和树脂等化工产业中,它对人体有害,不可用于食品加工或食品添加。但是由于三聚氰胺含氮量很高且便宜,将其作为富含蛋白质原料的添加剂添加到食品中可以明显提高蛋白质总的含量,所以有不法商家往牛奶、饲料等中添加三聚氰胺。三聚氰胺在人体内可水解成三聚氰酸,二者结合形成网状不溶物,该不溶物在体内堆积过多会对人体肾脏造成伤害,近而损伤人体甚至造成死亡。因此,检测三聚氰胺非常重要。
目前检测三聚氰胺的方法有高效液相色谱法、气相色谱-质谱法、毛细管电泳法、拉曼光谱法等。但这些方法都很复杂,而且要借用大型仪器设备,更谈不上现场随机检测。纳米金具有适宜的物理特性,如粒径可控、溶胶颜色可变、稳定性好等,并具有好的生物相容性,广泛用于分子成像、癌症的诊断及治疗,尤其是用于传感检测。邢海波等人(邢海波,张素霞,唐意红,周培.适配体修饰的纳米au比色法检测牛奶中的三聚氰胺.应用技术学报.2017,17(2):151-159.)提出用纳米au检测三聚氰胺,该方法是用化学的方法如用柠檬酸三钠作为保护剂及还原剂制备纳米金,但在处理工序中增加了成本,带来了污染,并且检出限在0.1μmol/l左右,灵敏度有待提升。后来衍生出很多纳米金可视化检测三聚氰胺的方法,例如专利cn101300551a、cn101701260a,文献1(赵静,李永生,高秀峰.流动注射纳米au分光光度法快速测定乳制品中的三聚氰胺.分析试验室2016,35(8):961-965)、文献2(caoqian,zhaoh,heyj,etal.hydrogen-bonding-inducedcolorimetricdetectionmelaminebynonaggregation-basedau-npsasaprobe.biosensorsandbioelectronics,2010,25:2680-2685.)、文献3(nangao,pengchenghuang,fangyingwu.colorimetricdetectionofmelamineinmilkbasedontritonx-100modifiedgoldnanoparticlesanditspaper-basedapplication.spectrochimicaactaparta:molecularandbiomolecularspectroscopy192(2018)174-180.)。这些可视化检测方法多数是在纳米金溶胶中加入适配体,使纳米金颗粒上含有一层适配体如寡聚腺嘿吟核普酸、寡聚核苷酸、谷胱甘肽、dna,利用含有适配体的纳米金与牛奶中三聚氰胺发生特异性反应,从而检测三聚氰胺,该方法虽然达到了检测三聚氰胺的目的,但无形中增加了很多反应步骤,而且对环境造成了污染。
因此,如何寻找一种成本低、环境污染少、简便快捷、灵敏度高的三聚氰胺检测方法是一个非常有挑战性而且有意义的设想。
技术实现要素:
为了解决现今三聚氰胺检测方法存在的成本低、环境污染大、程序复杂等不足,本发明提供了一种无适配体纳米金水溶胶可视化检测三聚氰胺的方法,该方法不使用适配体,操作简便、快速、流程短,灵敏度高,对环境友好,能够三聚氰胺样品的现场随机可视化检测。
本发明具体技术方案如下:
一种无适配体纳米金水溶胶可视化检测三聚氰胺的方法,该方法包括以下步骤:
(1)将植物加入无水乙醇中,煮沸提取、过滤,得滤液;
(2)将滤液加入活性炭脱色后静置1天,得淡黄色植物提取液;
(3)将淡黄色植物提取液稀释,所得稀释液冷藏备用;
(4)取步骤(3)的稀释液,向其中加入待检样品,混合均匀后再加入氯金酸水溶液,调整ph为5.5~6.5后进行反应,通过目视比色法或紫外可见分光光度法检测三聚氰胺。
进一步的,上述方法中,所述目视比色法是指通过反应液颜色的变化来对三聚氰胺进行定性检测,随着三聚氰胺浓度的增加,反应液的颜色由酒红色逐渐向紫红色--紫色--蓝色--黄绿色变化,最终为黄绿色。
进一步的,上述方法中,所述紫外可见分光光度法是对三聚氰胺进行定量检测,步骤是:
(1)将植物加入无水乙醇中,煮沸提取、过滤,得滤液;
(2)将滤液加入活性炭脱色后静置1天,得淡黄色植物提取液;
(3)将淡黄色植物提取液稀释,所得稀释液冷藏备用;
(4)取步骤(3)的稀释液,向其中分别加入不同浓度的三聚氰胺标准溶液,混合均匀后再加入氯金酸水溶液,调整ph后进行反应,用紫外可见分光光度法检测反应后溶液的吸光度,建立三聚氰胺浓度和吸光度的标准曲线;
(5)取步骤(3)的稀释液,向其中加入待检样品,混合均匀后再加入氯金酸水溶液,调整ph后进行反应,用紫外可见分光光度法检测吸光度,根据标准曲线得到三聚氰胺的含量。
进一步的,采用紫外可见分光光度法检测时,检测波长为520-535nm。
进一步的,步骤(1)中,所述植物为龙眼叶、芦荟、红枣或绿茶,优选为绿茶。
进一步的,步骤(1)中,无水乙醇的用量为植物质量的35-45倍;煮沸提取时间为1-2h。
进一步的,步骤(2)中,加入活性炭脱色3-4h,然后静置1天进行充分脱色;活性炭的用量一般为滤液质量的0.5-1.5%。
进一步的,步骤(3)中,将淡黄色植物提取液用乙醇稀释3-10倍,所得稀释液在4℃的冰箱中冷藏储存。
进一步的,步骤(4)中,所述待检样品为牛奶,检测时,需要先对牛奶进行预处理,预处理步骤是:取待检牛奶样品,加入乙酸水溶液和乙酸铅水溶液使蛋白质沉淀,混合均匀后加入蒸馏水定容,离心取上清液,得预处理待检牛奶样品。优选的,乙酸水溶液的浓度为1-5wt%,乙酸铅水溶液的浓度为0.5-1.5wt%。优选的,乙酸水溶液的用量为牛奶质量的1-1.5倍,乙酸铅水溶液的用量为牛奶质量的1-1.5倍。
进一步的,步骤(4)中,氯金酸水溶液的浓度优选为1mmol/l。稀释液、待检样品与氯金酸水溶液的体积比为3-8:1:1。
进一步的,所述植物为龙眼叶、芦荟或红枣时,加入氯金酸水溶液后调整ph为9.5-10.5,在20-40℃下进行反应;所述植物为绿茶时,加入氯金酸水溶液后调整ph为5.5-6.5,在室温下进行反应。
进一步的,本发明植物提取液的有效成分为多糖、酚类化合物及黄酮类化合物,这些有效成分有空间位阻及静电吸附作用,能够吸附到au3+的周围,起到保护作用,阻止生成的纳米金团聚,而多糖、酚类化合物含有很多的羟基基团,能够将au3+还原为au0,多个au0团簇组成纳米au颗粒。与化学法即柠檬酸三钠还原au3+为au0法相比,本发明纳米金形成方法更为绿色环保,纳米金不易团聚,检测效果更好。
进一步的,经试验验证,本发明方法在氯化钠含量低于40mmol/l时仍能达到很高的检测灵敏度,对于恶劣环境下(比如海水被三聚氰胺污染)三聚氰胺的检测也能实现,且抗干扰能力强,具有很强的应用价值。
本发明方法中,可以通过溶液颜色的变化对三聚氰胺的含量进行可视化定性检测,当不含三聚氰胺时,溶液颜色为浅酒红色,随着三聚氰胺浓度的逐渐增加,溶液浅酒红色逐渐变浅,逐渐向紫红色—紫色—蓝色—黄绿色转变,最终变为黄绿色。变为黄绿色后,即使三聚氰胺浓度再增加,颜色也不再变化。
与现有技术相比,本发明有以下优点:
1、本发明以植物提取液作为保护剂和还原剂,温和条件下快速制备酒红色纳米金水溶胶,植物来源广泛、成本低,绿色环保,所得纳米金粒度小、在8nm左右、不团聚,植物提取液和纳米金水溶胶存放时间长,满足可视化检测三聚氰胺目的。
2、本发明纳米金溶胶无须用适配体进行修饰,步骤简单、快速、操作流程短、对环境友好。
3、本发明检测方法快速、简便,灵敏度高,抗干扰能力强,对三聚氰胺的检出限可达15nm。本发明方法能够对三聚氰胺样品进行可视化检测,可以现场采用采样检测,检测灵活度高,可以实现三聚氰胺的定性和定量检测。且可以对恶劣环境下的样品进行检测,样品适用范围广。
附图说明
图1纳米金溶胶的紫外吸收光谱(uv-vis)及外观照片。
图2含不同浓度三聚氰胺的纳米金的紫外吸收光谱(uv-vis),a、三聚氰胺浓度0μg/l,b、三聚氰胺浓度6μg/l,c、三聚氰胺浓度9μg/l。
图3检测不同浓度三聚氰胺标准溶液过程中产生的纳米金溶胶的tem图,a、三聚氰胺浓度0μg/l,b、三聚氰胺浓度6μg/l,c、三聚氰胺浓度9μg/l。
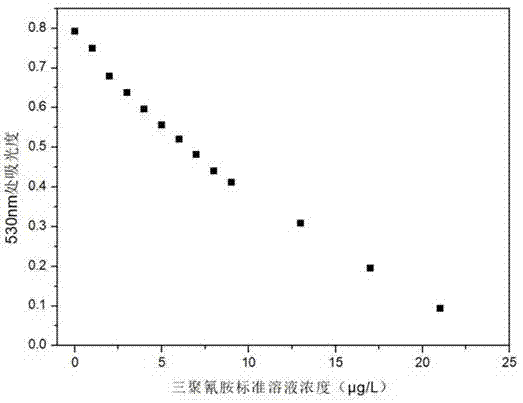
图4三聚氰胺浓度与纳米金吸光度关系的散点图。
图5三聚氰胺浓度与吸光度的标准曲线图。
图6ph及氯化钠浓度对三聚氰胺检测影响结果图。
图7三聚氰胺和其它可能存在干扰的物质对纳米金吸光度影响的柱状图,图中,1、空白,2、抗环血酸,3、精氨酸,4、组氨酸,5、赖氨酸,6、色氨酸,7、葡萄糖,8、尿素,9、氯化钠,10、氯化钙,11、乳酸,12、三聚氰胺。
具体实施方案
下面结合实施例和附图,对本发明技术方案进行更为清楚、完整地描述,显然,所描述的实施例仅仅是本发明的一部分实施例,而不是全部实施例,基于本发明中的实施例,本领域普通技术人员在没有做出创造性劳动的前提下所获得的所有其他实施例,都属于本发明保护的范围。
下述实施例中,所用原料均为市售产品。
实施例1
1、绿色快速制备纳米金水溶胶
1.1、白沙绿茶的有效成分的提取:称取4.0g粉碎过10目筛的白沙绿茶干粉于三口烧瓶中,量取160ml无水乙醇加入烧瓶,将烧瓶置于恒温磁力搅拌器中,温度设置为80℃,恒温煮沸1小时,冷却至室温,抽滤得到滤液。向滤液中加入1.5g活性炭,搅拌三小时脱色,过滤后放置一天,得到淡黄色植物提取液。用移液管准确量取植物提取液100ml于500ml容量瓶,蒸馏水稀释至刻度线,稀释后的提取液与原液均放置于4℃冰箱中保存备用。
1.2、纳米金水溶胶的制备:取稀释后的白沙绿茶提取液5ml于20ml圆底烧瓶中,加入1ml1mm氯金酸水溶液,用盐酸调整ph至6.5,常温反应8分钟,得浅酒红色纳米金水溶胶。
1.3、对制得的纳米金颗粒及其水溶胶进行表征,方法如下:
1.3.1uv-vis表征:在北京普析通用仪器有限责任公司生产的型号为t6新世纪紫外可见分光光度计下进行光谱分析,用二次蒸馏水扫基线后,将一定量纳米金溶胶装入比色皿中开始光谱扫描。参数设为:扫描范围400~1100nm,间隔1nm。
1.3.2tem表征:取纳米金水溶胶样品,以12000r/min离心,弃去上清液,加蒸馏水洗涤纳米金沉淀,再离心,至少洗涤三次,取洗涤后的纳米金溶胶滴在铜网上,在红外灯下烘干后,在日本产jem2100上200v电子束激发下测试。
、采用纳米金水溶胶检测三聚氰胺
2.1、配制三聚氰胺标准溶液
准确称取三聚氰胺固体粉末0.0100g,加入适量蒸馏水超声5分钟充分溶解,移入100ml容量瓶,用蒸馏水定容至刻度线,三聚氰胺浓度为0.1g/l。
取1ml0.1g/l的三聚氰胺溶液,将其稀释成1mg/l,然后将该1mg/l的三聚氰胺溶液分别配制成0μg/l、1μg/l、2μg/l、3μg/l、4μg/l、5μg/l、6μg/l、7μg/l、8μg/l、9μg/l、10μg/l、13μg/l、17μg/l、21μg/l的标准溶液,同时以0μg/l的蒸馏水为对照。
2.2、三聚氰胺与吸光度标准曲线的绘制
分别取5ml稀释后的白沙绿茶提取液,向各稀释后的白沙绿茶提取液中分别加入1ml上述不同浓度的三聚氰胺标准溶液,常温下混匀,再加入1ml1mm的氯金酸水溶液,用盐酸调节ph为6.5,常温反应8分钟溶液颜色不再变化,得不同颜色的纳米金水溶胶。记录各浓度三聚氰胺标准溶液得到的纳米金水溶液的颜色,并采用紫外分光光度计检测所得纳米金水溶胶的吸光度和特征峰变化,绘制三聚氰胺浓度与吸光度的标准曲线,计算得到方程式。
2.3、牛奶中三聚氰胺的检测
2.3.1、对牛奶进行预处理
取1g牛奶样品(伊利、蒙牛)于10ml容量瓶中,加入1g3wt%的乙酸溶液,再加入1g1wt%的乙酸铅水溶液,摇匀,用蒸馏水定容,取适量溶液以4000r/min离心10分钟,取上清液保存于冰箱备用。
2.3.2牛奶中三聚氰胺的检测
取5ml稀释后的白沙绿茶提取液,向稀释后的白沙绿茶提取液中加入1ml预处理的牛奶上清液,常温下混匀,再加入1ml1mm的氯金酸水溶液,用盐酸调节ph为6.5,常温反应8分钟溶液颜色不再变化。采用紫外分光光度计检测所得反应液的吸光度,根据标准方程式得到牛奶中三聚氰胺含量。
、结果与讨论
3.1、白沙绿茶提取液环境下纳米金溶胶的紫外可见分光光谱分析
图1是上面1.2制得的纳米金溶胶的紫外可见分光谱及照片,其肉眼看为酒红色纳米金,紫外可见分光谱上530nm处有强的吸收峰,半峰宽比较窄,说明纳米金颗粒分布相对均匀,粒径大小及分布需要tem进一步验证。
3.2、检测不同浓度的三聚氰胺标准溶液过程中产生的纳米金溶胶的紫外可见光谱分析
根据2.2,在白沙绿茶提取液环境下生成纳米金溶胶之前加入配置好的三聚氰胺标准溶液,随着三聚氰胺量的增加,纳米au在合成过程中受到一定影响,初步表现为颜色变化,肉眼可见纳米au颜色由酒红变为紫红,再到紫色,再到蓝色,最后是黄绿色。随着三聚氰胺量的增加,530nm处的吸收峰强度也明显降低。图2为三聚氰胺浓度为0μg/l、6μg/l、9μg/l的纳米金溶胶颜色图和紫外分光光谱图,从图中可以看出,随着三聚氰胺量的增加,纳米金溶胶的颜色分别为酒红色、深红色、紫色,530nm处的吸收峰强度明显降低。这说明纳米颗粒的尺寸增大了,分散在在溶胶里的大颗粒纳米金的浓度降低,因此吸收强度降低,而且该纳米金溶胶体系不能稳定,放置一段时间后会有沉淀析出。
3.3检测不同浓度的三聚氰胺标准溶液过程中产生的纳米金溶胶的tem检测
图3是2.2中三聚氰胺浓度为0μg/l、6μg/l、9μg/l时得到的纳米金溶胶的tem图,从图中可以看出,随着三聚氰胺量的增加,纳米金颗粒的粒径发生了明显的变化,颗粒粒径逐渐增大,溶胶不稳定。
3.4根据三聚氰胺标准溶液浓度与纳米金溶胶最大吸光度的关系,作出三聚氰胺标准溶液浓度与纳米金溶胶吸光度的关系图,见图4。由图4可以看出,随着三聚氰胺浓度的增加,纳米金溶胶吸光度有减小的趋势。选取线性相关性高的点做标准曲线。
3.5三聚氰胺溶液标准曲线图
根据所得的三聚氰胺标准溶液与吸光度的散点图(图4),绘制标准曲线,如图5所示,根据标准曲线得标准曲线y=0.75499-0.03895x,相关系数r=-0.99906,sd=0.004。根据标准差法,lod(检出限)=3s0/k,s0是空白样(n=10)的标准偏差,k是曲线斜率,k=-0.03895,s0=-0.19865,经计算,检出限为15.3nm,远低于我国液态奶三聚氰胺最大含量不超过20000nm的规定。
3.6牛奶中三聚氰胺检测结果
按照2.3.2的方法对蒙牛和伊利纯牛奶中三聚氰胺的含量进行检测,同时取1ml预处理好的牛奶样品,检测三聚氰胺含量,蒙牛牛奶530nm处吸光度为0.655,伊利牛奶为0.646,根据上述标准曲线,计算得到蒙牛牛奶中三聚氰胺含量为0.18mg/kg,伊利牛奶中三聚氰胺含量为0.20mg/kg。我国规定液态奶三聚氰胺含量在2.5mg/kg以内,这两种牛奶中三聚氰胺含量均未超标。
同时,取100μg/l三聚氰胺标准溶液50μl、100μl、200μl分别加入这两种牛奶中做加标回收实验,每个条件三个平行实验,结果如下表1所示。
从上表结果可以看出,本发明检测方法回收率高,准确性好。
实施例2ph和nacl浓度对检测三聚氰胺的影响
1、绿色快速制备植物提取液
白沙绿茶的有效成分的提取:称取4.0g粉碎过10目筛的白沙绿茶干粉于三口烧瓶中,量取160ml无水乙醇加入烧瓶,将烧瓶置于恒温磁力搅拌器中,温度设置为80℃,恒温煮沸1小时,冷却至室温,抽滤得到滤液。向滤液中加入1.5g活性炭搅拌三小时脱色,过滤后放置一天,得到淡黄色植物提取液。用移液管准确量取植物提取液100ml于500ml容量瓶,蒸馏水稀释至刻度线,稀释后的提取液与原液均放置于4℃冰箱中保存备用。
2、ph和nacl浓度对检测三聚氰胺的影响的研究
2.1配制浓度为6μg/l的三聚氰胺标准溶液,方法同实施例1。
2.2分别取5ml稀释后的白沙绿茶提取液,向各稀释后的白沙绿茶提取液中分别加入1ml上述浓度6μg/l的三聚氰胺标准溶液,常温下混匀,再加入1ml1mm的氯金酸水溶液,分别调节ph为5.5、5.7、6.0、6.3、6.5、6.8、7.0,常温反应8分钟至溶液颜色不再变化,采用紫外分光光度计检测所得纳米金水溶胶的吸光度。
2.3分别取5ml稀释后的白沙绿茶提取液,向各稀释后的白沙绿茶提取液中分别加入1ml上述浓度6μg/l的三聚氰胺标准溶液,常温下混匀,再加入1ml1mm的氯金酸水溶液,调节ph为6.5,再分别加入氯化钠至浓度为0mmol/l、10mmol/l、20mmol/l、30mmol/l、40mmol/l、60mmol/l、80mmol/l,常温反应8分钟至溶液颜色不再变化,采用紫外分光光度计检测所得纳米金水溶胶的吸光度。
2.4结果
不同ph和nacl浓度下的溶液吸光度如图6所示。植物提取液本身的ph是在5.5左右,从图6可以看出,当ph在5.5到6.5之间时,加入三聚氰胺后,纳米au吸光度几乎不变,说明ph不会影响纳米金的吸光度,但当ph大于6.5时,吸光度开始下降,说明ph大小开始影响纳米au对三聚氰胺的检测。所以该体系适合在ph为5.5至6.5之间检测三聚氰胺。另外,nacl浓度也不宜过高,在氯化钠浓度为0~40mmol/l时,纳米金吸光度几乎不变,对体系检测三聚氰胺影响不大,但是盐浓度超过40mmol/l时,纳米金在530nm处吸光度增加,并且最大吸收峰位置红移,粒径变大,由此可知,氯化钠浓度较高也会影响三聚氰胺的检测。所以,本发明方法ph和氯化钠浓度需要维持在一定范围才能用于检测三聚氰胺,本发明适合的ph和氯化钠浓度条件都比较温和,正适合于正常情况下对牛奶中三聚氰胺的检测。
实施例3抗干扰性实验
为了证明本发明方法检测的准确性、高选择性,同时选取其它一些可能对检测结果存在干扰的盐或者含羟基和氨基的试剂(抗坏血酸,精氨酸,组氨酸,赖氨酸,色氨酸,葡萄糖,尿素,氯化钠,氯化钙及乳糖)采用本发明方法进行检测,步骤是:
分别取5ml稀释后的白沙绿茶提取液,向各稀释后的白沙绿茶提取液中分别加入三聚氰胺、抗坏血酸、精氨酸、组氨酸、赖氨酸、色氨酸、葡萄糖、尿素、氯化钠、氯化钙、乳糖,各试剂在体系中的浓度均为0.1g/l,常温下混匀,再加入1ml1mm的氯金酸水溶液,调节ph为6.5,常温反应至溶液颜色不再变化,同时以不加任何试剂的空白纳米金溶胶为对照。结果显示:除了加入三聚氰胺的溶液颜色变为紫色外,其与溶液依然为浅酒红色;采用紫外分光光度计检测各溶液的吸光度,除了加入三聚氰胺的溶液在530nm处吸光度明显减小外,其与溶液吸光度与纯纳米金溶胶对照相比无明显变化,结果如图7所示。由此可以看出,本发明方法可以实现三聚氰胺的可视化检测,并且对三聚氰胺的选择性好,抗干扰能力强。
实施例4与现有同类方法的比较
将本发明检测方法与现有技术中报道的三种类似方法进行比较,方法1为文献1公开的方法,方法2为文献2公开的方法,方法3为文献3公开的方法。其中,文献1:赵静,李永生,高秀峰.流动注射纳米au分光光度法快速测定乳制品中的三聚氰胺.分析试验室2016,35(8):961-965.文献2:caoqian,zhaoh,heyj,etal.hydrogen-bonding-inducedcolorimetricdetectionmelaminebynonaggregation-basedau-npsasaprobe.biosensorsandbioelectronics,2010,25:2680-2685.文献3:nangao,pengchenghuang,fangyingwu.colorimetricdetectionofmelamineinmilkbasedontritonx-100modifiedgoldnanoparticlesanditspaper-basedapplication.spectrochimicaactaparta:molecularandbiomolecularspectroscopy192(2018)174-180.
按照实施例1的方法,配制不同浓度的三聚氰胺标准溶液,按照现有技术和本发明的方法对三聚氰胺进行检测,计算灵敏度和回收率,各方法检测结果和特点如下表2所示。
实施例5
芦荟提取液与稀释液的制备:同实施例1,只是将白沙绿茶替换为芦荟。提取过程中,所得芦荟提取液粘稠度大,脱色过滤难度大,耗时较长。
准确称取三聚氰胺固体粉末0.0100g,加入适量蒸馏水超声5分钟充分溶解,移入100ml容量瓶,用蒸馏水定容至刻度线,三聚氰胺浓度为0.1g/l。
取1ml0.1g/l的三聚氰胺溶液,将其稀释成1mg/l,然后将该1mg/l的三聚氰胺溶液分别配制成0μg/l、1μg/l、2μg/l、3μg/l、4μg/l、5μg/l、6μg/l、7μg/l、8μg/l、9μg/l、10μg/l、13μg/l、17μg/l、,21μg/l的标准溶液,同时以0μg/l的蒸馏水为对照。
分别取5ml稀释后的芦荟提取液,向各稀释后的芦荟提取液中分别加入1ml上述不同浓度的三聚氰胺标准溶液,常温下混匀,再加入1ml1mm的氯金酸水溶液,用盐酸调节ph为10.0,常温反应8分钟溶液颜色不再变化,得不同颜色的纳米金水溶胶。记录各浓度三聚氰胺标准溶液得到的纳米金水溶液的颜色,并采用紫外分光光度计检测所得纳米金水溶胶的吸光度和特征峰变化,绘制三聚氰胺浓度与吸光度的标准曲线,计算方程式,计算得检测限为30nm。
实施例6
红枣提取液与稀释液的制备:同实施例1,只是将白沙绿茶替换为红枣。
准确称取三聚氰胺固体粉末0.0100g,加入适量蒸馏水超声5分钟充分溶解,移入100ml容量瓶,用蒸馏水定容至刻度线,三聚氰胺浓度为0.1g/l。
取1ml0.1g/l的三聚氰胺溶液,将其稀释成1mg/l,然后将该1mg/l的三聚氰胺溶液分别配制成0μg/l、1μg/l、2μg/l、3μg/l、4μg/l、5μg/l、6μg/l、7μg/l、8μg/l、9μg/l、10μg/l、13μg/l、17μg/l、21μg/l的标准溶液,同时以0μg/l的蒸馏水为对照。
分别取5ml稀释后的红枣提取液,向各稀释后的红枣提取液中分别加入1ml上述不同浓度的三聚氰胺标准溶液,常温下混匀,再加入1ml1mm的氯金酸水溶液,用盐酸调节ph为10.0,40℃反应30分钟溶液颜色不再变化,得不同颜色的纳米金水溶胶。记录各浓度三聚氰胺标准溶液得到的纳米金水溶液的颜色,并采用紫外分光光度计检测所得纳米金水溶胶的吸光度和特征峰变化,绘制三聚氰胺浓度与吸光度的标准曲线,计算方程式,计算得检测限为50nm。
对比例1
金银花提取液与稀释液的制备:同实施例1,只是将白沙绿茶替换为金银花。
按照实施例1的方法,先采用稀释后的金银花提取液与氯金酸反应制得酒红色纳米金溶胶,其颗粒为18nm,进一步的,采用该稀释后的金银花提取液按照实施例1的方法检测不同浓度的三聚氰胺标准溶液,所得溶液均不显色,无法实现三聚氰胺的检测。
对比例2
玫瑰花提取液与稀释液的制备:同实施例1,只是将白沙绿茶替换为玫瑰花。
按照实施例1的方法,先采用稀释后的玫瑰花提取液与氯金酸反应,无法制得酒红色纳米金溶胶,产物为紫色悬浊液,不能用于三聚氰胺的检测。
对比例3
取实施例1制得的稀释后的白沙绿茶提取液5ml于20ml圆底烧瓶中,加入1ml1mm氯金酸水溶液,用盐酸调整ph至6.5,常温反应8分钟,得浅酒红色纳米金水溶胶。
向上述所得纳米金水溶胶中加入1ml三聚氰胺标准溶液,用盐酸调节ph为6.5,常温反应;或者是将上述所得纳米金水溶胶离心,所得纳米金溶胶颗粒重新分散于6ml蒸馏水中,再加入1ml三聚氰胺标准溶液,用盐酸调节ph为6.5,常温反应。
无论是在酒红色纳米金水溶胶中加入三聚氰胺进行检测,还是将纳米au从提取液体系中离心出来再分散在蒸馏水中,再加入三聚氰胺进行检测,放置几个月都没有任何显色反应,在紫外可见分光光度计下检测,也未发现有任何特征峰位置变化,吸光度虽稍有变化,但这种变化无法支持三聚氰胺含量检测。
- 还没有人留言评论。精彩留言会获得点赞!