AO-CoOOH纳米荧光探针及其制备方法和应用与流程
本发明涉及检测技术,具体涉及ao-coooh纳米荧光探针及其制备方法和应用。
背景技术:
焦磷酸根离子(ppi)不仅是工业废水中很难去除的磷源之一,而且也是一种非常重要的生物目标阴离子。研究表明,ppi可以参与许多生命过程中的能量传递和新陈代谢,如在dna聚合酶的催化下参与dna的复制,由此可通过对ppi的检测实现dna序列的实时测定。ppi也可以作为早期诊断和治疗癌症、关节炎、软骨钙化和其他疾病的潜在生物标记物。此外,ppi也被用于食品添加剂。因此,建立一种快速、简单、选择性好且能应用于活细胞和活体中ppi检测的方法具有重要的意义。
目前,检测ppi的方法包括电化学法、比色法、荧光光度法等。然而,电化学检测法虽然精度高,选择性好,但重复性差。比色法存在灵敏度低、干扰严重等问题。荧光分析法已广泛应用于化学分析,但大部分方法存在需要荧光探针合成制备复杂、操作步骤繁琐等不足。最近,基于纳米材料的ppi传感器研究引起了越来越多研究者的关注,如金纳米颗粒、纳米簇、纳米棒、量子点和碳纳米材料等。然而,这些纳米材料存在合成制备工艺繁琐、耗时、原料昂贵等限制,且合成的纳米材料很少能实现在活体中的检测应用。因此,发展一种简单、灵敏的检测ppi及其活体成像的方法具有重要意义。
技术实现要素:
为了解决现有技术的不足,本发明提供了ao-coooh纳米荧光探针及其制备方法和应用。
本发明的技术方案是:ao-coooh纳米荧光探针的制备方法,其特征在于,将coooh纳米片与ao溶液混合,混合物孵育15分钟,ao-coooh纳米探针即制备获得。
本发明的进一步改进包括:
所述coooh纳米片与ao溶液的浓度分别为12μg/ml和0.01mm。
本发明进一步提供了按照上述方法制得的ao-coooh纳米荧光探针。
本发明还提供了ao-coooh纳米荧光探针在血清、活细胞和活体中ppi的检测中的应用。
在本申请中,本发明构建了一种基于羟基氧化钴(coooh)纳米片联合碱性橙(ao)染料的“混合即检测”型荧光纳米探针,用于检测ppi并实现在细胞和活体中成像。与其它纳米材料相比,本申请中的coooh纳米片由于其成本低、合成操作简便、安全等优点,具有一定的优势。特别是纳米探针可以通过将ao和coooh纳米片简单混合获得。ao的荧光可以被coooh纳米片猝灭,当添加ppi时,荧光强度会进一步降低。该方法具有操作简单、灵敏度高、选择性高等特性,可用于细胞和活体中ppi的检测和成像。本申请的方法可能为ppi相关的生理和病理研究提供一个新的分析平台。
附图说明
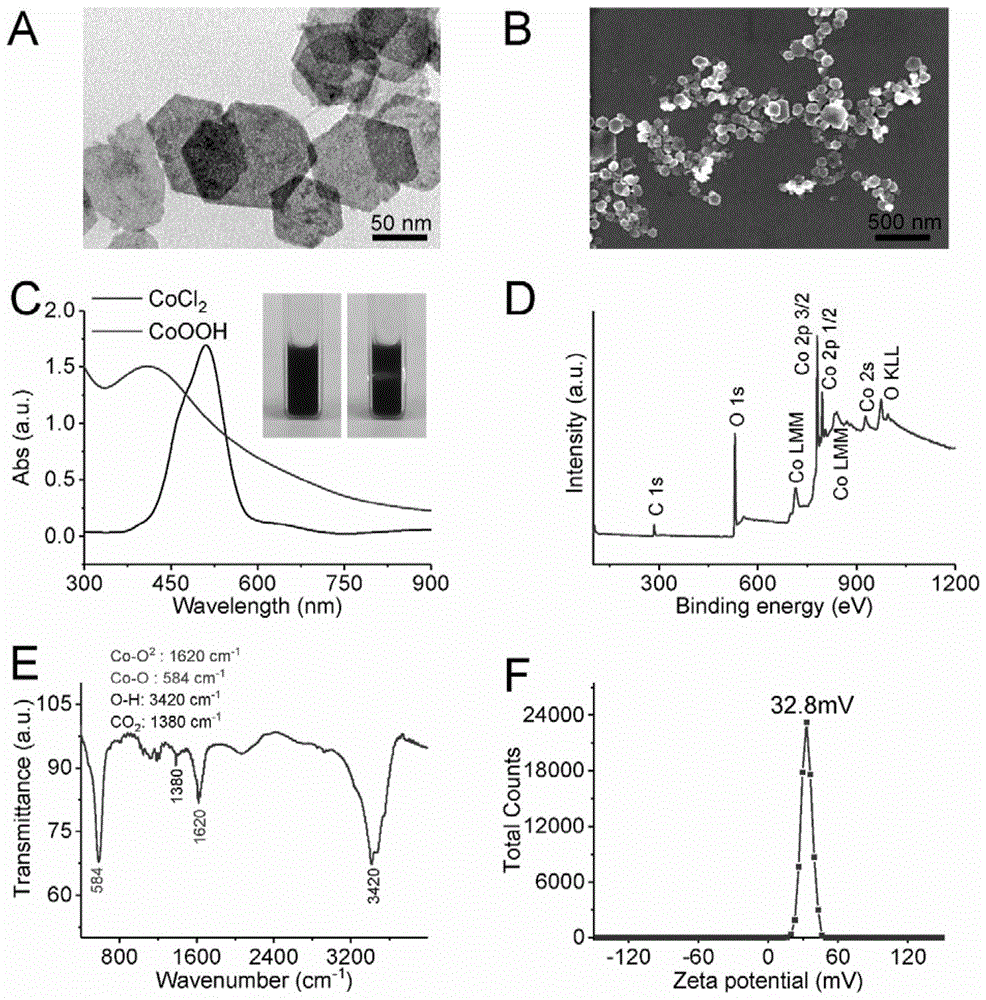
图1.coooh纳米片的tem(a)和sem(b)结果。其中:(c)cocl2(黑色)和coooh纳米片(红色)的uv-vis吸收光谱。插图:coooh纳米片溶液颜色及其丁达尔效应照片。(d)coooh纳米片的xps光谱。(e)coooh纳米片的傅里叶变换红外光谱结果。(f)coooh纳米片的zeta电位结果。
图2.(a)ao(a)、ao-coooh纳米探针(b)、b+ppi(c)的荧光发射光谱。浓度:ao(0.01mm),coooh(12μg/ml),ppi(47.5μm)。(b)不同物质混合后的紫外-可见光吸收光谱。
图3.(a)不同配比ao-coooh纳米探针对ppi的荧光响应效果。(碱性橙0.01mm,coooh纳米片6,12,24,36,48μg/ml,ppi23.8μm).(b)纳米复合探针在不同ph下对ppi的响应效果。δf=f-f0,f和f0分别代表ppi存在与不存在时的荧光强度。(碱性橙0.01mm,coooh纳米片12μg/ml,ppi23.8μm。ph4-6为醋酸-醋酸钠缓冲液;ph7-9为tris-醋酸缓冲液,浓度均为10mm)。(c)coooh纳米片加入ao溶液后的荧光强度随时间的变化曲线。(d)ao-coooh荧光纳米探针对ppi的反应动力学曲线。(碱性橙0.01mm,coooh纳米片12μg/ml,ppi23.8μm)。
图4.(a)将不同浓度的ppi(0,50,200,400,800,1600,3200,6400,12800,25600nm)加入ao-coooh纳米探针(碱性橙0.01mm,coooh纳米片12μg/ml)的荧光发射光谱图。(b)不同浓度ppi与其引起荧光变化的关系图。插图;ppi浓度(50-6400nm)与δf(δf=f-f0)线性关系图。f和f0分别代表ppi存在与不存在时的荧光强度。
图5.ao-coooh纳米探针对ppi检测的选择性分析,以上物质浓度均为1.6μm。δf=f-f0,f和f0分别代表ppi存在与不存在时的荧光强度。(碱性橙0.01mm,coooh纳米片12μg/ml)。
图6.ct26细胞加入不同物质后的激光共聚焦显微镜照片。(a)ao-coooh纳米探针,(b)-(d)为在a基础上再加入(0.025,0.1,2mm)ppi。(碱性橙0.01mm;coooh纳米片12μg/ml);显微镜成像放大倍数为630倍。
图7.鲫鱼体内被注射ao-coooh纳米探针及不同浓度ppi后的荧光成像结果。(a)将200μlao-coooh纳米探针(碱性橙:0.67mm;coooh纳米片:80μg/ml)注射到鱼体内50分钟后观察结果;(b)(a)+40μl焦磷酸根(0.1m)被注射到鱼体内40分钟后观察结果;(c)(a)+240μl焦磷酸根(0.1m)被注射到鱼体内40分钟后观察结果。
具体实施方式
下面结合实施例对本发明做详细说明。
实施例
试剂
六水氯化钴是从国药试剂公司(上海,中国)购买的。三磷酸腺苷(atp)是从麦克林试剂公司(中国)购买的。次氯酸钠、氢氧化钠、葡萄糖(glu)、果糖(fru)、腺嘌呤(a)、胸腺嘧啶(t)、二磷酸腺苷(adp)、一磷酸腺苷(amp)、甘氨酸(gly)、丙氨酸(ala)是从阿拉丁试剂公司(上海,中国)购买的。磷酸钠、十二水磷酸钠、二水磷酸氢二钠、二水磷酸二氢钠、碳酸氢钠、碳酸钠、硫酸钠、九水硫化钠、硝酸钠、氯化钠和醋酸钠、氯化镁、二水氯化钙、二水氯化铜、氯化钾、氯化锌是从阿拉丁试剂公司(上海,中国)购买的。麻醉剂(ms-222)是从上海吉荧生物科技公司购买的。所有试剂都是分析纯级别的,由去离子水(millipore,bedford,ma,usa,18.2mω·cm)配制。
仪器
美国分子公司spectramaxm5多功能酶标仪、哈希多功能参数水质仪dr6000(美国)、透射电镜jem-1200ex(日本)、日立su8010冷场发射扫描电子显微镜(日本)、x-ray光电子能谱仪(美国)、傅里叶红外光谱仪(美国)、zeta电位仪(英国)、lsm710激光共聚焦显微镜(德国)、超纯水仪f3hn00200d(美国)、细胞培养箱heracell240ithermo公司(美国)、电子天平mettlertoledo仪器公司(美国)、梅特勒ph计mettlertoledo公司(瑞士)、小动物活体成像(ivisspectrum,caliper-pe)。
coooh纳米片及ao-coooh纳米荧光探针的制备
本发明合成的coooh纳米片是参照现有文献中的方法制得。首先,125μl氢氧化钠(1m)添加到500μl的氯化钴溶液(10mm)中,混合后超声1分钟。然后,将25μl次氯酸钠溶液(0.9m)加入混合物中,超声10分钟。随后,将混合物离心,用去离子水清洗三次。最后将产物重新分散在1ml水中,其最终浓度为0.25mg/ml。将coooh纳米片(12μg/ml)与ao(0.01mm)溶液混合,混合物孵育15分钟,ao-coooh纳米探针即制备获得。
缓冲液中ppi的检测
将不同浓度的ppi(50,200,400,800,1600,3200,6400,12800,25600nm)加入到制得ao-coooh纳米探针中,孵育60分钟后,在激发波长为490nm,在510到750nm范围内收集荧光发射光谱。
荧光显微镜成像
为了探究纳米探针在细胞水平下对ppi的检测效果,首先将ct26接种在铺有玻片(直径14mm)的24孔板里培养18小时,然后用500μl的pbs将细胞洗涤两次,将一定浓度的ao-coooh纳米探针加入细胞培养板后放入37℃含5%co2的培养箱中培养2小时,再用pbs洗涤两次加入ppi孵育1小时,在蔡司axioabservera1荧光显微镜和蔡司lsm710激光共聚焦显微镜下观察结果。
小动物活体成像
为了研究纳米探针在活体中对ppi的检测效果,本发明将200μl纳米探针腹腔注射到鲫鱼体内,50分钟后,在水体中加入麻醉剂三卡因将鱼麻醉,在小动物活体成像仪(激发500nm,荧光发射540nm)下观察结果。观察后,在鱼体的同一部位注射一定浓度的ppi,40分钟后,在小动物活体成像仪下观察结果。
coooh纳米片表征
coooh纳米片用透射电镜(tem),扫描电镜(sem),紫外可见吸收光谱(uv-vis),x射线光电子能谱(xps),傅里叶变换红外光谱和zeta电位等技术进行表征。如图1a、b所示,coooh纳米片的tem和sem图像清晰地显示了coooh纳米片的形貌是六边形的,与之前的报道一致。插图中显示羟基氧化钴纳米片溶液颜色是棕黑色,有明显的丁达尔效应,其在300nm到800nm范围内具有宽的吸收带(图1c),这使其成为针对多种荧光剂的潜在猝灭剂,包括本申请中使用的ao荧光染料也具有良好的猝灭效果。利用x射线光电子能谱(xps)的成分分析表明该材料确实含有co和o元素(图1d)。图1e显示coooh纳米片的傅里叶变换红外光谱结果,584cm-1、1620cm-1和3420cm-1处的峰分别代表co-o、co-o2、o-h官能团。coooh纳米片的ζ电位的测量约32.8mv(图1f),其表面带正电荷。上述数据充分证明了coooh纳米片是成功制备的。
ao-coooh纳米探针检测ppi的原理
如图2a所示,ao在530nm处显示强烈的荧光发射峰(曲线a),在coooh纳米片的存在下,coooh纳米片将ao的荧光有效地猝灭(曲线b)。当加入ppi后,荧光得到进一步的猝灭。通过图2b的紫外-可见光吸收光谱可见,只有当ao、coooh、ppi共同存在时,三者混合物的吸收光谱才发生明显蓝移,这说明三者形成了一定形式的耦合作用,推测正是因为这种耦合作用引起了ppi存在时ao-coooh复合物的荧光进一步明显猝灭。
实验条件优化
为了达到更好的传感检测性能,本发明优化了实验条件。本发明研究了滴加不同浓度的coooh纳米片到ao溶液中,再加入等量ppi引起的体系荧光变化(图3a)。结果显示,当coooh纳米片浓度为12μg/ml时,加入多少浓度的ppi引起的荧光猝灭程度最大。因此,本发明选择比例为0.01mm:12μg/mlao-coooh复合物为最优探针比例。本发明接着探究了ph对检测体系荧光变化的影响。如图3b所示,在ph为3.0-9.0的范围内,检测体系的荧光强度都得到猝灭,当ph4.0时,荧光猝灭效果最显著。同时,本发明也对孵育时间进行了考察,首先是对coooh纳米片与ao溶液的孵育时间进行优化。如图3c所示,coooh加入到ao溶液后,其荧光迅速猝灭,5分钟后基本平衡,因此,本发明选择5分钟的反应时间用于接下来的实验。接着,本发明将ppi加入荧光纳米探针,用于探究荧光探针对ppi的反应时间。如图3d所示,加入ppi后,荧光探针的荧光逐渐缓慢猝灭,且在60分钟时基本达到稳定状态。
ao-coooh纳米探针对ppi的检测
在最优化的条件下,本发明进行了ppi的检测实验。如图4a所示,当ppi浓度在0-25600nm范围内,随着ppi浓度的增加,体系的荧光强度逐渐减小,并且在高浓度ppi时荧光猝灭逐渐减缓。图4b是不同浓度ppi与其引起荧光变化的关系图,插图为其相应的标准曲线,结果显示其线性相关系数为0.999,ppi的浓度与f具有良好的线性关系(y=0.16238x+208.47075),其最低检测限为50nm。与之前报道的方法相比较,ao-coooh纳米探针对ppi的检测效果较好。
表1.对比已报道不同检测ppi方法的线性范围与灵敏度
选择性考察
选择性是分析检测方法的关键指标之一。因此,本发明选用一些常见阴离子、生物分子和金属离子进行干扰性分析实验。如图5所示,只有目标物ppi对体系的响应是最显著的。因此,该纳米探针对ppi的选择性较好。
ao-coooh纳米探针检测血清样品中的ppi
为了考察纳米探针在实际样品中的检测效果,本发明选用健康人血清来进行加标回收实验。在健康人血清样品中未检测到ppi。因此,本发明将终浓度为3.2μm和6.4μmppi加入血清样品中,利用ao-coooh纳米探针来进行检测,检测结果如表2所示,其回收率达到102.34%和114.06%,相对标准偏差为0.49%到1.20%,由此可见,本发明设计的纳米传感体系在实际样品中的应用是成功的。
表2.ao-coooh纳米探针检测血清样品中的ppi(n=3)
ao-coooh纳米探针用于细胞内ppi的检测
本发明将ao-coooh纳米探针应用于细胞内ppi的检测,选用小鼠结肠癌细胞(ct26)进行实验。ao-coooh纳米探针与ct26细胞孵育2小时,用pbs洗涤两次,再加入终浓度分别为0.025,0.1,2mmppi孵育1小时,在激光共聚焦显微镜下进行观察。结果如图6所示,单独加入纳米探针的细胞中具有较强烈的荧光,ppi的加入使荧光得到进一步猝灭,且随着ppi浓度的增加,荧光强度逐渐被减弱。上述结果表明,本发明设计的荧光纳米探针可实现对细胞内ppi的检测。
ao-coooh纳米探针用于鲫鱼体内ppi的检测
为了研究纳米探针在活体中对焦磷酸根的检测及荧光成像效果效果,本发明将ao-coooh纳米探针及ppi注射到鲫鱼体内,并在小动物荧光成像仪下观察结果。结果如图7所示,单独被注射纳米探针的鱼体中具有较强烈的荧光,ppi的加入使荧光得到进一步猝灭,且随着ppi浓度的增加,荧光强度减小。以上结果表明,本申请的荧光纳米探针对活体中ppi的检测及荧光成像是可行的。
结论
总而言之,本发明发展的基于coooh纳米片联合ao染料的“混合即检测”型荧光纳米探针,可应用于检测ppi并实现在细胞和活体中成像。同时,该纳米探针可成功应用于实际样品的检测。该方法操作简单方便更容易被生理学家所采用。本申请不仅为细胞的检测提供了一种新方法,同时也为细胞在生理和病理的分析中提供了一个分析平台。
以上显示和描述了本发明的基本原理和主要特征和本发明的优点。本行业的技术人员应该了解,本发明不受上述实施例的限制,上述实施例和说明书中描述的只是说明本发明的原理,在不脱离本发明精神和范围的前提下,本发明还会有各种变化和改进,这些变化和改进都落入要求保护的本发明范围内。本发明要求保护范围由所附的权利要求书及其等效物界定。
- 还没有人留言评论。精彩留言会获得点赞!
- 一种纳米粉体工业生产系统的制作方法
- 一种高红外辐射粉体及其制备方法
- 一种铈锌共掺NiFe<sub>2</sub>O<sub>4</sub>纳米粉体及其制备方法
- 一种纳米Al<sub>2</sub>O<sub>3</sub>/Er<sub>3</sub>Al<sub>5</sub>O<sub>12</sub>/ZrO<sub>2</sub>复合粉体材料的制备方法
- 一种β?氢氧化镍纳米片的制备方法
- 一种硫化亚铜纳米玫瑰花的制备方法
- 一种球形氧化钇粉体的制备方法
- 一种亚微米级碳化硼粉体及其制备方法和用图
- 一种B<sub>4</sub>C纳米片的制备方法及B<sub>4</sub>C纳米片的制作方法
- 氮化铝粉体的制备方法