黏着剂组成物、电极组成物、电极及锂电池的制作方法
本发明涉及一种黏着剂组成物、电极组成物、电极及锂电池,尤其涉及一种侧链具有多种官能基团的黏着剂组成物、包括所述黏着剂组成物的电极组成物、由所述电极组成物所制得的电极以及使用所述电极的锂电池。
背景技术:
近年来可重复充电放电兼具重量轻、高电压值与高能量密度等特点的二次锂电池之市场需求量与日剧增,并且二次锂电池尤其在轻型电动车、电动车、大型储电产业上的应用及拓展潜力极高。因此,现今对二次锂电池诸如轻质耐用、高电压、高能量密度、高安全性与高稳定性等性能的要求也越来越高。然而,在已知二次锂电池中,由于负极中的黏着剂通常无法同时与活性物质、集电体及助导剂皆具有良好的黏接性,使得在充放电过程中,负极的结构容易因锂离子的迁入与迁出而受到破坏,进而导致二次锂电池的稳定性不佳且电容量下降。因此,提供一种新颖的黏着剂,使得二次锂电池能够具有良好的电容量及稳定性是目前此领域技术人员所欲达成的目标之一。
技术实现要素:
有鉴于此,本发明提供一种黏着剂组成物、电极组成物、电极及锂电池,其中黏着剂组成物用于锂电池的阳极且使锂电池具有良好电容量及稳定性。
本发明的黏着剂组成物包括溶剂以及聚酰胺酸。聚酰胺酸由式I表示:
其中A为芘基、蒽基、苯并[a]芘基、苯并[e]芘基、萘并[2,3-a]芘基、二苯并[a,e]芘基、二苯并[a,h]芘基或萘基,n为0至10,X为大于0且小于1。
本发明的电极组成物包括活性物质、助导剂以及前述的黏着剂组成物。
本发明的电极由前述的电极组成物所制得。
本发明的锂电池包括阳极、阴极、隔离膜、电解液以及封装结构。阳极为前述的电极。阴极与阳极分离配置。隔离膜设置于阳极与阴极之间,且隔离膜、阳极及阴极定义出容置区域。电解液设置于容置区域中。封装结构包覆阳极、阴极及电解液。
基于上述,本发明的黏着剂组成物为一新颖的黏着剂组成物,包括由式I表示的聚酰胺酸及溶剂。另外,本发明的电极组成物通过包括由式I表示的聚酰胺酸,使得所述聚酰胺酸、活性物质与助导剂彼此之间能够稳固相连接。另外,本发明的电极通过使用所述电极组成物而制得,使得电极中的活性物质与助导剂能够稳固黏附在集电体上。另外,通过包括所述电极,本发明的锂电池同时具有良好的组件稳定性、循环寿命以及电容量。
为让本发明的上述特征和优点能更明显易懂,下文特举实施方式,并配合附图作详细说明如下。
附图说明
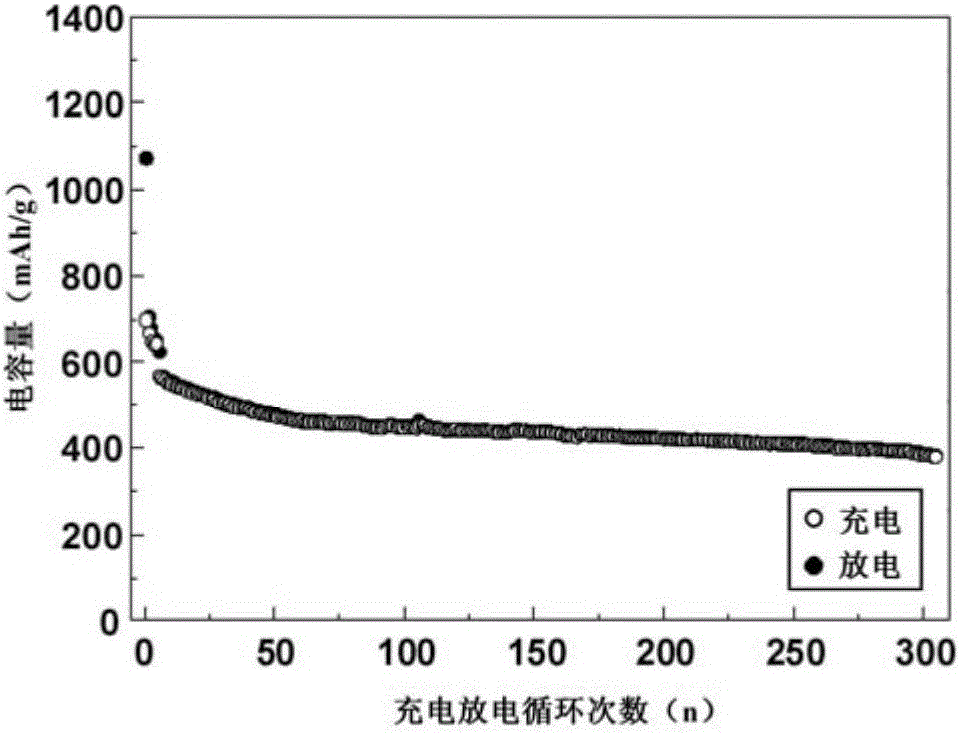
图1、图2、图3及图4分别是实施例1、比较例1、比较例2及比较例3的锂电池的充电放电循环次数及电容量的关系图;
图5是实施例1、比较例1-3的锂电池的第6圈至第305圈的放电电容量对第6圈的放电电容量进行规一化后的充电放电循环次数及电容量残余率的关系图;
图6A及图6B分别是未进行充电放电循环测试前及进行第105圈充电放电循环测试后的实施例1的锂电池的工作电极的扫描电子显微镜影像;
图7A及图7B分别是未进行充电放电循环测试前及进行第105圈充电放电循环测试后的比较例1的锂电池的工作电极的扫描电子显微镜影像;
图8A及图8B分别是未进行充电放电循环测试前及进行第105圈充电放电循环测试后的比较例2的锂电池的工作电极的扫描电子显微镜影像;
图9A及图9B分别是未进行充电放电循环测试前及进行第105圈充电放电循环测试后的比较例3的锂电池的工作电极的扫描电子显微镜影像;
图10A及图10B分别是是未进行充电放电循环测试前及进行第105圈充电放电循环测试后的实施例1的锂电池的工作电极的截面扫描电子显微镜影像;
图11A及图11B分别是未进行充电放电循环测试前及进行第105圈充电放电循环测试后的比较例1的锂电池的工作电极的截面扫描电子显微镜影像;
图12A及图12B分别是未进行充电放电循环测试及进行第105圈充电放电循环测试后的比较例2的锂电池的工作电极的截面扫描电子显微镜影像;
图13A及图13B分别是未进行充电放电循环测试及进行第105圈充电放电循环测试后的比较例3的锂电池的工作电极的截面扫描电子显微镜影像;
图14是实施例1、比较例1-3的锂电池的电化学阻抗频谱分析(electrochemical impedance spectroscopy,EIS)图。
具体实施方式
本发明的一实施方式提供一种黏着剂组成物,其包括溶剂以及由式I表示的聚酰胺酸:
其中A为芘基、蒽基、苯并[a]芘基、苯并[e]芘基、萘并[2,3-a]芘基、二苯并[a,e]芘基、二苯并[a,h]芘基或萘基,n为0至10,X为大于0且小于1。
在本实施方式中,聚酰胺酸均匀溶解于溶剂中。详细而言,以黏着剂组成物的总重计,溶剂的含量为50wt%至99wt%,以及聚酰胺酸的含量为1wt%至50wt%。
另外,由式I表示的聚酰胺酸能够通过一种四羧酸二酐化合物与两种二胺化合物进行反应而制备。在本文中,将制备聚酰胺酸所使用的四羧酸二酐化合物称为二酐单体,而二胺化合物称为二胺单体。具体而言,制备式I表示的聚酰胺酸所使用的二酐单体为均苯四甲酸二酐(1,2,4,5-Benzenetetracarboxylic anhydride,PMDA),而二胺单体包括经羧酸基取代的4,4’-二氨基联苯(4,4’-diaminobiphenyl)以及经带有芘基、蒽基、苯并[a]芘基、苯并[e]芘基、萘并[2,3-a]芘基、二苯并[a,e]芘基、二苯并[a,h]芘基或萘基的酯基取代的4,4’-二氨基联苯。也就是说,在本实施方式中,由式I表示的聚酰胺酸为一种侧链上具有多种官能基团(即羧酸基及芘基、蒽基、苯并[a]芘基、苯并[e]芘基、萘并[2,3-a]芘基、二苯并[a,e]芘基、二苯并[a,h]芘基或萘基)的聚酰胺酸。
在一实施方式中,所述聚酰胺酸例如是由以下式II表示:
详细而言,对应于式I,在式II表示的聚酰胺酸中,A即为芘基、n为1且X为0.5。另外,式II表示的聚酰胺酸的制备方法将于后文中进行详细描述。
在本实施方式中,作为溶剂,可使用所属技术领域中普通技术人员所周知的有机溶剂,例如可列举:N,N-二甲基甲酰胺(DMF)、N,N-二甲基乙酰胺(DMAc)、N-甲基-2-吡咯酮(NMP)、二甲基亚砜(DMSO)。该等溶剂可单独使用或将2种以上混合使用。
本发明的另一实施方式提供一种电极组成物,其包括活性物质、助导剂以及任一种前述实施方式中的黏着剂组成物。详细而言,在本实施方式中,以电极组成物的总重计,活性物质的含量为70wt%至90wt%,黏着剂组成物的含量为10wt%至30wt%以及助导剂的含量为大于0wt%至18wt%。另外,电极组成物例如是藉由将活性物质、助导剂以及任一种前述实施方式中的黏着剂组成物进行混练而得。
在本实施方式中,活性物质包括碳材料或硅材料,其中碳材料例如可列举:石墨、非晶质碳、碳纤维、焦炭、活性碳;硅材料例如可列举:硅粉末、硅镍复合物、硅合金、奈米结构化硅材料。也就是说,在本实施方式中,活性物质只要是可使得锂离子在其中可逆地迁入与迁出者即可。
在本实施方式中,助导剂包括石墨碳、碳黑或其组合。详细而言,助导剂用以提高活性物质彼此间的电性接触。
值得说明的是,在本实施方式中,黏着剂组成物中由式I表示的聚酰胺酸与活性物质、助导剂之间皆具有良好的作用力。详细而言,这是因为由式I表示的聚酰胺酸的主链及侧链上的羧酸基与硅材料表面的SiO2会形成氢键,而产生氢键作用力;以及因为由式I表示的聚酰胺酸的侧链上的芘基、蒽基、苯并[a]芘基、苯并[e]芘基、萘并[2,3-a]芘基、二苯并[a,e]芘基、二苯并[a,h]芘基或萘基与碳材料之间会形成π-π堆栈(π-πstacking)结构,而产生分子间的π-π堆栈力(π-πstacking force)。如此一来,由式I表示的聚酰胺酸与助导剂之间会产生良好的π-π堆栈力,而由式I表示的聚酰胺酸与活性物质之间会产生良好的氢键作用力或者是良好的π-π堆栈力,藉此使得在电极组成物中,聚酰胺酸、活性物质与助导剂彼此之间能够稳固相连接。
本发明的又一实施方式提供一种电极,其由任一种前述实施方式中的电极组成物所制得。在本实施方式中,电极例如是以下列方式来制备:首先,将电极组成物涂布于集电体上。详细而言,涂布电极组成物的方法可使用一般所进行的涂布法,例如浸渍涂布法、旋涂法、喷涂法、刷毛涂布法、辊转印法、网版印刷法、喷墨法或胶版印刷法。所述集电体例如是铜箔、镍箔或金箔,且其形状无特别限制,较佳为使用厚度为0.001mm至0.5mm的片状者。接着,对涂布有电极组成物的集电体进行加热处理,以使由式I表示的聚酰胺酸进行酰亚胺化反应而形成聚酰亚胺,并移除溶剂。详细而言,所述加热处理的方法并无特别限制,例如可列举:真空干燥、送风干燥、温风干燥、红外线加热、远红外线加热等,而加热处理的温度条件例如是100℃至150℃,且时间条件例如是420分钟至600分钟。另外,在本实施方式中,所述聚酰亚胺即为黏着剂(binder)。
另外一提的是,在进行加热处理之前或之后,选择性地可还包括进行压制处理,以提高电极的活性物质的密度,以及使电极结构中位在上层的材料层与集电体的距离更加靠近。详细而言,所述压制处理的方法并无特别限制,例如可列举模具压制、辊压制或碾压制等方法。
值得说明的是,在本实施方式中,电极中的黏着剂与活性物质、助导剂及集电体之间皆具有良好的作用力。详细而言,由于由式I表示的聚酰胺酸的主链及侧链上皆具有羧酸基,故在所述聚酰胺酸的主链上的羧酸基因进行酰亚胺化反应而失去后,所得的黏着剂在侧链上仍具有羧酸基。更详细而言,所述羧酸基不但能够与硅材料产生氢键作用力,还能够与集电体形成错合物而相连接。另一方面,由于由式I表示的聚酰胺酸的侧链上具有芘基、蒽基、苯并[a]芘基、苯并[e]芘基、萘并[2,3-a]芘基、二苯并[a,e]芘基、二苯并[a,h]芘基或萘基,故经酰亚胺化反应而得的黏着剂同样在侧链上也具有芘基、蒽基、苯并[a]芘基、苯并[e]芘基、萘并[2,3-a]芘基、二苯并[a,e]芘基、二苯并[a,h]芘基或萘基,藉此使得黏着剂与碳材料之间能够产生分子间的π-π堆栈力。如此一来,黏着剂与助导剂之间会产生良好的π-π堆栈力,而黏着剂与活性物质之间会产生良好的氢键作用力或者是良好的π-π堆栈力,以及黏着剂与集电体之间因形成错合物而相连接,藉此使得在电极结构中,活性物质与助导剂通过黏着剂能够稳固黏附在集电体上。进一步而言,如上所述,由于黏着剂可与助导剂及活性物质之间产生良好的π-π堆栈力,藉此使得本实施方式的电极的导电性增加。
本发明的再一实施方式提出一种锂电池,其包括阳极、阴极、隔离膜、电解液以及封装结构。阳极即为任一种前述实施方式中的电极。
阴极与阳极分离配置。阴极包括阴极金属箔及阴极材料,阴极材料通过涂布或是溅镀而配置于阴极金属箔上。阴极金属箔例如是铝箔。阴极材料包括锂与过渡金属混合氧化物(Lithium mixed transition metal oxide)。锂与过渡金属混合氧化物例如是LiMnO2、LiMn2O4、LiCoO2、Li2Cr2O7、Li2CrO4、LiNiO2、LiFeO2、LiNixCo1-xO2、LiFePO4、LiMn0.5Ni0.5O2、LiMn1/3Co1/3Ni1/3O2、LiMc0.5Mn1.5O4或其组合,其中0<x<1,Mc为二价金属。另外,阴极可还包括高分子黏着剂,其中高分子黏着剂与阴极反应,以增加电极的机械性质。详言之,阴极材料可藉由高分子黏着剂黏着于阴极金属箔上。高分子黏着剂例如是聚二氟乙烯(PVDF)、苯乙烯丁二烯橡胶(SBR)、聚酰胺、三聚氰胺树脂(melamine resin)或上述化合物的组合。
隔离膜设置于阳极与阴极之间,以将阳极与阴极隔开。隔离膜的材料例如是绝缘材料,而绝缘材料可为聚乙烯(PE)、聚丙烯(PP)或上述材料的多层复合结构如PE/PP/PE。
电解液设置于容置区域中,且电解液包括有机溶剂、锂盐以及添加剂,其中有机溶剂的添加量占电解液的95wt%至90wt%,锂盐的添加量占电解液的5wt%至10wt%,添加剂的添加量则占电解液的0wt%至10wt%。
有机溶剂并无特别限制,可以是所属技术领域中普通技术人员所周知的有机溶剂,例如可列举:γ-丁基内酯、碳酸乙烯酯(EC)、碳酸丙烯酯、碳酸二乙酯(DEC)、乙酸丙酯(PA)、碳酸二甲酯(DMC)、碳酸甲乙酯(EMC)或上述的组合。
锂盐并无特别限制,可以是所属技术领域中普通技术人员所周知的锂盐,例如可列举:LiPF6、LiBF4、LiAsF6、LiSbF6、LiClO4、LiAlCl4、LiGaCl4、LiNO3、LiC(SO2CF3)3、LiN(SO2CF3)2、LiSCN、LiO3SCF2CF3、LiC6F5SO3、LiO2CCF3、LiSO3F、LiB(C6H5)4、LiCF3SO3或上述的组合。
添加剂并无特别限制,可以是所属技术领域中普通技术人员所周知的添加剂,例如可列举:单马来酰亚胺、聚马来酰亚胺、双马来酰亚胺、聚双马来酰亚胺、双马来酰亚胺与单马来酰亚胺的共聚物、碳酸亚乙烯酯(vinylene carbonate,VC)、氟代碳酸乙烯酯(fluoroethylene carbonate,FEC)或其混合物。
封装结构则用以包覆阳极、阴极及电解液。封装结构的材料例如是铝箔或不锈钢。
特别说明的是,锂电池的阳极使用了前述实施方式中的电极,因此如前文所述,在阳极中,活性物质与助导剂通过黏着剂能够稳固黏附在集电体上,藉此可缓冲活性物质在充放电过程中因锂离子的迁入与迁出而造成体积膨胀与收缩的效应。如此一来,阳极结构不易因体积剧烈变化而崩解,使得本发明的锂电池能够具有良好的电容量、稳定性及循环寿命。
另外,在上述实施方式中,虽然本发明的锂电池是以二次锂电池为例来进行说明,然而本发明的应用并不限定于此。在其他实施方式中,锂电池也可以是其他不同型态的锂电池,例如一次锂电池。
下文将参照实施例1及比较例1~3,更具体地描述本发明的特征。虽然描述了以下实施例1,但是在不逾越本发明范畴的情况下,可适当地改变所用材料、其量及比率、处理细节以及处理流程等等。因此,不应由下文所述的实施例对本发明作出限制性地解释。
<实施例1>
黏着剂组成物的制备
依序以以下的合成步骤来制备实施例1的黏着剂组成物,其包括上述由式II表示的聚酰胺酸以及作为溶剂的N,N-二甲基乙酰胺。然而,以下的合成步骤仅为例示性而不限制本发明的范围。
首先,合成式1表示的二胺单体,其反应式如下:
详细而言,所述式1表示的二胺单体的合成反应包括下列步骤。首先,在0℃下,在三颈圆底烧瓶中将2,2’-联苯二甲酸(biphenyl-2,2’-dicarboxylic acid)(10g,41mmol)溶解于浓硫酸(86g)中。接着,将浓硝酸(70%,30.8g,340mmol)与浓硫酸(4g)混合,并将所述混合酸液缓慢加入所述三颈圆底烧瓶中。待完全加入后,在室温下,将所得的混合物持续搅拌反应24小时。接着,将所得的混合物倾注入冰浴中并进行过滤后,再使用乙醇/水进行纯化以得到呈浅黄色结晶体的由式a表示的化合物(产率为90%)。1H NMR(400MHz,DMSO-d6):δ(ppm)13.41(s,2H),8.67(s,2H),8.44(d,2H,J=8.36Hz),7.53(d,2H,J=8.36Hz);13C NMR(100MHz,DMSO-d6):δ(ppm)165.68,148.17,147.02,131.72,131.50,126.16,124.57。
接着,在氮气气氛下,将由式a表示的化合物(1g,3.01mmol)和10%钯碳触媒(Pd/C)(0.025g)均匀分散于乙醇(13ml)中。之后,将联胺(hydrazine monohydrate,H2NNH2·H2O)缓慢加入所述混合物中。待加完联胺后,在80℃下,将所得的混合物持续搅拌反应24小时后,趁热进行过滤以移除10%钯碳触媒(Pd/C)并取得滤液。接着,藉由旋转蒸发器进行浓缩后,再使用甲醇/乙醇进行纯化以得到呈白色粉状固体的由式1表示的二胺单体(产率为75%)。1H NMR(400MHz,DMSO-d6):δ(ppm)6.98(sd,2H,J=2.40Hz),6.73(d,2H,J=8.2Hz),6.62(dd,J1=8.14Hz,J2=2.44Hz);13C NMR(100MHz,DMSO-d6):δ(ppm)169.50,146.75,131.97,131.75,130.91,116.60,114.97。
接着,合成由式2表示的二胺单体,其合成反应式如下:
详细而言,所述式2表示的二胺单体的合成反应包括下列步骤。首先,将草酰氯(oxalyl chloride)(1.03ml,12.11mmol)与两滴作为催化剂的DMF(于反应式中以Cat.DMF标示)加入由式a表示的化合物(1g,3.01mmol)及二氯甲烷(dichloromethane,DCM)(7.52ml)的混合溶液中。接着,在室温下,将所得的混合物持续搅拌反应12小时后,藉由旋转蒸发器进行浓缩以得到呈淡黄色的油状物。之后,在氮气气氛下,将所得的油状物(0.50g,13.5mmol)以及1-芘甲醇(1-pyrenemethanol)(1.26g,5.42mmol)溶解于除水的NMP(于反应式中以dry NMP标示)中。接着,在室温下,将所得的混合物持续搅拌反应24小时。之后,将所得的混合物倾注入去离子水浴中并进行过滤后,再使用二氯甲烷/甲醇进行纯化以得到呈浅黄色结晶体的由式b表示的化合物(产率为80%)。1H NMR(400MHz,CDCl3):δ(ppm)8.23(d,2H,J=7.56Hz),8.14-8.09(m,6H),8.02-7.92(m,8H),7.79(d,2H,J=9.2Hz),7.60(d,2H,J=7.8Hz),7.52(dd,2H,J1=8.3Hz,J2=2.2Hz),6.85(d,2H,J=8.3Hz),5.68-5.57(m,4H);13C NMR(100MHz,CDCl3):δ(ppm)164.07,146.97,146.27,132.00,131.21,130.37,130.09,129.84,129.42,128.33,128.11,127.19,126.76,126.34,126.22,125.97,125.62,125.24,125.01,124.57,124.35,124.28,122.24,65.82。
接着,将由式b表示的化合物(1g,1.31mmol)以及氯化锡(II)二水合物(tin(II)chloride dihydrate)(2.96g,13.12mmol)溶解于乙醇(13ml)与乙酸乙酯(ethyl acetate,EA)(13ml)的混合液中。接着,在80℃下,将所得的混合物进行加热回流并持续搅拌反应24小时。之后,将所得的混合物倾注入氢氧化钾溶液中并使用乙酸乙酯进行萃取三次,以收集有机层。接着,使所收集的有机层以无水硫酸镁除水,以旋转蒸发器除去溶剂,并最后使用乙酸乙酯/正己烷(1:2)作为冲提液通过硅胶管柱层析来进行纯化,以得到呈黄色的粉状固体的由式2表示的二胺单体(产率为60%)。1H NMR(400MHz,CDCl3):δ(ppm)8.14(d,2H,J=7.48Hz),8.05-7.83(m,14H),7.71(d,2H,J=7.76Hz),6.66-6.62(m,4H),6.13(dd,2H,J1=8.0Hz,J2=2.3Hz),5.70-5.57(m,4H),2.79(s,4H);13C NMR(100MHz,CDCl3):δ(ppm)167.45,144.51,133.21,131.35,131.31,130.96,130.60,130.09,129.49,128.88,127.93,127.64,127.49,127.28,125.92,125.27,125.22,124.62,124.46,124.24,123.20,117.47,115.86,64.50。
之后,合成由式II表示的聚酰胺酸(即制备实施例1的黏着剂组成物),其合成反应式如下:
首先,在氮气气氛下,在架设有另一烧瓶的三颈圆底烧瓶中,使由式1表示的二胺单体(0.15g,0.57mmol)以及由式2表示的二胺单体(0.4g,0.57mmol)溶解于DMAc(2.6ml)中,以形成二胺单体溶液。接着,将置于所述另一烧瓶中的PMDA(0.25g,1.14mmol)加入所述二胺单体溶液中。之后,在室温下,将所得的混合物持续搅拌反应12小时后即获得实施例1的黏着剂组成物。1H NMR(400MHz,DMSO-d6):δ(ppm)10.72(s,-COOH-),8.38-7.63(m,Ar H),7.19(s,Ar H),5.72-5.63(m,-CH2-)。
电极的制作
首先,将70wt%的硅镍复合物(Si:Ni=2:1)(前述的活性物质)、15wt%的石墨碳(KS-6)(前述的助导剂)、3wt%的碳黑(Super P)(前述的助导剂)以及12wt%的实施例1的黏着剂组成物进行混练以得到实施例1的电极组成物。接着,将所述实施例1的电极组成物以涂布机涂布(由乐利士股份有限公司制造(All Real Technology Co.,Ltd.))于铜箔(前述的集电体)上。之后,经由碾压机碾压以得到厚度大约为35-40μm的具有实施例1的电极组成物的铜箔,其中铜箔的厚度约为15μm。接着,经由裁切机以13mm的裁切刀将所述铜箔裁切成盘状后,置入真空烘箱中并在150℃下真空干燥七小时,以获得实施例1的电极。
锂电池的制作
组装2032型硬币半电池(coin half cell),其中使用实施例1的电极作为工作电极、锂箔作为相对极、额外添加10wt%的FEC的1M LiPF6(其中溶剂为体积比为1:2的EC与EMC的混合液)作为电解液、聚丙烯膜作为隔离膜以及不锈钢304盖作为封装结构。至此,制得实施例1的锂电池。
<比较例1>
黏着剂组成物的制备
以以下的合成方法来制备比较例1的黏着剂组成物,其包括下述由式III表示的聚酰胺酸以及作为溶剂的N,N-二甲基乙酰胺。然而,以下的合成方法仅为例示性而不限制本发明的范围。
合成式III表示的聚酰胺酸(即制备比较例1的黏着剂组成物),其反应式如下:
首先,在氮气气氛下,在架设有另一烧瓶的三颈圆底烧瓶中,使由式1表示的二胺单体(0.5g,1.84mmol)溶解于DMAc(3.6ml)中,以形成二胺单体溶液。接着,将置于所述另一烧瓶中的PMDA(0.4g,1.84mmol)加入所述二胺单体混合溶液中。之后,在室温下,将所得的混合物持续搅拌反应12小时后即获得比较例1的黏着剂组成物。1H NMR(400MHz,DMSO-d6):δ(ppm)10.72(s,-COOH-),8.36-8.28(m,Ar H),8.03(s,Ar H),7.82(s,Ar H),7.17(s,Ar H)。
电极及锂电池的制作
按照与实施例1相同的制造程序制作比较例1的电极及锂电池,其差异之处仅在于:实施例1的电极组成物包括实施例1的黏着剂组成物,而比较例1的电极组成物包括比较例1的黏着剂组成物;以及实施例1的锂电池使用实施例1的电极作为工作电极,而比较例1的锂电池使用比较例1的电极作为工作电极。
<比较例2>
黏着剂组成物的制备
以以下的合成方法来制备比较例2的黏着剂组成物,其包括下述由式IV表示的聚酰胺酸以及作为溶剂的N,N-二甲基乙酰胺。然而,以下的合成方法仅为例示性而不限制本发明的范围。
合成式IV表示的聚酰胺酸(即制备比较例2的黏着剂组成物),其反应式如下:
首先,在氮气气氛下,在架设有另一烧瓶的三颈圆底烧瓶中,使由式2表示的二胺单体(0.50g,0.71mmol)溶解于DMAc(2.6ml)中,以形成二胺单体溶液。接着,将置于所述另一烧瓶中的PMDA(0.155g,0.71mmol)加入所述二胺单体混合溶液中。之后,在室温下,将所得的混合物持续搅拌反应12小时后即获得比较例2的黏着剂组成物。1H NMR(400MHz,DMSO-d6):δ(ppm)10.69(s,-COOH-),8.36-7.63(m,Ar H),7.22(s,Ar H),5.73-5.63(m,-CH2-)。
电极及锂电池的制作
按照与实施例1相同的制造程序制作比较例2的电极及锂电池,其差异之处仅在于:实施例1的电极组成物包括实施例1的黏着剂组成物,而比较例2的电极组成物包括比较例2的黏着剂组成物;以及实施例1的锂电池使用实施例1的电极作为工作电极,而比较例2的锂电池使用比较例2的电极作为工作电极。
<比较例3>
黏着剂组成物的制备
将0.05g的海藻酸钠(sodium alginate)(由ACROS公司制造)溶解于2ml的水中,以获得比较例3的黏着剂组成物。值得一提的是,海藻酸钠为目前所述技术领域中常用来作为黏着剂使用的材料。
电极及锂电池的制作
按照与实施例1相同的制造程序制作比较例3的电极及锂电池,其差异之处仅在于:实施例1的电极组成物包括实施例1的黏着剂组成物,而比较例3的电极组成物包括比较例3的黏着剂组成物;以及实施例1的锂电池使用实施例1的电极作为工作电极,而比较例3的锂电池使用比较例3的电极作为工作电极。
在制得实施例1、比较例1-3的锂电池后,分别对实施例1、比较例1-3的锂电池进行充电放电循环测试,而其量测结果分别如图1至图4所示。
<充电放电循环测试>
将实施例1、比较例1-3的锂电池分别在下述测试条件下进行充放电:第1圈、第2圈的电流密度为0.05A/g,第3圈、第4圈、第5圈的电流密度为0.1A/g,第6圈至第305圈的电流密度为0.5A/g。图1、图2、图3及图4分别是实施例1、比较例1、比较例2及比较例3的锂电池的充电放电循环次数及电容量的关系图。另外,实施例1、比较例1-3的锂电池在完成第305圈的充放电循环的电池电容量如下表1所示。
表1
由图1至图4以及表1可知,与比较例1-3的锂电池相比,实施例1的锂电池具有较佳的稳定性、循环寿命及电容量。此结果证实,与使用侧链上仅有单一官能基团(即羧酸基或芘基)的黏着剂的比较例1、比较例2的锂电池以及使用已知黏着剂的比较例3的锂电池相比,使用侧链上具有两种不同官能基团(即羧酸基以及芘基)的黏着剂以使得活性物质与助导剂能够稳固黏附在集电体上的实施例1的锂电池能够同时具有良好的稳定性、循环寿命及电容量。
另外,为了更明确地比较锂电池的稳定性,分别将实施例1、比较例1-3的锂电池的第6圈至第305圈的放电电容量对第6圈的放电电容量进行规一化(normalize),并根据所得结果绘制图5。详细而言,由图5可知,与比较例1-3的锂电池相比,实施例1的锂电池具有较佳的稳定性。具体而言,在经过三百圈的充放电后,实施例1、比较例1-3的锂电池的电容量残余率分别为79%、69.49%、70.65%及66.95%。
另外,藉由扫描式电子显微镜(SEM)来分别评估进行第105圈充电放电循环测试后的实施例1、比较例1-3的锂电池的工作电极的表面状况,而其观测结果分别如图6A至图9B以及图10A至图13B所示。详细而言,由图6A至图9B可知,在经过105圈的充电放电循环测试后,比较例1-3的锂电池的工作电极的表面都有明显的裂缝产生,而实施例1的锂电池的工作电极的表面则没有明显的裂缝产生。另外,由图10A至图13B可知,与比较例1-3的锂电池相比,实施例1的锂电池有效地缓冲活性物质在充放电过程中的体积膨胀的效应。具体而言,经由计算后可得,实施例1、比较例1-3的锂电池的工作电极的膨胀率分别为43%、193%、100%及105%。
另外,在制得实施例1、比较例1-3的锂电池后,分别对实施例1、比较例1-3的锂电池进行交流阻抗测试,而其量测结果分别如图14所示。
<交流阻抗测试>
首先,将实施例1、比较例1-3的锂电池分别进行充放电五圈,其中测试状态为第五圈充电时,使其达到50%的总电容量的电位后,以交流振幅电压为5mV,频率范围在100000到0.01Hz进行阻抗值的量测,其中所得到的原始数据为阻抗值和相角,而经过转换之后可得电容阻抗Z”(Ohm)和电阻Z’(Ohm)。之后,藉由该些数据绘制图14。
详细而言,在EIS图中,图形一开始的半圆的直径大小得以分辨出锂电池的阻抗大小。由图14可知,与比较例1和比较例3的锂电池相比,实施例1和比较例2的锂电池的阻抗明显较小。此表示,通过在聚酰胺酸中导入芘基能够使得活性物质与助导剂之间有好的接触,并进而使得电极的导电性增加,藉此降低电荷传递时的阻抗。
虽然本发明已以实施方式揭示如上,然其并非用以限定本发明,任何所属技术领域中普通技术人员,在不脱离本发明的精神和范围内,当可作些许的改动与润饰,故本发明的保护范围当所附权利要求界定范围为准。
- 还没有人留言评论。精彩留言会获得点赞!