阿可拉定在制备用于治疗GP80相关疾病药物中的用途的制作方法
本发明涉及阿可拉定在制备用于治疗GP80相关疾病药物中的用途,属于医药领域。
背景技术:
GP80又称为IL-6R或IL-6Rα,白介素-6受体,其分子量为80kDa,是含有449个氨基酸的跨膜糖蛋白。GP80作为细胞因子IL-6的受体,细胞因子IL-6通过它的受体GP80和分子GP130发挥其生物活性。与GP130表达在所有细胞上不同的是,GP80仅在人体内包括肝细胞和白血病细胞在内的很少细胞上有表达。
已经有研究证实,IL-6/GP130(IL-6/GP130)信号通路的异常活化在多种肿瘤发生发展过程中发挥着关键性的作用。在《临床调查》(“The Journal of Clinical Investigation”)中公开了名称为“肝脏细胞中的IL6-GP130-STAT3通路形成了T-细胞调节的肝损伤肝保护”的文章(The IL-6-GP130-STAT3Pathway in Hepatocytes Triggers Liver Protection in T Cell-mediated Liver Injury)。文中提到IL-6引发导致肝保护的分子机制还不能完全清楚,对于信号转换,IL-6结合其受体GP80,形成的IL-6-GP80二聚体复合物与GP130 相互作用,进行信号传导。
在申请号为201110376649.X的中国专利申请中公开了名称为“拮抗和/或阻断白介素-6/白介素-6R/GP130信号通路在抗肝癌治疗中的用途。”文中提到白介素-6/白介素-6受体/GP 130信号途径的拮抗剂和/或阻断剂用于抗肝癌。因此可以看出,IL-6受体,即作为标志物在肝癌治疗中起着非常重要的作用。
阿可拉定,又名淫羊藿素,是从中药淫羊藿中提取分离得到的主要活性成分淫羊藿苷经酶转化得到的新的有效单体,其结构式如下式(I)所示:
该化合物的制备方法公开于CN101302548,该方法以淫羊藿苷为原料,以β-葡萄糖苷酶进行水解,水解产物离心得到的沉淀用丙酮溶解,离心过滤得到上清液。再将离心得到的上清液用水进行重结晶,得到阿可拉定纯品。
在申请号为200780039276.9的中国专利中公开了一种用于治疗与雌激素受体相关的疾病的化合物和方法,该专利中公开了阿可拉定用于治疗与雌激素受体ER-α36相关的肝癌。
在现有技术中,并没有针对阿可拉定对ER-α36以外的其他靶点的进一步研究。
技术实现要素:
本发明人惊奇地发现,阿可拉定能够治疗与GP80相关的疾病。
本发明的目的是提供阿可拉定在制备用于治疗与GP80相关疾病的药物中的用途。
本发明一方面提供了阿可拉定在制备用于治疗与GP80相关疾病的药物中的用途。
优选地,所述的GP80相关疾病包括与GP80相关的肝癌。
优选地,所述的药物为口服制剂或注射剂。
优选地,所述的注射剂为肌肉注射剂或静脉注射剂。
本发明的有益效果在于:本发明的阿可拉定在治疗与GP80相关疾病中取得了非常好的效果,特别是对于与GP80相关的肝癌,阿可拉定都表现出了良好的药学效果。因此,本发明为阿可拉定在治疗癌症中的靶向提供了进一步的研究方向。
附图说明
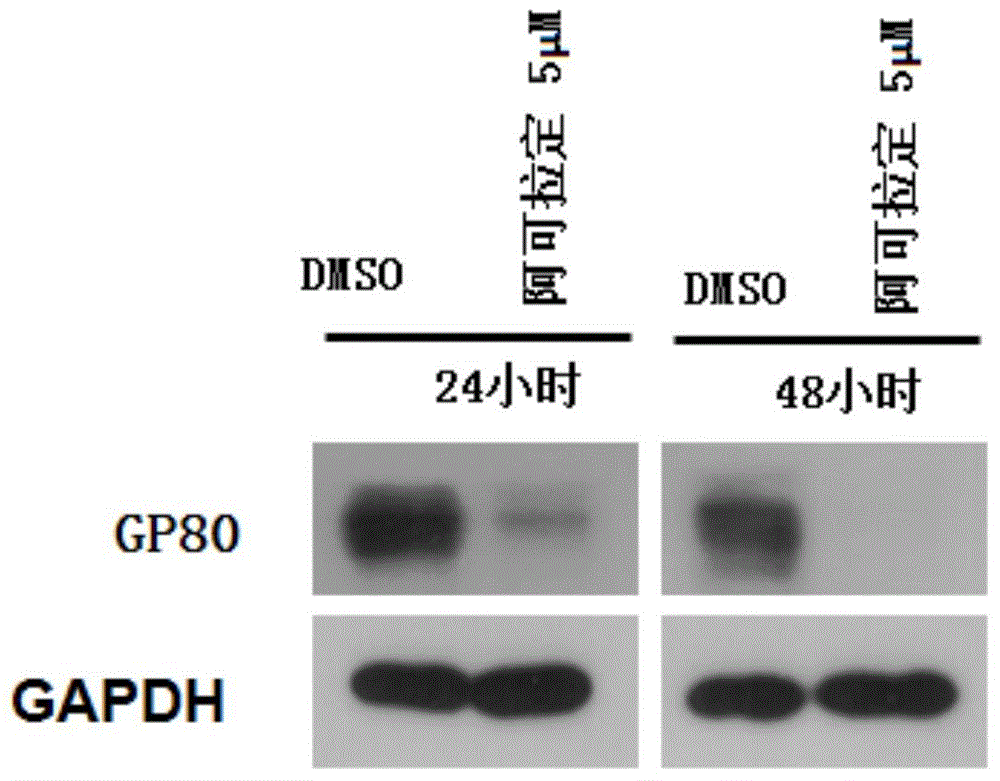
图1表示实施例2的阿可拉定对肝癌细胞PLC/PRF/5中的GP80蛋白抑制图。
图2表示实施例3的阿可拉定对肝癌细胞HUH-7中的GP80蛋白抑制图。
图3表示阿可拉定抑制PLC/PRF/5肝癌细胞的生长曲线。
图4表示阿可拉定抑制HUH-7肝癌细胞的生长曲线。
具体实施方式
以下实施例仅用于对本发明进行示例性说明,不用于限制本发明,在本发明保护范围内所做的修改、改变、变型等都在本发明的保护范围内。
术语“GP80”又称为IL-6R或IL-6Rα,白介素-6受体,其分子量为80kDa,是含有449个氨基酸的跨膜糖蛋白。GP80作为细胞因子IL-6的受体,细胞因子IL-6通过它的受体GP80和分子GP130发挥其生物活性。与GP130表达在所有细胞上不同的是,GP80仅在人体内包括肝细胞和白血病细胞在内的很少细胞上有表达
术语“GP80相关疾病”指的是在与疾病相关的组织细胞中的GP80表达超过正常水平。
术语“治疗GP80相关疾病的药物”指的是在治疗前,疾病细胞中的GP80表达超过正常水平,通过药物治疗,疾病细胞中的GP80表达达到正常值。
术语“肌肉注射剂”指的是注射于肌肉组织中的注射剂。
术语“静脉注射剂”指的是注入静脉进入血液的注射剂。
本发明中的“人肝癌细胞PLC/PRF/5”购自于日本癌症研究银行Japanese Cancer Research Bank(JCRB),Tokyo,Japan,商品名称PLC/PRF/5,商品编号为JCRB0406。
本发明中的“肝癌细胞株HUH-7”购自于日本癌症研究银行Japanese Cancer Research Bank(JCRB),Tokyo,Japan,商品名称Huh-7,商品编号为JCRB0403。
肝癌细胞株PLC/PRF/5和肝癌细胞株HUH-7的区别为均为人肝细胞肝癌,来源于不同的人。
除非另外说明,本发明中“阿可拉定”通过实施例1方法制备。
实施例1
阿可拉定的制备
阿可拉定又名淫羊藿素,是从中药淫羊藿中提取分离得到。
在公开号为CN 101302548的专利中公开了淫羊藿的制备方法。该方法以淫羊藿苷为原料,以β-葡萄糖苷酶进行水解,水解产物离心得到的沉淀用丙酮溶解,离心过滤得到上清液。再将离心得到的上清液用水进行重结晶,得到淫羊藿纯品。本发明中的淫羊藿苷购自陕西嘉禾植物化工有限责任公司,纯度90%。
实施例2
检测阿可拉定对肝癌细胞PLC/PRF/5细胞的抑制。
实验步骤:细胞培养:首先将PLC/PRF/5肝癌细胞在含有体积浓度为10%胎牛血清的氨基酸和葡萄糖培养基(即DMEM培养基)中培养至细胞密度为80%;再将培养后的细胞分至含有活性炭处理的体积浓度为2.5%体积浓度的胎牛血清的无酚红培养基中,培养24小时。
加入二甲基亚砜(DMSO)和阿可拉定:在培养体系中分别加入DMSO对照(即不含有阿可拉定的DMSO溶液)和5μM阿可拉定DMSO溶液,并使每个反应体系中DMSO的体积终浓度为0.1%。
分别于12、24和48小时收细胞,分别向细胞加入甘油醛-3-磷酸脱氢酶(GAPDH)抗体和GP80(IL-6R)抗体进行蛋白质印迹法(western blot)进行检测。
检测结果通过图1上半图可见,加入阿可拉定12小时、24小时和48小时,肝癌细胞PLC/PRF/5中的GP80蛋白表达明显降低,即 药物作用具有时间依赖性。阿可拉定处理细胞12小时后,随着药物浓度的提高,GP80蛋白水平下调越明显。通过图1下半图可见,阿可拉定对于细胞中GAPDH不产生任何改变。
实施例3
检测阿可拉定对肝癌细胞HUH-7细胞的抑制。
实验步骤:细胞培养:首先将HUH-7细胞在含有10%体积浓度胎牛血清的氨基酸和葡萄糖培养基(即DMEM培养基)中培养至细胞密度80%左右;再将培养后的细胞分至含有活性炭处理的体积浓度为2.5%的胎牛血清的无酚红培养基中,培养24小时。
加入二甲基亚砜(DMSO)和阿可拉定:在培养体系中分别加入DMSO对照(即不含有阿可拉定的DMSO溶液)和5μM浓度的阿可拉定DMSO溶液,并使每个反应体系中DMSO的体积终浓度为0.1%。
分别于12、24和48小时收细胞,分别向细胞加入甘油醛-3-磷酸脱氢酶(GAPDH)和GP80抗体进行蛋白质印迹法(western blot)进行检测。
检测结果通过图2上半图可见,加入阿可拉定24小时和48小时,肝癌细胞HUH-7中的GP80蛋白表达明显降低,并且随着作用时间延长,细胞内GP80蛋白水平下调越明显,即药物作用具有时间依赖性。通过图2下半图可见,阿可拉定对于细胞中GAPDH不产生任何改变。
实施例4
PLC/PRF/5肝癌细胞在阿可拉定作用下的增殖能力受到抑制
实验步骤:
1.PCL/PRF/5肝癌细胞培养在含有10%体积浓度胎牛血清的DMEM培养基中培养至细胞密度80%。
2.将细胞分至含有活性炭处理的2.5%体积浓度的胎牛血清的无酚红培养基中,培养24小时。
3.分别将2.5、5.0、7.5及10.0μM的阿可拉定加入到培养体系中,并使每个反应体系中DMSO体积浓度的终浓度为0.1%。将不含有阿可拉定的DMSO加入到培养体系中,作为空白对照组。
4.使用细胞计数试剂盒(CCK-8)检测细胞的增殖能力
4.1将步骤3的培养体系培养48小时后,加入10μM的2-(2-甲氧基-4-硝基苯基)-3-(4-硝基苯基)-5-(2,4-二磺酸苯)-2H-四唑单钠盐(CCK-8液);
4.237℃孵育2小时,酶标仪检测检测450及630nM处的吸光度;
4.3以阿可拉定的浓度做横坐标,并以相对于空白对照组的细胞比例为纵坐标,绘制出药物抑制PLC/PRF/5肝癌肿瘤细胞的生长曲线,见图3。
5.由图3可见,阿可拉定处理PLC/PRF/5肝癌细胞48小时,随着药物浓度的升高,活细胞被抑制的程度加深,呈现浓度依赖关系,阿可拉定对PLC/PRF/5细胞的IC50值为4.5μM。
实施例5
HUH-7肝癌细胞在阿可拉定作用下的增殖能力受到抑制
实验步骤:
1.HUH-7肝癌细胞培养在含有10%体积浓度的胎牛血清DMEM培养基中培养至细胞密度80%。
2.将细胞分至含有活性炭处理的2.5%体积浓度胎牛血清的无酚红培养基中,培养24小时。
3.分别将2.5、5.0、7.5及10.0μM浓度的阿可拉定加入到培养体系中,并使每个反应体系中DMSO的体积终浓度为0.1%。将不含有阿可拉定的DMSO加入到培养体系中,作为空白对照组。
4.使用细胞计数试剂盒(CCK-8)检测细胞的增殖能力
4.1将步骤3的培养体系培养48小时后,加入10μM的2-(2-甲氧基-4-硝基苯基)-3-(4-硝基苯基)-5-(2,4-二磺酸苯)-2H-四唑单钠盐(CCK-8液);
4.237℃孵育2小时,酶标仪检测检测450及630nM处的吸光度;
4.3以阿可拉定的浓度做横坐标,并以相对于空白对照组的细胞比例为纵坐标,绘制出药物抑制HUH-7肝癌肿瘤细胞的生长曲线,见图4。
5.由图4可见,阿可拉定处理HUH-7肝癌细胞48小时,随着药物浓度的升高,活细胞被抑制的程度加深,呈现浓度依赖关系,阿可拉定对HUH-7肝癌细胞的IC50值为4.5μM。
- 还没有人留言评论。精彩留言会获得点赞!