长寿基因表达增强剂的制作方法
本发明提供sirtuin-1激活剂、和含有该激活剂的用于抑制由氧化应激引起的细胞衰老的制剂。
背景技术:
近年来,作为长寿基因,依赖nad+的去乙酰化酶sirtuin基因受到关注。最初在酵母中鉴定了sir2基因,通过使用酵母、线虫等低等生物的实验系统,报告了sir2缺损则寿命缩短,过表达则寿命延长(非专利文献1和2)。在哺乳类中也保有sir2基因,鉴定了从sirtuin-1至sirtuin-7。其中,sirtuin-1由于与酵母sir2结构、功能最相似而尤其受到瞩目。
sirtuin-1的目标蛋白质已经被鉴定,从其研究认为其参与细胞内代谢、能量消耗、炎症和应激途径等。另外,认为sirtuin-1基因的激活在抗动脉硬化、抗糖尿病、心脏病、抗癌作用、糖尿病性并发症、神经性疼痛、微血管功能障害、寿命延长、线粒体性疾病、线粒体性肌病、神经变性病(例如,阿尔茨海默病、肌萎缩性硬化症、帕金森病)、慢性阻塞性肺疾病(copd)、和银屑病的治疗中有用(非专利文献3和4)。
到目前为止,作为sirtuin激活物质,已知葡萄的果皮等中包含的白藜芦醇、草莓等、苹果中包含的非瑟酮(fisetin)这样的多酚化合物、srt1720等非多酚化合物。英国的大公司glaxosmithkline致力于进行sirtuin-1激活物质的开发,报告了例如srt2104对2型糖尿病、骨质疏松症·肌少症(sarcopenia)、以及骨格肌萎缩的预防有效果(引用文献5),现在正在进行临床试验。
另一方面,已知滨海前胡(peucedanumjaponicumthunb.)的植物体或其提取物具有抑制二糖类分解酶的作用,在糖尿病的预防·治疗、减肥等中有效(专利文献1);具有细胞活化作用、抗氧化作用、黑色素产生抑制作用(专利文献2);具有乙酰肝素酶活性抑制作用;对皱纹的防止、改善有效(专利文献3)、具有神经酰胺合成促进作用(专利文献4)等。
滨海前胡在冲绳县作为传说“吃1株就多活1天”的植物,被称为长命草。另外,sirtuin基因作为长寿基因被知晓已经15年以上。然而,关于滨海前胡的植物体或其提取物具有sirtuin-1激活作用到目前为止完全没有报告,可以说发现本相关性不是容易的。从关于滨海前胡与长寿相关的传说没有显示任何科学根据这点来看,也可以说发现本相关性不是容易的。
在先技术文献
专利文献
专利文献1:日本特开2003-26694号公报
专利文献2:日本特开2004-26697号公报
专利文献3:国际公开第2009/123215号
专利文献4:日本特开2005-194239号公报
非专利文献
非专利文献1:genesdev.,13(19):2570-80(1999)
非专利文献2:nature,410(6825):227-30(2001)
非专利文献3:nat.rev.drugdiscov.,7(10):841-853(2008)
非专利文献4:j.invest.dermatol.,129(1):41-49(2009)
非专利文献5:aging.cell,13(5):787-796(2014)
非专利文献6:proc.natl.acad.sci.usa,92(20):9363-9367(1995)
非专利文献7:nat.protoc.,4(12):1798-1806(2009)
非专利文献8:j.atheroscler.thromb.,17(9):970-979(2010)
非专利文献9:j.atheroscler.thromb.vasc.biol.,30(11):2205-2211(2010)
技术实现要素:
发明所要解决的课题
本发明的课题是提供sirtuin-1激活剂、和含有该激活剂的用于抑制由氧化应激引起的细胞衰老的制剂。
用于解决课题的方法
发明者们进行了深入研究,结果发现,滨海前胡(peucedanumjaponicumthunb.)(别名“长命草”)的植物体或其溶剂提取物作为sirtuin-1激活剂发挥功能,从而完成了以下的发明:
(1)一种sirtuin-1激活剂,其特征在于,包含滨海前胡(peucedanumjaponicumthunb.)的植物体或其溶剂提取物。
(2)根据(1)所述的sirtuin-1激活剂,其特征在于,所述溶剂提取物是含水乙醇提取物。
(3)根据(1)或(2)所述的sirtuin-1激活剂,其特征在于,滨海前胡的植物体是其叶、茎或全草。
(4)一种制剂,其特征在于,是用于抑制由氧化应激引起的细胞衰老的制剂,包含sirtuin-1激活剂,所述sirtuin-1激活剂包含滨海前胡(peucedanumjaponicumthunb.)的植物体或其溶剂提取物。
(5)根据(4)所述的制剂,其特征在于,所述溶剂提取物是含水乙醇提取物。
(6)根据(4)或(5)所述的制剂,其特征在于,滨海前胡的植物体是其叶、茎或全草。
(7)根据(4)~(6)的任一项所述的制剂,其特征在于,所述制剂是口服摄取制剂。
(8)滨海前胡(peucedanumjaponicumthunb.)的植物体或其溶剂提取物,用于抑制由氧化应激引起的细胞衰老。
(9)根据(8)所述的滨海前胡(peucedanumjaponicumthunb.)的植物体或其溶剂提取物,其特征在于,所述溶剂提取物是含水乙醇提取物。
(10)根据(8)或(9)所述的滨海前胡(peucedanumjaponicumthunb.)的植物体或其溶剂提取物,其特征在于,滨海前胡的植物体是其叶、茎或全草。
(11)sirtuin-1激活剂在用于抑制由氧化应激引起的细胞衰老的制剂的制造中的使用,其特征在于,所述sirtuin-1激活剂包含滨海前胡(peucedanumjaponicumthunb.)的植物体或其溶剂提取物。
(12)根据(11)所述的使用,其特征在于,所述溶剂提取物是含水乙醇提取物。
(13)根据(11)或(12)所述的使用,其特征在于,滨海前胡的植物体是其叶、茎或全草。
(14)根据(11)~(13)的任一项所述的使用,其特征在于,所述制剂是口服摄取制剂。
(15)用于抑制由氧化应激引起的细胞衰老的方法,其特征在于,对需要抑制由氧化应激引起的细胞衰老的对象,施与包含滨海前胡(peucedanumjaponicumthunb.)的植物体或其溶剂提取物的sirtuin-1激活剂。
(16)根据(15)所述的方法,其特征在于,所述溶剂提取物是含水乙醇提取物。
(17)根据(15)或(16)所述的方法,其特征在于,滨海前胡的植物体是其叶、茎或全草。
(18)根据(15)~(17)的任一项所述的方法,其特征在于,口服施与所述sirtuin-1激活剂。
(19)用于预防或治疗选自抗动脉硬化、抗糖尿病、心脏病、抗癌作用、糖尿病性并发症、神经障害性疼痛、微血管功能障害、寿命延长、线粒体性疾病、线粒体性肌病、神经变性病(例如,阿尔茨海默病、肌萎缩性硬化症、帕金森病)、慢性阻塞性肺疾病(copd)和银屑病中的疾病的方法,其特征在于,对需要治疗所述疾病的对象施与包含滨海前胡(peucedanumjaponicumthunb.)的植物体或其溶剂提取物的sirtuin-1激活剂。
(20)根据(19)所述的方法,其特征在于,所述溶剂提取物是含水乙醇提取物。
(21)根据(19)或(20)所述的方法,其特征在于,滨海前胡的植物体是其叶、茎或全草。
(22)根据(19)~(21)的任一项所述的方法,其特征在于,口服施与所述sirtuin-1激活剂。
发明的效果
通过施与本发明的sirtuin-1激活剂,能够激活sirtuin-1。根据本发明,能够提供含有sirtuin-1激活剂的口服摄取制剂。
附图说明
图1显示通过蛋白质印迹(westernblot)法来评价sirtuin-1的表达量。
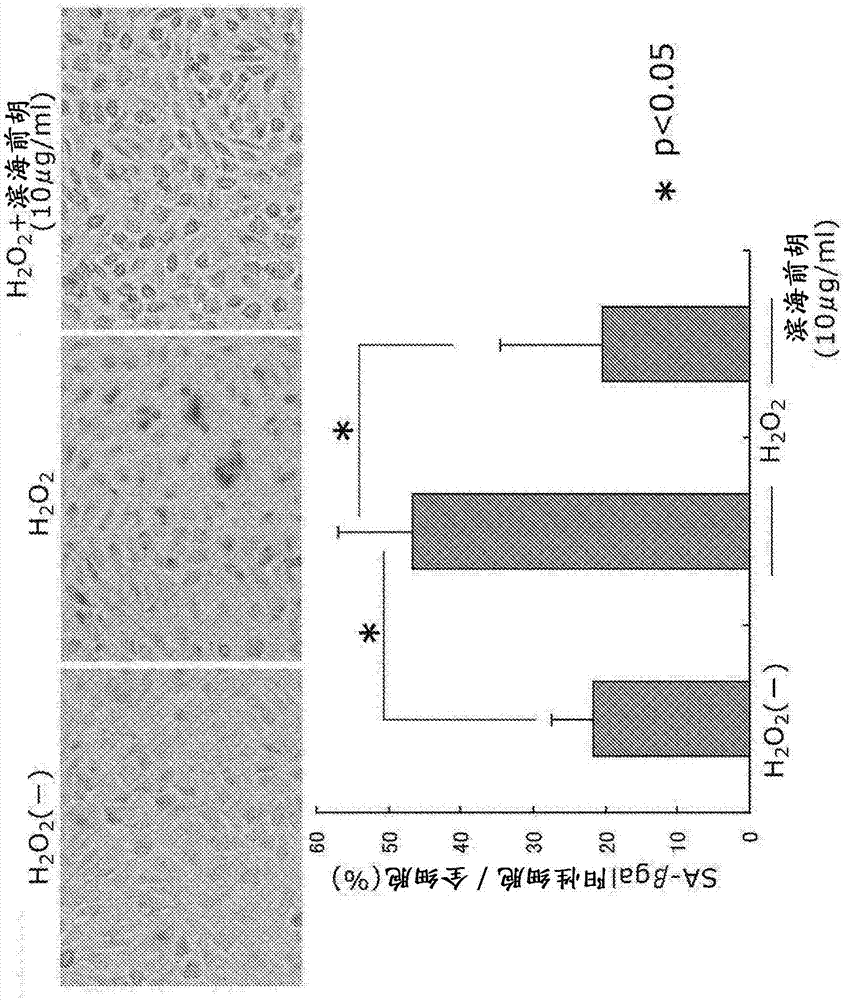
图2显示针对氧化应激的滨海前胡的细胞衰老抑制作用。
具体实施方式
通过施与本发明的sirtuin-1激活剂,能够激活sirtuin-1。
通过激活sirtuin-1基因,能够抑制由氧化应激引起的细胞衰老。由氧化应激引起的细胞衰老,是指由于由吸烟、暴饮暴食、对引起活性氧生成的化学药品等的暴露、过劳、对紫外线、放射线的暴露等氧化应激而产生的过氧化物、自由基,造成细胞内的蛋白质、脂质、dna等损伤,从而不可逆地引发细胞停止分裂而不能增殖的状态,与由年龄增长等细胞增殖活性降低引起的衰老现象不同。细胞衰老的评价在本领域常规地进行,作为衰老标志物,例如,可以使用细胞衰老相关β半乳糖苷酶(saβ-gal)(非专利文献6和7)。已知sirtuin-1基因与由氧化应激引起的细胞衰老相关,例如,报告了白藜芦醇、斯达汀(statin)激活sirtuin-1基因,能够抑制由氧化应激引起的细胞衰老(非专利文献8和9)。因此,sirtuin-1基因的激活对由氧化应激引起的细胞衰老的抑制有用。
sirtuin-1基因的激活在抗动脉硬化、抗糖尿病、心脏病、抗癌作用、糖尿病性并发症、神经障害性疼痛、微血管功能障害、寿命延长、线粒体性疾病、线粒体性肌病、神经变性病(例如,阿尔茨海默病、肌萎缩性硬化症、帕金森病)、慢性阻塞性肺疾病(copd)、和银屑病的预防或治疗中也有用。
本发明中的sirtuin-1基因的激活,可以指使例如sirtuin-1基因的表达增强,例如与不付与任何物质的状态(对照)相比,付与了sirtuin-1激活剂的情况下sirtuin-1基因的表达以例如显著性水平为5%的统计学的显著性差异(例如学生t检验)增强。或者,本发明中的sirtuin-1基因的激活,可以指例如与不付与任何物质的状态(对照)相比,付与了sirtuin-1激活剂的情况下sirtuin-1基因的表达增强例如10%以上、20%以上、30%以上、40%以上、50%以上、60%以上、70%以上、80%以上、90%以上、100%以上、200%以上、300%以上、400%以上、或500%以上。
本发明的sirtuin-1激活剂含有能口服摄取的滨海前胡(peucedanumjaponicumthunb.)提取物作为有效成分。
本发明中使用的滨海前胡(peucedanumjaponicumthunb.)(别名“长命草”)是伞形科(umbelliferae)前胡属(peucedanuml.)的植物,分布于日本本州石川县、关东地区以西、四国、九州、冲绳,以及朝鲜半岛、中国、中国台湾、菲律宾,是生长在海边的向阳地的多年生草本植物(新订原色牧野和汉药草大图鉴368页(2002))。
滨海前胡可以活着直接使用也可以干燥后使用,从使用性、制剂化等观点考虑,优选制成干燥粉末或提取物使用。
作为获得干燥粉末的方法,有将植物的全草或各种部位(叶、花、根等)切碎或粉碎,然后干燥的方法,和/或将植物干燥后切碎或粉碎而获得干燥粉末的方法。另外,可以适宜采用将植物切碎或粉碎,进行发酵、酶处理后干燥,再根据需要粉碎成规定的粒径的方法等。
本发明中使用的提取物的提取方法可以通过溶剂提取来进行。在溶剂提取时,根据需要使植物的全草或各种部位(叶、花、根等)干燥,再根据需要切碎或粉碎后,使用水性提取剂、例如冷水、温水、或沸点或温度低于沸点的热水、或含水有机溶剂、有机溶剂、例如甲醇、乙醇、1,3-丁二醇、醚等在常温或加热下进行提取。然而,提取方法不限于溶剂提取,可以通过本领域已知的常用方法来进行。上述提取物的形态不仅是提取液自身,也可以是通过常用的方法适宜稀释或浓缩后的物质,还可以是将提取液干燥而得的粉状或块状的固体。
本发明中使用的提取溶剂优选为含水有机溶剂,特别优选选择含水甲醇、含水乙醇或含水1,3-丁二醇等含水低级醇,最优选含水乙醇。此时的含水率为例如20~80质量%。
本发明的sirtuin-1激活剂可以口服摄取或外用施与,但优选口服摄取。
在口服摄取本发明的sirtuin-1激活剂时,滨海前胡的植物体或其溶剂提取物的配合量可以根据它们的种类、目的、形态、利用方法等来适宜决定。优选调制成成人每一天的植物体或其溶剂提取物的摄取量为约0.16g~约16g(干燥质量换算)左右。更优选调制成约0.8~约8g(干燥质量换算)左右。另外,在作为口服摄取制剂利用时,优选以充分发挥sirtuin-1激活的效果那样的量含有本发明的有效成分。
将本发明的sirtuin-1激活剂配合到口服摄取制剂中时,可以根据需要任意选择添加剂来并用。作为添加剂可以包含赋形剂等。
作为赋形剂,只要是在制成所希望的剂型时通常使用的即可,可列举例如,小麦淀粉、稻淀粉、玉米淀粉、马铃薯淀粉、糊精、环糊精等淀粉类、结晶纤维素类、乳糖、葡萄糖、砂糖、还原麦芽糖、水饴、低聚果糖、低聚乳果糖等糖类、山梨糖醇、赤藓糖醇、木糖醇、乳糖醇、甘露糖醇等糖醇类。这些赋形剂可以单独使用或二种以上组合使用。
关于其他的着色剂、保存剂、增稠剂、结合剂、崩解剂、分散剂、稳定剂、胶凝剂、抗氧化剂、表面活性剂、保存剂、ph调节剂等,可以适宜选择公知的物质使用。
作为口服摄取的形态,可以任意选择例如液体状、固体状、颗粒状、粒状、糊状、凝胶状等。
实施例
接着通过实施例更详细地说明本发明。此外,本发明不受这些实施例限定。
实验1:试样的制备
将滨海前胡干燥粉末浸渍在70%乙醇中,室温搅拌一晚。将过滤液减压浓缩而回收,实验时溶解在dmso液中进行评价。
实验2:滨海前胡对sirtuin-1表达的作用
利用蛋白质印迹(westernblot)法的评价
将人脐静脉内皮细胞(huvec)(lonza,md)接种在collagen-coatedmicroplate6well(胶原蛋白包被6孔微板)上,培养至亚融合(subconfluent)。然后,在包含滨海前胡提取物(终浓度:10μg/ml)、或白藜芦醇(5μm)的培养基(ebm2)中孵育48小时,用phosphosafeextractionreagent(emdchemicals,ca)回收蛋白,使用bcakit(piercebiotechnology,rockford,il)测定蛋白浓度。进行调整使得样品的蛋白浓度为等量,1抗使用anti-sirtuin-1(santacruzbiotechnology,ca)、anti-βactin(sigmaaldrich,st.louis,mo),2抗分别使用anti-rabbit(gehealthcare,buckinghamshire,uk)anti-mouse(gehealthcare,buckinghamshire,uk)通过蛋白质印迹(westernblot)法进行评价。统计学显著性差异检验使用学生t检验。
结果示于图1。在添加滨海前胡提取物(10μg/ml)进行孵育的情况下,与添加对照和已知的sirtuin-1激活剂白藜芦醇(5μm)进行孵育的情况相比,sirtuin-1表达增加(p<0.05)。
此外,已知滨海前胡中包含绿原酸、芸香苷和橘皮苷,但绿原酸被报告没有sirtuin-1的激活作用(plosone,2014,9(2),e89166),关于芸香苷,报告了在生物体内由芸香苷转换生成的槲皮苷具有sirtuin-1的表达抑制作用(j.pharmacol.sci.,2008,108,364-71)。另一方面,在滨海前胡的植物体中微量存在的橘皮苷被报告了以5μm而具有sirtuin-1激活作用(biosci.biotechnol.biochem.,2012,76(4),640-645)。然而,将试验样品提取物的制备中使用的粉末用hplc测定,结果橘皮苷含量为0.62%重量。效应浓度(提取物10μg/ml)的提取物中所含的橘皮苷(分子量610)浓度最大也不过0.102μm,因此滨海前胡的优异sirtuin-1激活作用不能通过已知的含有成分来说明。
实验3.针对氧化应激的细胞衰老的抑制作用
对于针对由h2o2添加产生的氧化应激的滨海前胡的细胞衰老抑制作用,通过衰老标志物saβ-gal(衰老相关的β-半乳糖苷酶,senescence-associatedβ-galactosidase)的活性增加来评价。发生细胞衰老的细胞saβ-gal活性增加,添加底物则被染色成青色。
将huvec在100mm/collagen-coateddish(胶原蛋白包被平皿)中用培养基(ebm2)(lonza,basal,switzerland)培养至亚融合(subconfluent)。然后,添加h2o2(终浓度:0,100μm)孵育1小时(37℃,0.5%co2),使用包含滨海前胡提取物(终浓度:10μg/ml)的培养基(ebm2)再接种至5×104个细胞/平皿。然后培养5天,使用cellularsenescenceassaykit(millipore,ma)进行评价。统计学显著性差异检验使用学生t检验。
结果示于图2。在不含滨海前胡提取物的培养基中孵育的细胞通过添加h2o2而saβ-gal活性增加,细胞被染色成青色。与此相对,在包含滨海前胡提取物(10μg/ml)的培养基中孵育的细胞,其青色的染色性减弱(p<0.05)。这显示,通过滨海前胡提取物,saβ-gal的活性被抑制,进而细胞衰老被抑制。
- 还没有人留言评论。精彩留言会获得点赞!