一种用于抗急性脑缺血药物的制备方法、应用及检测设备与流程
本发明涉及一种用于抗急性脑缺血药物的制备方法、应用,本发明涉及一种抗急性脑缺血药物的检测设备。
背景技术:
目前国内因心脑血管疾病死亡的,是最主要病因。而目前市场上销售治疗急性脑缺血疾病的药物包括盐酸氟桂利嗪、血栓通、三七皂甙、黄铜类等。虽然都有一定疗效,但有含碳元素,且制药成本高;对于植物提取的药物,由于药材产地不同,收采地不同,质量标准难以控制,疗效具有不确定性。
国家知识产权局1998年12月30日,以公开号cn1203080a公开了的专利申复方硫化钠注射液;2006年8月30日,以公开号cn1823815a公开了的专利申硫化钠静脉注射液在制备治疗脑梗死后遗症药剂中的应用。这两项专利虽然公开了硫化钠注射液在制备治疗脑梗死后遗症药剂中的应用,但没有公开硫化钠注射液制作方法、应用的实验数据、药物的检测方法和检测设备。特别是这两项专利申请没有公开应用的实验数据,这两项专利申请的内容实际上并没有真正成为本领域专业技术人员所认可的已有技术,不能被所述领域的技术人员认真考虑和接收,以及使用。
所述硫化钠的分子式:na2s,分子量:78.04;
硫化钠的结构式:
技术实现要素:
本发明的目的是提供一种用于抗急性脑缺血药物的制备方法,在脑梗后采用本发明注射液药物治疗效果较好,对离体脑血管有较好的舒张作用相符合,对降低血液粘稠度有一定作用,对缺氧的耐受性有非常显著的作用,对抗血小板聚集,防止血栓形成有非常显著的作用,对降低大鼠脑血管通透性有明显作用,能显著提高原代培养脑神经细胞的活力,对降低细胞凋亡有显著作用;本发明的目的还提供一种在制备治疗抗急性脑缺血药物中的应用;本发明的目的还提供一种抗急性脑缺血药物的检测设备。
为了达到上述目的,本发明有如下技术方案:
本发明的一种用于抗急性脑缺血药物的制备方法,有以下步骤:
1)将硫化钠0.11克—10.0克,氯化钠0.9克,注射用水100克,混合在一起,搅拌3—5分钟,存放2—3分钟;
2)按照注射小针剂规格,制成2毫升/支、5毫升/支、10毫升/支、20毫升/支或40毫升/支的注射液,放入西林瓶或安瓿中;所述药物配制后为无色或淡黄色澄明注射液;
3)流动蒸汽100℃,消毒30分钟;
4)所述药物检测杂质采用激光光源平行照射,通过计算机控制电机控制装置驱动注射液支撑台旋转,采用500万像素工业相机采集药物正反面图像,通过与工业相机连接的计算机对采集的杂质图像进行对照处理,存在直径大于15um的颗粒注射液为不合格,剔除。
本发明上述方法制得的药物在制备治疗抗急性脑缺血药物中的应用。
本发明的一种抗急性脑缺血药物的检测设备,包括:
电机控制装置、计算机、夹具、注射液支撑台、激光器、工业相机,所述夹具固定在注射液支撑台一侧,所述注射液放在注射液支撑台上,由夹具固定,所述计算机分别与电机控制装置、激光器、工业相机连接;
所述电机控制装置包括运动控制卡、x轴伺服电机、x轴伺服电机驱动器、x轴伺服电机编码器、y轴伺服电机、y轴伺服电机驱动器、y轴伺服电机编码器、z轴伺服电机、z轴伺服电机驱动器、z轴伺服电机编码器、旋转轴伺服电机、旋转轴伺服电机驱动器、旋转轴伺服电机编码器;
所述计算机还与运动控制卡连接,运动控制卡分别与x轴伺服电机驱动器、y轴伺服电机驱动器、z轴伺服电机驱动器、旋转轴伺服电机驱动器连接,x轴伺服电机驱动器分别与x轴伺服电机编码器、x轴伺服电机连接,y轴伺服电机驱动器分别与y轴伺服电机编码器、y轴伺服电机连接,z轴伺服电机驱动器分别与z轴伺服电机编码器、z轴伺服电机连接,旋转轴伺服电机驱动器分别与旋转轴伺服电机编码器、旋转轴伺服电机连接,x轴伺服电机、y轴伺服电机、z轴伺服电机分别通过涡轮蜗杆与注射液支撑台连接,旋转轴伺服电机通过螺杆旋转轴与注射液支撑台连接,所述x轴、y轴为平行于地面的轴向,且x轴与y轴垂直,所述z轴为垂直于地面的轴向。
其中,所述夹具包括升降螺杆、压板、固定框、固定螺栓,所述压板与升降螺杆垂直,压板用于压住注射液,使注射液固定,压板一端与升降螺杆连接,升降螺杆下部与固定框上的螺孔连接,固定框固定在注射液支撑台侧面,固定螺栓穿过固定框,固定螺栓能与升降螺杆接触,固定螺栓用于锁定升降螺杆。
本发明的优点在于:
在脑梗后采用本发明注射液药物治疗效果较好,对离体脑血管有较好的舒张作用相符合,对降低血液粘稠度有一定作用,对缺氧的耐受性有非常显著的作用,对抗血小板聚集,防止血栓形成有非常显著的作用,对降低大鼠脑血管通透性有明显作用,能显著提高原代培养脑神经细胞的活力,对降低细胞凋亡有显著作用。
本发明的一种抗急性脑缺血药物的检测设备,检测精度高,能保证药品的安全使用。
附图说明
图1为本发明药物与尼莫地平抗大鼠mcao的量效关系和效价强度比较示意图;
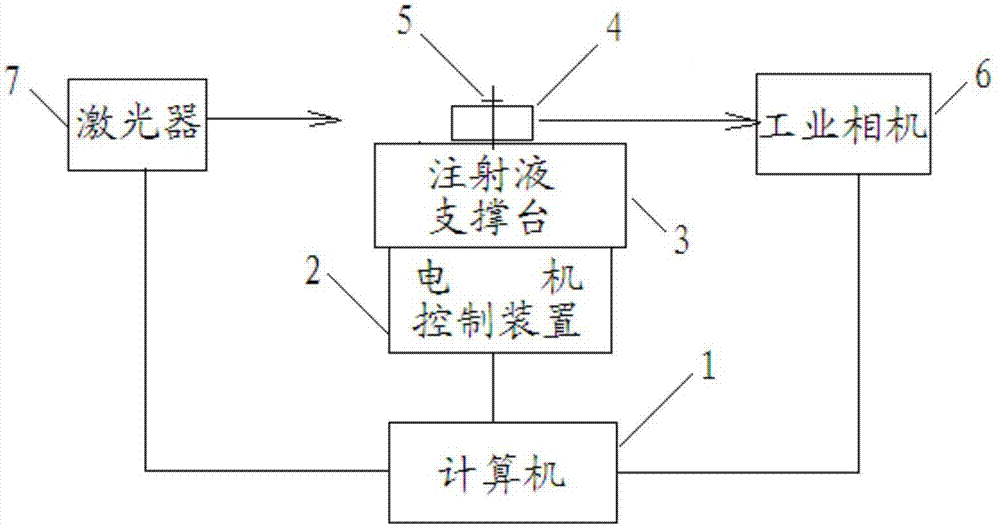
图2为本发明检测设备的整体结构的方框示意图;
图3为本发明检测设备电机控制装置的方框图示意图。
图中,1、计算机;2、电机控制装置;3、注射液支撑台;4、待检药物;5、夹具;6、工业相机;7、激光器。
具体实施方式
以下实施例用于说明本发明,但不用来限制本发明的范围。
实施例1:本发明的一种用于抗急性脑缺血药物的制备方法,有以下步骤:
1)将硫化钠0.11克,氯化钠0.9克,注射用水100克,混合在一起,搅拌3分钟,存放2分钟;
2)按照注射小针剂规格,制成2毫升/支、5毫升/支、10毫升/支、20毫升/支或40毫升/支的注射液,放入西林瓶或安瓿中;所述药物配制后为无色或淡黄色澄明注射液;
3)流动蒸汽100℃,消毒30分钟;
4)所述药物检测杂质采用激光光源平行照射,通过计算机控制电机控制装置驱动注射液支撑台旋转,采用500万像素工业相机采集药物正反面图像,通过与工业相机连接的计算机对采集的杂质图像进行对照处理,存在直径大于15um的颗粒注射液为不合格,剔除。
实施例2:本发明的一种用于抗急性脑缺血药物的制备方法,有以下步骤:
1)将硫化钠10.0克,氯化钠0.9克,注射用水100克,混合在一起,搅拌5分钟,存放3分钟;
2)按照注射小针剂规格,制成2毫升/支、5毫升/支、10毫升/支、20毫升/支或40毫升/支的注射液,放入西林瓶或安瓿中;所述药物配制后为无色或淡黄色澄明注射液;
3)流动蒸汽100℃,消毒30分钟;
4)所述药物检测杂质采用激光光源平行照射,通过计算机控制电机控制装置驱动注射液支撑台旋转,采用500万像素工业相机采集药物正反面图像,通过与工业相机连接的计算机对采集的杂质图像进行对照处理,存在直径大于15um的颗粒注射液为不合格,剔除。
实施例3:本发明的一种用于抗急性脑缺血药物的制备方法,有以下步骤:
1)将硫化钠5克,氯化钠0.9克,注射用水100克,混合在一起,搅拌4分钟,存放2.5分钟;
2)按照注射小针剂规格,制成2毫升/支、5毫升/支、10毫升/支、20毫升/支或40毫升/支的注射液,放入西林瓶或安瓿中;所述药物配制后为无色或淡黄色澄明注射液;
3)流动蒸汽100℃,消毒30分钟;
4)所述药物检测杂质采用激光光源平行照射,通过计算机控制电机控制装置驱动注射液支撑台旋转,采用500万像素工业相机采集药物正反面图像,通过与工业相机连接的计算机对采集的杂质图像进行对照处理,存在直径大于15um的颗粒注射液为不合格,剔除。
注射用水指符合中国药典注射用水项下规定的水。注射用水为蒸馏水或去离子水经蒸馏所得的水,故又称重蒸馏水。
本发明上述方法制得的药物在制备治疗抗急性脑缺血药物中的应用。
如图1、图2所示,本发明的一种抗急性脑缺血药物的检测设备,包括:
电机控制装置、计算机、夹具、注射液支撑台、激光器、工业相机,所述夹具固定在注射液支撑台一侧,所述注射液放在注射液支撑台上,由夹具固定,所述计算机分别与电机控制装置、激光器、工业相机连接;
运动控制卡、x轴伺服电机、x轴伺服电机驱动器、x轴伺服电机编码器、y轴伺服电机、y轴伺服电机驱动器、y轴伺服电机编码器、z轴伺服电机、z轴伺服电机驱动器、z轴伺服电机编码器、旋转轴伺服电机、旋转轴伺服电机驱动器、旋转轴伺服电机编码器;
所述计算机还与运动控制卡连接,运动控制卡分别与x轴伺服电机驱动器、y轴伺服电机驱动器、z轴伺服电机驱动器、旋转轴伺服电机驱动器连接,x轴伺服电机驱动器分别与x轴伺服电机编码器、x轴伺服电机连接,y轴伺服电机驱动器分别与y轴伺服电机编码器、y轴伺服电机连接,z轴伺服电机驱动器分别与z轴伺服电机编码器、z轴伺服电机连接,旋转轴伺服电机驱动器分别与旋转轴伺服电机编码器、旋转轴伺服电机连接,x轴伺服电机、y轴伺服电机、z轴伺服电机分别通过涡轮蜗杆与注射液支撑台连接,旋转轴伺服电机通过螺杆旋转轴与注射液支撑台连接,所述x轴、y轴为平行于地面的轴向,且x轴与y轴垂直,所述z轴为垂直于地面的轴向。
其中,所述夹具包括升降螺杆、压板、固定框、固定螺栓,所述压板与升降螺杆垂直,压板用于压住注射液,使注射液固定,压板一端与升降螺杆连接,升降螺杆下部与固定框上的螺孔连接,固定框固定在注射液支撑台侧面,固定螺栓穿过固定框,固定螺栓能与升降螺杆接触,固定螺栓用于锁定升降螺杆。
本发明的一种抗急性脑缺血药物的检测设备的控制方法,包括步骤:
1)将所述药物放置在注射液支撑台,通过夹具固定;通过计算机控制电机控制装置驱动注射液支撑台在x轴、y轴、z轴三个方向上移动调整,实现待检药物在激光器输出光轴和工业相机受光光轴上定位;
2)通过计算机控制电机控制装置驱动注射液支撑台旋转,通过计算机控制激光器出光,使激光器能在药物正反面照射;
3)通过通过计算机控制工业相机采集药物正反面图像,通过与工业相机连接的计算机对采集的杂质图像与计算机中已存储的标准图像进行对照比较,若存在大于15um的颗粒注射液则为不合格,剔除。
本发明激光器为半导体激光器。
工业相机:工业相机又俗称摄像机,相比于传统的民用相机(摄像机)而言,它具有高的图像稳定性、高传输能力和高抗干扰能力等,具体是基于ccd(chargecoupleddevice)芯片的相机。
ccd是目前机器视觉最为常用的图像传感器。它集光电转换及电荷存贮、电荷转移、信号读取于一体,是典型的固体成像器件。ccd的突出特点是以电荷作为信号,而不同于其它器件是以电流或者电压为信号。这类成像器件通过光电转换形成电荷包,而后在驱动脉冲的作用下转移、放大输出图像信号。典型的ccd相机由光学镜头、时序及同步信号发生器、垂直驱动器、模拟/数字信号处理电路组成。ccd作为一种功能器件,与真空管相比,具有无灼伤、无滞后、低电压工作、低功耗等优点。
本发明使用方法为:每次5-10毫升加入250-500毫升5%葡萄糖溶液中由静脉徐徐滴入,每日1次,10天为一疗程;本发明使用时对注射液中杂质要求高,即注射液中不能含有直径15um的颗粒物。
实验例:
实验例1.本发明注射液对大鼠急性脑缺血的影响
1.1.实验目的
了解本发明注射液静脉给药对大鼠急性脑缺血的治疗作用。
了解本发明注射液静脉给药抗急性脑缺血的剂量与效应的关系、时间与效应关系和药物的效价强度比较。
1.2.实验材料
1.2.1.受试药物
本发明制作方法实施例1所得注射液。
本发明制作方法所得注射液,无色透明状液体。
尼莫地平注射液:德国拜耳仙灵医药股份公司生产,规格:50ml:10mg,
批准文号:国药准字j20100002,产品批号:bxg2g01。
1.2.2.实验试剂
水合氯醛:国药集团化学试剂有限公司生产,规格:250g,生产批号:20120522。
2,3,5-三苯基氯化四氮唑(ttc):国药集团化学试剂有限公司生产,规格:10g/瓶,生产批号:20110715,临用前用磷酸缓冲液配制成0.5%的浓度。
多聚甲醛:国药集团化学试剂有限公司生产,规格:250g/瓶,生产批号:20111017。
0.9%氯化钠注射液:山东华鲁制药有限公司生产,规格:500ml,批准文号:
国药准字h37022749,生产批号:a13011703。
1.2.3.剂量设置及分组
1.2.3.1.量效关系实验剂量设置及分组
溶剂对照组:本发明溶媒20ml/kg;
受试药myns设:2.5mg/kg、5mg/kg、10mg/kg、20mg/kg、40mg/kg,共5个剂量组。
阳性对照药尼莫地平注射液设:25ug/kg、50ug/kg、100ug/kg、500ug/kg、1000ug/kg,共5个剂量组。
共计11组,每组动物数量n≧10只。
1.2.3.2.时效关系实验剂量设置及分组
通过量效关系实验发现,本发明药物抗急性脑缺血的中剂量为10mg/kg,因此,选用10mg/kg做为时效关系的给药剂量。
给药时间点预设急性脑缺血后0.5h、1h、2h、4h,如果急性脑缺血后4h给药仍有效,继续以每小时为单位延长,直至脑梗死面积与溶剂对照组接近为止,每个给药时间点分别设置溶剂对照组。
1.2.4.给药途径及给药容积
给药途径:恒速推注泵缓慢静脉给药,与临床拟用静脉滴注给药途径药相符合。药物使用时临时配制,给药容积为20ml/kg,给药时间为15min。给药次数为单次。
1.2.5.实验动物
品系:sd大鼠。级别:清洁级。性别:雄性。数量:190只。
动物生产许可证号:scxk(沪)2008-0016。
实验动物质量合格证编号:2008001628443、2008001629154、2008001630165、2008001648070、2008001648545、2008001648548。
体重:250g±20g。
来源:上海西普尔-必凯实验动物有限公司。
动物购回后在实验室分笼适应性饲养三天,用普通大鼠饲料喂养,自由饮水,光线12小时明暗自动转换,室内温度20-22℃。
1.2.6.实验仪器
图像分析软件:imagej,version1.41。
mcao栓线:北京沙东生物技术有限公司生产,产品号:2432-a4、2634-a4。栓线直径依大鼠体重决定,见附录1。
电子天平:上海舜宇恒平科学仪器有限公司制造,型号:fa/ja1003型
电热恒温水浴锅:常州金坛城西春兰实验仪器厂生产,型号:hh-1。
双道微量注射泵:浙江史密斯医学仪器有限公司,型号:wzs-50f6,注册号浙食药监械(准)字2007第2540156号(更),出厂编号:no:100504447。
聚乙烯管:pe10,内径0.3mm,外径0.5mm;pe50,内径0.58mm,外径0.96mm,法国biotrol公司。
手术剪,手术镊,手术线等常用手术器械。
1.3.实验方法
大鼠称重后用水合氯醛300mg/kg腹腔注射麻醉,麻醉后仰卧固定在手术台,颈部皮肤剪毛,75%乙醇消毒,手术暴露一侧颈静脉做颈静脉插管用于给药。分离另一侧颈总动脉并结扎颈总动脉近心端,沿颈总动脉上行分离颈外动脉,在颈总动脉的远心端放置动脉夹阻断血流,于动脉夹后方用眼科手术剪剪一个小口,插入一头呈圆球状的栓线(栓线根据大鼠体重进行选择,见附录1),缓缓推入栓线至大脑前动脉(深度约20mm)再往回拉约2mm即至大脑中动脉口,固定栓线,记录插线时间并开始给药,给药用恒速推注泵缓慢推注,药物配制按照等容积不等浓度的方法进行配制,给药容积20ml/kg,静脉给药时间15min。给药结束拔出静脉管,缝合皮肤。动脉栓线2h后抽出,大鼠放回笼中继续饲养。
术后24h对大鼠进行行为学评分。评分后断头处死大鼠,取出大脑,放入模具中切成7片。将脑片放入温度为37℃,浓度0.5%的ttc染液中,不时轻轻摇动,经约5min后正常脑组织被染成红色,坏死脑组织不着色。染色结束后把脑片放入4%多聚甲醛中浸约12小时取出,用数码相机为脑片拍照,用imagej软件对图像进行处理,计算每一片脑片的梗死面积并计算与正常脑组织面积的比例。
1.4.观察指标
本发明抗急性脑缺血的剂量与效应的关系。
本发明抗急性脑缺血的时间与效应的关系。
本发明抗急性脑缺血与尼莫地平注射液的效价强度比较。
急性脑缺血24小时后神经学行为评分。
zealonga5分制评分标准:0分:无神经损伤症状;1分:不能完全伸展对侧前爪;2分:向对侧转圈;3分:向对侧倾倒;4分:不能自发行走,意识丧失;5分:死亡。
1.5.统计处理
实验结果以均数±标准差(_x±s)表示,用spss18.0对组间进行统计分析,以p<0.05为具有统计学显著性差异标准。
1.6.实验结果
1.6.1.本发明实施例1所得注射液抗大鼠急性脑缺血的剂量与效应关系研究
本实验中,大鼠mcao后立即静脉给予相应受试药物。受试药本发明药物2.5mg/kg组(f=3.625,p=0.073)与溶剂对照组比较无统计学差异,随着受试药物剂量的增加,本发明药物5mg/kg(f=13.0,p=0.002)、10mg/kg(f=38.4,p=0.000)、20mg/kg(f=51.5,p=0.000)和40mg/kg(f=56.9,p=0.000),大鼠脑梗死面积也随之缩小,与溶剂对照组比较差异非常显著。
本发明药物剂量至20mg/kg时,脑梗死面积缩小到24.5%,在此基础上再增加受试药的剂量,脑梗死面积却没有相应缩小(表1-1),据此可以确定,本发明药物治疗大鼠急性脑缺血的低、中、高剂量分别为5mg/kg、10mg/kg和20mg/kg。
采用同样的方法对阳性药尼莫地平注射液也做了抗大鼠急性脑缺血的剂量与效应关系实验,以便于比较受试药的效价强度和药物的最大效应;与溶剂对照组比较,尼莫地平注射液25ug/kg(f=7.08,p=0.016)、50ug/kg(f=14.8,p=0.01)、100ug/kg(f=40.2,p=0.000)、500ug/kg(f=55.3,p=0.000)、1000ug/kg(f=62.1,p=0.000),差异非常显著(见表1-1)。
表1-1本发明实施例1所得注射液注射液液对大鼠急性脑缺血的影响(单位:脑梗死面积
*p<0.05,**p<0.01,***p<0.001vs溶剂对照组
1.6.2.本发明实施例1所得注射液抗大鼠急性脑缺血的效价强度比较
从表1-1可以看出,尼莫地平抗急性脑缺血的效价强度明显较本发明药物强,即在脑梗死面积接近的基础上,尼莫地平所使用的剂量显著低于本发明药物,但就抗急性脑缺血的药物最大效应,本发明药物略优于阳性对照药尼莫地平注射液。
1.6.3.本发明实施例1所得注射液抗大鼠急性脑缺血时间与效应的关系
为了解受试药治疗急性脑缺血的时间窗,大鼠在mcao后0.5h、1h、2h、和4h注射受试药物。结果发现,在mcao后2h注射本发明药物(f=8.82,p=0.008),仍能显著地缩小脑梗死面积;4h(f=0.112,p=0.741)后再给药对缩小脑梗死面积的作用低于2h以内的作用。因此,药物治疗急性脑梗死的最佳时间窗在2h以内。
表1-2本发明实施例1所得注射液抗大鼠急性脑缺血的时效关系研究(
**p<0.01,***p<0.001vs溶剂对照组
1.7.实验结论
1.7.1.本发明实施例1所得注射液静脉给药有非常显著的抗大鼠急性脑缺血的作用。
1.7.2.本发明实施例1所得注射液静脉给药抗大鼠急性脑缺血有很好的量效关系。
1.7.3.本发明实施例1所得注射液静脉给药抗大鼠急性脑缺血的最大药物效价优于阳性对照药尼莫地平注射液。
1.7.4.本发明实施例1所得注射液静脉给药抗大鼠急性脑缺血的时间窗在2h以内效果较好。
1.7.5.本发明实施例1所得注射液静脉给药适合大鼠实验的低中高剂量分别为5mg/kg、10mg/kg和20mg/kg。
实验例2.本发明实施例2注射液对beagle犬脑血流量的影响
2.1.实验目的
了解本发明注射液静脉给药对麻醉beagle犬脑血流量和脑血管阻力的影响。
2.2.实验材料
2.2.1.受试药物
本发明实施例2注射液。
尼莫地平注射液:德国拜耳仙灵医药股份公司生产,规格:50ml:10mg,
批准文号:国药准字j20100002,产品批号:bxg2g01。
2.2.2.实验试剂
戊巴比妥钠:德国merck生物技术公司生产,进口分装,规格:25g/瓶,生产批号:ws20130112。
肝素钠:国药集团化学试剂有限公司生产,规格:1g/瓶,技术条件符合q/cydz66-2012,生产批号:20130617。
2.2.3.剂量设置及分组
剂量设置如下:
溶剂对照组:本发明实施例2溶媒;阳性对照组:尼莫地平注射液:30ug/kg;
本发明实施例2注射液低剂量组:1.5mg/kg;本发明实施例2中剂量组:3mg/kg;
本发明实施例2注射液高剂量组:6mg/kg;
每组动物数量为6只。
2.2.4.给药途径及给药容积
给药途径为使用恒速推注泵缓慢静脉给药,相当于临床静脉滴注给药。给药容积1ml/kg。
2.2.5.实验动物
种属:健康beagle犬。来源:上海甲干生物科技有限公司。数量:30只。性别:雄雌兼用。体重:8~10kg。许可证:scxk(沪)2010-0028。
质量合格证编号:2010002800929。
2.2.6.实验仪器
powerlab数据采集分析系统:ad公司,型号:ml870/p型,产地:澳大利亚。
超声血流量仪:transonic公司,型号:t420型(美国),s系列精密血流探头ma4psb、ma6psb。
动物呼吸机:上海奥尔科特生物科技有限公司生产,型号:alc-v8型。
恒速推注泵:上海瑞曼rm-500i型单道注射泵。
2.3.实验方法
beagle犬用3%无巴比妥钠静脉注射麻醉,仰卧位固定,手术区域剃毛、消毒。用卵圆钳将舌头牵出口腔外以防舌后坠引起窒息。分离一侧股动脉插入导管记录血压,分离同侧股静脉插入导管用于静脉给药。将针状电极插入四肢皮下记录心电图。取颈部正中稍向上部位切开皮肤,分离右颈总动脉,沿颈总动脉向上分离,找到颈外动脉和颈内动脉的分叉处,结扎颈外动脉和其他小动脉分支,留颈内动脉。在胸骨上端切开皮肤,分离肌肉,找到气管,在气管的正下方摸到一个突起的骨性标志,即为第六颈椎,在第六颈椎的下外侧可以摸到骨缝,骨缝中可摸到有血管脉搏处即是椎动脉,小心将其剥离。将与血管直径匹配的流量探头分别挂在颈总动脉和椎动脉,涂抹耦合剂,连接超声血流量仪,将流量仪与powerlab连接,通过计算机实时显示血流量曲线。
系统连接好后稳定15min记录一次指标作为基础值,然后给药,记录给药后15、30、60、90、120min血压、一侧颈总动脉和椎动脉血流量的变化。记录结束后用气栓法处死动物,立即取脑称重。以右颈总动脉血流量+椎动脉流量乘以2代表全脑血流量(cbf)。
2.4.观察指标
记录指标:给药前后平均动脉压、心率、颈内动脉血流量和椎动脉血流量。计算指标:
脑血流量:
2.5.统计分析
实验结果以均数±标准差(_x±s)表示,用spss18.0对组内进行前后比较统计分析,以p<0.05为具有统计学显著性差异标准。
2.6.实验结果
2.6.1.对beagle犬心率和平均动脉压的影响
对心率的影响:溶剂对照组犬的心率在给药前到给药后120min内,心率稳定,平均心率在150次分左右;阳性药尼莫地平给药后60min内心率显著减慢,心率由给药前的168次/min,降到给药后15min的148次/min和30min的137次/min,和给药前比较心率减慢非常显著。而本发明实施例2的低、中、高三个剂量组在给药后各个时间点均不影响beagle犬的心率。
对血压的影响:给药后对血压影响最明显的是阳性对照药尼莫地平注射液,平均动脉压由给药前的127mmhg降低到给药后最低的86mmhg,血压降低作用非常明显,直到实验结束(给药后120min)血压仍明显低于给药前水平。从表3-2可以看出,本发明实施例2注射液静脉给药后,低、中、高三个剂量组的平均动脉压与给药前相比都非常稳定,说明本发明实施例2给药后对beagle犬的血压影响较小。
表2-1本发明实施例2注射液对beagle犬心率的影响(单位:次/min
*p<0.05,**p<0.01与给药前比较
表2-2本发明实施例2注射液对beagle犬平均动脉压的影响(单位:mmhg
*p<0.05,**p<0.01,***p<0.001与给药前比较
2.6.2.对beagle犬脑血流量的影响
给药前后比较,溶剂对照组犬的脑血流量随着时间延长而逐渐降低;阳性对照药尼莫地平注射液给药后犬的脑血流量增加显著;给予受试药本发明实施例2注射液低剂量,对增加犬的脑血流量作用并不明显,给予本发明实施例2注射液中剂量后犬的脑血流量增加,维持时间约60min,到实验结束时脑血流量又降低接近给药前水平;当给本发明实施例2注射液高剂量后,脑血流量的增加直到实验结束,一直处于较高水平,因此,可以看出本发明实施例2注射液不仅有增加麻醉beagle犬脑血流量的作用,而且有明显的量效关系存在。
表2-3本发明实施例2注射液对beagle犬脑血流量的影响(ml/min/100g脑组织
*p<0.05,**p<0.01与给药前比较
2.6.3.对beagle犬脑血管阻力的影响
用药前后比较,溶剂对照组犬由于有用药前后血压稳定但脑血流量随着时间延长而降低的现象,因此,其脑血管阻力也会在给药后随着时间延长而升高;对脑血管阻力降低最明显的是阳性对照药尼莫地平注射液,给药后脑血管阻力一直处于较低水平;而本发明实施例2低、中剂量组在给药后各个时间点脑血管阻力虽有降低,但降低水平没有达到统计学显著意义,只有高剂量组给药后脑血管阻力逐渐降低较为明显且与给药前比较降低相差显著。
表2-4本发明实施例2对beagle犬脑血管阻力的影响(mmhg﹒min﹒100g/ml,
*p<0.05,**p<0.01与给药前比较
2.7.实验结论
2.7.1.本发明实施例2注射液静脉给药不影响beagle犬的心率和平均动脉压。
2.7.2.本发明实施例2注射液静脉给药有增加麻醉beagle脑血流量的作用。
2.7.3.本发明实施例2注射液静脉给药可显著降低麻醉beagle犬的脑血管阻力。
实验例3.本发明注射液对急性脑缺氧的影响:
3.1.实验目的
了解本发明实施例3静脉给药是否能增加受试动物对急性缺氧的耐受性。
3.2.实验材料
3.2.1.受试药物
本发明实施例3注射液;
尼莫地平注射液:德国拜耳仙灵医药股份公司生产,规格:50ml:10mg,批准文号:国药准字j20100002,产品批号:bxg2g01。
3.2.2.实验试剂
0.9%氯化钠注射液:山东华鲁制药有限公司生产,批准文号:国药准字h37022749,生产批号:a13011703。
3.2.3.实验动物
实验涉及sd大鼠和icr小鼠两种动物,低压缺氧实验用icr小鼠,乏氧性缺氧用sd大鼠。
3.2.3.1.低压缺氧实验:
品系:icr小鼠级别:清洁级。
性别:雄性体重:18-20g。数量:60只。
来源:上海西普尔必凯实验动物有限公司。
生产许可证:scxk(沪)2008-0016。
动物治疗合格证编号:2008001631372。
3.2.3.2.乏氧性缺氧实验:
品系:sd大鼠。级别:清洁级。
性别:雄性。体重:200g。数量:50只。
来源:上海西普尔必凯实验动物有限公司。
生产许可证:scxk(沪)2008-0016,
动物治疗合格证编号:2008001632340。
动物购回后在本单位实验动物房分笼适应性饲养三天,用普通大鼠饲料喂养,自由饮水,光线12小时明暗自动转换,室内温度20-22℃。
3.2.4.剂量设置及分组
溶剂对照组:本发明实施例3溶媒;
阳性对照组:尼莫地平注射液,小鼠150ug/kg,大鼠100ug/kg。
sd大鼠本发明实施例3剂量分别为:5mg/kg;10mg/kg;20mg/kg共三个剂量组。
每组动物数量10只。
icr小鼠本发明实施例3剂量分别为:7.5mg/kg;15mg/kg;30mg/kg共三个剂量组。
每组动物数量12只。
3.2.5.给药途径及给药容积
尾静脉给药,给药时间为15min。给药次数为单次。给药容积:小鼠10ml/kg,大鼠20ml/kg。
3.3.实验方法
实验用小鼠和大鼠分别进行,小鼠低压缺氧实验是将小鼠放入250ml的广口瓶中,瓶中放置10g钠石灰以吸收水分和co2,瓶口涂抹凡士林以确保密封,将小鼠放入瓶中盖紧瓶盖开始计时,到呼吸停止而死亡,记录在密闭环境中存活的时间。
大鼠乏氧性缺氧实验是将大鼠放入自制的相对密闭的有机玻璃笼中,笼子的一端有一个进气口,另一端有一个出气口,从进气口持续向笼中充97%的氮气和3%氧气的混合气体,将大鼠放入笼中开始计时,记录大鼠从放入笼中到呼吸停止而死亡的时间。
3.4.观察指标
大鼠和小鼠在缺氧环境中的生存时间。
3.5.统计处理
实验结果以均数±标准差
3.6.实验结果
3.6.1.对小鼠在低压缺氧环境中生存时间的影响
溶剂对照组小鼠在密闭缺氧的环境中生存时间平均为41.2min;阳性对照组尼莫地平注射液(f=21.4,p=0.000)平均为52.2min,生存时间比溶剂对照组延长了26.7%,与溶剂对照组比较相差非常显著;本发明实施例3注射液能显著提高小鼠对缺氧的耐受能力,在缺氧的环境中,低剂量(f=6.63,p=0.017)、中剂量(f=15.2,p=0.001)和高剂量(f=15.4,p=0.001)三个组的小鼠生存时间与溶剂对照组比较,分别提高了15.6%、16.6%和24.7%,该结果表明本发明实施例3注射液可显著延长小鼠在缺氧环境中的存活时间,而且存活时间的延长在低、中、高剂量之间存在明显的量效关系。
表3-1本发明实施例3对小鼠急性缺氧时生存时间的影响
*p<0.05***p<0.001vs溶剂对照组
3.6.2.对大鼠在缺氧环境中生存时间的影响
大鼠耐缺氧试验在有气体流动的环境中进行,但氧气含量只有3%,其余的均为氮气,在该环境中溶剂对照组的大鼠平均生存时间只有6.24min,阳性对照组尼莫地平注射液(f=29.7,p=0.000)的大鼠平均生存时间为8.25min,与溶剂对照组比较生存时间延长了32.2%。受试品本发明实施例3注射液低剂量(f=1.40,p=0.253)和中剂量组(f=3.67,p=0.0.071)与溶剂对照组比较生存时间虽有延长,但没有统计学意义。但本发明实施例3高剂量组(f=11.8,p=0.003)的大鼠生存时间达到了7.43min,生存时间延长了19.0%,显著高于溶剂对照组。
表3-2本发明实施例3对大鼠急性缺氧时生存时间的影响
**p<0.01***p<0.001vs溶剂对照组
3.7.实验结论
3.7.1.本发明实施例3注射液可显著提高小鼠在低压缺氧环境中的生存时间。
3.7.2.本发明实施例3注射液高剂量可显著提高大鼠在乏氧性缺氧环境中的生存时间。
实验例4.本发明注射液对大鼠在体血栓形成的影响
4.1.实验目的
了解本发明实施例2注射液对血小板在生理条件下功能的影响。
4.2.实验材料
4.2.1.受试药物
本发明实施例2注射液,无色透明状液体。
阿司匹林:郑州晨旭化工产品有限公司生产,原料药,白色针状或板状结晶或粉末,在干燥空气中稳定,水溶性3.3g/l,使用时直接溶于生理盐水。生产批号:20120518。
4.2.2.实验试剂
0.9%氯化钠注射液:山东华鲁制药有限公司生产,批准文号:国药准字h37022749,生产批号:a13011703。
4.2.3.剂量设置及分组
溶剂对照组:本发明实施例2溶媒;
阳性对照组:阿司匹林,20mg/kg;
本发明实施例2注射液低剂量组:5mg/kg;
本发明实施例2注射液中剂量组:10mg/kg;
本发明实施例2注射液高剂量组:20mg/kg;
共5组,每组动物数量为10只。
4.2.4.给药途径和给药容积
给药途径为股静脉给药,符合临床现用静脉注射给药途径,给药容积为20ml/kg。给药时间为15min。给药次数为单次。
4.2.5.实验动物
品系:sd大鼠。级别:清洁级。
性别:雄性。数量:60只。
体重:200g±20g。
来源:上海西普尔必凯实验动物有限公司。
动物生产许可证号:scxk(沪)2008-0016。
实验动物质量合格证编号:2008001637729。
动物购回后在本单位实验动物房分笼适应性饲养三天,用普通大鼠饲料喂养,自由饮水,室内温度控制在20-22℃,光线12小时明暗自动转换。
4.2.5.仪器与材料
4号手术丝线:上海浦东金环医疗用品股份有限公司生产。
电子秤:上海良平仪器仪表有限公司生产,型号ja2003。
聚乙烯管:pe10,内径0.3mm,外径0.50mm,法国biotrol公司生产。
4.3.实验方法
实验前量取6cm长的4号手术丝线若干,修剪使丝线重量一致。
准备长约10cm的硅胶管,管内放置一根长6cm的4号手术丝线,硅胶管两端连接聚乙烯塑料管,结扎固定后向管内充满50u/ml肝素盐水,备用。
大鼠称重后用15%水合氯醛300mg/kg腹腔注射麻醉。仰卧位固定在鼠台,手术分离大鼠一侧股静脉,用于静脉插管给药。分离右侧颈总动脉和左侧颈外静脉,将充满肝素盐水的聚乙烯管两端分别插入右侧颈总动脉和左侧颈外静脉,打开动脉夹,血液从右颈总动脉流经管道返回左颈外静脉。开放15分钟后阻断血流,取出丝线称重,总重量减去丝线干重量即是血栓湿重。
4.4.观察指标
在体血栓重量。
4.5.统计处理
实验结果以均数±标准差(_x±s)表示,用spss18.0对组间进行统计分析,以p<0.05为具有统计学显著性差异标准。
4.6.实验结果
用导管将颈总动脉和颈静脉短路后,松开动脉夹,动脉血流经导管进入颈静脉,由于导管内固定有丝线,血液中的血小板会迅速附着在丝线上形成血栓,在单位时间内附着越多,血栓的重量就越重,如果药物有抗血小板聚集附着的作用,血栓的重量就会较轻。实验发现,血液经过动静脉短路流动15min后,溶剂对照组的血栓湿重平均为43.5mg,而阳性对照药阿司匹林组(f=66.9,p=0.000)丝线的重量平均为26.5mg,血栓重量降低39.1%,明显小于溶剂对照组。本发明实施例2注射液低中高三个剂量组也有非常好的抗血小板粘附作用,从表6-1可以看出,低剂量组血栓重量平均为40.5mg,随着本发明实施例2注射液剂量的增加,血栓的重量随之减轻,中(f=8.14,p=0.011)、高剂量组(f=33.8,p=0.000)的血栓平均湿重36.1mg和31.3mg,血栓重量分别降低17.0%、28.0%,与溶剂对照组比较差异非常显著,说明本发明实施例2有显著地抗血栓形成作用。
表4-1本发明实施例2注射液对大鼠在体血栓重量的影响
*p<0.05,***p<0.001vs溶剂对照组
4.7.实验结论
本发明实施例2注射液中、高剂量组有非常显著地抗大鼠在体血栓形成的作用。
实验例5.本发明注射液对大鼠脑血管通透性的影响
5.1.实验目的
了解本发明实施例1的注射液对大鼠脑血管通透性的影响。
5.2.实验材料
5.2.1.受试药物
发明实施例1的注射液,无色透明状液体,批号:130501。
尼莫地平注射液:德国拜耳仙灵医药股份公司生产,规格:50ml:10mg,
批准文号:国药准字j20100002,产品批号:bxg2g01。
5.2.2.实验试剂
甲酰胺:国药集团化学试剂有限公司生产,规格:500ml/瓶,生产批号:20130515。
0.9%氯化钠注射液:山东华鲁制药有限公司生产,批准文号:国药准字h37022749,生产批号:a13011703。
伊文思蓝:由国药集团化学试剂有限公司进口分装,批号:lotnow20100705,规格:10g/瓶。注射剂量:50mg/kg,使用时配制成5%的浓度。
5.2.3.剂量设置及分组
溶剂对照组:本发明实施例1的药物溶媒;
阳性对照组:尼莫地平,100ug/kg;
本发明实施例1的药物低剂量组:5mg/kg;
本发明实施例1的药物中剂量组:10mg/kg;
本发明实施例1的药物高剂量组:20mg/kg;
共5组,每组动物数量为10只。
5.2.4.给药途径及给药容积
股静脉给药,符合临床现用静脉注射给药途径,给药容积为20ml/kg。给药时间为15min。给药次数为单次。
5.2.5.实验动物
品系:sd大鼠。级别:清洁级。性别:雄性。数量:60只。体重:200g±20g。来源:上海西普尔必凯实验动物有限公司。
动物生产许可证号:scxk(沪)2008-0016。
实验动物质量合格证编号:2008001633403。
动物购回后在本单位实验动物房分笼适应性饲养三天,用普通大鼠饲料喂养,自由饮水,室内温度控制在20-22℃,光线12小时明暗自动转换。
5.2.6.仪器与材料
酶标仪:赛默飞世尔(上海)仪器有限公司,型号:multiskanmk3。
5.3.实验方法
大鼠给药1h后用15%水合氯醛300mg/kg腹腔注射麻醉,仰卧位固定,手术切开颈部皮肤分离暴露双侧颈总动脉。经舌下静脉注射伊文思蓝50mg/kg,5分钟后结扎双侧颈总动脉,3小时后断头处死动物,取出大脑,称重后按组别标号分别浸泡于装有10ml甲酰胺溶液的瓶中,在45℃恒温箱中温育72小时,脑组织中的伊文思蓝会浸出到甲酰胺溶液中,取色素液用酶标仪调整波长在492nm测定吸光度(od值),根据标准曲线计算出脑内伊文思蓝的含量,以ug/g脑湿重表示。
5.4.观察指标
每克脑组织中伊文思蓝含量
5.5.统计处理
实验结果以均数±标准差
5.6.实验结果
通过测定各组脑组织内浸出伊文思蓝的含量发现,溶剂对照组每克脑组织中伊文思蓝的含量为0.084ug;和溶剂对照组比较,在发明实施例1的注射液低中高三个剂量组中,伊文思蓝浸出量随着剂量的增加而减少,显示出各组之间有良好的量效关系存在;其中本发明实施例1的药物低剂量组(f=1.32,p=0.265)虽降低伊文思蓝浸出量,但与溶剂对照比较无统计意义;中剂量(f=5.07,p=0.037)和高剂量组(f=8.15,p=0.011)伊文思蓝的浸出量进一步减少,并显示出统计学差异,提示本发明实施例1的药物注射液对降低血管通透性有较好的作用。
表5-1发明实施例1的注射液对大鼠脑血管通透性的影响(
*p<0.05vs溶剂对照组
5.7.实验结论
发明实施例1的注射液静脉给药可显著降低大鼠脑血管的通透性,减少伊文思蓝从脑组织的浸出量。
缩略词表
如上所述,便可较为充分的实现本发明。以上所述仅为本发明的较为合理的实施实例,本发明的保护范围包括但并不局限于此,本领域的技术人员任何基于本发明技术方案上非实质性变性变更均包括在本发明包括范围之内。
- 还没有人留言评论。精彩留言会获得点赞!