一种采用氧化铁磷制备γ‑Fe2O3粉末的方法与流程
本发明涉及γ-Fe2O3制备技术,特别是一种采用氧化铁磷制备γ-Fe2O3粉末的方法。
背景技术:
铁氧化物是一种普遍存在于自然界并且在实验室条件下能容易获得的常见氧化物。铁和铁的氧化物能以7种晶相的形式存在,常见的铁氧化合物包括α-Fe2O3、γ-Fe2O3、Fe3O4、FeO,同时还有少量的以ε-Fe2O3和β-Fe2O3结晶系存在。磁铁氧化物具有奇异的特性广泛地应用于半导体、磁记录材料、增强磁共振成像对比度、组织修复、癌症的诊断和治疗、生物流体的解毒、电致变色器件、锂电池电极、药物载体以及光催化制氢等领域。
由于磁铁氧化中的γ-Fe2O3为尖晶石结构,具有磁性能和较高的化学稳定性,使得γ-Fe2O3作为磁性材料得以广泛的应用。
当前,γ-Fe2O3磁性材料制备方法已经成为材料科学领域的研究热点之一,并且科研人员已经研究出许多制备γ-Fe2O3磁性材料的方法,如氧化还原法、水热法、溶胶-凝胶法、离子交换法、共沉淀法等等。
现有技术中制备γ-Fe2O3的常用原料是γ-FeOOH和Fe3O4。即以γ-FeOOH为前驱体,然后经过加热获得γ-Fe2O3;另外,以Fe3O4为前驱体,通过控制氧化温度和气氛来制备γ-Fe2O3。
上述制备工艺中的关键是先获得γ-FeOOH或者Fe3O4前驱体,传统的过程是从溶液法出发,利用铁盐和沉淀剂通过控制反应过程的温度、pH值和时间等参数制备出上述γ-FeOOH前驱体。但是在其制备过程中损耗了大量的酸和碱,有时还会产生具有毒性的废液。如果制备的是Fe3O4前驱体,则还要经过还原氧化过程,在此过程中还额外的需要还原剂,造成能源的消耗。上述不仅制备过程复杂还容易造成能源消耗和环境污染。
轧钢铁鳞(又称氧化铁皮)是在钢铁材料锻造和热轧加工时,由于高温的钢铁和空气中的氧发生反应而产生的。虽然各钢铁企业在减少轧钢铁鳞的生产,提高成材率方面做了大量的工作,但是仍然约有1.3%的铁鳞产生。全国钢铁企业每年产生的氧化铁皮约1000万吨,铁鳞的主要成分为Fe2O3、Fe3O4、FeO,其经过氧化焙烧后形成氧化铁红,其主要成分为α-Fe2O3,其含量能达到99%(不同的钢种可能有差别)。按照传统的制备方法,若以氧化铁红为原料制备γ-Fe2O3,其必须经过还原先制取Fe3O4,然后在经过低温氧化得到γ-Fe2O3。其过程复杂并且对温度和制备环境有比较高的要求。
为此,亟需一种以氧化铁红为原料制备γ-Fe2O3粉末,且工艺简单,不对环境造成污染的方法。
技术实现要素:
针对现有技术中制备γ-Fe2O3粉末的缺陷,本发明的采用氧化铁磷制备γ-Fe2O3粉末的方法不需要经过还原先制备Fe3O4的过程,进而使得制备工艺简单,且不污染环境,同时充分利用轧钢铁磷氧化焙烧后的氧化铁红。
第一方面,本发明提供一种采用氧化铁红制备γ-Fe2O3粉末的方法,包括:
步骤A:以氧化铁红为制备原料,将其和熔盐按照预设配比均匀混合,得到混合后的反应物料;
步骤B:将反应物料在180-750℃温度下煅烧1-100h,得到煅烧后的中间物料;
步骤C:去除中间物料中未反应/未完全反应的熔盐,对去除熔盐的中间物料在180-750℃温度下热处理0.5-4h,冷却至室温,得到γ-Fe2O3粉末。
第二方面,本发明还提供一种采用氧化铁磷制备γ-Fe2O3粉末的方法,包括:
步骤一:收集轧钢铁磷在氧化焙烧后形成的氧化铁红,并去除杂质,得到制备原料;
步骤二:将制备原料和熔盐按照预设配比均匀混合,得到混合后的反应物料;
步骤三:将反应物料在180-750℃温度下煅烧1-100h,得到煅烧后的中间物料;
步骤四:去除中间物料中未反应/未完全反应的熔盐,对去除熔盐的中间物料在180-750℃温度下热处理0.5-4h,冷却至室温,得到γ-Fe2O3粉末。
进一步地,在步骤A或步骤二中,将制备原料和熔盐按照质量比1:(0.8-12)混合均匀。
进一步地,在步骤A或步骤二中,将制备原料和熔盐按照质量比1:(1-10)在混料罐中混合均匀,混匀时间为0.5-5h;
或者,
在步骤A或步骤二中,将制备原料和熔盐按照质量比1:(1-10)在球磨机中混合均匀,混匀时间为0.5-5h。
进一步地,所述熔盐为:KOH、NaOH、或二者的混合物。
进一步地,在步骤B或步骤三中,将反应物料放置在耐腐蚀的容器中,将该容器放置在马弗炉中煅烧2-72h,煅烧温度为200-600℃。
进一步地,在步骤C或步骤四中,采用清水在80-120℃温度下多次清洗中间物料并过滤,以去除中间物料中的熔盐;以及
将清洗过滤后的中间物料在70-90℃温度的真空干燥箱中烘干10-12h;
将烘干的中间物料在200-600℃温度下热处理0.5-4h。
进一步地,在步骤C或步骤四中,将烘干的中间物料放置在耐腐蚀的容器中,将该容器放置在马弗炉中在200-600℃温度下热处理0.5-3h。
进一步地,所述氧化铁红的主要成分是α-Fe2O3。
进一步地,所述马弗炉的升温速度为5-10℃/min。
本发明制备γ-Fe2O3粉末的方法,采用熔盐和氧化铁红混合均匀,并将混合均匀的反应物料煅烧,在煅烧后进行热处理,进而可得到γ-Fe2O3粉末,该方法省去了现有技术中还需要还原制备Fe3O4的过程,简化了γ-Fe2O3的制备工艺,同时充分利用了废弃的轧钢铁磷,达到节省能源消耗的目的。
附图说明
图1为本发明提供的γ-Fe2O3粉末的方法的流程示意图;
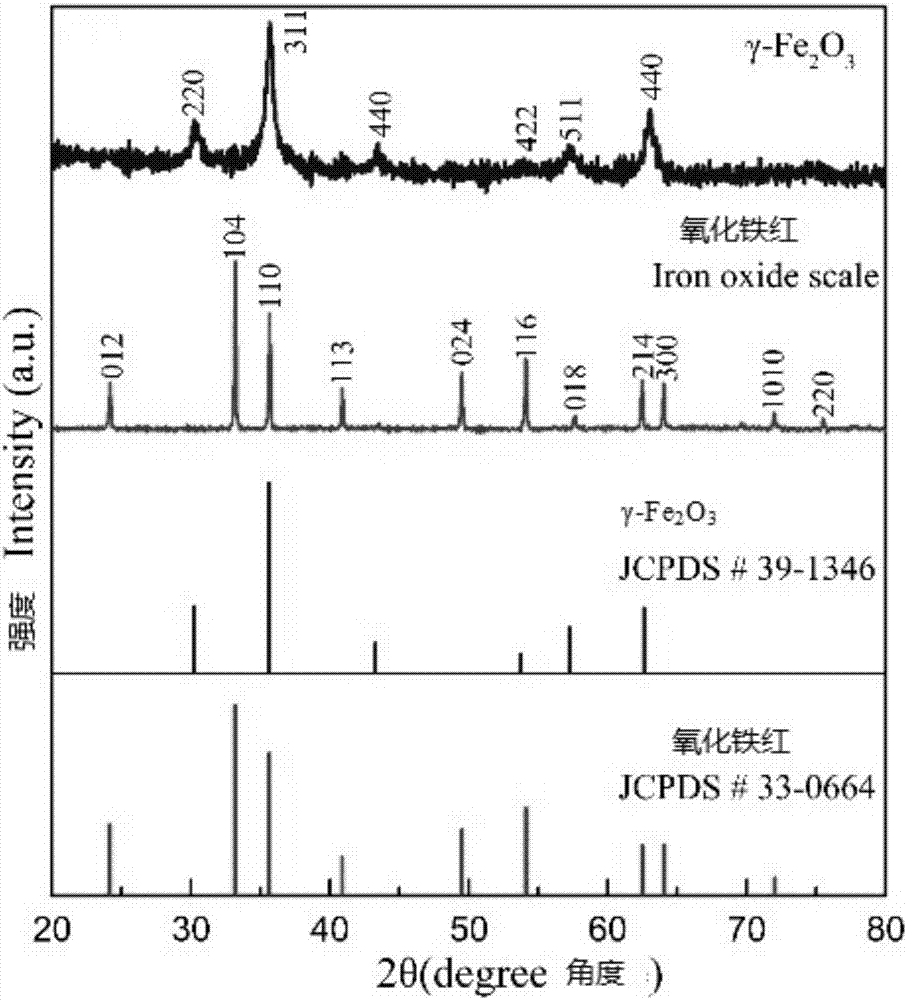
图2为本发明实施例二种氧化铁红和γ-Fe2O3粉末的X射线粉末衍射(XRD)图;
图3为本发明实施例二种氧化铁红和γ-Fe2O3粉末的傅里叶红外光谱的示意图;
图4为本发明实施例三中制备的γ-Fe2O3粉末的紫外漫反射光谱及其半导体禁带宽度的示意图;
图5为本发明实施例四中制备的γ-Fe2O3粉末在扫描电子显微镜(SEM)下的形貌示意图。
具体实施方式
为了更好的解释本发明,以便于理解,下面结合附图,通过具体实施方式,对本发明作详细描述。
实施例一
如图1所示,本实施例提供一种采用氧化铁磷制备γ-Fe2O3粉末的方法,该方法包括:
步骤01:收集轧钢铁磷在氧化焙烧后形成的氧化铁红,并去除杂质,得到制备原料。
本实施例中的氧化铁红的主要成分是α-Fe2O3。上述步骤中的制备原料通常可为粉末状的原料。若收集到的氧化铁红非粉末状结构,则可对其进行加工,以使其成为粉末状结构。
步骤02:将制备原料和熔盐按照预设配比均匀混合,得到混合后的反应物料。
另外,需要说明的是,本实施例还可以直接以氧化铁红为制备原料,将该氧化铁红和熔盐按照预设配比均匀混合。此时,可以省去上述的步骤01。上述步骤可根据实际需要调整,本实施例并不对其进行限定;
举例来说,可将制备原料和熔盐按照质量比1:(0.8-12)混合均匀。
进一步地,可将制备原料和熔盐按照质量比1:(1-10)在混料罐/球磨机中混合均匀,混匀时间为0.5-5h。上述制备原料和熔盐的质量比还可为2:8、3:9、4:8等。混匀时间还可为2-4h,或2.5-3h。
本实施例中的熔盐为KOH或NaOH;或者,熔盐为KOH和NaOH的混合物。
步骤03:将反应物料在180-750℃温度下煅烧1-100h,得到煅烧后的中间物料。
例如,在实验室的操作中,可以将反应物料放置在耐腐蚀的容器(如高纯的三氧化二铝坩埚)中,将该容器放置在马弗炉中煅烧2-72h,煅烧温度为200-600℃。
步骤04:去除中间物料中未反应/未完全反应的熔盐,对去除熔盐的中间物料在180-750℃温度下热处理0.5-4h,冷却至室温,得到γ-Fe2O3粉末。
举例来说:在步骤04中,采用清水在80-120℃温度下多次清洗中间物料并过滤,以去除中间物料中的熔盐;以及
将清洗过滤后的中间物料在70-90℃温度的真空干燥箱中烘干10-12h;
对烘干的中间物料在200-600℃温度下热处理0.5-4h。
在实验室中,可以采用去离子水在80-100℃下多次清洗中间物料并过滤,直至中间物料中的所有熔盐全部被清洗掉;
将清洗过滤后的中间物料在80℃温度的真空干燥箱中烘干12h,对烘干的中间物料放置在耐腐蚀的容器(如高纯的三氧化二铝坩埚)中,将该容器放置在马弗炉中在200-600℃温度下热处理0.5-3h。
上述马弗炉的升温速度为5-10℃/min。
本实施例的方法,采用熔盐和氧化铁红混合均匀,并将混合均匀的反应物料煅烧,在煅烧后进行热处理,进而可得到γ-Fe2O3粉末,该方法省去了现有技术中还需要还原制备Fe3O4的过程,简化了γ-Fe2O3的制备工艺,同时充分利用了废弃的轧钢铁磷,达到节省能源消耗的目的。
实施例二
本实施例的制备γ-Fe2O3粉末的方法中的制备原料为粉末状的氧化铁红,该氧化铁红的主要成分是α-Fe2O3。
步骤A01、将质量比为1:5的氧化铁红和NaOH在球磨机上混合0.5h,球磨机上的球磨介质为氧化锆球。
步骤A02、将上述混合均匀的反应物料置于高纯三氧化二铝坩埚中,将坩埚盖上盖并置于马弗炉中在400℃下进行煅烧5h,马弗炉的升温速度为10℃/min;保温结束后自然冷却到室温;
步骤A03、用80℃的去离子水多次清洗煅烧后的中间物料,并过滤,直到所得中间物料中的NaOH全部清洗掉,然后将清洗后的中间物料置于80℃的真空干燥箱内烘干12h;
步骤A04、干燥后的中间物料置于马弗炉中在300℃下热处理2h;冷却后所得的粉体。
步骤A05、利用X射线粉末衍射、光谱检测等表征手段对氧化铁红和冷却后的粉体进行表征分析。
图2为X射线粉末衍射图,由该图可知,冷却后的粉体中含有磁性材料γ-Fe2O3,其图谱和γ-Fe2O3的标准图谱(JCPDS#39-1346)相吻合。另外,结合图3的检测分析结果确定上述冷却后的粉体为γ-Fe2O3粉末。
实施例三
本实施例的制备γ-Fe2O3粉末的方法中的制备原料为粉末状的氧化铁红,该氧化铁红的主要成分是α-Fe2O3。
步骤B01、将氧化铁红和KOH(质量比为1:1),以氧化锆球为球磨介质,在球磨机上混合5h;
步骤B02、将混合均匀的反应物料置于高纯三氧化二铝坩埚中,将坩埚盖上盖并置于马弗炉中在600℃下进行煅烧2h,马弗炉的升温速度为8℃/min;保温结束后自然冷却到室温;
步骤B03、用100℃的去离子水多次清洗煅烧后的中间物料,并过滤,直到所得中间物料中的KOH全部清洗掉,然后将清洗后的中间物料置于80℃的真空干燥箱内烘干12h;
步骤B04、干燥后的中间物料置于马弗炉中在200℃下热处理3h;冷却后所得的粉体;
步骤B05、对冷却后的粉体进行光谱检测,如图4所示,检测分析结果确定上述冷却后的粉体即为γ-Fe2O3粉末,图4中示出的是γ-Fe2O3粉末的紫外漫反射光谱及其半导体禁带宽度(如图4中嵌套的方框)。
实施例四
本实施例的制备γ-Fe2O3粉末的方法中的制备原料为粉末状的氧化铁红,该氧化铁红的主要成分是α-Fe2O3。
步骤C01、将氧化铁红和(NaOH+KOH)混合熔盐,以氧化锆球为球磨介质,在球磨机上混合3h;
氧化铁红和混合熔盐的质量比为1:10。
步骤C02、将上述混合均匀的反应物料置于高纯三氧化二铝坩埚中,将坩埚盖上盖并置于马弗炉中在200℃下进行煅烧72h,马弗炉的升温速度为5℃/min;保温结束后自然冷却到室温;
步骤C03、用120℃的去离子水多次清洗并过滤煅烧后的中间物料,直到所得中间物料中的NaOH和KOH全部清洗掉,然后将清洗后的中间物料置于80℃的真空干燥箱内烘干12h;
步骤C04、干燥后的中间物料置于马弗炉中在600℃下热处理0.5h;冷却后所得的粉体即为γ-Fe2O3粉末,如图5所示的粉末结构。
图5为本发明的方法制备的γ-Fe2O3粉末的扫描电子显微镜图,由此图可知,该方法得到的γ-Fe2O3是均匀的球形颗粒,粒径在200nm左右。
最后应说明的是:以上所述的各实施例仅用于说明本发明的技术方案,而非对其限制;尽管参照前述实施例对本发明进行了详细的说明,本领域的普通技术人员应当理解:其依然可以对前述实施例所记载的技术方案进行修改,或者对其中部分或全部技术特征进行等同替换;而这些修改或替换,并不使相应技术方案的本质脱离本发明各实施例技术方案的范围。
- 还没有人留言评论。精彩留言会获得点赞!