一种可溶性重组蛋白及其制备方法和用途与流程
本发明属生物技术领域,涉及一种可溶性重组蛋白。具体涉及一种通过基因工程表达的可溶性重组蛋白M1型Kunin型多肽(M1type Kunin polypeptide,M1KP)及其制备方法和在制备治疗子宫内膜异位症疾病的药物中的用途
背景技术:
现有技术公开了子宫内膜异位症(endometriosis,EMs)是指具有生长能力的子宫内膜腺体和间质出现在子宫腔以外的部位,该疾患虽为良性病变,但实践显示,其具有类似恶性肿瘤的行为,表现为侵袭、种植及“远处”播散、复发等。据统计,在中国,因EMs而接受手术的患者占1/4的妇科手术总量。研究显示EMs是导致育龄期妇女痛经、慢性盆腔痛以及不孕的重要原因之一,且与痛经的严重程度密切相关,因此,严重影响了妇女的生活质量,增加了社会的经济负担,成为当今危害妇女身心健康的一种重要疾病。因其发病机制目前尚不明确,导致临床治疗面临巨大的困难与挑战。目前,临床治疗实践中多采用手术去除病灶和/或抗雌激素类药物干预等治疗方案,上述干预措施虽然有助于改善病情、缓解症状,但均存在如激素类药物疗效短且副作用明显,手术费用及耽误工作所产生经济损失高昂,但最终仍难以避免再次复发的缺陷,等等。因此,深入地探讨EMs的发病机制以及寻找特异有效的干预治疗方案是该疾患的治疗、研究中尚待解决的问题。其中,研发疗效显著,副作用更少更弱的新的药物是目前本领域关于EMs治疗、研究的重要课题之一,尤其是阐明其发病机制,寻求新的治疗靶点,缓解疼痛,提高生育能力,改善患者生活质量,乃至最终治愈EMs这一特殊疾病将具有重要临床和现实意义。
研究显示,P-选择素(P-selectin,granular membrane protein 140,CD62p)是血小板活化依赖性颗粒表面膜蛋白(platelet activation dependent granule external membrane protein,PADGEM),为一种分子量为140K D的膜糖蛋白,其定位于血小板的α颗粒和内皮细胞棒管状(Weibel一Palade)小体内,是血小板活化 的表面标志;P-选择素可以可溶性形式存在于血浆中,该可溶性P-选择素主要来源于血管内皮细胞,其由789个氨基酸残基构成:N末端730个氨基酸构成胞外区,C末端24个氨基酸组成跨膜区,35个氨基酸组成胞浆短尾,胞外区有一个凝集素样区(lectin like domain)、一个表皮生长因子样区(epidermal growth factor-like domain)和九个补体调节蛋白重复单位(complement regulatory protein consensus repeat units);在受到组织胺、凝血酶、佛波酯和钙离子载体的刺激后,其迅速在质膜上表达,缺氧/再氧化或氧自由基也可诱导表达,其高亲和力的配体是P-选择素糖蛋白配体1(P-selectin glycoprotein ligand 1,PSGL-1),主要表达于中性粒细胞和单核细胞,因此,P-选择素主要介导粒细胞和单核细胞在内皮细胞表面的滚动及血小板黏附,在炎症反应中介导炎症细胞向受损部位趋化及肿瘤生长转移过程中起重要作用。
迄今,尚未见有关P-选择素蛋白治疗子宫内膜异位症的报道。
基于目前临床治疗子宫内膜异位症的现状,结合P-选择素蛋白的特性,本申请的发明人拟提供一种新的有效的治疗子宫内膜异位症的药物,且毒副作用小,安全可靠。
技术实现要素:
本发明的目的是针对目前临床治疗子宫内膜异位症存在的问题,提供一种新的有效的治疗子宫内膜异位症的药物,尤其是一种治疗内异症的非激素类药物,该药物疗效显著,耐受性好,毒副作用小,安全可靠,能改善患者疼痛,提高患者生育能力及生活质量,以及节约社会医疗资源及成本。
本发明提供了一种可溶性重组P-选择素蛋白(又称M1型Kunin型多肽,M1type Kunin polypeptide,M1KP),及其在制备治疗子宫内膜异位症药物中的用途。
本发明中,通过下述方法制备可溶性P-Selectin蛋白,
采用基因工程方法,用E.coli(DH5α)制备P-selectin目的DNA质粒,然后与表达载体重组,转化相应的表达细胞,筛选高表达工程菌或工程细胞;工程菌或工程细胞经扩增,收集表达相,应用分离纯化方法获得高纯度可溶性P-Selectin蛋白。
更具体的,本发明的可溶性重组P-选择素蛋白通过下述方法制备:
1,可溶性P-Selectin蛋白的表达
采用基因工程手段,用E.coli(DH5α)制备P-selectin目的DNA的质粒,载体(vector)带G418抗生素行抗药性筛选:
以Dg44CHO cell line(Chinese hamster ovary cell line,)为真核工具细胞株,所述质粒转染该细胞株,MTX 1uM(Sigma,St Louis,MO,USA)刺激细胞株表达P-selectin-Fc,选择表达量最高的克隆进行筛选鉴定,获得稳定的高表达的细胞株;
2,获得的细胞于75cm2的培养瓶中传代扩增,收集CHO cell培养上清,获得可溶性分泌型蛋白P-selectin-Fc tag;
3,可溶性P-Selectin蛋白的吸附洗脱
将上述细胞培养上清过蛋白吸附凝胶(protein A beads,Adar Biotech,Rehovot,Israel)柱,该吸附凝胶柱可吸附人/鼠等大多数种类的免疫球蛋白;基于本发明获得的P-selectin-Fc是一种带有Fc tag(标记)的蛋白,而且所述的Fc是人丙种球蛋白的重链,因此,过蛋白吸附凝胶(protein A beads)柱时其可被凝胶吸附;
用蛋白洗脱缓冲液(protein elution buffer)从柱子上洗脱蛋白;PBS透析过夜,去除蛋白洗脱缓冲液(上述实验均在4℃冷房中进行);
获得的蛋白液用紫外分光光度计测定OD值,初步估计蛋白量;蛋白液置入蛋白专用浓缩离心管(50mL,Vivaspin Turbo 15,Sartorius,Germany)在4℃3,000r.p.m.离心15分钟进行蛋白液浓缩;
4.,可溶性P-Selectin蛋白的鉴定
取少量蛋白液进行考马斯亮蓝染色(Brilliant Blue R Staining solution,Sigma),以及Western Blot鉴定,鉴定结果表明,所述的可溶性P-Selectin蛋白为分子量为140K D的P-选择素蛋白(如图1所述);
5.去除内毒素
按照Detoxi-Gel使用说明书步骤,将蛋白液滤过内毒素吸附柱子(Detoxi-Gel Endotoxin Removing Gel column,Thermo Scientific,Rockford,IL,USA),去除内毒素;使用内毒素测试棒(Limulus amebocyte lysate(LAL)PYROTELL endotoxin positive control reagent,Single TestVial(0.2ml/vial),Associates ofCape Cod,East Falmouth,MA,USA)行内毒素测试过关试验检测过关后;BCA法(Pierce,Thermo Scientific,Rockford,IL,USA)进行蛋白浓度定量测定,确定为P-选择素蛋白(如图1所述),分装后-80℃冻存,备体内应用。
以上技术方案中所有基本分子生物学操作均可参照《分子克隆实验指南》。
本发明通过基因工程方法表达制备可溶性重组P-选择素蛋白,并进行体内用于干预内异症模型小鼠实验,结果表明,制得的可溶性重组P-选择素蛋白能通过竞争性拮抗血小板,封闭P-选择素结合位点(主要是P-选择素glycoprotein ligand 1,PSGL-1)的作用,达到抑制血小板在内异症病灶聚集的作用,且能明显缩小内异症病灶大小,缓解热痛觉过敏[Guo,submitted for publication]。
进一步,本发明制得的可溶性P-selectin蛋白可用于制备治疗子宫内膜异位症的药物。
本发明的可溶性P-selectin蛋白毒副作用小,耐受性好,安全有效,极有潜力成为新的内异症干预措施。将有效提高患者生育能力及生活质量,大量节约社会医疗资源及成本,并产生巨大的社会经济效益。本发明对解析内异症的发病机理,探求更为安全有效的治疗药物具有重要意义。
附图说明
图1是本发明制得的可溶性P-Selectin蛋白(P-选择素蛋白),其分子量为140K D。
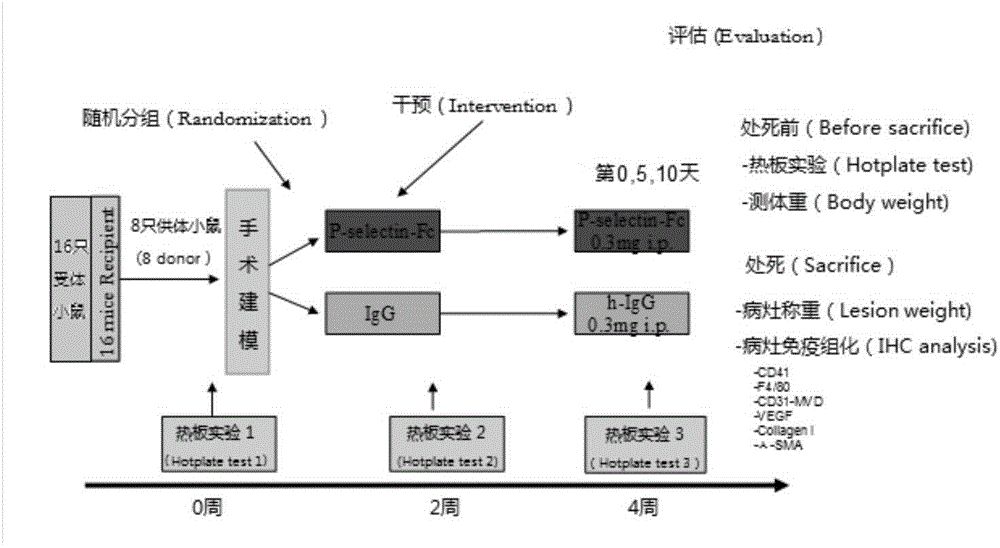
图2显示了进行体内实验采用的技术路线。
图3.C57bl手术模型小鼠腹壁内异症样病灶。
图4显示应用可溶性P-selectin-Fc蛋白治疗,p-sel-Fc组比IgG组热痛觉过敏得到明显改善(P<0.01),病灶明显缩小(P<0.01)。
图5.显示p-sel-Fc组与IgG组CD41、F4/80、VEGF、CD31-MVD、p-p65(p-NF-kB)、PCNA、COX-2、collagen I和α-SMA代表性免疫组化染色图。
图6显示p-sel-Fc组与IgG组代表性Masson染色图,其中分别显示了不同染色的胶原纤维和肌性纤维。
具体实施方式
实施例1制备可溶性P-Selectin蛋白
采用基因工程方法,用E.coli(DH5α)制备P-selectin目的DNA质粒,然后与表达载体重组,转化相应的表达细胞,筛选高表达工程菌或工程细胞;工程菌或工程细胞经扩增,收集表达相,应用分离纯化方法获得高纯度可溶性P-Selectin蛋白;其包括下述步骤:
1,可溶性P-Selectin蛋白的表达
采用基因工程手段,用E.coli(DH5α)制备P-selectin目的DNA的质粒,载体(vector)带G418抗生素行抗药性筛选:
以Dg44CHO cell line(Chinese hamster ovary cell line,)为真核工具细胞株,所述质粒转染该细胞株,MTX 1uM(Sigma,St Louis,MO,USA)刺激细胞株表达P-selectin-Fc,选择表达量最高的克隆进行筛选鉴定,获得稳定的高表达的细胞株;
2,获得的细胞于75cm2的培养瓶中传代扩增,收集CHO cell培养上清,获得可溶性分泌型蛋白P-selectin-Fc tag;
3,可溶性P-Selectin蛋白的吸附洗脱
将上述细胞培养上清过蛋白吸附凝胶(protein A beads,Adar Biotech,Rehovot,Israel)柱,该吸附凝胶柱可吸附人/鼠等大多数种类的免疫球蛋白;基于本发明获得的P-selectin-Fc是一种带有Fc tag(标记)的蛋白,而且所述的Fc是人丙种球蛋白的重链,因此,过蛋白吸附凝胶(protein A beads)柱时其可被凝胶吸附;
用蛋白洗脱缓冲液(protein elution buffer)从柱子上洗脱蛋白;PBS透析过夜,去除蛋白洗脱缓冲液(上述实验均在4℃冷房中进行);
获得的蛋白液用紫外分光光度计测定OD值,初步估计蛋白量;蛋白液置入蛋白专用浓缩离心管(50mL,Vivaspin Turbo 15,Sartorius,Germany)在4℃3,000r.p.m.离心15分钟进行蛋白液浓缩;
4.,可溶性P-Selectin蛋白的鉴定
取少量蛋白液进行考马斯亮蓝染色(Brilliant Blue R Staining solution, Sigma),以及Western Blot鉴定,鉴定结果表明,所述的可溶性P-Selectin蛋白为分子量为140K D的P-选择素蛋白(如图1所述);
5.去除内毒素
按照Detoxi-Gel使用说明书步骤,将蛋白液滤过内毒素吸附柱子(Detoxi-Gel Endotoxin Removing Gel column,Thermo Scientific,Rockford,IL,USA),去除内毒素;使用内毒素测试棒(Limulus amebocyte lysate(LAL)PYROTELL endotoxin positive control reagent,Single TestVial(0.2ml/vial),Associates ofCape Cod,East Falmouth,MA,USA)行内毒素测试过关试验检测过关后;BCA法(Pierce,Thermo Scientific,Rockford,IL,USA)进行蛋白浓度定量测定,确定为P-选择素蛋白(如图1所述),分装后-80℃冻存,备体内应用。
实施例2体内实验
建立C57bl/WT小鼠内异症模型,研究可溶性P-选择素蛋白干预治疗对痛觉及病灶的影响。
本实验基于如下机理:出血是组织损伤的标志,而子宫内膜异位症是一个出血性疾病;异位内膜和在位内膜一样,随月经周期也会发生周期性出血、脱落和组织修复,而参与伤口愈合的一个重要角色,且首先到达损伤组织局部的则是血小板,血小板不仅在止血中起着关键的作用,而且在募集免疫细胞参与组织修复、愈合伤口中起着重要的作用;本发明在确定子宫内膜异位症病灶是一个反复损伤、出血、愈合、修复的伤口,伤口愈合过程主要包括3个阶段:止血、炎症反应以及组织重建的基础上,经动物模型实验证实:异位内膜病灶明显存在血小板聚集,活化血小板可上调子宫内膜异位间质细胞VEGF,COX-2,MMP-9,Bcl-2的表达,且促进异位间质细胞增殖;血小板借助伤口愈合的固有机制,释放大量趋化因子、细胞因子及各种生长因子,募集炎症细胞,促进炎症反应,增强病灶血管新生,促进病灶生长、组织纤维化,进而促进疾病发展[Ding and Guo,submitted for publication];而体内破坏外周血血小板或应用奥扎格雷抗血小板治疗均可抑制模型小鼠病灶生长,并改善痛觉过敏[Ding and Guo,submitted for publication]。
采用如图2所示的技术路线,进行体内实验:
1)建立动物模型:
常规用水合氯醛(0.4mg/g/只)腹腔注射麻醉动物,5%酒精消毒腹部,开腹分离,结扎,取得子宫,无菌生理盐水漂洗后,制成组织块,用7-0带针缝线分别将组织块连接在腹壁四个象限腹膜上,关腹,术中给予青霉素钠15000U肌注预防感染,手术时起给予苯甲酸雌二醇3ug/只肌注,每周2次,共2周;
2)热板实验
在无风、恒温环境中,将热板温度设置为55。C,快速、轻柔的将小鼠置于热板上,观察小鼠反应,以舔后足、剧烈扇动后足或跳跃为阳性反应。记录反应出现的时间,作为热板痛阈时间(hotplate latency,HPL),分别于手术建模前、建模2周治疗前以及治疗2周处死前对小鼠进行热板实验,
3)分组处理
(1)可溶性P-Selectin蛋白输注组(p-sel-Fc组):human P-selectin-Fc(h P-sel-Fc)0.3mg/只,腹腔注射,建模2周开始第0,5,10天;
(2)对照IgG组(IgG组):人丙种球蛋白0.3mg/只,腹腔注射,建模2周开始第0,5,10天;
4免疫组化染色
1)开腹提取各组病灶,记录测量大小,病灶行石蜡切片,免疫组化检测病灶
CD41、F4/80、CD163、VEGF、CD31(MVD)、PCNA、p-NF-kB、COX-2、collagen I、fibronectin、α-SMA;
2)免疫组化染色评分标准
读片,显微镜下随机选择5个视野,i.p.p.软件扫描获得各视野平均光密度值并再取平均值;
病灶的石蜡切片行Masson染色。
本发明的可溶性P-选择素蛋白体内干预试验结果显示:手术建立内异症模型成功,所有小鼠开腹后,均可见其腹壁上有2~4个囊泡样病灶,如图3所示,
可溶性P-selectin蛋白能治疗,改善内异症模型小鼠热痛觉过敏并抑制病灶生长,结果显示:可溶性P-selectin-Fc蛋白治疗组(p-sel-Fc组)与人丙种球蛋白对照抗体组(IgG组)在手术建模2周后,热痛觉耐受时间均有明显下降且差异没有统计学意义,而应用可溶性P-selectin-Fc蛋白治疗2周后,与对照抗体组 相比,模型小鼠热痛觉过敏得到明显改善(P<0.01),差异具有统计学意义,可溶性P-selectin-Fc蛋白治疗组可明显抑制病灶生长,与对照抗体组相比病灶平均缩小59.4%(P<0.01),差异具有统计学意义(如图4所示)。
可溶性P-选择素治疗可降低病灶CD41、F4/80、VEGF、CD31-MVD、p-p65(p-NF-kB)、PCNA、COX-2、collagen I和α-SMA的表达,降低病灶纤维化;
可溶性P-选择素治疗组CD41、F4/80、VEGF、CD31-MVD、p-p65(p-NF-kB)、PCNA、COX-2、collagen I和α-SMA均明显低于对照抗体组(如图5所示),并减少病灶中胶原纤维(Masson染色呈蓝色)的含量(如图6所示)(P均<0.01);结果表明,拮抗血小板,封闭P-选择素结合位点(主要是P-选择素glycoprotein ligand 1,PSGL-1)的作用,从而达到抑制血小板在内异症病灶聚集的作用,可以减少炎症细胞如巨噬细胞等在病灶的浸润,减轻病灶炎症反应,减少血管生成及细胞增殖,并且减轻病灶纤维化。
- 还没有人留言评论。精彩留言会获得点赞!