水凝胶、用于制备水凝胶的组合物及水凝胶制备方法与流程
本发明涉及一种医疗材料,尤其涉及一种水凝胶。本发明进一步提供一种用于制备水凝胶的组合物。本发明还进一步涉及水凝胶的制备。
背景技术:
凝胶一般包括成胶组分和分散介质,其中该成胶组分形成三维结构,以允许分散介质,如水,分散分布在该成胶组分形成的三维结构。水凝胶因其良好的亲水性,生物相容性以及三维结构保持性,被广泛应用在多个领域。水凝胶的这些特性其在生物医学材料领域具有独有的优势和具有巨大的发展空间。它优异的生物相容性使其在组织工程领域得到广泛应用,如用于人造皮肤、人造血管、人工角膜、隐形眼镜、人工关节以及各种人造脏器和药物缓释载体等。此外,基于甲基丙烯酸羟乙酯(HEMA)制成的水凝胶由于其内部存在的氢键作用,使其具有较高的机械性能。因此,甲基丙烯酸羟乙酯类水凝胶因其较好的生物相容性和机械性能,而被广泛应用于接触镜材料,人造血管以及其他组织工程方面。然而,甲基丙烯酸羟乙酯水凝胶具有含水率低(一般不高于50%)、透氧性能差、抗蛋白吸附能力低(20%)、透明度不高、模量损耗高导致皮肤触觉差、耐磨性和润滑度不够等缺点,这些缺点限制了甲基丙烯酸羟乙酯水凝胶在生物医用材料领域的广泛应用。
技术实现要素:
本发明的主要目的在于其提供一种用于制备水凝胶(材料)的组合物,其中该组合物的主要组成成分是甲基丙烯酸羟乙酯,其中该甲基丙烯酸羟乙酯的结构式为:
本发明的另一目的在于其提供一种用于制备高性能水凝胶的组合物,其中该组合物进一步包括甜菜碱衍生物,如磺酸基甜菜碱(SBMA)和/或羧酸基甜菜碱(CBMA),其中该甜菜碱衍生物具有以下结构式:
本发明的另一目的在于其提供一种用于制备高性能水凝胶(材料)的组合物,其中由含有该组合物制成的水凝胶具有高含水率和良好生物相容性。
本发明的另一目的在于其提供一种用于制备高性能水凝胶(材料)的组合物,其中由含有该组合物制成的水凝胶具有良好抗菌抗蛋白吸附效果。
本发明的另一目的在于其提供一种用于制备高性能水凝胶(材料)的组合物,其中由含有该组合物制成的水凝胶具有良好透氧性的水凝胶(材料)。
本发明的另一目的在于其提供一种用于制备高性能水凝胶(材料)的组合物,其中由含有该组合物制成的水凝胶在具有较高的含水率的同时,具有良好的柔韧性和较高的光滑度。
本发明的另一目的在于其提供一种用于制备高性能水凝胶(材料)的组合物,其中由含有该组合物制成的水凝胶的成胶组分为甲基丙烯酸羟乙酯,辅助组分为甜菜碱衍生物。
本发明的另一目的在于其提供一种用于制备高性能水凝胶(材料)的组合物,其中该组合物包括甲基丙烯酸羟乙酯-甜菜碱衍生物,其中该甜菜碱衍生物可以是磺酸基甜菜碱(SBMA)和/或羧酸基甜菜碱(CBMA)。
本发明进一步提供一种用于制备高性能水凝胶(材料)的组合物,其中由该组合物包括甲基丙烯酸羟乙酯和甜菜碱衍生物,其中该甜菜碱衍生物是磺酸基甜菜碱和/或羧酸基甜菜碱,其中在该组合物中,甲基丙烯酸羟乙酯与甜菜碱衍生物的质量比为0.875/1至14/1。
本发明进一步提供一种用于制备高性能水凝胶(材料)的组合物,其中由该组合物进一步包括交联剂和引发剂,其中在该组合物中,交联剂的质量分数为0.01%-1%,引发剂的质量分数为0.1%-1%。
本发明进一步提供一种用于制备高性能水凝胶(材料)的组合物,其中由含有该组合物制成的水凝胶水凝胶(材料)的价格低廉,和当使用该组合物制造水凝胶时,其制造工艺简单和不需要精密的仪器和复杂的结构,制造成本低。
本发明进一步提供一种适于用作生物医学材料的水凝胶,其中该水凝胶包括成胶组分、辅助组分和分散介质,其中该成胶组分包括甲基丙烯酸羟乙酯,该辅助组分包括甜菜碱衍生物,该水凝胶的分散介质是水,其中该甜菜碱衍生物是磺酸基甜菜碱和/或羧酸基 甜菜碱,其中在该水凝胶中,甲基丙烯酸羟乙酯的质量分数为2.33%至56%,该甜菜碱衍生物的质量分数为2.67%至32%。
本发明进一步提供一种适于用作生物工程材料的水凝胶,其中在该水凝胶中,甲基丙烯酸羟乙酯的质量分数为2.33%至56%,该甜菜碱衍生物的质量分数为2.67%至32%。优选地,在该水凝胶中,甲基丙烯酸羟乙酯的含量为2.33%至45%(质量分数),甜菜碱衍生物(SBMA)的含量不大于25%(质量分数)。
本发明进一步提供一种适于用作生物工程材料的水凝胶,其中该水凝胶,进一步包括引发剂,其中在该水凝胶中,该引发剂的质量分数为0.04%-0.4%,其中该引发剂为2,4,6-三甲基苯甲酰基二苯基氧化膦、(2-羟基-4′-(2-羟乙氧基)-2-甲基苯丙酮或偶氮二异丁腈或过氧化苯甲酰。
本发明进一步提供一种用于制造水凝胶的方法,其中使用本发明制造方法和本发明组合物制得的水凝胶中,甲基丙烯酸羟乙酯的质量分数为2.33%至56%,该甜菜碱衍生物的质量分数为2.67%至32%。优选地,在该水凝胶中,甲基丙烯酸羟乙酯的含量为2.33%至-45%(质量分数),甜菜碱衍生物(SBMA)的含量不大于25%(质量分数)。
本发明的其它目的和特点通过下述的详细说明得以充分体现并可通过所附权利要求中特地指出的手段和装置的组合得以实现。
依本发明,能够实现前述目的和其他目的和优势的本发明水凝胶包括成胶组分、辅助组分和分散介质,其中该成胶组分包括甲基丙烯酸羟乙酯,该辅助组分包括甜菜碱衍生物,该水凝胶的分散介质是水,其中该甜菜碱衍生物是磺酸基甜菜碱和/或羧酸基甜菜碱,其中在该水凝胶中,甲基丙烯酸羟乙酯的质量分数为2.33%至56%,该甜菜碱衍生物的质量分数为2.67%至32%。
本发明进一步提供一种水凝胶制备方法,其包括以下步骤:
(A)去离子水溶解成胶组分、辅助组分、交联剂和热引发剂,并充分混合,以得到反应混合物,其中该成胶组分为甲基丙烯酸羟乙酯(HEMA),该辅助组分为[2-(甲基丙烯酰基氧基)乙基]二甲基-(3-磺酸丙基)氢氧化铵(SBMA)和/或羧酸基甜菜碱(CBMA);
(B)利用惰性气体或氮气去除该反应混合物中的氧气;
(C)加热该反应混合物,使该反应混合物的温度被升高到该热引发剂需要被引发的温度,并保温至该热引发剂被完全引发,以制备得到水凝胶;和
(D)去离子水洗涤水凝胶。
本发明还进一步提供一种水凝胶制备方法,其包括以下步骤:
(A)去离子水溶解成胶组分、辅助组分、交联剂和光引发剂,并充分混合,以得到反应混合物,其中该成胶组分为甲基丙烯酸羟乙酯(HEMA),该辅助组分为[2-(甲基丙烯酰基氧基)乙基]二甲基-(3-磺酸丙基)氢氧化铵(SBMA)和/或羧酸基甜菜碱(CBMA);和
(B)紫外光照射反应该混合物直至该光引发剂被完全引发。
因此,如上所述,本发明水凝胶(材料)具有下述有益效果中的至少其中之一:
1、本发明用于制造水凝胶的组合物制备得到的水凝胶(材料)具有较高含水率(含水率最高可达95%);
2、本发明用于制造水凝胶的组合物制备得到的水凝胶(材料)具有良好生物相容性;
3、本发明用于制造水凝胶的组合物制备得到的水凝胶(材料)具有良好透氧性;
4、本发明用于制造水凝胶的组合物制备得到的水凝胶(材料)具有良好抗菌抗蛋白吸附(不大于10%)效果;
5、本发明用于制造水凝胶的组合物制备得到的水凝胶(材料)具有良好的柔韧性和较高的光滑度;
6、本发明用于制造水凝胶的组合物制备得到的水凝胶(材料)具有更好的透光率(不低于95%)。
通过对随后的描述和附图的理解,本发明进一步的目的和优势将得以充分体现。
本发明的这些和其它目的、特点和优势,通过下述的详细说明,附图和权利要求得以充分体现。
附图说明
图1为依本发明较佳实施例的水凝胶正视图。
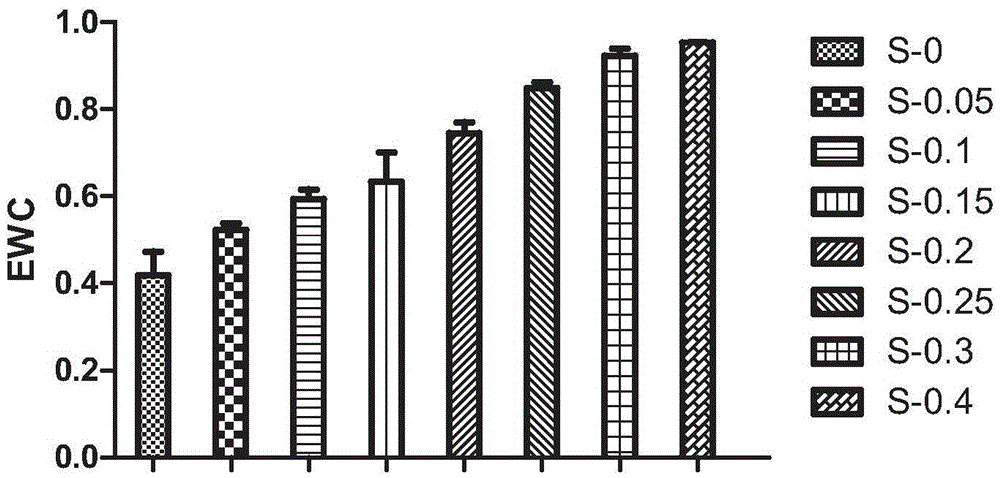
图2为依本发明较佳实施例的水凝胶的含水率变化示意图,其中根据该图所示,随着本发明水凝胶中甜菜碱衍生物含量的增加,其含水率也随之增加。
图3为依本发明较佳实施例的水凝胶的失水曲线图,其中根据该图所示,随着本发明水凝胶中甜菜碱衍生物含量的增加,在相同的环境下,经同样的失水时间,其最终含水率也随之增加。
图4为依本发明较佳实施例的水凝胶的失水曲线图,其中根据该图所示,随着本发明水凝胶中甜菜碱衍生物含量的增加,其透光率从20%左右提高到90%左右。
图5为依本发明较佳实施例的水凝胶的G″变化图,该图显示的是随着振动应力的变化,材料的储能模量和损耗模量的变化。
图6为依本发明较佳实施例的水凝胶的抗蛋白质吸附能力变化图,其中根据该图所示,随着本发明水凝胶中甜菜碱衍生物含量的增加,其抗蛋白质吸附能力得到提高。
图7为依本发明较佳实施例的水凝胶的抗菌吸附能力变化图,复合水凝胶均具有良好的抗菌吸附能力。
图8为依本发明较佳实施例的水凝胶制造方法。图9为依本发明较佳实施例的另一种水凝胶制造方法。
具体实施方式
下述描述被揭露以使本领域技术人员可制造和使用本发明。下述描述中提供的较佳实施例仅作为对本领域技术人员显而易见的示例和修改,其并不构成对本发明范围的限制。下述描述中所定义的一般原理可不背离本发明精神和发明范围地应用于其它实施例、可选替代、修改、等同实施和应用。
本发明提供一种用于制造水凝胶的组合物,其包括用于制造水凝胶的成胶组分和改善水凝胶性质的辅助组分,其中该组合物包括甲基丙烯酸羟乙酯,该辅助组分包括甜菜碱衍生物,其中甲基丙烯酸羟乙酯具有以下结构式:
该甜菜碱衍生物具有以下结构式:
优选地,甜菜碱衍生物为磺酸基甜菜碱(SBMA)和/或羧酸基甜菜碱(CBMA),如上述结构式所示。
本发明用于制造水凝胶的组合物可单独作为水凝胶制备的有效成分(包括成胶组分和辅助组分)与交联剂、引发剂等用于水凝胶的制备,或和交联剂、引发剂等以及一种或多种其他适用于制造水凝胶的化合物或组合物组合使用,以用于水凝胶的制备。
本发明还进一步提供一种水凝胶,其中该水凝胶的成胶组分为甲基丙烯酸羟乙酯(HEMA),该辅助组分为[2-(甲基丙烯酰基氧基)乙基]二甲基-(3-磺酸丙基)氢氧化铵(SBMA)和/或羧酸基甜菜碱(CBMA),分散介质是水,其中该水凝胶中的成胶组分和辅助组分的质量和占水凝胶总质量的百分比为5%-60%。
优选地,该水凝胶的交联剂具有以下分子结构式:
其中该交联剂的分子量不小于300,不大于20000。
更优选地,该水凝胶的交联剂为聚乙二醇二甲基丙烯酸酯。可以理解的是,本发明所使用的交联剂也可以是其它本领域技术人员所熟知的交联剂。
优选地,该水凝胶的引发剂为光引发剂,其中该光引发剂为2,4,6-三甲基苯甲酰基二苯基氧化膦(TPO)、(2-羟基-4′-(2-羟乙氧基)-2-甲基苯丙酮(Irgacure2959)或其它本领域技术人员所熟知的光引发剂。
可选地,该水凝胶的引发剂为热引发剂,其中该热引发剂为偶氮二异丁腈(ABIN)、过氧化苯甲酰(BPO)或其它本领域技术人员所熟知的热引发剂。
如附图之图8所示,本发明还进一步提供一种水凝胶制备方法,其包括以下步骤:
(A)去离子水溶解成胶组分、辅助组分、交联剂和热引发剂,并充分混合,以得到反应混合物,其中该成胶组分为甲基丙烯酸羟乙酯(HEMA),该辅助组分为[2-(甲基丙烯酰基氧基)乙基]二甲基-(3-磺酸丙基)氢氧化铵(SBMA)和/或羧酸基甜菜碱(CBMA);
(B)利用惰性气体或氮气去除该反应混合物中的氧气;
(C)加热该反应混合物,使该反应混合物的温度被升高到该热引发剂需要被引发的温度,并保温至该热引发剂被完全引发,以制备得到水凝胶;和
(D)去离子水洗涤水凝胶。
其中,该水凝胶的交联剂具有以下分子结构式:
其中该交联剂的分子量不小于300,不大于20000。
一般地,该反应混合物的热反应时间不高于1小时。优选地,该反应混合物中,甲 基丙烯酸羟乙酯(HEMA)的质量分数为20%-45%,[2-(甲基丙烯酰基氧基)乙基]二甲基-(3-磺酸丙基)氢氧化铵(SBMA)的质量分数为0-25%,交联剂的质量分数为0.01%-1%,热引发剂的质量分数为0.1%-1%。
更优选地,该反应混合物中,交联剂与成胶组分的摩尔比为1:1000至1:100;热引发剂与成胶组分和交联剂的总量的质量比为1:1000至5:1000。
最优选地,热引发剂与成胶组分和交联剂的总量的质量比为1:1000至3:1000。
本领域技术人员可以理解,步骤(D)在对步骤(C)制得的水凝胶进行清洗时,水凝胶将会进一步吸水溶胀。因此,在步骤(C)制得的水凝胶被放入去离子水洗涤之前,水凝胶中的含水量一般较低。在步骤(D)之后,也就是将步骤(C)制得的水凝胶放入去离子水洗涤之后,步骤(C)制得的水凝胶将会吸水膨胀,从而使制得的水凝胶最终产品的水凝胶的含水量最高可达95%。
如附图之图9所示,本发明还进一步提供一种水凝胶制备方法,其包括以下步骤:
(A)去离子水溶解成胶组分、辅助组分、交联剂和光引发剂,并充分混合,以得到反应混合物,其中该成胶组分为甲基丙烯酸羟乙酯(HEMA),该辅助组分为[2-(甲基丙烯酰基氧基)乙基]二甲基-(3-磺酸丙基)氢氧化铵(SBMA)和/或羧酸基甜菜碱(CBMA);
(B)紫外光照射反应该混合物直至该光引发剂需要被引发的温度并维持该温度至该光引发剂被完全引发;和
(C)去离子水洗涤水凝胶。
其中,该水凝胶的交联剂具有以下分子结构式:
其中该交联剂的分子量不小于300,不大于20000。
一般地,该紫外线的波长为300nm-415nm,优选波长为365nm。
一般地,该反应混合物的光反应时间为25min至60min。
优选地,该反应混合物中,甲基丙烯酸羟乙酯(HEMA)的质量分数为20%-45%,[2-(甲基丙烯酰基氧基)乙基]二甲基-(3-磺酸丙基)氢氧化铵(SBMA)的质量分数为0-25%,交联剂的质量分数为0.01%-1%,光引发剂的质量分数为0.1%-1%。
更优选地,该反应混合物中,交联剂与成胶组分的摩尔比为1:1000至1:100;热引发剂与成胶组分和交联剂的总量的质量比为1:1000至5:100。
最优选地,热引发剂与成胶组分和交联剂的总量的质量比为1:1000至3:1000。
值得注意的是,本文中的交联剂可以是聚乙二醇二甲基丙烯酸酯,热引发剂可以是 偶氮二异丁腈(ABIN)或过氧化苯甲酰(BPO),光引发剂可以是2,4,6-三甲基苯甲酰基二苯基氧化膦(TPO)或(2-羟基-4′-(2-羟乙氧基)-2-甲基苯丙酮(Irgacure2959)。
本领域技术人员可以理解,步骤(C)在对步骤(B)制得的水凝胶进行清洗时,水凝胶将会进一步吸水溶胀。因此,在步骤(B)制得的水凝胶被放入去离子水洗涤之前,水凝胶中的含水量一般较低。在步骤(C)之后,也就是将步骤(B)制得的水凝胶放入去离子水洗涤之后,步骤(B)制得的水凝胶将会吸水膨胀,从而使制得的水凝胶最终产品的水凝胶的含水量最高可达95%。
示例1:水凝胶制备
在室温(优选25℃)条件下,取0.75mL甲基丙烯酸羟乙酯(HEMA),加入1mL超声20min后的去离子水,混合均匀,然后加入0.75uL交联剂(聚乙二醇二甲基丙烯酸酯,分子量330)和7.5mg光引发剂(2-羟基-4′-(2-羟乙氧基)-2-甲基苯丙酮,Irgacure2959),均匀混合后,得到反应混合物。随后,将含HEMA、交联剂和引发剂的溶液(反应混合物)注入密闭模具,紫外灯照射1h,引发自由基聚合和制备水凝胶。随后,将模具和水凝胶一同放入去离子水中,每隔12h换一次水,记录脱胶时间,脱胶后用去离子水反复冲洗并浸泡5天,得到如图1所示的HEMA水凝胶。
示例2:水凝胶制备
在室温(优选25℃)条件下,取0.05g的[2-(甲基丙烯酰基氧基)乙基]二甲基-(3-磺酸丙基)氢氧化铵(SBMA),加入1mL超声20min后的去离子水,充分溶解。然后加入0.7mL甲基丙烯酸羟乙酯(HEMA),混合均匀,然后加入0.75uL交联剂(聚乙二醇二甲基丙烯酸酯,分子量330)和7.5mg光引发剂(2-羟基-4′-(2-羟乙氧基)-2-甲基苯丙酮,Irgacure2959),均匀混合后,得到反应混合物。随后,将含有SBMA、HEMA、交联剂和引发剂的溶液(反应混合物)注入密闭模具,紫外灯照射1h,引发自由基聚合和制备水凝胶。随后,将模具和水凝胶一同放入去离子水中,每隔12h换一次水,记录脱胶时间,脱胶后用去离子水反复冲洗并浸泡5天,得到的水凝胶中的HEMA与SBMA的质量比为0.70:0.05。
示例3:水凝胶制备
在室温(优选25℃)条件下,取0.1g的[2-(甲基丙烯酰基氧基)乙基]二甲基-(3-磺酸丙基)氢氧化铵(SBMA),加入1mL超声20min后的去离子水,充分溶解。然后加入0.65mL甲基丙烯酸羟乙酯(HEMA),混合均匀,然后加入0.75uL交联剂(聚乙二醇二甲基丙烯酸酯,分子量550)和7.5mg光引发剂(2-羟基-4′-(2-羟乙氧基)-2-甲基苯丙酮, Irgacure2959),均匀混合后,得到反应混合物。随后,将含有SBMA、HEMA、交联剂和引发剂的溶液(反应混合物)注入密闭模具,紫外灯照射1h,引发自由基聚合和制备水凝胶。随后,将模具和水凝胶一同放入去离子水中,每隔12h换一次水,记录脱胶时间,脱胶后用去离子水反复冲洗并浸泡5天,得到的水凝胶中的HEMA与SBMA的质量比为0.65:0.10。
示例4:水凝胶制备
在室温(优选25℃)条件下,取0.15g的[2-(甲基丙烯酰基氧基)乙基]二甲基-(3-磺酸丙基)氢氧化铵(SBMA),加入1mL超声20min后的去离子水,充分溶解。然后加入0.6mL的甲基丙烯酸羟乙酯(HEMA),混合均匀,然后加入0.75uL交联剂(聚乙二醇二甲基丙烯酸酯,分子量1000)和7.5mg光引发剂(2-羟基-4′-(2-羟乙氧基)-2-甲基苯丙酮,Irgacure2959),均匀混合后,得到反应混合物。随后,将含有SBMA、HEMA、交联剂和引发剂的溶液(反应混合物)注入密闭模具,紫外灯照射1h,引发自由基聚合和制备水凝胶。随后,将模具和水凝胶一同放入去离子水中,每隔12h换一次水,记录脱胶时间,脱胶后用去离子水反复冲洗并浸泡5天,得到的水凝胶中的HEMA与SBMA的质量比为0.60:0.15。
示例5:水凝胶制备
在室温(优选25℃)条件下,取0.2g的[2-(甲基丙烯酰基氧基)乙基]二甲基-(3-磺酸丙基)氢氧化铵(SBMA),加入1mL超声20min后的去离子水,充分溶解。然后加入0.55mL的甲基丙烯酸羟乙酯(HEMA),混合均匀,然后加入0.75uL交联剂(聚乙二醇二甲基丙烯酸酯,分子量20000)和7.5mg光引发剂(2-羟基-4′-(2-羟乙氧基)-2-甲基苯丙酮,Irgacure2959),均匀混合后,得到反应混合物。随后,将含有SBMA、HEMA、交联剂和引发剂的溶液(反应混合物)注入密闭模具,紫外灯照射1h,引发自由基聚合和制备水凝胶。随后,将模具和水凝胶一同放入去离子水中,每隔12h换一次水,记录脱胶时间,脱胶后用去离子水反复冲洗并浸泡5天,得到的水凝胶中的HEMA与SBMA的质量比为0.55:0.20。
示例6:水凝胶制备
在室温(优选25℃)条件下,取0.25g的[2-(甲基丙烯酰基氧基)乙基]二甲基-(3-磺酸丙基)氢氧化铵(SBMA),加入1mL超声20min后的去离子水,充分溶解。然后加入0.5mL的甲基丙烯酸羟乙酯(HEMA),混合均匀,然后加入0.75uL交联剂(聚乙二醇二甲基丙烯酸酯,分子量330)和7.5mg光引发剂(2-羟基-4′-(2-羟乙氧基)-2-甲基苯丙酮, Irgacure2959),均匀混合后,得到反应混合物。随后,将含有SBMA、HEMA、交联剂和引发剂的溶液(反应混合物)注入密闭模具,紫外灯照射1h,引发自由基聚合和制备水凝胶。随后,将模具和水凝胶一同放入去离子水中,每隔12h换一次水,记录脱胶时间,脱胶后用去离子水反复冲洗并浸泡5天,得到的水凝胶中的HEMA与SBMA的质量比为0.50:0.25。
示例7:水凝胶制备
在室温(优选25℃)条件下,取0.3g的[2-(甲基丙烯酰基氧基)乙基]二甲基-(3-磺酸丙基)氢氧化铵(SBMA),加入1mL的去离子水,充分溶解。然后加入0.45mL的甲基丙烯酸羟乙酯(HEMA),混合均匀,然后加入0.75uL交联剂(聚乙二醇二甲基丙烯酸酯,分子量330)和7.5mg光引发剂(2-羟基-4′-(2-羟乙氧基)-2-甲基苯丙酮,Irgacure2959),均匀混合后,得到反应混合物。随后,将含有SBMA、HEMA、交联剂和引发剂的溶液(反应混合物)注入密闭模具,紫外灯照射1h,引发自由基聚合和制备水凝胶。随后,将模具和水凝胶一同放入去离子水中,每隔12h换一次水,记录脱胶时间,脱胶后用去离子水反复冲洗并浸泡5天,得到水凝胶中的HEMA与SBMA的质量比为0.45:0.30。
示例8:水凝胶制备
在室温(优选25℃)条件下,取0.4g的[2-(甲基丙烯酰基氧基)乙基]二甲基-(3-磺酸丙基)氢氧化铵(SBMA),加入1mL超声20min后的去离子水,充分溶解。然后加入0.35mL的甲基丙烯酸羟乙酯(HEMA),混合均匀,然后加入0.75uL交联剂(聚乙二醇二甲基丙烯酸酯,分子量330)和7.5mg光引发剂(2-羟基-4′-(2-羟乙氧基)-2-甲基苯丙酮,Irgacure2959),均匀混合后,得到反应混合物。随后,将含有SBMA、HEMA、交联剂和引发剂的溶液(反应混合物)注入密闭模具,紫外灯照射1h,引发自由基聚合和制备水凝胶。随后,将模具和水凝胶一同放入去离子水中,每隔12h换一次水,记录脱胶时间,脱胶后用去离子水反复冲洗并浸泡5天,得到的水凝胶中的HEMA与SBMA的质量比为0.35:0.40。
示例9:水凝胶制备
在室温(优选25℃)条件下,取0.1g的[2-(甲基丙烯酰基氧基)乙基]二甲基-(3-磺酸丙基)氢氧化铵(SBMA),加入1mL水,充分溶解然后加入0.65mL甲基丙烯酸羟乙酯(HEMA),混合均匀,然后加入0.75uL交联剂(聚乙二醇二甲基丙烯酸酯,分子量330)和7.5mg光引发剂2,4,6-三甲基苯甲酰基二苯基氧化膦(TPO),均匀混合后,得到反应混合物。随后,将含有SBMA、HEMA、交联剂和引发剂的溶液(反应混合物)注入密闭 模具,紫外灯照射1h,引发自由基聚合和制备水凝胶。随后,将模具和水凝胶一同放入去离子水中,每隔12h换一次水,记录脱胶时间,脱胶后用去离子水反复冲洗并浸泡5天,得到的水凝胶中的HEMA与SBMA的质量比为0.65:0.10。
示例10:水凝胶制备
在室温(优选25℃)条件下,取0.1g的[2-(甲基丙烯酰基氧基)乙基]二甲基-(3-磺酸丙基)氢氧化铵(SBMA),加入1mL超声20min后的去离子水,充分溶解。然后加入0.65mL甲基丙烯酸羟乙酯(HEMA),混合均匀,然后加入0.75uL交联剂(聚乙二醇二甲基丙烯酸酯,分子量550)和7.5mg热引发剂AIBN,均匀混合后,得到反应混合物。随后,以氮气提前除去反应混合物中的氧。再随后,将含有SBMA、HEMA、交联剂和引发剂的溶液(反应混合物)注入密闭模具,室温下反应30-60分钟,引发自由基聚合和制备水凝胶。随后,将模具和水凝胶一同放入去离子水中,每隔12h换一次水,记录脱胶时间,脱胶后用去离子水反复冲洗并浸泡5天,得到的水凝胶中的HEMA与SBMA的质量比为0.65:0.10。
示例11:水凝胶制备
在室温(优选25℃)条件下,取0.1g的[2-(甲基丙烯酰基氧基)乙基]二甲基-(3-磺酸丙基)氢氧化铵(SBMA),加入1mL超声20min后的去离子水,充分溶解。然后加入0.65mL的聚乙二醇甲基丙烯酸甲酯(PEGDMA),混合均匀,然后加入0.75uL交联剂(聚乙二醇二甲基丙烯酸酯,分子量330)和7.5mg光引发剂(2-羟基-4′-(2-羟乙氧基)-2-甲基苯丙酮,Irgacure2959),均匀混合后,得到反应混合物。随后,将含有SBMA、HEMA、交联剂和引发剂的溶液(反应混合物)注入密闭模具,紫外灯照射1h,引发自由基聚合和制备水凝胶。随后,将模具和水凝胶一同放入去离子水中,每隔12h换一次水,记录脱胶时间,脱胶后用去离子水反复冲洗并浸泡5天,得到的水凝胶中的HEMA与SBMA的质量比为0.65:0.10。
示例12:水凝胶制备
在室温(优选25℃)条件下,取0.1g的羧基甜菜碱(CBMA),加入1mL超声20min后的去离子水,充分溶解。然后加入0.65mL甲基丙烯酸羟乙酯(HEMA),混合均匀,然后加入0.75uL交联剂(聚乙二醇二甲基丙烯酸酯,分子量330)和7.5mg光引发剂(2-羟基-4′-(2-羟乙氧基)-2-甲基苯丙酮,Irgacure2959),均匀混合后,得到反应混合物。随后,将含有SBMA、HEMA、交联剂和引发剂的溶液(反应混合物)注入密闭模具,紫外灯照射1h,引发自由基聚合和制备水凝胶。随后,将模具和水凝胶一同放入去离子水中, 每隔12h换一次水,记录脱胶时间,脱胶后用去离子水反复冲洗并浸泡5天,得到的水凝胶中的HEMA与SBMA的质量比为0.65:0.10。
示例13:水凝胶制备
在室温(优选25℃)条件下,取0.4g的[2-(甲基丙烯酰基氧基)乙基]二甲基-(3-磺酸丙基)氢氧化铵(SBMA),加入1mL超声20min后的去离子水,充分溶解。然后加入0.35mL的甲基丙烯酸羟乙酯(HEMA),混合均匀,然后加入1.5uL交联剂(聚乙二醇二甲基丙烯酸酯,分子量330)和15mg光引发剂(2-羟基-4′-(2-羟乙氧基)-2-甲基苯丙酮,Irgacure2959),均匀混合后,得到反应混合物。随后,将含有SBMA、HEMA、交联剂和引发剂的溶液(反应混合物)注入密闭模具,紫外灯照射1h,引发自由基聚合和制备水凝胶。随后,将模具和水凝胶一同放入去离子水中,每隔12h换一次水,记录脱胶时间,脱胶后用去离子水反复冲洗并浸泡5天,得到的水凝胶中的HEMA与SBMA的质量比为0.35:0.40。
示例14:水凝胶制备
在室温(优选25℃)条件下,取0.4g的[2-(甲基丙烯酰基氧基)乙基]二甲基-(3-磺酸丙基)氢氧化铵(SBMA),加入1mL超声20min后的去离子水,充分溶解。然后加入0.35mL的甲基丙烯酸羟乙酯(HEMA),混合均匀,然后加入7.5uL交联剂(聚乙二醇二甲基丙烯酸酯,分子量330)和75mg光引发剂(2-羟基-4′-(2-羟乙氧基)-2-甲基苯丙酮,Irgacure2959),均匀混合后,得到反应混合物。随后,将含有SBMA、HEMA、交联剂和引发剂的溶液(反应混合物)注入密闭模具,紫外灯照射1h,引发自由基聚合和制备水凝胶。随后,将模具和水凝胶一同放入去离子水中,每隔12h换一次水,记录脱胶时间,脱胶后用去离子水反复冲洗并浸泡5天,得到的水凝胶中的HEMA与SBMA的质量比为0.35:0.40。
示例15:含水量测定
在室温(优选25℃)条件下,取干燥的EP管并称重,质量记为m。之后,分别取示例1、示例2、示例3、示例4、示例5、示例6、示例7和示例8中制得的水凝胶适量,用滤纸拭去表面游离水后,放入EP管中并称重,记为m1。将取好的样品在冷冻干燥机中冷冻干燥24h,取出并称重,记为m2。水凝胶含水率可通过以下公式算得:
EWC%=[(m1-m)-(m2-m)]/(m1-m)×100%
每组样品测3个平行组,取算术平均值。
其中该检测结果如附图之图2所示。
示例16:失水率测定
在室温(优选25℃)条件下,取干燥的EP管并称重,质量记为m。之后,分别取示例1、示例3和示例8中制得的水凝胶适量,用滤纸拭去表面游离水后,放入EP管中并称重,记为m1。将加入样品的EP管放入60℃烘箱中,以使水凝胶迅速失水,每隔10min取出EP管并称重,记为m2。水凝胶失水率可通过以下公式获得:
失水率(%)=[(m1-m)-(m2-m)]/(m1-m)×100%
每组样品测3个平行组,取算术平均值。其中该检测结果如附图之图3所示。
示例17:透光率测定
在室温(优选25℃)条件下,分别将示例1、示例3和示例8中制得的水凝胶自水中取出,用擦镜纸擦干表面的游离水,用酶标仪表征其光学透明性,得到OD值(X),检测波长可为400nm-650nm,实际测定为450nm。并通过以下公式计算透光率:
T=10^(-X)×100%
其中该检测结果如附图之图4所示。
示例18:损耗模量与储能模量的流变性能测定
在室温(优选25℃)条件下,分别将示例1、示例3和示例8中制得的水凝胶自水中取出,饱和溶胀后,置于TA-AR-G2,用25mm,2.008°的锥形板对水凝胶进行剪切。设置剪切应变0.1%到100%,剪切频率为10rad/s,温度为25℃,得到储能模量G′与损耗模量G″。
其中该检测结果如附图之图5所示。
示例19:抗蛋白吸附能力测定
用改进后的酶联免疫吸附试验(ELISA)的方法来测定水凝胶样品对非特异性蛋白质的吸附能力。模型蛋白质是辣根过氧化物酶标记的羊抗人免疫球蛋白(HRP-IgG),对照组为组织培养聚苯乙烯(TCPS)。加入HRP的底物邻苯二胺后,邻苯二胺被HRP催化成为有色产物,产物的量与HRP-IgG物质的量直接相关,故可根据呈色的深浅进行定量分析。
首先,分别取示例1、示例3和示例8中制得的水凝胶适量,并将水凝胶样品和TCPS片放入24孔板中,加入1μg/mL的HRP-IgG溶液1mL后,孵育1.5小时,随后用PBS溶液冲洗5次,然后取出样品放到新的孔中。加入1mL含0.03%过氧化氢和1mg/mL邻苯二胺(OPD)的柠檬酸-磷酸缓冲液(0.1mol/L,pH值为5.0)。15分钟后,加入等体积的1mol/L H2SO4终止酶活性。使用酶标仪在492nm处测定光密度值(OD值)。
其中该检测结果如附图之图6所示。
示例20:抗菌吸附能力测定
使用灭毒的金黄色葡萄球菌作为模型细菌来检测水凝胶的抗细菌粘附性能。首先,将金黄色葡萄球菌接种在无菌LB琼脂平板上,37℃培养过夜。接着在37℃、200rpm条件下,在60mL含无菌LB培养基的烧瓶中培养单菌落(从初始培养物中获得)12小时。然后将培养物倒入两个50mL的离心管中,于4℃、4750rpm条件下离心20分钟。弃去上清液,将细胞沉淀物再次悬浮于30mL的无菌PBS溶液中,洗涤细菌2次后通过紫外分光光度计将菌液浓度调整到1×106/mL,用于测量细菌粘附的实验。测定前,分别取示例3、示例5和示例8中制得的水凝胶适量,并分别浸泡在70%(体积分数)乙醇中预处理5分钟,随后用PBS浸泡10分钟。然后将水凝胶放置细菌悬浮液中吸附1小时,PBS溶液洗涤后进行革兰氏染色。使用Nikon Ti-E系列显微镜在40倍镜头下直接观察粘附结果。
其中该检测结果如附图之图7所示。
根据上述示例1至示例20可知,向凝胶反应混合物中加入较少的SBMA(或CBMA)的即可极大的改善HEMA水凝胶的透光率。且随着SBMA的含量增加,材料的透光率明显改善,储能模量和损耗模量逐步下降,完全含水率也有明显的提高,表明其润滑度和透氧率均有明显的改善。而蛋白吸附实验和细菌实验都表明了随着SBMA的含量增加,材料的抗蛋白吸附和抗菌吸附也得到了明显的提高。
本领域技术人员会明白附图中所示的和以上所描述的本发明实施例仅是对本发明的示例而不是限制。
由此可以看到本发明目的可被充分有效完成。用于解释本发明功能和结构原理的该实施例已被充分说明和描述,且本发明不受基于这些实施例原理基础上的改变的限制。因此,本发明包括涵盖在附属权利要求书要求范围和精神之内的所有修改。
- 还没有人留言评论。精彩留言会获得点赞!