一种N‑甲基‑2,3,7,8‑四羟基苯并菲啶类化合物、制备方法和应用与流程
本发明属于天然药物技术领域,具体地说,涉及一种N-甲基-2,3,7,8-四羟基苯并菲啶季铵盐的在制备抑制多巴脱羧酶药物中的应用。
背景技术:
多巴脱羧酶(Dopa decarboxylase,DDC)又称芳香氨基酸脱羧酶,可通过催化L-3,4-二羟基苯丙氨酸(L-DOPA)和L-5-羟色氨酸脱羧合成具有重要生理活性的神经递质多巴胺和5-羟色胺(Moore B M,et.al.J Biol.Chem,1996,271:23954-23959.);同时还可催化部分芳香氨基酸脱羧生成对应的生物胺。脑内5-羟色胺含量降低将导致抑郁、焦虑等常见心境障碍;黑质和纹状体病变致使多巴胺合成减少还可导致帕金森症发生(陈茹.中国康复理论与实践,2007,13(7):637-639.)。由于血脑屏障的存在,血液中的5-羟色胺和多巴胺很难进入大脑(张月战.疑难病杂志,2013,12(5):401-403.)。由于DDC在神经系统和肾脏中活性较高,外周DDC抑制剂如卡比多巴能够有效降低色氨酸、L-多巴在外周组织中脱羧降解率,临床上目前被用于治疗帕金森症和缓解外周生物胺含量较高导致的不良症状(Burkhard P,Donminici P,et.al.Nature Structure Biology,2001,8(11):963-967.)。此外,动物肠道微生物分泌的色氨酸脱羧酶通过催化色氨酸在动物肠道中代谢,影响色氨酸等限制性氨基酸吸收(印遇龙.猪氨基酸营养与代谢[M].北京:科学出版社,2008.)。有效抑制色氨酸脱羧酶能够提高色氨酸等芳香氨基酸在肠道中的吸收率,促进动物生长。因此,进一步研究多巴脱羧酶抑制剂在抗帕金森综合症和动物生长促进剂方面都有重要研究价值。文献表明,目前已证实的DDC抑制剂主要有DDC底物类似物如卡比多巴、苄丝肼;表没食子儿茶素没食子酸酯、表儿茶素没食子酸酯(Bertoldi M,Gonsalvi M,et.al.2001,284(1):90-93.);季胺类苯并菲啶类生物碱如血根碱等(Drata J,Ulrichova J,Walterova D.Journal of Enzyme Inhibition,1996,10(4):231-237.)。其中,卡比多巴和苄丝肼对DDC的抑制机制已基本探明,是由抑制剂结构中的肼基与DDC的辅酶磷酸吡哆醛之间形成腙键而与酶结合到一起,其邻苯二酚结构单元嵌入活性位点的裂缝并穿透到辅酶环平面的后方从而与DDC发生作用(Vassiliou A,Fragoulis E G,Vassilacopoulou D.Neurochemical Research,2009,34(6):1089-1100.)。儿茶素没食子酸酯、表儿茶素没食子酸酯等化合物对DDC的抑制机制尚无文献进行详尽报道,但研究者根据被儿茶素没食子酸酯钝化后的DDC的特性做出推断,抑制作用应该归因于DDC活性位点中不明残基的共价修饰。由于血根碱具有与其他DDC抑制剂完全不同的结构,血根碱对DDC抑制作用很存在新的机制:血根碱季铵正离子中心的C=N双键可接受DDC活性位点半胱氨酸残基上的巯基(-SH)亲核加成形成共价复合物影响DDC的催化活性,(Cheng P,Zhou J,Qing Z.et.al.Bioorg.Med.Chem.Lett.2014,24,2712-2716)。
虽然目前已有文献报道了血根碱具有DDC抑制活性,但其抑制效果有限。血根碱在偏碱性条件下或在生物体内容易转化为6-羟基血根碱,还可以与巯基化合物共价复合,这些是血根碱的主要代谢失活方式。上述因素限制了血根碱在DDC抑制剂中的深入应用。
技术实现要素:
为解决血根碱的DDC抑制活性不理想,容易被巯基化合物例如二硫苏糖醇键合失活等技术问题,本发明公开了一种N-甲基-2,3,7,8-四羟基苯并菲啶类化合物的DDC抑制剂,旨在提升DDC抑制活性。
另外,本发明还包括N-甲基-2,3,7,8-四羟基苯并菲啶类化合物及其制备方法。
一种N-甲基-2,3,7,8-四羟基苯并菲啶类化合物的应用,用作多巴脱羧酶的抑制剂;所述的N-甲基-2,3,7,8-四羟基苯并菲啶类化合物具有式1结构:
式1中,X-为药理上可接受的阴离子。
本发明中,苯并[C]菲啶母核上的多邻酚羟基结构配合所述的季铵正离子中心,有助于协同提升DDC的抑制活性,可应用于制备多巴脱羧酶抑制剂类药物等研究领域。
作为优选,所述的应用中,式1中,X-为草酸根、醋酸根、苯磺酸根、甲磺酸根、硫酸氢根离子、卤化物离子中的至少一种;进一步优选为硫酸氢根负离子。
本发明中,通过将所述的式1化合物(N-甲基-2,3,7,8-四羟基苯并菲啶季铵盐)对人重组的多巴脱羧酶(DDC)的体外抑制活性来评价所述的式1化合物的DDC抑制性能。所述式1化合物对DDC的抑制活性评价步骤例如为:
依次在离心管中加入磷酸吡哆醛(PLP)、磷酸缓冲液、不同浓度式1化合物及人重组多巴脱羧酶(human recombinized DDC)溶液,密封37℃恒温振荡10min,加入左旋多巴(L-Dopa)溶液,密封37℃恒温振荡35min,取出立即沸水浴2min,冰浴2min,移入超滤离心管离心15min,取滤液液相检测,依据液相色谱检测结果确定L-Dopa脱羧转化率,获得抑制率-抑制剂浓度曲线,计算IC50。通过实验发现,本发明所述的式1化合物的DDC的抑制活性较血根碱提高一个数量级。
此外,本发明还探索了所述的式1化合物在巯基化合物条件下的DDC抑制活性;步骤例如为:
依次在离心管中加入PLP、磷酸缓冲液、一定浓度式1化合物(也称为化合物I)和不同浓度二硫苏糖醇(DTT)的磷酸缓冲溶液,密封37℃恒温振荡10min,随后加入人重组DDC溶液,密封37℃恒温振荡10min,再加入L-Dopa溶液,密封37℃恒温振荡35min,取出立即沸水浴2min,冰浴2min,移入超滤离心管离心15min,取滤液液相检测。依据L-dopa脱羧转化率获得抑制率-DTT浓度曲线,研究DTT浓度对化合物I的抑制活性的影响。
通过所述的研究发现,高浓度的DTT处理后的所述的化合物I仍具有较好的DDC抑制活性,具有良好的抗巯基化合物键合失活优势;可能是因为式1化合物具有多个新的活性位点,通过各活性位点协同提升DDC的抑制效果的缘故。
本发明所述的式1化合物可有效抑制色氨酸、L-多巴在外周组织中脱羧降解率,可应用于治疗帕金森症和缓解外周生物胺含量较高导致的不良症状等药物的制备领域。例如,将所述的式1化合物或其药学可接受的盐和药用载体和/或赋形剂应用于制备多巴脱羧酶抑制剂类药物。
所述的应用中,作为优选,将所述的式1化合物用于制备抗帕金森症的药物。
所述的优选的应用中,将式1化合物和/或药用载体、药用赋形剂制备抗帕金森症的药物。例如,将所述的式1化合物和/或药用赋形剂应用于制备抗帕金森症的注射液、无菌粉针剂、片剂、口服液或胶囊。
所述的应用中,作为优选,将所述的式1化合物用于制备抗抑郁、焦虑药物。
所优选的应用中,将所述的式1化合物和/或药用载体、药用赋形剂制备抗抑郁、焦虑药物。例如,将所述的式1化合物和/或药用赋形剂应用于制备抗抑郁、焦虑的注射液、无菌粉针剂、片剂、口服液或胶囊。
本发明中,还提供了所述式1化合物的制备方法:由血根碱在酸液下水解而得;反应方程式为方程式1:
其中,水解反应过程的温度为85~95℃;优选为95℃。
本发明中,采用色谱法对反应得到的粗产品进行纯化;纯化过程中,采用AB-8树脂,洗脱液为体积百分比为40~50%的甲酸水溶液,洗脱液流速为1~3BV/h。
作为优选,所述的酸液为浓度为50~70wt%的硫酸水溶液;优选为60wt%的硫酸水溶液。
作为优选,水解反应过程中还投加有间苯三酚,其中,血根碱、间苯三酚的投料摩尔比为1∶1~1.2。作为优选,血根碱、间苯三酚的投料摩尔比1∶1。
本发明中,一种优选的制备方法,包括以下步骤:
步骤(1):水解:
以血根碱为起始原料,与一倍当量的间苯三酚在70wt%的硫酸水溶液中95℃下水解反应90分钟;将水解反应液倾入超纯水中析晶,随后再离心、超纯水洗涤得式I的粗产物;
步骤(2):纯化:
将步骤(1)的粗产物用44%甲酸超声溶解,随后在AB-8大孔树脂中进行色谱分离,色谱分离采用的洗脱液为44vol%甲酸的水溶液,洗脱液流速为2BV/h。
有益效果
本发明所述的N-甲基-2,3,7,8-四羟基苯并菲啶类化合物具有优良的抑制DDC作用,其对DDC抑制作用相较于血根碱提升了一个数量级;在巯基化合物二硫苏糖醇的作用下DDC抑制活性仍然得到了保留。
附图说明
图1为实施例1的血根碱水解反应中控的HPLC--QTOF曲线图;
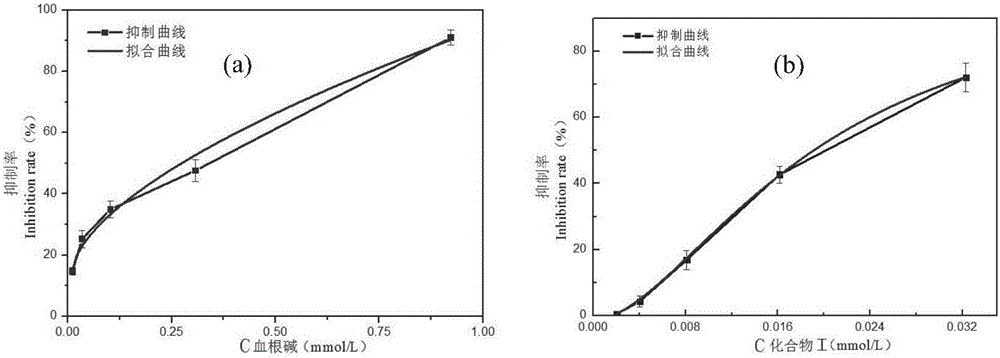
图2为实施例3的血根碱和化合物1的DDC抑制活性曲线图;其中,(a)部分为血根碱的DDC抑制活性曲线及拟合曲线图;(b)部分为化合物1的DDC抑制活性曲线及拟合曲线图;
图3为实施例4的不同浓度DTT处理下血根碱和化合物I对DDC的抑制率;其中,(a)部分为DTT处理下血根碱的DDC抑制活性曲线及拟合曲线图;(b)部分为DTT处理下化合物I的DDC抑制活性曲线及拟合曲线图。
具体实施方式
通过以下实施例对本发明作进一步的详细说明,但本发明的内容并不局限于此。
实施例1
N-甲基-2,3,7,8-四羟基苯并菲啶季铵盐(I)制备(见方程式2):
准确称取1g氯化血根碱及当量间苯三酚(phloroglucinol),加入30ml的60%浓硫酸,95℃下搅拌,分别在5、10、15、20、25、30、38、46、54、70min取少量反应液滴入装有少量超纯水小瓶中,离心取沉淀和上清液进行HPLC--QTOF检测。由于血根碱具有两个亚甲二氧基,脱去一个亚甲基将得到两个酚羟基衍生物(II),反应时间延长,目标产物I的转化率逐步升高。根据不同反应时间产物中氯化血根碱、化合物I的硫酸氢盐和化合物II的硫酸氢盐浓度与时间作图,获得化合物I转化率-反应时间曲线,如图1所示,反应时间为70min时,具有良好的选择性。
实施例2
N-甲基-2,3,7,8-四羟基苯并菲啶季铵盐(I)分离纯化
将实施例1反应产物加入200mL超纯水中离心,弃去上清液,取沉淀反复用超纯水洗涤3次,除去硫酸。沉淀用44%甲酸超声溶解制成上样液,备用。将预处理后的AB-8树脂装柱,所装树脂为内径4cm,树脂高度为54cm,柱体积1BV=678mL,树脂上方用脱脂棉保护,使用1BV44%甲酸以3BV/h流速预淋洗树脂柱,待树脂柱上方液面距离脱脂棉5cm时准备上样,上样流速控制为2BV/h,上样完成后使用44%甲酸(水溶液)持续冲柱,流出液每100ml接一瓶,使用液相色谱进行检测,液相色谱检测条件为:色谱柱(Unitary C18);流动相为0.1%甲酸-水(A)与乙腈(B),洗脱程序为0-30min,10%B-90%B,流速为1mL/min;柱温30℃,进样量5μL;检测波长为270nm。根据检测结果,将化合物I浓度为95%以上洗脱液合并,旋转蒸发浓缩得到纯品棕红色粉末即为化合物I硫酸氢盐。
性状:棕红色无定型粉末
分子式:C18H14NO4+
理论分子量:308.0917,HPLC-QTOF-HRMS实测分子量:308.0915
1H NMR(400MHz,DMSO-d6)δ:9.86(s,1H),8.52(d,J=8.8Hz,1H),8.44(d,J=8.8Hz,1H),8.13(d,J=8.8Hz,1H),8.10(s,1H),8.09(d,J=8.8Hz,1H),7.46(s,1H),4.90(s,3H,NCH3).13C NMR(100MHz,DMSO-d6)δ:151.9,150.5,151.0,150.1,147.3,134.0,133.1,132.0,128.9,127.4,126.5,121.5,121.4,120.6,119.5,106.8,105.0,52.8,
实施例3
血根碱和化合物I(根据实施例2纯化而得)对DDC的抑制活性研究
根据DDC抑制活性预实验结果将血根碱配制为2.29×10-6mol/ml,化合物I浓度为3.044×10-7mol/ml的溶液。酶促反应体系使用的其余组分分别为:磷酸缓冲溶液为Na2HPO4-KH2PO4(0.02M,pH6.8),人重组多巴脱羧酶(human recombinized DDC)磷酸缓冲溶液浓度为10μg/mL,PLP的磷酸缓冲溶液浓度为5×10-6mol/mL,L-Dopa磷酸缓冲溶液为2.5×10-6mol/ml。在确保反应体系总体积为2mL和DDC浓度为40ng/uL的前提下,依次在离心管中加入15μL PLP溶液、磷酸缓冲液、不同浓度梯度的血根碱或化合物(I)的磷酸缓冲溶液以及DDC磷酸缓冲溶液,密封37℃恒温振荡10min,加入60μL左旋多巴(L-Dopa)磷酸缓冲溶液,密封37℃恒温振荡35min,取出立即沸水浴2min,冰浴2min,移入超滤离心管离心15min,取滤液液相检测,依据液相色谱检测结果确定L-Dopa脱羧转化率,获得抑制率-抑制剂浓度曲线如图2所示。图2很清晰的显示出血根碱和化合物I均对AAD(也称为DDC)表现出较明显的抑制作用,抑制率随抑制剂在体系中浓度增加呈非线性上升趋势,根据Origin8.5分别对抑制曲线使用非线性拟合,根据得到的拟合方程进行计算得出血根碱化合物I的IC50分别为0.274mM和0.019mM。化合物I的抑制活性较血根碱提高一个数量级。
实施例4
N-甲基-2,3,7,8-四羟基苯并菲啶季铵盐I(实施例2纯化得到的化合物I)对DDC双重抑制机理研充
血根碱等季铵类苯并菲啶生物碱抑制DDC的机理可能为生物碱中烯胺正离子中心接受
DDC半胱氨酸残基游离巯基(-SH)亲核加成后形成生物碱-S-DDC共价复合物,从而影响酶的催化活性。二硫苏糖醇(DTT)的巯基能够与血根碱形成共价化合物,从而使血根碱失去DDC抑制活性,本发明中,可通过对比观察血根碱与化合物I的在不同浓度DTT处理下对DDC的抑制活性差异来探充其抑制机制。
控制DTT处理的酶促反应溶液总体积为2mL,DDC浓度为40ng/uL。在确保酶促反应体系中的血根碱和化合物I浓度分别为0.922mmol/L和0.0323mmol/L的前提下,向离心管中加入不同浓度DTT溶液、15μL PLP溶液、磷酸缓冲液以37℃恒温振荡10分钟。随后向离心管中加入DDC的磷酸缓冲溶液,密封37℃恒温振荡10min,再加入60μL左旋多巴(L-Dopa)磷酸缓冲溶液,密封37℃恒温振荡35min,取出立即沸水浴2min,冰浴2min,移入超滤离心管离心15min,取滤液液相检测,依据液相色谱检测结果确定L-Dopa脱羧转化率,获得抑制率-抑制剂浓度曲线如图3所示。当反应体系中DTT浓度为血根碱三倍时(2.5mmol/L),血根碱对DDC的抑制活性消失。就化合物I而言,即使DTT在反应体系中的浓度达到0.08mmol/L(超过化合物I浓度20倍),化合物I对DDC仍然保持55%以上的抑制率,对DTT具有良好的耐受性。DTT处理实验可发现,化合物I对DDC的抑制活性可能具有新的机制,例如为:(1)化合物I的正离子中心能够接受DDC活性位点残基巯基的亲核加成生成共价复合物,降低DDC催化活性;(2)化合物I的多酚羟基结构能够促进其与DDC活性位点结合。
实施例5
含有式I的N-甲基-2,3,7,8-四羟基苯并菲啶季铵盐及可药用载体和/或赋形剂及其在多巴脱羧酶抑制剂类药物中的应用:
按实施例1和实施例2的方法先制得N-甲基-2,3,7,8-四羟基苯并菲啶季铵盐,制成注射液、无菌熔封得粉针剂、制成粉剂、加入赋形剂制粒压片、按常规口服液制法制成口服液、加入赋形剂制成胶囊或加入赋形剂制成胶囊。
本发明的化合物、用途和方法已经通过具体的实施例进行了描述。本领域技术人员可以借鉴本发明的内容适当改变原料、工艺条件等环节来实现相应的其它目的,其相关改变都没有脱离本发明的内容,所有类似的替换和改动对于本领域技术人员来说是显而易见的,都被视为包括在本发明的范围之内。
- 还没有人留言评论。精彩留言会获得点赞!