快速并灵敏基因型鉴定及核酸检测的制作方法
相关申请本申请要求以2013年3月15日提交的美国临时专利申请号61/791,933为优先权基础,所述专利申请的所有内容都以引用方式被纳入本申请中。
技术领域:
本发明涉及的领域在于鉴定与人类疾病有关的各种基因型。
背景技术:
:本发明涉及识别不同基因型。序列特异性引物-聚合酶链式反应(SSP-PCR)、DNA测序、DNA指纹,和单核苷酸多态性(SNP)基因分型等技术,已被应用于基因分型(PCT申请公开号WO/2011/139750)。在这些技术中,单核苷酸多态性(SNP)基因分型有较高的识别力。然而,大多数涉及DNA杂交的基因分型检测都要求较高的运行成本和较长的操作时间,因此有必要开发更有效的基因分型方法,达至更快、更便宜及覆盖更多基因型。结核分枝杆菌(MTB)检测结核病(TB)是由结核分枝杆菌(MycobacteriumtuberculosisMTB)引起的。耐药性结核分枝杆菌(DR-MTB)的出现是在工业化国家和发展中国家结核病控制项目中的一个严重问题。除了在临床和流行病学上的重要性,耐药性结核病(DR-MTB)更有重要的经济影响,因其治疗成本比普通的MTB为高。DR-MTB被定义为对至少两个最有效的第一线药物有耐药性,包括利福平(rifampinRIF)和异烟肼(isoniazidINH)。DR-MTB病例在全球有上升的趋势,显着的发病率和死亡率。一线抗结核药物的耐药性已被发现与几个MTB基因突变有关:rpoB(耐RIF);katG基因和inhA基因(耐INH)。DR-MTB的检测有几种不同技术可用。虽然传统的表型药物敏感性试验(DST)仍然是测试MTB耐药性的“黃金标准”,但DST可能要长达八个星期才能完成。结核分枝杆菌是生长缓慢的细菌。MTB每15-20小时才分裂一次,并取决于所使用的介质一般需要4至6周才能生长成菌落。此后,当DST所培养的MTB被识别,药敏试验通常再还需时2周。DST因此需要较长时间,导致了治疗疾病的延误,尤其通常的做法是在DST完成前已经要开始治疗。业界开发中的替代培养或能缩短测试所需的时间;然而,某些类型样品中的MTB不适合用替代培养。商业环境中并不经常使用常规的DNA测序来检测MTB耐药突变,因为其耗时和需要专门的知识。市场上有不同技术的试剂盒,包括实时PCR和用于检测单一类型MTB或耐药性MTB的常规杂交。特别是实时PCR,由于其可用信道数量有限,所以通常难以同时检测多种耐药MTB。虽然常规杂交也适用于检测多药耐药MTB;然而,它需要长的温育时间(至少4小时)。对比下,本发明通过利用聚合酶链反应(PCR)和“导流”杂交技术,提供了一种阵列测试,可以在一个平台上同时检测单一耐药MTB和多重耐药MTB,检测时间比常规的杂交短(~35分钟)。从提取样品中DNA到分析的整个测试只需少于4小时,检测结果有高度的特异性和敏感性。β地中海贫血的检测β地中海贫血由常染色体突变引起,是一种血红蛋白疾病,可根据β-球蛋白的生产受影响的程度再分类。其中有些突变导致β球蛋白(表示为β+)轻度减产,有些导致β-球蛋白基因的绝对沉默而不能生产或只生产出失去功能的β球蛋白(表示为β0)。据估计,世界约有1.5%的人口有β-地中海贫血基因型的杂合体,父母都是杂合体的话其后代可能是纯合体。β地中海贫血有三个严重程度:轻度(轻型地中海贫血,β+/β或β0/β)、中度(中度地中海贫血:β+/β或β0/β)和严重(重型地中海贫血:β+/β+,β0/β+或β0/β0)。遗传了地中海贫血的人主要会出现低色素性贫血,并可能需要终身输血。控制β-地中海贫血的最好方法是避免β地中海贫血患儿的出生,这要准父母做产前检测和遗传咨询;这已被证实是最有效管理地中海贫血的方法。β-地中海贫血流行于温带地区,如地中海沿岸国家,中东和东南亚地区。β-地中海贫血的分子基础已有被广泛研究,发现β-球蛋白基因的点突变在不同的地区有不同的突变方式和突变频率。当前的检测技术包括微阵列,等位基因特异性PCR(AS-PCR)和直接测序。微阵列可以同时检测多个目标DNA芯片上,因此适用于同时检测多个样品。然而,它的应用是因其高成本的限制,结果不能用肉眼观察,需使用高性能扫描器和复杂的分析软件进行解释。等位基因特异性PCR是使用等位基因特异性引物,以检测多态性或突变,这技术中只有与目标DNA完全匹配的寡核苷酸能够充当引物以扩增目标DNA。该技术的限制是在一个反应的有限的吞吐量。直接DNA测序涉及体外DNA复制过程其中DNA聚合酶选择性地掺入链终止双脱氧核苷酸,该技术的吞吐量低和需要长时间操作,因此检测效率低。另一方面,本发明提供了一种结合使用PCR和反向斑点杂交的DNA检测,能够提供了一个高度敏感和特异的检测的β-球蛋白基因的突变,以协助β-地中海贫血的检测。乙型肝炎病毒检测乙型肝炎病毒是最小的DNA病毒,其包括3000个由蛋白质衣壳围绕的核苷酸。乙型肝炎病毒通过与受感染者的血液或体液接触传播。约二十亿人感染乙肝病毒;其中超过3.5亿成为乙肝病毒携带者。大约五分之一乙型肝炎病毒感染会发展出肝硬化或肝癌。检测乙型肝炎病毒可以通过简单的表面抗原血液测试,或使用应用聚合酶链反应(PCR)和乙型肝炎病毒DNA的测量进行诊断。此外,通过分析乙型肝炎病毒基因组序列的差异已鉴定了10种乙型肝炎病毒基因型(A至J)和几种亚型。乙型肝炎病毒基因型和亚型明显表现出不同的地域分布。各种乙型肝炎病毒基因型在致病和治疗上存在差异。乙型肝炎病毒基因型的确定可以为慢性乙型肝炎病毒感染和治疗前的评估提供信息。DNA测序被认为是对乙型肝炎病毒基因型检测的黃金标准方法。但它在检测混合基因型的效率较低。另外,分子DNA技术提供了一个用于高度敏感地检测乙型肝炎病毒基因型的具体方法。性病病原体检测性病是常见的世界性疾病。根据2005年世界卫生组织估计,每年有448万新发并可治愈的性病病例(梅毒,淋病,衣原体和滴虫),主要发生在世界各地的15至49岁的成年人。香港在2010年每550个孕妇有一个被检测出患有性传播疾病(不包括艾滋病)。性病能传染孕妇的孩子,无论是在怀孕期间或在宝宝出生后。当中,淋球菌和衣原体可导致不育。因此,准婚夫妇和孕前妇女有检测性病的潜在需要。此外,中国也是检测性病病原体的潜在市场,在过去20年性病患者数量急剧增加。因此中国需要快速,低价,准确的性病病原体检试剂盒帮助控制性病。目前市场上的性病检试剂盒可用于检测单个病原体或同时检测3-4个病原体,一般没有包括人类乳头状瘤病毒(HPV)。由于性病的发病率增加,有需要同时筛选分析和检测多个性病病原体。血栓形成倾向检测血栓形成倾向是指血液有异常的凝固,增加了出现血栓形成的风险。研究报告显示,有血栓形成倾向并出现血栓形成的病人中,约40%与遗传因素有关,并且被证实有较高风险患上静脉血栓形成等心血管疾病和复发性流产等生殖障碍。也有越来越多的意见认为带有遗传性血栓形成倾向的孕妇较易出现妊娠不良,症状包括复发性流产、胎死宫内、胎儿宫内发育迟缓、先兆性子痫和胎盘早剥等。在过去的二十年间,一些基因突变已被确定与遗传性血栓形成倾向有关。最常见的四个基因突变为:莱顿凝血第五因子FactorVLeiden(FVL)[1691G>A],凝血酶原FactorII(FII或称为凝血第二因子)[20210G>A],亚甲基四氢叶酸还原酶MethylenetetrahydrofolateReductase(MTHFR)[677C>T]及亚甲基四氢叶酸还原酶MethylenetetrahydrofolateReductase(MTHFR)[1298A>C]。检测这些基因突变有助于识别有血栓形成倾向和复发性流产的高危人群,从而帮助个別人士预防疾病及降低患病风险,并提供预防性治疗的指导。发明概要SNP基因分型作为诊断工具SNP基因分型除了可用于DNA指纹外,还可以用于鉴定基因片段、多态性基因、具有改变的基因,或功能有问题的基因。本发明提供方法和试剂盒用于快速,明确地鉴定具传染性的病原体,或由于特定DNA序列的存在或缺失所引起的遗传性疾病。如以上所论,市场上的杂交格式需要由具高解象度的图像分析仪进行分析。以膜为基础的等位特异寡核苷酸探针-反向点杂交(ASO-RDB)导流杂交格式(例如美国专利号5,741,647)可被应用于SNP基因分型。微阵列杂交格式能产生可见的点,并可以通过目测和/或使用成本较低的图像分析仪进行分析。导流杂交DNA杂交一直是现代生物科学研究并涉及基因分子生物学研究中的最重要方法。各种基因组的核酸序列复杂性能通过特定互补的DNA序列在溶液中杂交被揭示和分析。简言之,目标DNA被扩增或消化,并使其与在固体支持介质(如硝酸纤维素膜)上的互补DNA探针杂交。然而,传统的杂交技术原则上受限于膜的面积,并通常需要较长的温育时间。导流杂交方法和设备可以准确地控制杂交条件,不会有传统杂交技术需时较长的问題。导流DNA杂交技术可将杂交时间从数小时或数天减至数分钟(整个杂交测定可以在5-30分钟内完成,具体时间取决于用于产生检测信号的方法)。导流杂交设备的制造成本低廉,并且使用比传统杂交设备少10倍的试剂量,因此使DNA检测技术比前更经济实惠。导流杂交技术提供更灵敏、准确的检测和鉴定结果,并普遍适用于各种不同技术例如传统DNA印迹法(Southernblotting)、RNA印迹法(Northernblotting)、斑点印迹法、狭槽印迹法和反向斑点印迹法的杂交。PCT申请WO/2011/139750描述了一个连接到中央控制单元的多个横向快速导流检测设备。杂交设备包含一个连接到一个或多个横流设备的中央控制单元。横流设备进行杂交过程和显影程序,并由中央控制单元控制和供电。单个横流设备或几个设备可以同时测试若干反应(或者若干样品和/或分析物),并在独立的控制下以不同条件进行程序。横流设备可以是“nxm”点阵(矩阵)的形式,也可以是线阵的形式。更多有关于执行导流杂交的方法和设备的描述可参见美国专利5,741,647、美国专利6,020,187和PCT申请WO/2011/139750。本
技术领域:
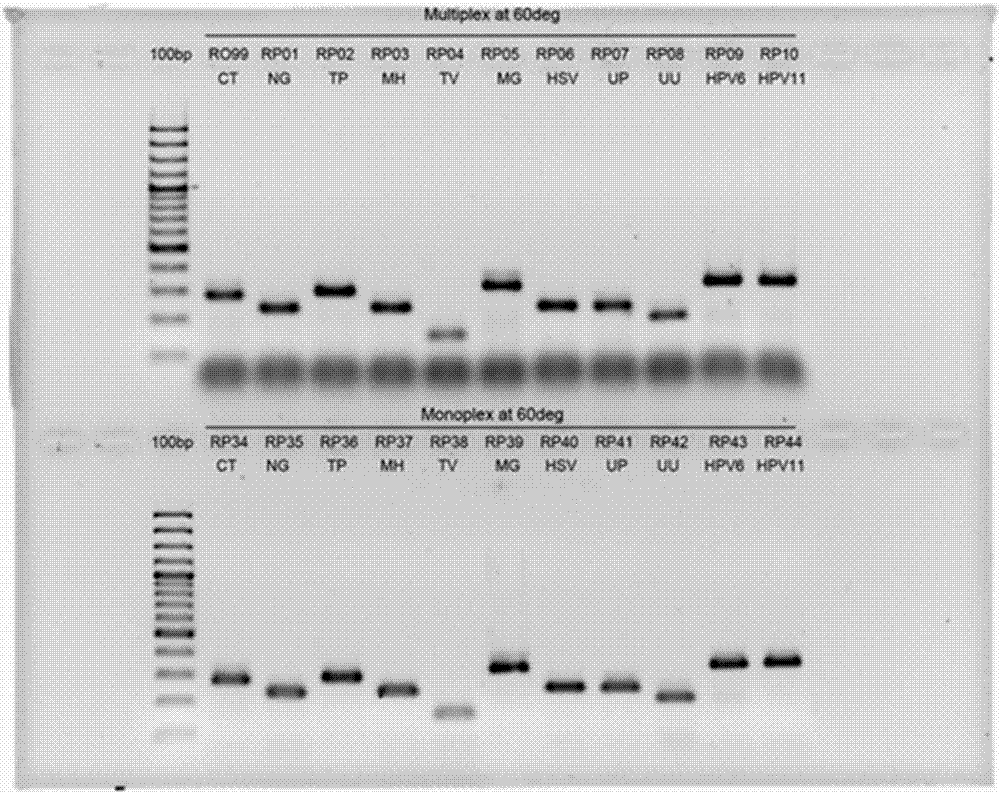
的普通技术人员可以使用美国专利5,741,647或美国专利6,020,187中所述的类近导流杂交技术,或者能够执行导流杂交技术的任何新方法或设备来实践本发明。杂交设备附有的成像系统,例如FT-Pro,可以将信号检测数码化。本发明所述的杂交设备可以是自动化的设备,可以使用其内置的数码化功能以进行所有分析。导流杂交法比传统杂交技术有更高的效率、准确度和灵敏度。耐药性结核分支杆菌(MTB)检测本发明提供方法和试剂盒以PCR和“导流”式杂交技术检测对利福平(RIF)和异烟肼(INH)有耐药性的结核分支杆菌(MTB)。MTB的RNA聚合酶β亚基的rpoB基因突变与对利福平的耐药性有关;而katG基因(过氧化氢酶)和INHA基因(烯酰基ACP还原酶)的突变与对异烟肼的耐药有关。在本发明中,特异性引物被用于扩增INHA、rpoB基因,和katG基因;特异性引物已被证实没有与人类基因组有交叉反应。引物RS-IAC充当内部控制,其不针对任何人类或MTB基因组,用于监测PCR扩增过程。探针包括有十个用于检测耐药性的基因突变DNA探针;这基因突变有rpoB(D516V,D516G,H526D,H526Y,H526L1,S531L和S531W),katG(S315T1和S315T2),和inhA(-15TC/T)。探针也包括有五个用于检测野生型MTB基因组的DNA探针,这有助于验证rpoB基因,katG基因和inhA基因的PCR扩增反应是否已完成。杂交引物可以是已被生物素化来支持。β地中海贫血检测本发明提供检测β-球蛋白基因突变的方法及试剂盒,突变包括TATA-28(A>G),TATA-29(A>G)的检测,起始密码子(G>A),密码子5(-CT),密码子8/9(+G),密码子15(G>A),密码子16n(-C),密码子17(A>T),密码子19(A>G),密码子26(G>A)密码子27/28(+C),密码子为30G>C,IVS1.1(G>T),IVS1.1(G>A),IVS1.5(G>C),密码子41/42(-TCTT),密码子43(G>T),密码子71/72(+A),IVS2.1(G>A),IVS2.654(C>T)和619bp的缺失。乙型肝炎病毒检测本发明提供方法和试剂盒以检测8个乙型肝炎病毒基因型(乙型肝炎病毒基因型A,B,C,D,E,F,G和H)是否存在于病人的血清样品中的。检测性病病原体本发明提供方法和试剂盒,以检测在各个标本中,如尿液,泌尿生殖系统拭子(尿道、阴道、子宫颈和各种病变)和液基细胞学标本(PreservCytTM和SurePathTM)的原生物、细菌,和病毒的存在。扩增控制(AC)包括用于检测人类DNA,以检查结果有足够的细胞含量和有效性。AC可用来监测在PCR扩增过程中PCR抑制剂的存在和提取的DNA量是否足够。没有AC信号表示在PCR扩增过程的存在抑制剂或DNA量不足(或不存在检体)。正控制(PC)包含一个正模板核酸分子来监测PCR试剂的性能。DNA杂交和PCR技术可更快的检测在尿、泌尿生殖系统拭子(尿道、阴道、子宫颈和各种病变),和液基细胞学标本(PreservCytTM和SurePathTM)中的性病病原体。在一个实施方案中,所述方法和试剂盒可检测的12种常见性病病原体:1种原生动物(阴道毛滴虫),7种菌(沙眼衣原体、淋病奈瑟菌、生殖支原体、人型支原体、解脲支原体、解孢子虫和梅毒螺旋体)和4种病毒(单纯疱疹病毒1&2型,人乳头瘤病毒6型和11型)。这些病原体都与子宫颈炎、尿道炎、滴虫病和盆腔炎有关。本发明提供的通用引物和病原体特异性引物,用于检测性病病原体。通用引物用来实现多种不同的目标同时的PCR平衡扩增。通用引物序列已通过PCR和凝胶电泳来测试特异性,以证明不与其他病原体和人类基因组有交叉反应。两个通用引物序列分别被加入到病原体特异性引物和AC特异性引物的5'端。通用引物和病原体特异性引物标记再通过PCR和凝胶电泳进一步测试,证明没有与其它病原体和人类基因组有交叉反应(图1)。在一个实施方案中,病原体特异性引物和两个通用序列标记(引物)包括在单个PCR扩增。在第一轮PCR,病原体特异性引物结合其特定的目标,并创建一个携带通用序列的PCR扩增产物。接着,在第二轮PCR中,通用引物结合到通用序列标记的PCR产物(图2)。在优化的PCR下,我们可以实现平衡扩增以避免因不同目标病原体DNA序列有不同的扩增效率而导致结果有偏差。所述实施方案还确保病原体的扩增产物仅由通用引物产生,与DNA探针从而有更精确的检测。本文所描述的通用引物系统也可应用到其他方法和试剂盒来检测未在本发明中描述的DR-MTB,β球蛋白,乙肝病毒和血栓形成倾向,以及与其它疾病有关的核酸或基因。血栓形成倾向检测本发明提供检测与遗传性血栓形成倾向有关的基因突变的方法,所述基因突变包括莱顿凝血第五因子FactorVLeiden(FVL)[1691G>A],凝血酶原FactorII(FII或称为凝血第二因子)[20210G>A],亚甲基四氢叶酸还原酶MethylenetetrahydrofolateReductase(MTHFR)[677C>T]和甲基四氢叶酸还原酶MethylenetetrahydrofolateReductase(MTHFR)[1298A>C]。尽管本发明的验证数据实验使用PCR以扩增序列,任何可以产生足够份量特定目标序列以进行鉴定和导流杂交分析的方法亦可被使用。如果所得到的目标序列份量足够,就可能不需要使用PCR扩增。检测可以通过检测目标DNA或接合物上的标记来实现。附图说明图1a示出了使用通用引物(序列号285和286)扩增临床样品PCR反应物的电泳图像。仅在存有病原体的阳性样品(即CT-阳性,NG-阳性,HPV-6和HPV-11阳性)中观察到特定频带,这表明通用引物不会与人类DNA有反应。图1b示出了使用病原体特异性引物(序列号263-282)和通用引物(序列号285和286)扩增人类临床样品的PCR反应物的电泳图像。每个样品观察到对应特定病原体的特定频带,表明引物与其对应的病原体有高度特异性。类似的情况在单个和多个PCR反应中都可以观察到。图2示出了一个用在单个PCR扩增反应中的通用引物和基因特异性引物的实施例。图3示出了一个DR-MTB匣子(左图)和一个实施方案的DR-MTB检测的信号位置(右图)(格线仅供说明用途)。IAC内部控制监测PCR的扩增过程。HC是杂交控制,监测杂交过程。图4示出了不同的MTB突变体的视觉解释的一个例子。图5示出了一种β-地中海贫血匣子和信号位置实施方案(格线仅供说明用途)。图6a示出了一个解释不同的β-地中海贫血基因型的一个例子。图6b示出了使用β-地中海贫血匣子的各种临床样品的测试结果。图7示出了乙型肝炎病毒检验试剂盒检测的一个实施例,有个8个乙型肝炎病毒基因型(乙型肝炎病毒的A,B,C,D,E,F,G和H)的存在。通用引物IAC和HC也包括在内。图8示出了一个例子去解释不同乙型肝炎病毒基因型。图9a示出了本发明和其他制造厂一个性病试剂盒的敏感性的比较。图9b示出的本发明的性能和其它生产厂家的性病试剂盒的临床样品比较。图10a示出了一种性病试剂阵列,匣子格式和信号位置的实施方案。所述芯片可以检测12种常见致病原体的存在:1种原生动物(阴道毛滴虫),7种菌(沙眼衣原体,淋球菌,支原体,人型支原体,解脲支原体,解脲孢子虫,梅毒螺旋体)和4种病毒(单纯疱疹病毒1&2型,人乳头瘤病毒6型和11型)。放大控制(AC)用于监测在PCR扩增过程中有抑制剂的存在和提取的DNA量是否足够。放大控制信号不存在表示在PCR扩增中有抑制剂或DNA量不足(或不存在检体)。梅毒螺旋体(TP),可以提供作为阳性对照(PC),其含有的正模板核酸分子来监测PCR试剂的性能。图10b示出了性病试剂盒阵列的一个例子。图11示出了一个血栓形成倾向试剂盒阵列的实施例。图12示出了一个血栓形成倾向试剂盒阵列的实施例,以及其测试结果的诠释。技术实现要素:以下术语用于描述本发明。如没有阐述特定定义,用于描述本发明的术语应当给予由普通技术人员所理解的普通含义。如本文所述,“等位特异寡核苷酸探针-反向点杂交(ASO-RDB)”指的是使用能够通过杂交方法捕获在固体中的ASO-RDB靶分子的检测。如本文所用的术语“导流杂交”指的是利用在美国专利号5,741,647中描述的技术的杂交过程。如本文所用的术语“导流杂交设备”或“导流装置”指的是在美国专利号6,020,187中所描述的设备和/或在PCT申请号WO/2011/139,750中所描述的侧向液流装置或随后设计的任何导流装置。检测病原体和目标DNA本发明提供的方法、引物、探针和试剂盒用于检测各种核酸、突变、物质、和病原体/或疾病。在一个实施方案中,本发明应用于检测结核病、乙型肝炎、丙型肝炎、SARS、呼吸道感染病毒、性病病原体、β-珠蛋白、血栓形成倾向和/或有关核酸的存在(单独一种或多种)。所述方法的PCR使用特异性引物来产生扩增产物,所述扩增产物与寡核苷酸探针杂交。所得杂交谱将反映核酸、基因突变、物质、病原体和/或疾病的存在。在一个实施方案中,扩增产物和寡核苷酸探针的杂交采用导流方法、横向导流方法或逆向导流方法。在一个实施方案中,用于杂交的寡核苷酸探针是被固定在膜的。在导流方法的实施方案中,杂交的敏感性取决于包括所述探针阵列的膜的总面积。在横向导流方法的实施方案中,杂交的敏感性取决于包括所述探针跨越流动方向上的膜的总截面面积。在一个实施方案中,本发明提供了一种用于检测核酸和/或外源物质的存在的方法,包括以下步骤:(a)扩增来自受试者样品中的核酸模板核酸分子,其中引物选自序列号为:174-181,201-205,241-244,263-286和299-306,以产生单独一种或多种扩增产物;和(b)所述扩增产物与寡核苷酸探针杂交,探针包括选自序列号182-200,206-240,245-260,287-298,和307-314,以单独一种或多种寡核苷酸探针来产生杂交谱,示出目标核酸和/或外源物质是否存在于受试者样品。在一个实施方案中,所选择引物的数量为2-49;所选定探针的数目是2-92。在另一个实施方案中,所选定引物的数量为2-24;所选定探针的数目是2-35。在另一个实施方案中,本发明提供了一种方法用于检测样品中是否存在核酸和/或外源物质,所述方法包括以下步骤:(a)扩增来自受试者样品中的模板核酸分子,其中所用引物选自序列号为:174-181,201-205,241-244,263-286和299-306,以产生足够的单独一种或多种扩增产物;和(b)所述扩增产物与寡核苷酸探针杂交,探针包括选自序列号182-200,206-240,245-260,287-298,和307-314,以单独一种或多种寡核苷酸探针来产生杂交谱,示出目标核酸和/或外源物质是否存在于受试者样品。在一个实施例中,本发明提供了一种用于检测多重耐药性结核分枝杆菌(DR-MTB)或其核酸的方法,所述方法包含以下步骤:(a)获得包含模板核酸分子的样本;(b)使用选自引物序列号为174-181的引物扩增所述模板核酸分子,从而得到扩增产物;和(c)将所得的扩增产物与选自序列号为182-200的寡核苷酸探针杂交,所得杂交结果显示多重耐药性结核菌(DR-MTB)或其核酸是否存在。在一个实施例中,本发明提供了一种用于检测多重耐药性结核分枝杆菌(DR-MTB)或其核酸的方法,所述方法包含以下步骤:(a)获得包含模板核酸分子的样本;(b)使用序列号为174-181的引物扩增所述模板核酸分子,从而得到扩增产物;和(c)将所得的扩增产物与序列号为182-200的寡核苷酸探针杂交,所得杂交结果显示多重耐药性结核菌(DR-MTB)或其核酸是否存在。在一个实施方案中,引物包含一个产生信号的标签。在一个实施例中,所述扩增产物通过导流方法,横向导流方法或逆向导流方法和/或有关设备与多个寡核苷酸探针杂交。在一个实施例中,上述方法可以检测多重耐药性结核分枝杆菌的存在(DR-MTB),或具有以下一种或多种DR-MTB突变的核酸:rpoB基因的七个突变之一;katG基因两个突变之一;和inhA基因的一个突变。本发明还提供了一种试剂盒,用于检测多重耐药性结核分枝杆菌的存在(DR-MTB)或其核酸,试剂盒包含选自由序列号为182-200的引物和选自序列号为174-181的寡核苷酸探针。在一个实施例中,试剂盒用于检测多重耐药性分枝杆菌的存在(DR-MTB),或DR-MTB的核酸,试剂盒包含序列号为174-181的引物和序列号为182-200的寡核苷酸探针。本发明还提供了检测患有β-地中海贫血症的受试者其β-球蛋白突变的方法,包含以下步骤:(a)从受试者获得包含模板核酸分子的样本;(b)使用序列号为201-205的引物扩增所述模板核酸分子,从而得到扩增产物;和(c)将所得的扩增产物与选自序列号为206-240的寡核苷酸探针杂交,所得杂交结果显示β-地中海贫血症的基因型。在一个实施例中,检测患有β-地中海贫血症的受试者其β-球蛋白基因突变的方法包含以下步骤:(a)从受试者获得包含模板核酸分子的样本;(b)使用序列号为201-205的引物扩增所述模板核酸分子,从而得到扩增产物;和(c)将所得的扩增产物与序列号为206-240的寡核苷酸探针杂交,所得杂交结果显示β-地中海贫血症的基因型。在一个实施例中,引物包含一个产生信号的标签。在一个实施症中,所述扩增产物通过导流方法,横向导流方法,或逆向导流方法和/或有关设备与多个寡核苷酸探针杂交。在一个实施例中,上述检测β-球蛋白突变的方法可以检测出21个β-球蛋白的突变之一。本发明也提供用于检测β-球蛋白基因突变的试剂盒,试剂盒包含选自序列号为201-205的引物和选自序列号为206-240的寡核苷酸探针。在一个实施例中,用于检测β-球蛋白的突变的试剂盒含序列号为201-205的引物和序列号为206-240的寡核苷酸探针。本发明还提供了一种用于检测乙型肝炎病毒或其核酸的方法,步骤包含:(a)获得包含模板核酸分子的样本;(b)使用选自序列号为241-244的引物扩增所述模板核酸分子,从而得到乙型肝炎病毒的扩增产物;和(c)将所得的扩增产物与选自序列号为245-260的寡核苷酸探针杂交,所得杂交结果显示乙型肝炎病毒或其核酸是否存在。在一个实施例中,用于检测乙型肝炎病毒或其核酸的方法包含以下步骤:(a)获得包含模板核酸分子的样本;(b)使用序列号为241-244的引物扩增所述模板核酸分子,从而得到扩增产物;和(c)将所得的扩增产物与序列号为245-260的寡核苷酸探针杂交,所得杂交结果显示乙型肝炎病毒或其核酸是否存在。在一个实施例中,引物包含一个产生信号的标签。在一个实施例中,所述扩增产物通过导流方法,横向导流方法或逆向导流方法和/或有关设备与多个寡核苷酸探针杂交。在一个实施方案中,上述方法可以检测乙型肝炎病毒或其核酸,所述乙型肝炎病毒选自基因型A到H。本发明还提供了一种用于检测乙型肝炎病毒或其核酸的试剂盒,包含选自序列号为241-244的引物和序列号为245-260的寡核苷酸探针。在一个实施例中,用于检测乙型肝炎病毒或其核酸的试剂盒包含序列号为241-244的引物和序列号为245-260的寡核苷酸探针。本发明还提供了一种方法,用于检测受试者是否存在性病病原体或其核酸,所述方法包含以下步骤:(a)从所述受试者获得包含模板核酸分子的样本;(b)使用选自序列号为263-286的引物扩增所述模板核酸分子,从而得到扩增产物;和(c)将所得的扩增产物与选自序列号为287-298的寡核苷酸探针杂交,所得杂交结果显示样本是否存在来自或会引起性病的病原体的核酸。在一个实施例中,本发明提供了一种方法,用于检测受试者是否存在性病病原体或其核酸,包含以下步骤:(a)从所述受试者获得包含模板核酸分子的样本;(b)使用序列号为263-286的引物扩增所述模板核酸分子,从而得到扩增产物;和(c)将所得的扩增产物与序列号为287-298的寡核苷酸探针杂交,所得杂交结果显示样本是否存在来自或会引起性病的病原体的核酸。在一个实施例中,引物包含一个产生信号的标签。在一个实施例中,所述扩增产物通过导流方法,横向导流方法或逆向导流方法和/或有关设备与多个寡核苷酸探针杂交。在一个实施例中,用于检测受试者中性病病原体的方法可以检测以下性病病原体:阴道毛滴虫,沙眼衣原体,淋病奈瑟菌,生殖支原体,人型支原体,解脲支原体,解孢子虫,梅毒螺旋体,单纯疱疹病毒1型,单纯疱疹病毒2型,人乳头瘤病毒6型,和人乳头瘤病毒11型。本发明还提供了一种用于检测受试者中性病病原体或其核酸的存在的试剂盒,所述试剂盒包含选自序列号为263-286的引物和选自序列号为287-298的寡核苷酸探针。在一个实施例中,用于检测受试者样品中性病病原体或其核酸的试剂盒包含序列号为263-286的引物和序列号为287-298的寡核苷酸探针。本发明提供了用于检测与血栓形成倾向有关的基因突变的方法,所述方法包含以下步骤:(a)获得包含模板核酸分子的样本;(b)使用选自序列号为299-306的引物扩增所述模板核酸分子,从而得到扩增产物;和(c)将所得的扩增产物与选自序列号为307-314的寡核苷酸探针杂交,所得杂交结果显示与血栓形成倾向有关的基因突变是否存在。在一个实施例中,所述引物包含一个产生信号的标签。在另一个实施例中,所述方法用于检测与血栓形成倾向有关的基因突变,所述方法包含以下步骤:(a)获得包含模板核酸分子的样本;(b)使用序列号为299-306的引物扩增所述模板核酸分子,从而得到扩增产物;和(c)将所得的扩增产物与序列号为307-314的寡核苷酸探针杂交,所得杂交结果显示与血栓形成倾向有关的基因突变是否存在。在一个实施例中,所述引物包含一个产生信号的标签。在一个实施例中,所述扩增产物通过导流方法,横向导流方法,逆向导流方法和/或有关设备与多个寡核苷酸探针杂交。在一个实施例中,所述方法用于检测与血栓形成倾向有关的基因突变,所述基因选自莱顿凝血第五因子FactorVLeiden(FVL),凝血酶原FactorII(FII或凝血第二因子),和亚甲基四氢叶酸还原酶MethylenetetrahydrofolateReductase(MTHFR)。本发明还提供了用于检测与血栓形成倾向有关的基因突变的试剂盒,所述试剂盒包含选自序列号为299-306的引物和选自序列号为307-314的寡核苷酸探针。在一个实施例中,所述试剂盒包含序列号为299-306的引物和序列号为307-314的寡核苷酸探针。通过引用以下的实验细节,可以更好地理解本发明。然而,本领域技术人员应理解所提供的实施例仅作为说明作用,而非限制本发明的范围。本发明的范围将由随后的权利要求所界定。在本申请中的,引用了不同的参考文献或出版物。这些参考或出版物的全文和公开都结合到本申请中,从而更全面地描述本发明的情况。应当指出的是,过渡语“包含”与“包括”﹑“含有”或“以…为特征”是同义的,是包括性或开放式的,当中并不排除有另外未列举的元素或方法步骤。实施例1测试程序用于DNA,PCR扩增,杂交,检测样品及结果分析的分离步骤,如WO/2011/139750或已知为本领域技术人员在有关的程序和技术可以应用到本发明。各种内部对照(IC)可以包括在所述测试试验,以验证DNA样品,PCR扩增和结果显色。各个导流膜阵列的大小和格式,可用于根据个体的需要,或用于优化反应室的使用,以达到最大化的节约成本。实施例2基因分型耐多药结核病在一个实施方案中,本发明提供了DR-MTB基因分型的方法和试剂盒。所述方法与试剂盒采用聚合酶链反应(PCR)和“导流”杂交技术,用于检测对利福平(RIF)和异烟肼(INH)有耐药性的结核分支杆菌(MTB)。用于扩增rpoB基因,katG基因和INHA基因的相应引物已被证实没有与人类基因组有交叉反应。RS-IAC是一个内部控制引物,不针对人类或MTB基因组,用于监测PCR扩增过程。所用探针检测耐药性的基因突变包括rpoB基因(D516V,D516G,H526D,H526Y,H526L1,S531L和S531W),katG基因(S315T1和S315T2),和inhA基因(-15TC/T)。也有五个探针用于检测野生型MTB的突变,这有助于验证rpoB基因,katG基因和inhA基因的PCR扩增反应是否已完成。在一个实施方案中,引物被生物素化以便进行杂交。在一个实施方案中,本发明提供了用于检测多重耐药结核分枝杆菌(DR-MTB)的方法,包括以下步骤:(a)获得包含模板核酸分子的样品;(b)与选自序列号为:174-181的引物,扩增所述模板核酸分子,从而产生扩增产物;和(c)扩增产物与选自序列号为:182-200的寡核苷酸探针所组成的组杂交,所得杂交谱将显示多重耐药结核分枝杆菌的存在。在一个实施方案中,本发明可以检测多重耐药性结核分枝杆菌,并具有下列其中一个或多个突变的存在:rpoB基因中的七个突变;katG基因中的两个突变;inhA基因中的一个突变。在一个实施方案中,扩增产物是通过导流方法,横向导流方法,或逆向导流方法,与多个寡核苷酸探针的杂交。图3示出了一个DR-MTB匣子(左图)和探头和信号(右图)的各个位置体现。IAC是内部放大控制,以监测PCR扩增过程。HC是杂交控制,监测杂交过程。图4示出了一个用于检测DR-MTB阵列配置的实施方案。在一个实施方案中,分别对RIF和异烟肼有耐药性的MTB株被检测出来。在另一个实施方案中,对RIF和INH有耐药性(多重耐药性)的MTB菌株被检测出来。在一个实施方案中,既不是耐利福平(RIF),也不是耐异烟肼(INH)的MTB菌株被检测出来。检测包含各种控制。引物引物ID引物序列(5'-3')5'修饰序列号MTB-DR-Rpob-FTCAACATCCGGCCGGTGGTC生物素174MTB-DR-Rpob-RCCGGCACGCTCACGTGACAGA生物素175MTB-DR-KatG-FTGGCACCGGAACCGGTAAGGA生物素176MTB-DR-KatG-RCGCCAGCAGGGCTCTTCGT177MTB-DR-inhA-FAAGTTCCCGCCGGAAATCGCAG生物素178MTB-DR-inhA-RCCGGTAACCAGGACTGAACGGGAT179RS-IAC-FCGAGTTCCCGCCCATAACC180RS-IAC-RGGAAGTTGCAACGCCGTCC生物素181探针探针ID探针序列(5'-3')5'修饰序列号MTB-DR-Rpob-CTRLGCTGGTGCCGAAGAA胺基182MTB-DR-KatG-CTRLCGGGGTGTTCGTCCATAC胺基183MTB-DR-inhA-CTRLGGTATGTCCACGAGCGTAAC胺基184MTB-DR-Rpob-WTcGGTTGTTCTGGTCCATG胺基185MTB-DR-Rpob-WteTGACCCACAAGCGCCGA胺基186MTB-DR-Rpob-WtfGACTGTCGGCGCTGG胺基187MTB-DR-KatG-WTGATGCCGCTGGTGATCG胺基188MTB-DR-inhA-WTAACCTATCGTCTCGCCG胺基189MTB-DR-Rpob-MUTc1GGTTGTTCTGGACCATGA胺基190MTB-DR-Rpob-MUTc2GGTTGTTCTGGCCCATG胺基191MTB-DR-Rpob-MUTe1GACCGACAAGCGCCGA胺基192MTB-DR-Rpob-MUTe2GCGCTTGTAGGTCAACC胺基193MTB-DR-Rpob-MUTe3GCGCTTGAGGGTCAAC胺基194MTB-DR-Rpob-MUTf1CCCCAGCGCCAACAGT胺基195MTB-DR-Rpob-MUTf2GACTGTGGGCGCTGG胺基196MTB-DR-KatG-MUT1GATGCCGGTGGTGATC胺基197MTB-DR-KatG-MUT2GATGCCTGTGGTGATCG胺基198MTB-DR-inhA-MUT1CAACCTATCATCTCGCCG胺基199RS-IAC-PCTCGAATGCCTCGTATCAT胺基200下面是一些用于PCR和杂交的示例:杂交协议的一个实施例:实施例3β地中海基因分型本发明提供了一种系统的β-球蛋白基因突变的检测,所述基因突变包括TATA-28(A>G),TATA-29(A>G),起始密码子(G>A),密码子5(-CT)的检测,密码子8/9(+G),密码子15(G>A),密码子16(-C),密码子17(A>T),密码子19(A>G),密码子26(G>A)(血红蛋白E),密码子27/28(+三),密码子为30G>C,IVS1.1(G>T),IVS1.1(G>A),IVS1.5(G>C),密码子41/42(-TCTT),密码子43(G>T),密码子71/72(+A),IVS2.1(G>A),IVS2.654(C>T)和619bp的缺失。本发明还提供了检测受试者样品中β-球蛋白突变的方法,所述方法包括以下步骤:(a)从受试者获得包含模板核酸分子的样品;(b)与选自序列号为:201-205的引物所组成的组扩增所述模板核酸分子,从而产生扩增产物;和(c)扩增产物与选自序列号为:206-240的寡核苷酸探针所组成的组杂交,所得杂交谱将表明β-地中海贫血的基因型。在一个实施方案中,引物包括一个信号产生标签。在一个实施方案中,扩增产物通过导流方法,横向导流方法,或逆向导流方法,与多个寡核苷酸探针杂交。在一个实施方案中,上述方法球以检测21种β-珠蛋白突变之中的任何其中一种。图5示出了一种β-地中海贫血匣子和其信号位置(图中格线仅供说明用途)的实施方案。图6a示出了不同β-地中海贫血基因型的一个例子。图6b示出关于使用β-地中海贫血匣子各种临床样品的测试结果,表明本发明能从人类样品中识别β-地中海贫血的基因型。引物序列(加入号AF007546.1):引物ID方向5'修饰引物序列(5'到3')序列号HBB引物1正向引物生物素GTACGGCTGTCATCACTTAGACCTCA201HBB引物2反向引物生物素TTATCCCCTTCCTATGACATGAAC202HBB引物3正向引物生物素GTGTACACATATTGACCAAA203HBB引物4反向引物生物素GCAAGAAAGCGAGCTTAG204HBB引物5反向引物生物素GTATCTCTAAGCAAGAGAAC205探针序列(加入号AF007546.1):探针ID有义/反义链5'修饰探针序列(5'到3')序列号HBB2-A1有义链胺基AGACACCATGGTGCATCTG206HBB2-A1a有义链胺基AGACACCATGGTGCACCT207HBB2-A2有义链胺基CAAACAGACACCAGGGTG208HBB2-A3有义链胺基GCTGGGCATAAAAGTCAGG209HBB2-A4反义链胺基CCTGACTTCTATGCCCAGC210HBB2-A5反义链胺基CCCTGACTTTCATGCCC211HBB2-B1有义链胺基GCATCTGACTCCTGAGGA212HBB2-B1a有义链胺基GCACCTGACTCCTGAGG213HBB2-B2反义链胺基ACTTCTCCTCGAGTCAGAT214HBB2-B3反义链胺基CAGGGCCTCACCACCA215HBB2-B4有义链胺基GTTGGTGGTAAGGCCCT216HBB2-B5反义链胺基CCAGGGGCCTCACCA217HBB2-C1有义链胺基AGGAGAAGTCTGCCGTTACT218HBB2-C2有义链胺基AGGAGAAGGTCTGCCGTTA219HBB2-C3有义链胺基GAGGTTCTTTGAGTCCTTTGG220HBB2-C4反义链胺基CAAAGGACTCAACCTCTGG221HBB2-C5有义链胺基CCCAGAGGTTCTTTTAGTC222HBB2-D1有义链胺基TGTGGGGCAAGGTGAAC223HBB2-D2有义链胺基CCGTTACTGCCCTGTAGG224HBB2-D3有义链胺基CTGTGGGGAAGGTGAAC225HBB2-D4反义链胺基TGTGGGGCTAGGTGAACG226HBB2-D5反义链胺基CTTCATCCACGCTCACCT227HBB2-E1反义链胺基TGATACCAACCTGCCCAG228HBB2-E2有义链胺基CTGGGCAGATTGGTATCA229HBB2-E3有义链胺基CCCTGGGCAGTTTGGTATC230HBB2-E4有义链胺基GCAGGTTGCTATCAAGGTTAC231HBB2-E5反义链胺基ATACCAACGTGCCCAGG232HBB2-F1有义链胺基GGTGCCTTTAGTGATGGC233HBB2-F2有义链胺基TCGGTGCCTTTAAGTGATG234HBB2-F3有义链胺基TGGGTTAAGGCAATAGCAATAT235HBB2-F4反义链胺基ATATTGCTATTACCTTAACCC236HBB2-G1有义链胺基CATACCTCTTATCTTCCTCC237HBB2-G2有义链胺基TGTAACAAGTAGAGATTCAAGTA238HBB2-G3有义链胺基GAACTTCAGGGTGAGTCTAT239HBB2-G4反义链胺基GAACTTCAGGATGAGTCTATG240下面是一些用于PCR和杂交的示例协议:杂交协议的一个实施例:数据解读为β球突变:实施例4乙型肝炎病毒基因分型本发明还提供了一种用于检测乙型肝炎病毒的方法,所述方法包括步骤:(a)获得包含模板核酸分子的样品;(b)用选自序列号为:241-244的引物所组成的组扩增所述模板核酸分子,从而产生扩增产物;和(c)扩增产物与选自序列号为:245-260的寡核苷酸探针所组成的组杂交,所得杂交谱将显示乙型肝炎病毒的存在。在一个实施方案中,引物包括一个信号产生标签。在一个实施方案中,扩增产物通过导流方法,横向导流方法,或逆向导流方法,与多个寡核苷酸探针杂交。在一个实施方案中,通用探针序列号257被用于捕获各种基因型的乙型肝炎病毒的核酸。图7示出了一个的乙型肝炎病毒试剂盒所检测的8个乙型肝炎病毒基因型(乙型肝炎病毒的A,B,C,D,E,F,G和H型)的实施例。图8示出了检测不同乙型肝炎病毒基因型的一个例子。引物序列:探针序列:乙型肝炎病毒阳性对照序列[560bp](pUC57载体):TGGGATTCTATATAAGAGGGAAACTACACGTAGCGCCTCATTTTGCGGGTCACCATATTCTTGGGAACAAGAGCTACATCATGGGAGGTTGGTCATCAAAACCTCGCAAAGGCATGGGGACGAACCTTTCTGTTCCCAACCCTCTGGGATTCTTTCCCGATCATCAGTTGGACCCTGCATTCGGAGCCAATTCAAACAATCCAGATTGGGACTTCAACCCCATCAAGGACCACTGGCCACAAGCCAACCAGGTAGGAGTGGGAGCATTCGGGCCAGGGTTCACTCCCCCACACGGAGGTGTTTTGGGGTGGAGCCCTCAGGCTCAGGGCATATTGGCCACAGTGCCAGCAGTGCCTCCTCCTGCCTCCACCAATCGGCAGTCAGGAAGGCAGCCTACTCCCATCTCTCCACCTCTAAGAGACAGTCATCCTCAGGCCATGCAGTGGAATTCCACAGCTTTCCACCAAGCTCTGCAAGATCCCAGAGTCAGGGGCCTGTATTTTCCTGCTGGTGGCTCCAGTTCAGGAACACTCAACCCTGTTCCAACTATTGCCTCTCAC(序列号261)内部控制序列[500bp](pUC57载体):GAGACAGGTTCGTCCAATCCCGTGCCGCGGCCTTGGCAGGGGGTTCGCAGGCCCCACCCGAAGCGTTGCTGAAGGCTCAGGCCTCTGAGCGACAAAAGCTTTAAACGCGAGTTCCCGCCCATAACCTGGACCGAATGCGGGACCATGCATCGTTCCACTGTGTTTGTCCCATGTAGGACGGGCGCAAGGCGTGCTTAGCTCAGCCTCGAATGCCTCGTATCATTGTGCACCCGCCGGTCACCAGCCAACGATGTGCGGACGGCGTTGCAACTTCCGGGGCCCAACCTGACCGTCCTGGGTACCGCACTCTGGGCAGTGCGAGGTAATGCCAGTCGCCCAGTGCCGAACAACACCTGACCTAACGGTAAGAGGCTCACATAATGGCTCCGCCGGCGCGCCCAGGGTACATTAGGTCAGCATCGGATGGACTGACATGAACCTTCACACCGAAGCGGAAACGGGTGCGTGGACCAGCGAGGAGCAAACGAAAATTCCTGGCC(序列号262)以下是一些PCR协议和杂交协议的示例:成分容量(μL)乙型肝炎病毒引物预混合19.6IAC0.1Taq聚合酶0.3模板核酸分子5.0*无核酸酶水可变总计25.00*建议血清中总乙型肝炎病毒病毒DNA的多于4000IU/mL.这种温度曲线适用于应用生物系统公司珀金埃尔默(ABI-PE)9600,基因扩增PCR系统9700,Veriti(AppliedBiosystems公司),PTC-200(MJ研究)。杂交协议的一个实施例:实施例5基因分型,并同时检测多种性病病原体在一个实施方案中,本发明提供检测性病病原体的方法,所述病原体包括但不局限于,原生动物,细菌和病毒。在一个实施方案中,性病病原体存在于尿液,泌尿生殖系统拭子(尿道,阴道,子宫颈和损伤)和液基细胞学标本(PreservCytTM和SurePathTM)。在一个实施方案中,放大控制(AC)包括用于检测人类DNA的材料。用PCR扩增尿泌尿生殖系统拭子(尿道,阴道,子宫颈和损伤)和液基细胞学标本(PreservCytTM和SurePathTM)中提取的靶DNA,再通过杂交,达至更快速,更灵敏和更特异地检测性病。在一个实施方案中,所述方法可以检测的12种常见的性病病原体,包括1种原生动物(阴道毛滴虫),7种菌(沙眼衣原体,淋病奈瑟菌,生殖支原体,人型支原体,解脲支原体,解孢子虫,梅毒螺旋体)和4种病毒(单纯疱疹病毒1型&2型,人乳头瘤病毒6型和11型)。这些病原体都与子宫颈炎,尿道炎,滴虫病和盆腔炎有关。在另一个实施方案中,测试中包括有通用引物(S)和/或放大控制。本发明还提供了一种方法,用于检测受试者样品中存在的性病病原体,所述方法的步骤包括:(a)从受试者获得包含模板核酸分子的样品;(b)通过选自序列号为:263-286的引物所组成的组,扩增所述模板核酸分子,从而产生扩增产物;和(c)扩增产物与选自序列号为:287-298的寡核苷酸探针杂交,所得杂交谱将显示有核酸片段来源于性病病原体。在一个实施方案中,引物包括一个信号产生标签。在一个实施方案中,与多个寡核苷酸探针的扩增产物的杂交是在一个导流方法,横向导流方法或逆向导流方法和/或有关设备。序列号263-284的引物由两部分组成:5'部分是人工合成的核酸序列,和目标病原体并不同源,也没涉及任何可在人类中可找到的生物体的序列;3'部分是病原体特异性序列,使引物能有效结合到相应病原体的核酸,以产生扩增产物。所有引物序列的5'部分是通用序列。通用引物序列设计是经过深思熟虑和实验的,能排除扩增样本中的其他生物体,例如其他病原体和人类基因组的任何脱氧核糖核酸(图1)。诸如那些在本发明中公开的被选择验证为特定通用序列然后与各种病原体特异性序列合并,得到病原体特异性引物,其能够产生包含通用序列的扩增产物。这些扩增产物成为第二次PCR的模板核酸分子,然后再使用序列号为:285和286的通用引物以相同效率扩增所有模板核酸分子。因此线性产生的扩增产物最终浓度会和初始靶DNA的浓度成正比。就算样本中目标拷贝数低,仍然可以放大以达到相当浓度再检出阳性,使用通用引物可以纠正错误,大幅提高灵敏度。在一个实施方案中,两步骤的PCR反应在单一试管中进行;其中的病原体特异性引物通过其基因特异性3'区域结合到目标分子,以产生含有5'通用序列的初始扩增产物。这些扩增产物作为所述第二组引物(通用引物)的模板核酸分子,以产生含有信号的扩增产物并通过杂交被检测出来。图2示出一个扩增方案的实施例。由于本发明使用通用引物,因此比市场上其他性病病原体试剂盒的检测方法更准确、更灵敏。正如图9a所示,本发明能检测低至50-300个性病病原体拷贝数,而另一个制造厂的试剂盒的检测至少要有500个性病病原体拷贝数;因此本发明能够检测有较低病原体浓度的样品。图9b示出了本发明和市场上其他性病检试剂盒的性能比较。结果通过定量PCR(qPCR)确认四个测试和实际基因型。确认病原体的基因型后,本发明(如图中试验3和4)比其他试剂盒较少出现错误结果(如图中试验1和2)。另外,本发明可检测多种病原体(如图9b所示出),因此,与市场上其他试剂盒相比,本发明同时检测12种病原体为最高的数目。感染HPV6和HPV11后的发病率很高,因此本发明对HPV6型和11型的覆盖是非常有用的。生殖器疣是一种具有高度传染力的性病,其中90%的病例是由于感染HPV6和HPV11所引起。图10a示出了一个检测性病阵列的实施例,阵列可检测12种常见性病病原体的存在:1种原生动物(阴道毛滴虫),7种菌(沙眼衣原体,淋病奈瑟菌,生殖支原体,人型支原体,解脲支原体,解孢子虫,梅毒螺旋体)和4种病毒(单纯疱疹病毒1型和2型,人乳头瘤病毒6型和11型)。放大控制(AC)示出结果是否有效。图10b示出了一个解释性病阵列的例子。在一个实施方案中,原生动物、细菌和病毒被分别检测。在另一个实施方案中,原生动物、细菌和病毒(多重感染)被同时检测。在一个实施方案中,梅毒螺旋体(TP)的模板核酸分子被提供为阳性对照(PC)以用于监测PCR试剂的性能。如果一个测试中不出现TP的阳性对照(PC)信号,这可能是因为所述DNA因长期贮存或核酸酶受污染而已经退化。然而,如果测试样品产生的阳性信号为任何病原体,检测结果仍然是有效的。在阳性对照(PC)的测试,由于正对照样品仅包含梅毒螺旋体(TP),但没有内源性的人基因组DNA,将导致缺乏AC信号。在阳性对照的AC信号的存在(PC)的测试表明对照测试是无效的,这可能是由于污染和试验应所述重复。如AC信号不出现,这表示测试样品中的DNA量不足或不存在。然而,如果测试样品产生任何病原体的阳性信号,测试仍然是有效的。由于可能有来自其他病原体DNA的竞争,在一些样品中AC信号可能不出现。在这种情况下,只要阵列上有一个或多个正信号,检测结果仍然是有效的。在另一个实施方案中,在导流过程中使用的阵列盒和/或装置有不同的形式和尺寸。除了使用10个点的阵列外,也可用35点阵列,也可再加阵列点以用于检测例如额外的病原体基因亚型和/或耐药菌株的基因突变。检测信号也可通过使用伴随FT-Pro杂交设备的影像系统以达至数字化。在另一个实施方案中,所用杂交装置是一个自动化装置,有结合分析与数字化功能。本发明比市场上现有的检测方法和试剂盒更为便利,因本发明可同时扩增和检测多个目标,具有高灵敏度并涵盖12种性病病原体,包括被市场上大部分现有试剂盒所排除在外的HPV亚基因型。通过与导流杂交联接,本发明允许快速灵敏和高通量的性病病原体检测。引物序列:探针序列:下面是一些示例PCR和杂交协议:成分容量(μL)PCR预混合18.6性病引物预混合1.0DNATaq聚合酶0.4性病DNA正控制最多5.0*无核酸酶水可变总计25.0*总DNA的建议的范围:5ng–100ng.以上热循环程序是适合用于ThermalCycler(Lifetechnologies)和S1000TMThermalCycler(Bio-rad)。以上热循环程序可经修改后用于其它热循环仪(斜坡率达3℃/秒)。杂交协议的一个实施例:实施例6血栓形成倾向的有关基因分型本发明还提供了用于检测与血栓形成倾向有关的基因突变的方法,所述方法包含以下步骤:(a)获得包含模板核酸分子的样本;(b)使用选自序列号为299-306的引物扩增所述模板核酸分子,从而得到扩增产物;和(c)将所得的扩增产物与选自序列号为307-314的寡核苷酸探针杂交,所得杂交结果显示与血栓形成倾向有关的基因突变是否存在。在一个实施例中,所述引物包含一个产生信号的标签。在一个实施例中,所述扩增产物通过导流方法、横向导流方法或逆向导流方法与多个寡核苷酸探针杂交。在一个实施例中,上述方法可以检测选自莱顿凝血第五因子FactorVLeiden(FVL),凝血酶原FactorII(FII或凝血第二因子),和亚甲基四氢叶酸还原酶MethylenetetrahydrofolateReductase(MTHFR)的基因突变。图11示出了一个血栓形成倾向试剂盒阵列的实施例。图12示出了血栓形成倾向试剂盒其测试结果的一个诠释例子。引物序列:探针序列:探针探针序列(5'-3')5'修饰序列号FVL_WTGGACAGGCGAGGAAT胺基307FVL_MUTTGGACAGGCAAGGAAT胺基308FII_WTTCTCAGCGAGCCTC胺基309FII_MUTACTCTCAGCAAGCC胺基310MTH677_WTCGGGAGCCGATTTCA胺基311MTH677_MUTATGATGAAATCGACTCC胺基312MTH1298_WTCAGTGAAGAAAGTGTCT胺基313MTH1298_MUTGACCAGTGAAGCAAGTG胺基314反应混合液:成分容量(μL)ThrombophiliaPCR预混合21.6Thrombophilia引物预混合1.0酶混合液0.4模板核酸分子最多2.0无核酸酶水可变总计25.00*DNA总量的建议的范围:10ng–100ng。杂交程序的一个实施例:序列表<110>达雅高生物科技有限公司<120>快速并灵敏基因型鉴定及核酸检测<130>897-F-PCT-CN<140><141><150>PCT/CN2014/000275<151>2014-03-17<150>61/791,933<151>2013-03-15<160>141<210>174<211>20<212>DNA<213>人工序列<220><223>引物<400>174tcaacatccggccggtggtc20<210>175<211>21<212>DNA<213>人工序列<220><223>引物<400>175ccggcacgctcacgtgacaga21<210>176<211>21<212>DNA<213>人工序列<220><223>引物<400>176tggcaccggaaccggtaagga21<210>177<211>19<212>DNA<213>人工序列<220><223>引物<400>177cgccagcagggctcttcgt19<210>178<211>22<212>DNA<213>人工序列<220><223>引物<400>178aagttcccgccggaaatcgcag22<210>179<211>24<212>DNA<213>人工序列<220><223>引物<400>179ccggtaaccaggactgaacgggat24<210>180<211>19<212>DNA<213>人工序列<220><223>引物<400>180cgagttcccgcccataacc19<210>181<211>19<212>DNA<213>人工序列<220><223>引物<400>181ggaagttgcaacgccgtcc19<210>182<211>15<212>DNA<213>人工序列<220><223>探针<400>182gctggtgccgaagaa15<210>183<211>18<212>DNA<213>人工序列<220><223>探针<400>183cggggtgttcgtccatac18<210>184<211>20<212>DNA<213>人工序列<220><223>探针<400>184ggtatgtccacgagcgtaac20<210>185<211>17<212>DNA<213>人工序列<220><223>探针<400>185ggttgttctggtccatg17<210>186<211>17<212>DNA<213>人工序列<220><223>探针<400>186tgacccacaagcgccga17<210>187<211>15<212>DNA<213>人工序列<220><223>探针<400>187gactgtcggcgctgg15<210>188<211>17<212>DNA<213>人工序列<220><223>探针<400>188gatgccgctggtgatcg17<210>189<211>17<212>DNA<213>人工序列<220><223>探针<400>189aacctatcgtctcgccg17<210>190<211>18<212>DNA<213>人工序列<220><223>探针<400>190ggttgttctggaccatga18<210>191<211>17<212>DNA<213>人工序列<220><223>探针<400>191ggttgttctggcccatg17<210>192<211>16<212>DNA<213>人工序列<220><223>探针<400>192gaccgacaagcgccga16<210>193<211>17<212>DNA<213>人工序列<220><223>探针<400>193gcgcttgtaggtcaacc17<210>194<211>16<212>DNA<213>人工序列<220><223>探针<400>194gcgcttgagggtcaac16<210>195<211>16<212>DNA<213>人工序列<220><223>探针<400>195ccccagcgccaacagt16<210>196<211>15<212>DNA<213>人工序列<220><223>探针<400>196gactgtgggcgctgg15<210>197<211>16<212>DNA<213>人工序列<220><223>探针<400>197gatgccggtggtgatc16<210>198<211>17<212>DNA<213>人工序列<220><223>探针<400>198gatgcctgtggtgatcg17<210>199<211>18<212>DNA<213>人工序列<220><223>探针<400>199caacctatcatctcgccg18<210>200<211>19<212>DNA<213>人工序列<220><223>探针<400>200ctcgaatgcctcgtatcat19<210>201<211>26<212>DNA<213>人工序列<220><223>引物<400>201gtacggctgtcatcacttagacctca26<210>202<211>24<212>DNA<213>人工序列<220><223>引物<400>202ttatccccttcctatgacatgaac24<210>203<211>20<212>DNA<213>人工序列<220><223>引物<400>203gtgtacacatattgaccaaa20<210>204<211>18<212>DNA<213>人工序列<220><223>引物<400>204gcaagaaagcgagcttag18<210>205<211>20<212>DNA<213>人工序列<220><223>引物<400>205gtatctctaagcaagagaac20<210>206<211>19<212>DNA<213>人工序列<220><223>探针<400>206agacaccatggtgcatctg19<210>207<211>18<212>DNA<213>人工序列<220><223>探针<400>207agacaccatggtgcacct18<210>208<211>18<212>DNA<213>人工序列<220><223>探针<400>208caaacagacaccagggtg18<210>209<211>19<212>DNA<213>人工序列<220><223>探针<400>209gctgggcataaaagtcagg19<210>210<211>19<212>DNA<213>人工序列<220><223>探针<400>210cctgacttctatgcccagc19<210>211<211>17<212>DNA<213>人工序列<220><223>探针<400>211ccctgactttcatgccc17<210>212<211>18<212>DNA<213>人工序列<220><223>探针<400>212gcatctgactcctgagga18<210>213<211>17<212>DNA<213>人工序列<220><223>探针<400>213gcacctgactcctgagg17<210>214<211>19<212>DNA<213>人工序列<220><223>探针<400>214acttctcctcgagtcagat19<210>215<211>16<212>DNA<213>人工序列<220><223>探针<400>215cagggcctcaccacca16<210>216<211>17<212>DNA<213>人工序列<220><223>探针<400>216gttggtggtaaggccct17<210>217<211>15<212>DNA<213>人工序列<220><223>探针<400>217ccaggggcctcacca15<210>218<211>20<212>DNA<213>人工序列<220><223>探针<400>218aggagaagtctgccgttact20<210>219<211>19<212>DNA<213>人工序列<220><223>探针<400>219aggagaaggtctgccgtta19<210>220<211>21<212>DNA<213>人工序列<220><223>探针<400>220gaggttctttgagtcctttgg21<210>221<211>19<212>DNA<213>人工序列<220><223>探针<400>221caaaggactcaacctctgg19<210>222<211>19<212>DNA<213>人工序列<220><223>探针<400>222cccagaggttcttttagtc19<210>223<211>17<212>DNA<213>人工序列<220><223>探针<400>223tgtggggcaaggtgaac17<210>224<211>18<212>DNA<213>人工序列<220><223>探针<400>224ccgttactgccctgtagg18<210>225<211>17<212>DNA<213>人工序列<220><223>探针<400>225ctgtggggaaggtgaac17<210>226<211>18<212>DNA<213>人工序列<220><223>探针<400>226tgtggggctaggtgaacg18<210>227<211>18<212>DNA<213>人工序列<220><223>探针<400>227cttcatccacgctcacct18<210>228<211>18<212>DNA<213>人工序列<220><223>探针<400>228tgataccaacctgcccag18<210>229<211>18<212>DNA<213>人工序列<220><223>探针<400>229ctgggcagattggtatca18<210>230<211>19<212>DNA<213>人工序列<220><223>探针<400>230ccctgggcagtttggtatc19<210>231<211>21<212>DNA<213>人工序列<220><223>探针<400>231gcaggttgctatcaaggttac21<210>232<211>17<212>DNA<213>人工序列<220><223>探针<400>232ataccaacgtgcccagg17<210>233<211>18<212>DNA<213>人工序列<220><223>探针<400>233ggtgcctttagtgatggc18<210>234<211>19<212>DNA<213>人工序列<220><223>探针<400>234tcggtgcctttaagtgatg19<210>235<211>22<212>DNA<213>人工序列<220><223>探针<400>235tgggttaaggcaatagcaatat22<210>236<211>21<212>DNA<213>人工序列<220><223>探针<400>236atattgctattaccttaaccc21<210>237<211>20<212>DNA<213>人工序列<220><223>探针<400>237catacctcttatcttcctcc20<210>238<211>23<212>DNA<213>人工序列<220><223>探针<400>238tgtaacaagtagagattcaagta23<210>239<211>20<212>DNA<213>人工序列<220><223>探针<400>239gaacttcagggtgagtctat20<210>240<211>21<212>DNA<213>人工序列<220><223>探针<400>240gaacttcaggatgagtctatg21<210>241<211>20<212>DNA<213>人工序列<220><223>引物<400>241acgyagcgcctcattttgtg20<210>242<211>19<212>DNA<213>人工序列<220><223>引物<400>242cactgcatggcctgaggat19<210>243<211>19<212>DNA<213>人工序列<220><223>引物<400>243cgagttcccgcccataacc19<210>244<211>19<212>DNA<213>人工序列<220><223>引物<400>244ggaagttgcaacgccgtcc19<210>245<211>14<212>DNA<213>人工序列<220><223>探针<400>245ccacaagccaacca14<210>246<211>14<212>DNA<213>人工序列<220><223>探针<400>246ccagcagccaacca14<210>247<211>16<212>DNA<213>人工序列<220><223>探针<400>247gccaactcagaaaatc16<210>248<211>16<212>DNA<213>人工序列<220><223>探针<400>248gccaactccgacaatc16<210>249<211>16<212>DNA<213>人工序列<220><223>探针<400>249agaggcaaatcaggta16<210>250<211>16<212>DNA<213>人工序列<220><223>探针<400>250agcggcacaccaggta16<210>251<211>16<212>DNA<213>人工序列<220><223>探针<400>251ccaacaaggacacctg16<210>252<211>16<212>DNA<213>人工序列<220><223>探针<400>252ccaacaaggacccctg16<210>253<211>14<212>DNA<213>人工序列<220><223>探针<400>253ccactggacagaag14<210>254<211>15<212>DNA<213>人工序列<220><223>探针<400>254cagaccatcagctgg15<210>255<211>16<212>DNA<213>人工序列<220><223>探针<400>255gcaaataccaacaatc16<210>256<211>16<212>DNA<213>人工序列<220><223>探针<400>256caacctcgccaccaga16<210>257<211>16<212>DNA<213>人工序列<220><223>探针<400>257gtcaccatattcttgg16<210>258<211>19<212>DNA<213>人工序列<220><223>探针<400>258ctcgaatgcctcgtatcat19<210>259<211>19<212>DNA<213>人工序列<220><223>探针<400>259gttccaactaggaacatca19<210>260<211>19<212>DNA<213>人工序列<220><223>探针<400>260gttccaactaggaacatca19<210>261<211>560<212>DNA<213>人工序列<220><223>HBV阳性对照序列<400>261tgggattctatataagagggaaactacacgtagcgcctcattttgcgggtcaccatattc60ttgggaacaagagctacatcatgggaggttggtcatcaaaacctcgcaaaggcatgggga120cgaacctttctgttcccaaccctctgggattctttcccgatcatcagttggaccctgcat180tcggagccaattcaaacaatccagattgggacttcaaccccatcaaggaccactggccac240aagccaaccaggtaggagtgggagcattcgggccagggttcactcccccacacggaggtg300ttttggggtggagccctcaggctcagggcatattggccacagtgccagcagtgcctcctc360ctgcctccaccaatcggcagtcaggaaggcagcctactcccatctctccacctctaagag420acagtcatcctcaggccatgcagtggaattccacagctttccaccaagctctgcaagatc480ccagagtcaggggcctgtattttcctgctggtggctccagttcaggaacactcaaccctg540ttccaactattgcctctcac560<210>262<211>500<212>DNA<213>人工序列<220><223>内部扩增对照序列<400>262gagacaggttcgtccaatcccgtgccgcggccttggcagggggttcgcaggccccacccg60aagcgttgctgaaggctcaggcctctgagcgacaaaagctttaaacgcgagttcccgccc120ataacctggaccgaatgcgggaccatgcatcgttccactgtgtttgtcccatgtaggacg180ggcgcaaggcgtgcttagctcagcctcgaatgcctcgtatcattgtgcacccgccggtca240ccagccaacgatgtgcggacggcgttgcaacttccggggcccaacctgaccgtcctgggt300accgcactctgggcagtgcgaggtaatgccagtcgcccagtgccgaacaacacctgacct360aacggtaagaggctcacataatggctccgccggcgcgcccagggtacattaggtcagcat420cggatggactgacatgaaccttcacaccgaagcggaaacgggtgcgtggaccagcgagga480gcaaacgaaaattcctggcc500<210>263<211>40<212>DNA<213>人工序列<220><223>引物<400>263gaccacaacgctacgacgctaatcaatgcccgggattggt40<210>264<211>40<212>DNA<213>人工序列<220><223>引物<400>264ttctgcttgtccggctacgatccggagcgagttacgaaga40<210>265<211>40<212>DNA<213>人工序列<220><223>引物<400>265gaccacaacgctacgacgctaacgaggcattgaagcaaag40<210>266<211>40<212>DNA<213>人工序列<220><223>引物<400>266ttctgcttgtccggctacgactgctgtttcaagtcgtcca40<210>267<211>41<212>DNA<213>人工序列<220><223>引物<400>267gaccacaacgctacgacgctactgtggtagataccacacgc41<210>268<211>41<212>DNA<213>人工序列<220><223>引物<400>268ttctgcttgtccggctacgaacaggtaatggcctgtgactg41<210>269<211>43<212>DNA<213>人工序列<220><223>引物<400>269gaccacaacgctacgacgctgttgatgaaaccttaaccccttg43<210>270<211>43<212>DNA<213>人工序列<220><223>引物<400>270ttctgcttgtccggctacgagttgaggggttttccatttttgc43<210>271<211>44<212>DNA<213>人工序列<220><223>引物<400>271gaccacaacgctacgacgctgtcaggatcatcaaatcaattcac44<210>272<211>40<212>DNA<213>人工序列<220><223>引物<400>272ttctgcttgtccggctacgacaacttggataggacggtca40<210>273<211>41<212>DNA<213>人工序列<220><223>引物<400>273gaccacaacgctacgacgctcagagccatcagcccttttca41<210>274<211>42<212>DNA<213>人工序列<220><223>引物<400>274ttctgcttgtccggctacgagaagtttgtcccagttgcggtt42<210>275<211>40<212>DNA<213>人工序列<220><223>引物<400>275gaccacaacgctacgacgctactccatgaagtcggaatcg40<210>276<211>40<212>DNA<213>人工序列<220><223>引物<400>276ttctgcttgtccggctacgacccacgttctcgtagggata40<210>277<211>41<212>DNA<213>人工序列<220><223>引物<400>277gaccacaacgctacgacgctgttggagctggaatagttgct41<210>278<211>41<212>DNA<213>人工序列<220><223>引物<400>278ttctgcttgtccggctacgacagctgatgtaagtgcagcat41<210>279<211>41<212>DNA<213>人工序列<220><223>引物<400>279gaccacaacgctacgacgctccaccatgtactacaaagacg41<210>280<211>38<212>DNA<213>人工序列<220><223>引物<400>280ttctgcttgtccggctacgatggtcgtcccggtgaaac38<210>281<211>42<212>DNA<213>人工序列<220><223>引物<400>281gaccacaacgctacgacgctgtcgaacattggtcttaccctc42<210>282<211>40<212>DNA<213>人工序列<220><223>引物<400>282ttctgcttgtccggctacgatgtgccgtcttcaagtatgc40<210>283<211>40<212>DNA<213>人工序列<220><223>引物<400>283gaccacaacgctacgacgctgaagagccaaggacaggtac40<210>284<211>41<212>DNA<213>人工序列<220><223>引物<400>284ttctgcttgtccggctacgaccttgataccaacctgcccag41<210>285<211>20<212>DNA<213>人工序列<220><223>引物<400>285gaccacaacgctacgacgct20<210>286<211>20<212>DNA<213>人工序列<220><223>引物<400>286ttctgcttgtccggctacga20<210>287<211>19<212>DNA<213>人工序列<220><223>探针<400>287agtgcataaacttctgagg19<210>288<211>20<212>DNA<213>人工序列<220><223>探针<400>288tataaacgcccggcagttac20<210>289<211>20<212>DNA<213>人工序列<220><223>探针<400>289aaagattactggagagaacc20<210>290<211>20<212>DNA<213>人工序列<220><223>探针<400>290tgaacgaaggtagagaagca20<210>291<211>20<212>DNA<213>人工序列<220><223>探针<400>291tgcggtttacgaaattgaaa20<210>292<211>20<212>DNA<213>人工序列<220><223>探针<400>292actcatgacgaacgaagaag20<210>293<211>19<212>DNA<213>人工序列<220><223>探针<400>293gcagaaaaactatcctcag19<210>294<211>20<212>DNA<213>人工序列<220><223>探针<400>294cagctatgctgcggtgaata20<210>295<211>19<212>DNA<213>人工序列<220><223>探针<400>295cttgtcgatcacctcctcg19<210>296<211>19<212>DNA<213>人工序列<220><223>探针<400>296ttatgtgcatccgtaacta19<210>297<211>22<212>DNA<213>人工序列<220><223>探针<400>297gtagcagatttagacacagatg22<210>298<211>26<212>DNA<213>人工序列<220><223>探针<400>298aaggtgaacgtggatgaagttggtgg26<210>299<211>20<212>DNA<213>人工序列<220><223>引物<400>299gaaaatgatgcccagtgctt20<210>300<211>20<212>DNA<213>人工序列<220><223>引物<400>300ttgaaggaaatgccccatta20<210>301<211>20<212>DNA<213>人工序列<220><223>引物<400>301gaaccaatcccgtgaaagaa20<210>302<211>20<212>DNA<213>人工序列<220><223>引物<400>302agctgcccatgaatagcact20<210>303<211>19<212>DNA<213>人工序列<220><223>引物<400>303ggttaccccaaaggccacc19<210>304<211>20<212>DNA<213>人工序列<220><223>引物<400>304aagcggaagaatgtgtcagc20<210>305<211>20<212>DNA<213>人工序列<220><223>引物<400>305tttggggagctgaaggacta20<210>306<211>20<212>DNA<213>人工序列<220><223>引物<400>306ctttgtgaccattccggttt20<210>307<211>15<212>DNA<213>人工序列<220><223>探针<400>307ggacaggcgaggaat15<210>308<211>16<212>DNA<213>人工序列<220><223>探针<400>308tggacaggcaaggaat16<210>309<211>14<212>DNA<213>人工序列<220><223>探针<400>309tctcagcgagcctc14<210>310<211>14<212>DNA<213>人工序列<220><223>探针<400>310actctcagcaagcc14<210>311<211>15<212>DNA<213>人工序列<220><223>探针<400>311cgggagccgatttca15<210>312<211>17<212>DNA<213>人工序列<220><223>探针<400>312atgatgaaatcgactcc17<210>313<211>17<212>DNA<213>人工序列<220><223>探针<400>313cagtgaagaaagtgtct17<210>314<211>17<212>DNA<213>人工序列<220><223>探针<400>314gaccagtgaagcaagtg17当前第1页1 2 3
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1