一种用于检测口蹄疫的环介导等温扩增引物组及试剂盒的制作方法
本发明属于领域属于口蹄疫病毒检测技术领域,具体涉及一种用于检测口蹄疫的环介导等温扩增引物组及试剂盒。
背景技术:
口蹄疫(Food and mouth disease virus,FMD)是由口蹄疫病毒(Food And Mouth Disease Virus,FMDV)引起的一种急性高度接触性传染病,主要侵害偶蹄动物,如牛、猪、羊等;其特征是发热、皮肤或粘膜发生水溃疡,尤其是在口腔和蹄叉部位。
口蹄疫病毒属于小RNA病毒科,约有8500个核苷酸组成。病毒基因组有一个开放性阅读框(ORF)、一个5’端非编码区(NCR)和3’端非编码区(NCR)组成,ORF编码由4中结构蛋白(VP1、VP2、VP3和VP4)、RNA聚合酶(3D)、蛋白酶(L、2A、3C)以及其他非结构蛋白(如3A等)组成。口蹄疫病毒包括7个血清型和60余个亚型,7个血清型为:O型、Asia I型、A型、C型、SAT1型、SAT2型、SAT3型,并且各血清之间无交叉免疫反应。
口蹄疫在亚洲主要流行有A型、O型、C型、Asia I型4个血清型,截止目前,我国仅见O型、亚洲I型、A型三个血清型的口蹄疫。但是非洲型和C型出现在我国周边国家中,对我国威胁较大。因此建立快速、准确、灵敏、特异的现场检测方法对口蹄疫的预防与控制具有重大意义。
目前检测口蹄疫的方法有间接夹心酶联免疫吸附试验、反向间接血凝试验、中和试验、液相阻断酶联免疫吸附试验、非结构蛋白ELISA检测、正向间接血凝试验等。但这些方法都依赖检测相应的抗体,属于血清学检测方法。另一种方法是病源生物学方法,并且这种方法耗费时间长,并且对试剂样本有一定依赖性。由于口蹄疫病毒高度变异性和交叉性,其特异性难以保证,容易出现假阳性和假阴性。。
专利申请号为200810034124、201210221684和201310067020的发明专利分别提供了O型、C型和7种血清型分型的环介导等温扩增快速检测试剂盒,相对于PCR或血清学检测方法,灵敏度高,检测快。但是,发明专利200810034124和201210221684中提供的试剂盒只能检测到样本是否为O型或C型口蹄疫病毒,对于其他血清型口蹄疫病毒则呈现出阴性结果。而发明专利201310067020提供了7种血清型分型的试剂盒,但是在7个反应管中,每个管中单独检测一种类型血清型。其制造成本和使用成本相对较大,严重限制了其在现场实际应用价值。
技术实现要素:
为了解决现有技术存在的上述问题,本发明提供了一种能够快速、准确、灵敏的检测大型畜牧动物是否感染口蹄疫病毒的环介导等温扩增引物组及试剂盒。
本发明所采用的技术方案为:一种用于检测口蹄疫的环介导等温扩增引物组,包括内引物1、内引物2、外引物1、外引物2、环引物1和环引物2,所述内引物1的序列如SEQ ID NO:1所示,所述内引物2的序列如SEQ ID NO:2所示,所述外引物1的序列如SEQ ID NO:3所示,所述外引物2的序列如SEQ ID NO:4所示,所述环引物1的序列如SEQ ID NO:5所示,所述环引物2的序列如SEQ ID NO:6所示。
SEQ ID NO:1的序列为:TTCCGCAAATAGCAGCAG;
SEQ ID NO:2的序列为:CTGGAGCTATGCTTTATGC;
SEQ ID NO:3的序列为:TGGTGTGAGTCTCCACGTCAACGAACACAATCGACGTACTGT;
SEQ ID NO:4的序列为:TCTCCTACGGCGACGAGTTCGGAAGCAAGGGATGATACC;
SEQ ID NO:5的序列为:TCACGGTGCTTGAGCTAAGAC;
SEQ ID NO:6的序列为:GGTTGCAAGTGCGTACGTGGAG;
本发明还提供了一种含有所述环介导等温扩增引物组的试剂盒,所述试剂盒还包括反应液,所述反应液包括反应浓缩液和逆转录酶;所述反应浓缩液包括DNA聚合酶,酶缓冲液,dNTP,MgSO4,甘氨酸三甲胺内盐和荧光染料。
所述试剂盒能够快速、准确、灵敏的检测大型畜牧动物是否感染口蹄疫病毒。
使用所述试剂盒检测口蹄疫病毒的方法,包括以下步骤:
(1)病毒RNA提取:采集疑似感染口蹄疫病毒的牲畜的血清,提取样本RNA并逆转录为cDNA作为样品;
(2)引物处理:将内引物1、内引物2、外引物1、外引物2、环引物1和环引物2等体积混匀,得到引物试剂;在混合前,内引物1和内引物2的浓度为40nM,外引物1和外引物2的浓度为5nM,环引物1和环引物2的浓度为20nM;
(3)环介导等温扩增反应:将样品、引物试剂和反应液混合均匀后,放入定量PCR仪或等温扩增荧光检测系统,在65℃下,进行环介导等温扩增反应:共进行60个循环,每个循环的时间为30秒;
(4)溶解曲线分析:在环介导等温扩增反应过程中,对cDNA的浓度进行分析,得到扩增曲线和溶解曲线;
(5)结果判断:根据所获得扩增曲线和溶解曲线判定,若扩增曲线为明显的S型曲线,以及溶解曲线峰型单一且较为尖锐,则判定为阳性结果;扩增曲线没有出现明显S型曲线,则判定为阴性结果;扩增曲线有明显S型曲线,但溶解曲线峰型不单一,则判定为非特异性扩增。
需要说明的是,核酸的等温扩增法属于核酸体外扩增诸多方法中的一类,在核酸扩增过程中温度恒定不变,即不需要环境温度的反复变化即可完成DNA的复制和扩增,其技术的核心在于其独特的引物结构和扩增方式以及具有特殊活性的DNA聚合酶的使用,本申请中使用的是等温扩增荧光法。
等温扩增荧光法(Isothermal Amplification Fluorescent Identification Method)是核酸等温扩增和荧光技术的结合,其反应过程在恒温条件下进行,通过添加有特殊链置换活性的DNA聚合酶和针对目标基因特异性片段设计的特异性引物组使核酸扩增得以在恒温条件下来完成,同时在体系中加入荧光基团即荧光标记物,该荧光标记物能特异性结合到DNA双链氢键的小沟部分,且结合到DNA双链之后可被激发并发出特殊波长的荧光,该荧光标记物在单独存在的情况下不会被激发且只与DNA双链结合,故体系中的荧光强度即代表了体系中DNA双链的浓度,最后通过荧光信号累积实时监控整个核酸扩增过程,实现核酸扩增的实时监测,核酸复制扩增反应结束后可对产物做退火溶解曲线分析,溶解曲线可进一步坚定该核酸扩增产物是否是特异性扩增。结合技术的应用,实现了在确保实验结果准确性,该方法是一种高特异性的快速扩增法,非常适合口蹄疫病毒的现场快速检测。
因体系中加入了能特异性与DNA双链集合的荧光物质,故随着扩增的不断进行和产物的累积,能实时监测整个扩增反应的全过程并做到定性和简单的定量分析。
为进一步增加检测的准确性,方便实验人员对照使用,优选的技术方案是,所述试剂盒还包括对照物,所述对照物包括阳性对照物和阴性对照物。在检测时,同时使用阳性对照物和阴性对照物作为样本进行检测,当阳性对照物的检测结果是阳性结果,且阴性对照物的检测结果是阴性结果时,则本次测试有效,否则本次测试无效。
根据本发明的一个实施例,所述阳性对照物为含目的基因的大肠杆菌质粒DNA片段,所述目的基因的序列如SEQ ID NO:7所示,所述阴性对照物为不含目的基因的反应液或双蒸水。
SEQ ID NO:7的序列为:AAACGCATCA CTGTTGAGGG CGGGATGCCG TCTGGTTGTT CCGCAACAAG CATCATCAAC ACAATTTTGA ACAACATCTA TGTGCTCTAC GCCCTGCGTA GACACTATGA GGGAGTTGAG CTGGACACTT ACACCATGAT CTCCTACGGG GATGACATCG TGGTTGCAAG TGATTACGAT TTGGACTTCG AGGCCCTGAA GCCCCACTTT AAATCTCTTG GTCAAACCAT CACTCCAGCT GACAAAAGCG ACAAAGGTTT TGTTCTTGGT CACTCCATCA CCGACGTCAC TTTCCTCAAA;
为方便使用,所述内引物1和内引物2的浓度为40nM,所述外引物1和外引物2的浓度为5nM,所述环引物1和环引物2的浓度为20nM;所述环介导等温扩增引物组的体积为6ul,所述环介导等温扩增引物组中各引物的体积均为1ul,所述反应浓缩液的体积为15ul,逆转录酶的体积为1ul。
本发明的有益效果为:
1、本发明公开了一种能够快速、准确、灵敏的检测大型畜牧动物是否感染口蹄疫病毒的环介导等温扩增引物组,使用6条引物对应目的基因中的8个特异区域进行识别,保证了检测反应的高度特异性和准确性;检测反应的灵敏度比传统PCR方法更高,最低可检测到10个拷贝;同时,所述检测方法操作简单。只需要将样品、引物试剂和反应液混合均匀后,扩增30分钟即可得到检测结果。
2、本发明还公开了一种含有所述环介导等温扩增引物组的试剂盒,在测试时,只需使用一个反应管中即可对样品进行检测,避免了多次检测,降低了检测成本;另外,所述试剂盒中还包含荧光染料,方便实验人员采用等温扩增荧光检测系统进行扩增反应,实现了实时监控,并且可以针对扩增产物做溶解曲线分析,克服了之前分型检测试剂盒中没办法对产物特异性的分析。
3、所述试剂盒,能够用于多个检测平台上,不仅能够用于定量PCR仪或等温扩增荧光检测系统中,还能够用于其他能够提供恒定温度的设备(如金属浴)上。
附图说明
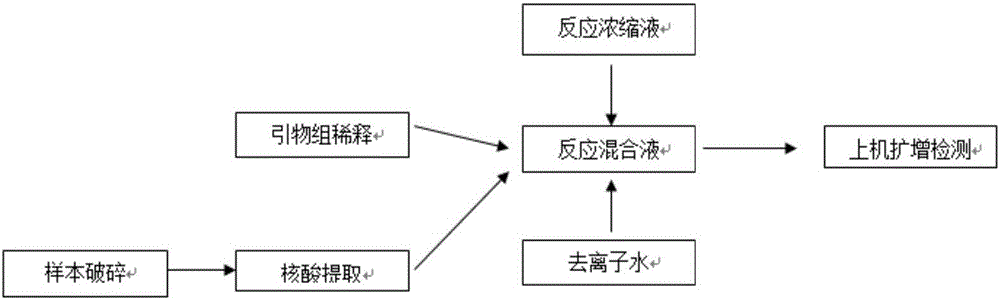
图1为使用所述试剂盒检测口蹄疫病毒的方法流程示意图;
图2是实施例4中准确性验证中的扩增曲线;
图3是实施例4中准确性验证中的溶解曲线;
图4是实施例5中敏感性验证中的扩增曲线;
图5是实施例5中敏感性验证中的溶解曲线。
具体实施方式
下面结合实施例,更具体地说明本发明的内容。应当理解,本发明的实施并不局限于下面的实施例,对本发明所做的任何形式上的变通和/或改变都将落入本发明保护范围。
在本发明中,若非特指,所有的份、百分比均为重量单位,所有的设备和原料等均可从市场购得或是本行业常用的。下述实施例中的方法,如无特别说明,均为本领域的常规方法。
实施例1
一种用于检测口蹄疫的环介导等温扩增引物组,包括内引物1、内引物2、外引物1、外引物2、环引物1和环引物2,所述内引物1的序列如SEQ ID NO:1所示,所述内引物2的序列如SEQ ID NO:2所示,所述外引物1的序列如SEQ ID NO:3所示,所述外引物2的序列如SEQ ID NO:4所示,所述环引物1的序列如SEQ ID NO:5所示,所述环引物2的序列如SEQ ID NO:6所示。
实施例2
一种含有所述环介导等温扩增引物组的试剂盒,所述试剂盒还包括反应液和对照组,所述反应液包括反应浓缩液和逆转录酶;所述反应浓缩液包括DNA聚合酶,缓冲液,dNTP,MgSO4,甘氨酸三甲胺内盐和荧光染料;所述对照物包括阳性对照物和阴性对照物,所述阳性对照物为含目的基因的大肠杆菌质粒DNA片段,所述目的基因的序列如SEQ ID NO:7所示,所述阴性对照物为不含目的基因的反应液或双蒸水。
一般来说,引物试剂的浓度需要使用前配置,为方便使用,所述内引物1和内引物2的浓度为40nM,所述外引物1和外引物2的浓度为5nM,所述环引物1和环引物2的浓度为20nM;所述环介导等温扩增引物组的体积为6ul,所述环介导等温扩增引物组中各引物的体积均为1ul,所述反应浓缩液的体积为15ul,逆转录酶的体积为1ul。
本实施例中,反应液直接使用Optigene公司的IMM。当然本领域技术人员也能够使用其他反应液,在此就不在赘述。
所述试剂盒能够快速、准确、灵敏的检测大型畜牧动物是否感染口蹄疫病毒。
实施例3
图1为使用所述试剂盒检测口蹄疫病毒的方法流程示意图,所述方法包括以下步骤:
(1)病毒RNA提取:采集疑似感染口蹄疫病毒的牲畜的血清,提取样本RNA并逆转录为cDNA作为样品;
(2)引物处理:将内引物1、内引物2、外引物1、外引物2、环引物1和环引物2等体积混匀,得到引物试剂;在混合前,内引物1和内引物2的浓度为40nM,外引物1和外引物2的浓度为5nM,环引物1和环引物2的浓度为20nM;
(3)环介导等温扩增反应:将样品、引物试剂和反应液混合均匀后,作为检测组;将阳性对照物、引物试剂和反应液混合均匀后,作为阳性对照组;将阴性对照物、引物试剂和反应液混合均匀后,作为阴性对照组;将检测组、阳性对照组和阴性对照组放入定量PCR仪(DNA-technology DT-Prime)或等温扩增荧光检测系统(Genie II),在65℃下,进行环介导等温扩增反应:共进行60个循环,每个循环的时间为30秒;其中,扩增总体系为25ul,其中包括反应浓缩液15ul,引物试剂6ul,逆转录酶1ul,样品或对照物3ul;
(4)溶解曲线分析:在环介导等温扩增反应过程中,对cDNA的浓度进行分析,得到扩增曲线和溶解曲线;
(5)结果判断:根据所获得扩增曲线和溶解曲线判定,若扩增曲线为明显的S型曲线,以及溶解曲线峰型单一且较为尖锐,则判定为阳性结果;扩增曲线没有出现明显S型曲线,则判定为阴性结果;扩增曲线有明显S型曲线,但溶解曲线峰型不单一,则判定为非特异性扩增。
实施例4
本实施例为实施例3中所述方法的准确性验证。
使用感染A型口蹄疫的血清样本、感染O型口蹄疫病毒的血清样本、感染Asia I型口蹄疫病毒的血清样本、感染C型口蹄疫的血清样本、感染SAT 1型口蹄疫的血清样本、感染SAT 2型口蹄疫的血清样本和感染SAT3型口蹄疫的血清样本分别提取样本RNA并逆转录为cDNA作为样品,使用实施例3中的检测方法,进行检测,检测结果如图2和图3所示,结果显示,所有的样品的扩增曲线为明显的S型曲线,以及溶解曲线峰型单一且较为尖锐,说明所述检测方法能够检测全部七种口蹄疫病毒类型。
实施例5
本实施例为实施例3中所述方法的敏感性的验证。
采集感染A型口蹄疫的血清样本提取样本RNA并逆转录为cDNA,并配置成100ng/ul、10ng/ul、10-1ng/ul、10-2ng/ul、10-3ng/ul、10-4ng/ul一系列浓度梯度的样品,后分别使用实施例3中的检测方法,进行检测,检测结果如图4和图5所示,结果显示,样品浓度为10-2ng/ul时,依旧会产生扩增曲线,并且溶解曲线峰型单一且尖锐。说明所述检测方法的灵敏度可达到10-2ng/ul。
最后所应说明的是,以上实施例仅用以说明本发明的技术方案而非限制,尽管参照较佳实施例对本发明进行了详细说明,所应理解的是,以上所述仅为本发明的具体实施方式而已,并不用于限定本发明的保护范围,凡在本发明的精神和原则之内,所做的任何修改、等同替换、改进等,均应包含在本发明的保护范围之内。
SEQUENCE LISTING
<110> 张薇
<120> 一种用于检测口蹄疫的环介导等温扩增引物组及试剂盒
<130> 2010
<160> 7
<170> PatentIn version 3.3
<210> 1
<211> 18
<212> DNA
<213> 未知
<400> 1
ttccgcaaat agcagcag 18
<210> 2
<211> 19
<212> DNA
<213> 未知
<400> 2
ctggagctat gctttatgc 19
<210> 3
<211> 42
<212> DNA
<213> 未知
<400> 3
tggtgtgagt ctccacgtca acgaacacaa tcgacgtact gt 42
<210> 4
<211> 39
<212> DNA
<213> 未知
<400> 4
tctcctacgg cgacgagttc ggaagcaagg gatgatacc 39
<210> 5
<211> 21
<212> DNA
<213> 未知
<400> 5
tcacggtgct tgagctaaga c 21
<210> 6
<211> 22
<212> DNA
<213> 未知
<400> 6
ggttgcaagt gcgtacgtgg ag 22
<210> 7
<211> 300
<212> DNA
<213> 未知
<400> 7
aaacgcatca ctgttgaggg cgggatgccg tctggttgtt ccgcaacaag catcatcaac 60
acaattttga acaacatcta tgtgctctac gccctgcgta gacactatga gggagttgag 120
ctggacactt acaccatgat ctcctacggg gatgacatcg tggttgcaag tgattacgat 180
ttggacttcg aggccctgaa gccccacttt aaatctcttg gtcaaaccat cactccagct 240
gacaaaagcg acaaaggttt tgttcttggt cactccatca ccgacgtcac tttcctcaaa 300
- 还没有人留言评论。精彩留言会获得点赞!
- 一种霍乱弧菌环介导等温扩增试剂盒及其应用的制造方法与工艺
- 用于检测番茄晚疫病菌的LAMP引物组合物和应用的制造方法与工艺
- 基于颜色判定的环介导等温扩增(LAMP)技术检测雪松疫霉根腐病菌的制造方法与工艺
- Sortase A介导的(S)‑羰基还原酶寡聚体高效催化(S)‑苯基乙二醇的合成的制造方法与工艺
- 用于旋转机器中的超导线圈的等温支承部和真空容器的制造方法与工艺
- 基于环介导等温扩增消光技术的转基因玉米MIR604检测方法与制造工艺
- 基于环介导等温扩增消光技术的玉米检测方法与制造工艺
- 一套鉴定甘蔗上三种短体线虫的环介导等温扩增引物及其试剂盒的制造方法与工艺
- RNA扩增方法与制造工艺
- 用于扩增核酸样品的等温方法与制造工艺
- 环介导等温扩增多重耐药基因oqxAB的检测引物、检测试剂盒及检测方法与制造工艺
- 一种气单胞菌的核酸等温扩增检测试剂盒及其检测方法与制造工艺
- 一种霍乱弧菌环介导等温扩增试剂盒及其应用的制造方法与工艺
- 用于检测番茄晚疫病菌的LAMP引物组合物和应用的制造方法与工艺
- 基于颜色判定的环介导等温扩增(LAMP)技术检测雪松疫霉根腐病菌的制造方法与工艺
- Sortase A介导的(S)‑羰基还原酶寡聚体高效催化(S)‑苯基乙二醇的合成的制造方法与工艺
- 用于旋转机器中的超导线圈的等温支承部和真空容器的制造方法与工艺
- 用于扩增细胞群的方法、试剂盒及装置与制造工艺
- 基于环介导等温扩增消光技术的转基因玉米MIR604检测方法与制造工艺
- 基于环介导等温扩增消光技术的玉米检测方法与制造工艺