N‑(N′‑油酰甘氨酰)‑壳寡糖磺酸钠及其制备方法与流程
本发明涉及化工医药
技术领域:
,具体涉及表面活性剂的制备方法。
背景技术:
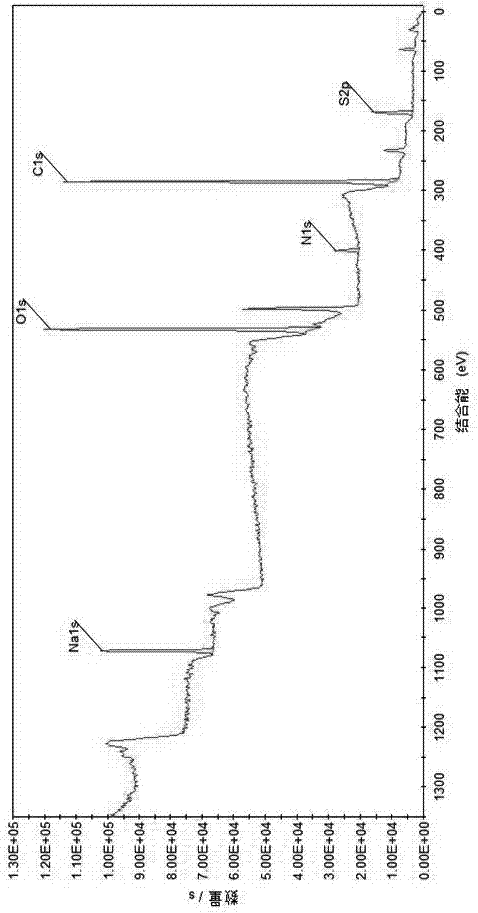
:由于表面活性剂具有优异的应用性能,在工业生产和人们的日常生活中具有广泛的应用。一直以来,人们从未停止过对新型表面活性剂的开发和研究。特别是原料来源广泛,生物相容性好,功能独特的表面活性剂的开发一直是研究的热点之一。壳寡糖又叫壳聚寡糖、低聚壳聚糖,是将壳聚糖经特殊的生物酶技术(也有使用化学降解、微波降解技术的报道)降解得到的一种聚合度在2~20之间寡糖产品,分子量≤3200da,是水溶性较好、功能作用大、生物活性高的低分子量产品。它具有壳聚糖所没有的较高溶解度,全溶于水,容易被生物体吸收利用等诸多独特的功能,其作用为壳聚糖的14倍。壳寡糖是自然界中唯一带正电荷阳离子碱性氨基低聚糖,是动物性纤维素。目前国内外对壳聚糖改性表面活性剂研究较多,制备的壳聚糖阴离子型、阳离子型和两性型表面活性剂都有报道。例如壳聚糖与不同长度碳链的烷基缩水甘油醚在碱性条件下可合成一系列新型两性表面活性剂;通过壳聚糖接枝环氧丙基十四烷基二甲基氯化铵,再进一步磺化引入磺酸基而合成了一种吸湿性极强的高分子表面活性剂;利用壳聚糖和2,3-环氧丙基三甲基氯化铵反应,可合成羟丙基三甲基氯化铵壳聚糖阳离子型表面活性剂。另外也有将壳聚糖和有机硅相结合的表面活性剂的报道。氨基酸是构成蛋白质的基本成分,是构成生命的基元物质。通常氨基酸表面活性剂主要是在氨基酸的氨基上引入长链脂肪酰基,然后中和成盐后可得到相应的表面活性剂。常用的氨基酸有肌氨酸、谷氨酸、丝氨酸、丙氨酸、撷氨酸、亮氨酸等,其中以肌氨酸、谷氨酸最为常用。所用到的脂肪酸分为饱和和不饱和两种,如油酸、油酸、椰子油酸、棕榈油酸、硬脂肪酸、辛酸、癸酸等。由于表面活性剂能定向排列于不相容的两相界面,这使得表面活性剂在涉及两相界面的某些特殊性能(比如界面的识别、催化、缓释性能等)方面有着得天独厚的优势。壳聚糖表面活性剂具有一定的成膜性能,但对某些物质的特异性作用较差;氨基酸表面活性剂对某些物质有一定的特异性作用(如某些金属离子),但成膜性相对较弱。另外,利用表面活性剂分子中的疏水侧链调节表面活性剂的性能也是表面活性剂研究中的重点内容之一。技术实现要素:针对以上两种表面活性剂存在的缺陷,本发明提出一种水溶性较好的n-(n′-油酰甘氨酰)-壳寡糖磺酸钠。本发明的n-(n′-油酰甘氨酰)-壳寡糖磺酸钠的分子结构式如下:其中n=6~15。本发明所述水溶性好的氨基酸壳寡糖表面活性剂的表面活性可利用氨基酸不同的疏水侧链来进行微调。本发明产品为一种具有生物相容性好、高效、无毒、表面活性可调节的绿色环保的表面活性剂,此类表面活性剂具有良好的成膜性能,性质温和,除了具有一般表面活性剂的特点外,还可用于脂溶性药物缓释微体的构建,在医药领域应用前景广泛。本发明的另一目的是提出以上产品的制备方法。本发明包括以下步骤:1)将n-羟基琥珀酰亚胺(nhs)和二环己基碳二亚胺(dcc)与油酸的dmf溶液混合搅拌反应,取得滤液;2)将甘氨酸和碳酸钾溶解于水中,冰水浴条件下滴加上述滤液,滴加完后置于室温下反应,制得n-酰基氨基酸溶液;3)将n-油酰谷氨酰胺溶液的ph值调至中性后与壳寡糖、1-(3-二甲氨基丙基)-3-乙基碳二亚胺盐酸盐和n-羟基琥珀酰亚胺混合进行反应,生成n-(n′-油酰甘氨酰)-壳寡糖;4)将n-(n′-油酰甘氨酰)-壳寡糖以dmf溶胀后与氯磺酸进行磺化反应,反应结束后将反应液的ph值调至中性,离心,取上清液用透析袋透析;5)将透析袋内的透析液过滤,取得滤液,经冷冻干燥,得n-(n′-油酰甘氨酰)-壳寡糖磺酸钠。本发明的反应式如下:其中n=6~15。本发明的优点是:合成反应简单,反应条件温和,收率高,反应可定量。由于第一步反应使用了nhs(n-羟基琥珀酰亚胺)活化脂肪酸,与氨基酸偶联后释放出nhs,在与壳寡糖偶联时可直接加入水性缩合试剂edc(1-(3-二甲氨基丙基)-3-乙基碳二亚胺盐酸盐)便可在水中完成反应,故第二步反应(与氨基酸偶联)不用分离即可进行第三步反应。这样可实现一锅法反应,大大节约反应成本。反应所用的碱选择碳酸钾,这是由于碳酸钾和甘氨酸的羧酸作用形成碳酸氢钾,反应不必另外再加碱,从而简化了工艺。本发明将n-油酰甘氨酸溶液的ph值调至中性后与壳寡糖、1-(3-二甲氨基丙基)-3-乙基碳二亚胺盐酸盐混合进行反应,得到的是含n-(n′-油酰甘氨酰)-壳寡糖的反应溶液。由于此反应体系为水相的体系,采用水溶性的1-(3-二甲氨基丙基)-3-乙基碳二亚胺盐酸盐为缩合剂,可使反应在一锅中完成,省去了中间物分离的麻烦。本发明还将步骤3)反应取得的反应溶液进行离心处理,将离心取得的沉淀采用乙醇混合抽提后30℃真空干燥,得n-(n′-油酰甘氨酰)-壳寡糖。目的是除去产物中夹带的沸点较高的dmf,使得产物易于真空干燥,同时也能将部分杂质除去。本发明将经干燥的n-(n′-油酰甘氨酰)-壳寡糖用dmf溶胀后,在室温下与一定量的氯磺酸磺化,这样可避免剧烈的反应条件带来的副反应。反应一定时间后,将反应液中和至中性,这样可以避免磺酸的强酸性引起壳寡糖的降解(或对酰胺键的水解)作用。另外,本发明所述透析袋的截止分子量为2000~3000mw。这是因为目标产物的平均分子量在2000以上,在透析时得以保留,而反应过程中产生的副产物的分子量都在2000以下,在透析过程中可以全部除去。附图说明图1为n-(n′-油酰甘氨酰)-壳寡糖磺酸钠的红外谱图。图2为xps元素分析能谱图。具体实施方式(1)先将0.2g(1.0mmol)油酸溶于无水dmf中,加入0.12g(1.05mmol)nhs(n-羟基琥珀酰亚胺)和0.226g(1.1mmol)二环己基碳二亚胺(dcc),搅拌反应10~12小时,反应10h后过滤,得滤液(ⅰ)。称取甘氨酸0.075g(1.0mmol)和碳酸钾0.138g(1.0mmol),加入适量水溶解,冰水浴中慢慢滴加滤液(ⅰ),滴加完后置于室温下反应24小时,制得n-酰基甘氨酸酸溶液。(2)以3n盐酸调节n-油酰甘氨酰溶液的ph至中性,加入0.17g壳寡糖(可事先用少量水溶解)、0.201g(1.05mmol)edac(1-(3-二甲氨基丙基)-3-乙基碳二亚胺盐酸盐),室温下反应24h,得到含n-(n′-油酰甘氨酰)-壳寡糖的反应溶液。将反应液离心,沉淀用乙醇抽提2次,30℃真空干燥8h,得n-(n′-油酰甘氨酰)-壳寡糖。(3)称取0.15gn-(n′-油酰甘氨酰)-壳寡糖用5mldmf(n,n-二甲基甲酰胺)溶胀过夜,加入1.2ml氯磺酸的dmf溶液(dmf和氯磺酸的混合体积比为1:3),室温下反应过夜,用10%的naoh水溶液中和至中性,离心,上清液用截止分子量为2000~3000mw的透析袋透析3天(每8小时换水一次),取透析液过滤,除去沉淀,取滤液冷冻干燥,所得产品即为水溶性较好的n-(n′-油酰甘氨酰)-壳寡糖磺酸钠。(4)此法所制备的n-(n′-油酰甘氨酰)-壳寡糖磺酸钠红外谱图,如图1所示。在图1中于3505cm-1附近的宽峰主要为壳寡糖上羟基上o-h、酰胺基上n-h伸缩振动峰,2928cm-1、2856cm-1附近吸收为甲基及亚甲基上c-h键的伸缩振动峰值,故确认了长链烷烃结构的存在;1662cm-1处吸收是主要是羰基的伸缩振动峰;1141cm-1处吸收为磺酸盐的强吸收峰。(5)目标化合物xps元素分析,如图2所示。图2为xps元素分析能谱图。由图2可见元素含量:元素原子含量(%)c66.83o22.55na3.71s4n2.91由(4)、(5)可见:采用本方法取得了n-(n′-油酰甘氨酰)-壳寡糖磺酸钠。(6)目标化合物在不同ph溶液中表面张力测定:将n-(n′-油酰甘氨酰)-壳寡糖磺酸钠溶于水中,超声0.5小时,高速离心(转速:12000r/min),取上清液测定表面张力(悬滴法)见下表:表1不同浓度水溶液中表面张力溶液浓度(质量百分比,%)表面张力(10-3n·m-1)0.538.7135.91.528.7225.5由上表可见,随着溶液的浓度升高,n-(n′-油酰甘氨酰)-壳寡糖磺酸钠的表面张力表现出明显的下降,可见n′-油酰甘氨酰壳寡糖磺酸钠可作为表面活性剂使用。(6)应用举例:本发明可用于新型的药物控制释放传输系统(如聚乳酸(pla)微球载药系统)的制备,方法如下。将一定量的药物(如非洛地平等)和100mgpla溶于5ml氯仿中,形成溶液;然后加入装有50ml,1%的n-(n′-油酰甘氨酰)-壳寡糖磺酸钠溶液的100ml烧杯中;之后再用细胞粉碎仪超声乳化(900w)6min形成水包油乳液;常温下磁力搅拌8h使氯仿完全挥发形成pla微球的悬浮液。用25,000rpm的速度离心微球的悬浮液45min收集pla微球。然后用蒸馏水重新分散微球、离心、悬浮3次除去剩余的basde以及未包封进去的药物。最后对微球进行冷冻干燥得到干燥的pla微球并将其保存在4℃的条件下备用。此法所制备微球的粒径在100nm~2000nm。当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1