一种水溶性单核镍配合物与制备方法及其应用与流程
本发明属于镍配合物领域,尤其是涉及一种水溶性单核镍配合物与制备方法及其应用。
背景技术:
自上世纪90年代以来,药物小分子与生物大分子dna、蛋白质相互作用的研究己经成为众多科研人员的共同关注和感兴趣的课题,因为进行药物小分子(包括潜在药物)与dna、蛋白质之间相互作用研究不仅有助于人们从分子水平上认识和理解药物与生物大分子相互作用的方式及其在体内作用机制,而且对抗癌药物的体外筛选具有重要意义,同时也为设计疗效更好、毒性更低的抗癌新药提供理论指导和有价值的信息。
癌症是严重威胁人类健康甚至生命的一类疾病,积极预防、诊治是广大科研学者的共同目标。而小分子与dna的相互作用是以dna为靶分子的,其键合状态一方面可能导致癌变、突变及细胞死亡,比如一些致癌物能与dna形成加合物,这种dna加合物是可能癌变的预警标志物,另一方面也可能是临床上广泛应用的抗癌药物,例如肿瘤组织是细胞分裂活跃的部位,而许多抗癌药物都是以dna为作用靶点,通过与癌细胞的dna发生相互作用破坏其结构,进而影响基因调控与表达功能,表现出抗癌活性。此外,小分子化合物与dna特异性的定位结合,在基因表达的调控过程及很多抗癌药物体内作用方式的研究中非常重要。因此小分子与dna的相互作用的研究不仅有利于探索和开发新的核酸探针,而且有助于从分子水平上了解抗癌药物的作用机理,阐明有毒物的致癌、致畸的分子生物学机理,为设计临床上更为有效地抗癌药物提供理论指导。
利用n-甲基-n,n-二吡啶甲基胺(bpma)为配体,以金属镍离子为活性中心,通过加热回流搅拌的合成方法,设计合成了一个新的水溶性单核镍配合物;并使用元素分析、红外光谱、x-单晶衍射分析、紫外-可见光谱、荧光光谱等手段对配合物进行表征和性质研究,发现配合物能够以插入方式与小牛胸腺dna发生相互作用,并且能够和bsa发生较强地相互作用。
技术实现要素:
有鉴于此,本发明旨在提出一种水溶性单核镍配合物与制备方法及其应用,采用加热回流搅拌在室温条件下,采用缓慢挥发的合成方法得到目标产物,制备方法简单可靠。
为达到上述目的,本发明的技术方案是这样实现的:
一种水溶性单核镍配合物,化学式为[ni(bpma)2](clo4)2,其中bpma为n-甲基-n,n-二吡啶甲基胺。
进一步的,所述该配合物的结构式为:
进一步的,所述该配合物属于正交晶系,p212121空间点群,晶胞参数为
进一步的,所述该配合物为单核结构,ni1金属离子分别与来自两个bpma配体的氮原子n1、n2、n3、n4、n5、n6配位,形成一个畸变的八面体构型,其中n2、n3、n4、n5组成八面体的赤道平面,n1和n6占据八面体的轴向位置;ni1-n1、ni1-n2、ni1-n3、ni1-n4、ni1-n5、ni1-n6的键长分别为
本发明还提供了一种制备如上所述的水溶性单核镍配合物的方法,包括如下步骤:
将nicl2·6h2o溶解于乙腈和水组成的混合溶液中,在上述溶液中加入含有bpma的乙腈溶液,然后加热回流搅拌,冷却至室温后;滴加naclo4的饱和水溶液,继续搅拌,然后过滤;滤液置于室温条件下,缓慢挥发数周后,得到适于x-单晶衍射分析的紫色块状晶体,经乙醚洗涤后、干燥。
进一步的,所述nicl2·6h2o与bpma的物质的量比为(0.2~0.5mmol):(0.4~1.0mmol)。
进一步的,所述加热回流搅拌的反应时间为2~6小时,温度为82~100℃。
进一步的,所述乙腈和水组成的混合溶液中乙腈与水的体积比为1.0:1.0~2.0。
进一步的,所述含有bpma的乙腈溶液的滴加速度为0.05ml/s。
本发明同时提供了一种如上所述的水溶性单核镍配合物或如上所述的制备方法制备的水溶性单核镍配合物在制备核酸识别试剂和潜在药物中的应用。
产物元素分析的实验值分别为:c45.63%、h4.40%、n12.30%。其中元素分析的理论值分别为:c45.60%、h4.38%、n12.28%。
用kbr压片的红外光谱分析,该配合物在1607cm-1处出现很尖的强吸收峰,为bpma上的c–n伸缩振动产生的吸收;在2964cm-1和2901cm-1的两个中等强度的尖锐吸收峰可以指派为bpma的c-h伸缩振动;622~760cm-1多重峰为吡啶环的伸缩振动峰;1081cm-1的强峰和622cm-1的中强峰可认为高氯酸根没有参与配位,与单晶结构相符。
通过配合物与ct-dna相互作用的吸收光谱研究和荧光淬灭实验证实所述单核镍配合物以部分插入的中等键合方式和dna发生相互作用。
通过配合物与bsa相互作用的吸收光谱研究证实所述单核镍配合物能够与bsa发生较强地相互作用。
相对于现有技术,本发明所述的水溶性单核镍配合物与制备方法及其应用具有以下优势:
本发明所述的水溶性单核镍配合物与制备方法及其应用,制备步骤简单,加热回流搅拌、室温缓慢挥发条件下即可得到配合物的单晶,配合物具有较好的水溶性,从而可以在生理条件下研究其生物活性,发现配合物能够以部分插入的键合方式和dna发生相互作用,可以作为潜在的核酸识别试剂,并且发现配合物还能够与bsa发生明显的相互作用,可以能够作为潜在的药物。
附图说明
图1为本发明实施例1所述的水溶性单核镍配合物的晶体结构图;
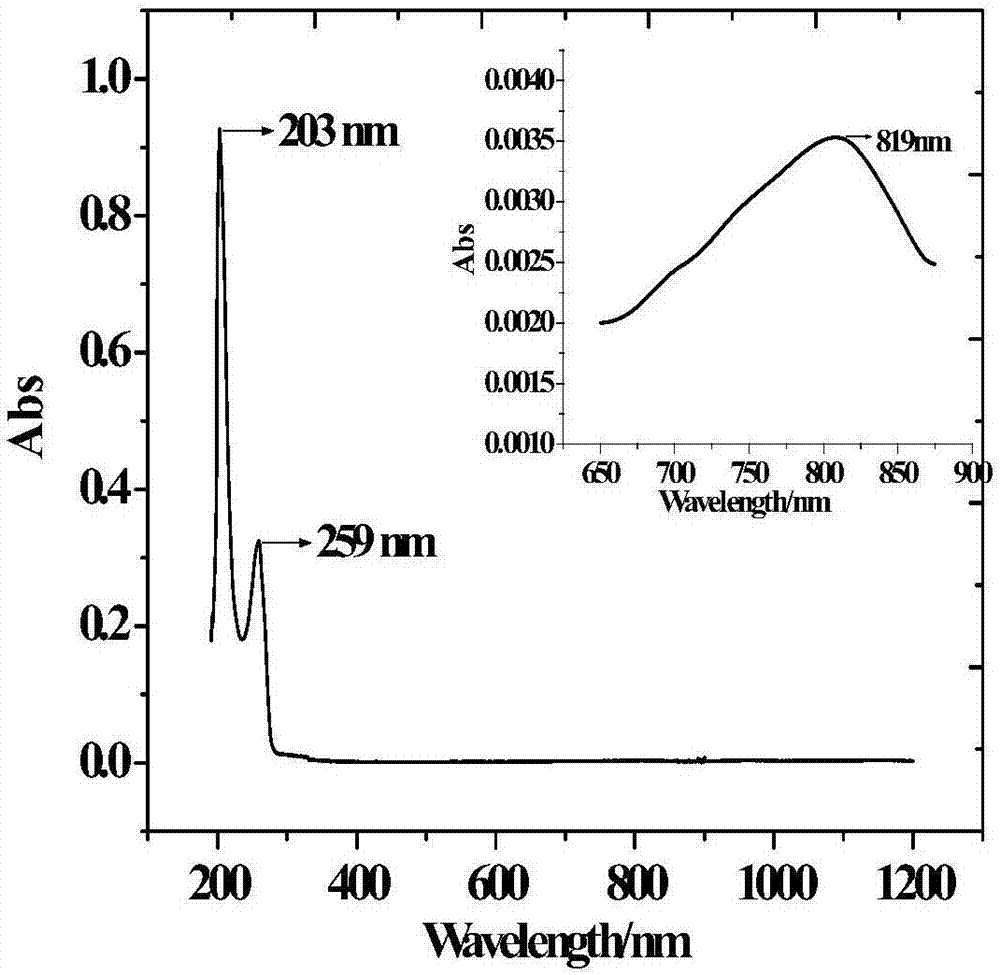
图2为本发明实施例1所述的水溶性单核镍配合物的紫外可见光谱图;
图3为本发明实施例1所述的水溶性单核镍配合物在加入不同量的ct-dna后的电子吸收光谱图;
图4为在273k和298k下,加入不同浓度的本发明实施例1所述的水溶性单核镍配合物的eb-dna的荧光淬灭光谱图;
图5为本发明实施例1所述的水溶性单核镍配合物在273k和298k对eb-dna复合物荧光的影响;
图6为本发明实施例1所述的水溶性单核镍配合物加入不同量的bsa后的电子吸收光谱图。
具体实施方式
除有定义外,以下实施例中所用的技术术语具有与本发明所属领域技术人员普遍理解的相同含义。以下实施例中所用的试验试剂,如无特殊说明,均为常规生化试剂;所述实验方法,如无特殊说明,均为常规方法。
下面结合实施例及附图来详细说明本发明。
实施例1
水溶性单核镍配合物的合成:
将0.3mmolnicl2·6h2o溶解于15ml由乙腈和水按照体积比1:1组成的混合溶液中,然后以0.05ml/s的滴速逐滴向上述溶液中加入1.00ml其中含有0.6mmolbpma的乙腈溶液,随后加热回流搅拌3小时,待冷却至室温后,滴加2.50mlnaclo4的饱和水溶液,室温下继续搅拌半小时后过滤,滤液置于室温条件下,缓慢挥发后,得到适于x-单晶衍射的紫色块状晶体,用乙醚洗涤后干燥,产率为:49%。
水溶性单核镍配合物的测试:
1、产物元素分析的实验值分别为:c45.57%、h4.46%、n12.24%。其中元素分析的理论值分别为:c45.60%、h4.38%、n12.28%,元素分析结果与晶体结构式相符合。
2、紫外-可见光谱分析:
如图2所示,从配合物的紫外可见光谱图中可以看出,配合物在200~1200nm的范围内有三个吸收带,分别是:203nm处的吸收,为π-π*跃迁,ε=6.5×103l·mol-1·cm-1,属于较强吸收;259nm处的吸收,为配体到金属离子的n-π荷移跃迁,ε=2.2×103l·mol-1·cm-1,属于较强吸收;819nm处的吸收,为金属离子的d-d跃迁,ε=27.1l·mol-1·cm-1,属于弱吸收。
3、ft-ir(kbr):用kbr压片的红外光谱分析,配合物在2964cm-1和2901cm-1的出现的中等强度、宽峰指派为bpma的c-h伸缩振动峰;在1607cm-1处出现尖、强峰,为bpma上的c–n伸缩振动峰;622~760cm-1多重峰为吡啶环的伸缩振动峰;1081cm-1的强峰和622cm-1的中强峰推测出高氯酸根没有参与配位,与单晶结构相符。
4、镍配合物的晶体结构测定:
1)实验过程:
在296(2)k下,选取大小合适的晶体,用经石墨单色器单色化的mo-kα
2)实验结果:
如图1所示,该配合物为单核结构,x-射线单晶衍射分析数据显示,在配合物中,金属离子ni1的配位数为六,分别和来自两个bpma配体的氮原子n1,n2,n3,n4,n5,n6配位,形成畸变八面体构型。其中n2,n3,n4,n5组成八面体的赤道平面,n1和n6占据在八面体的轴向位置,ni1-n1、ni1-n2、ni1-n3、ni1-n4、ni1-n5、ni1-n6的键长分别是
表1配合物的晶体结构的主要数据
表2配合物晶体的主要键长、键角
5、实施加入不同量的ct-dna,观察水溶性单核镍配合物的电子吸收光谱变化试验:
1)实验过程:
在室温下,向样品池和参比池中各加2.0ml缓冲溶液,缓冲溶液用三蒸水配制其中含有50mm的nacl和5mm的tris,然后用盐酸调至ph=7.4,然后向样品池加入一定量体积的配合物溶液,配合物浓度为1.45×10-4m,并向参比池中补加相应等体积的缓冲溶液。用微量进样器向样品池和参比池中加入一定量相同体积的ct-dna储备液,使ct-dna与配合物的浓度比值不断增加,ct-dna的浓度为0~3.94×10-4m,观察配合物吸收峰的变化。
2)实验结果:
如图3所示,配合物在204nm处有强的紫外吸收,随着ct-dna的逐渐等量加入,配合物的最大紫外吸收强度出现明显的下降,即出现了明显的“减色效应”,同时伴随了红移现象,红移距离△λ为5nm,减色率为39.2%,说明配合物在本实验条件下,以部分插入的键合方式和dna发生相互作用。
6、实施加入不同量的镍配合物,观察eb-dna的荧光淬灭试验:
镍配合物本身不产生荧光,采用配合物淬灭eb-dna结合物的荧光,通过研究eb-dna结合物荧光强度的变化来间接测定配合物与dna的结合程度。
1)实验过程:
配制ct-dna和eb的混合溶液,其含量分别为2.4×10-6meb和4.8×10-5mct-dna,储备于4℃冰箱中,镍配合物配制成3.0×10-3m储备液。淬灭滴定实验时,向样品池中加入2.0ml储备的eb-dna混合液,观察其荧光强度,然后用微量进样器每次向样品池中加入等体积的配合物储备液,观察发射光谱的变化并将数据保存以便拟合处理。
2)实验结果:
如图4所示,单核镍配合物淬灭eb-dna的荧光光谱,在加入镍配合物后,eb-dna的荧光强度出现明显的降低,并且随着配合物浓度的增加,其荧光强度逐渐降低,表明镍配合物与ct-dna的竞争结合取代了eb。
根据stern-volmer方程式:i0/i=1+k[q],以加入单核镍配合物前后eb-dna的荧光强度比值(i0/i)为纵坐标,镍配合物的浓度为横坐标,做出了stern-volmer图即图5,配合物的荧光淬灭曲线呈直线,基本上满足了stern-volmer方程,表明荧光淬灭是镍配合物取代了已插入dna的eb的结果。根据方程keb[eb]=kapp[complex],keb=1.0×107m-1([eb]=4.0μm),计算出镍配合物的表观键合常数分别为1.40×105m-1。结果显示配合物与dna是中等键合模式,小于溴化乙锭、典型的插入试剂的键合常数107m-1。
更进一步分析了在298k和273k下,镍配合物对eb-dna复合物荧光的影响。如图5所示,镍配合物随着温度升高,斜率k增大,说明该镍配合物与eb-dna形成的复合物随着温度的升高越来越稳定,荧光淬灭是由于扩散作用产生的,其荧光淬灭为动态淬灭机理。
7、实施加入不同量的bsa,观察镍配合物的电子吸收光谱变化试验:
紫外-可见吸收光谱法主要是利用血清白蛋白中色氨酸、苯丙氨酸、络氨酸等氨基酸残基吸收峰的变化来进行分析的,如果吸收峰在小分子配合物和血清白蛋白作用的前后发生了变化,则说明小分子配合物和血清白蛋白发生了作用。由此,我们通过电子吸收光谱研究了镍配合物与bsa的相互作用。
1)实验过程:
在室温下,向样品池和参比池中各加2.0ml缓冲溶液,缓冲溶液用三蒸水配制的浓度为10mmnah2po4/na2hpo4,ph=7.4,然后向样品池加入一定量体积的镍配合物溶液并向参比池中补加相应等体积的缓冲溶液。用微量进样器向样品池和参比池中加入一定量相同体积的bsa储备液,使bsa与镍配合物的浓度比值不断增加,观察镍配合物吸收峰的变化并将数据保存。
2)实验结果:
如图6所示,可以清晰地看出,随着bsa的不断加入,镍配合物在207nm处的π-π跃迁峰发生明显的减色现象并伴有红移,红移的距离为5nm;259nm处的荷移跃迁峰几乎未受bsa浓度增加的影响。说明在本实验条件下,表明该镍配合物与bsa之间发生了较强地相互作用。
实施例2
实验步骤:
将0.1mmolnicl2·6h2o溶解于15ml由乙腈和水按照体积比2:3组成的混合溶液中,然后以0.05ml/s的滴速逐滴向上述溶液中加入0.50ml其中含有0.2mmolbpma的乙腈溶液,随后加热回流搅拌5小时,待冷却至室温后,滴加2.50mlnaclo4的饱和水溶液,室温下继续搅拌半小时,过滤,滤液置于室温条件下,缓慢挥发。
实验结论:
一个月后得到浅紫色的微晶,不适于x-单晶衍射分析,未得到精细结构数据,用乙醚洗涤后干燥,产率为:27%。
实施例3
实验步骤:
将0.6mmolnicl2·6h2o溶解于15ml由乙腈和水按照体积比1:2组成的混合溶液中,然后以0.05ml/s的滴速逐滴向上述溶液中加入2.00ml其中含有1.2mmolbpma的乙腈溶液,加热回流搅拌4小时,待冷却至室温后,滴加2.50mlnaclo4的饱和水溶液,室温下继续搅拌半小时,过滤,滤液置于4℃冰箱中,缓慢挥发。
实验结论:
五周后得到浅紫色的固体粉末,未得到适合结构解析的单晶,用乙醚洗涤后干燥,产率为:51%。
以上所述仅为本发明的较佳实施例而已,并不用以限制本发明,凡在本发明的精神和原则之内,所作的任何修改、等同替换、改进等,均应包含在本发明的保护范围之内。
- 还没有人留言评论。精彩留言会获得点赞!