一种用于T细胞白血病微小残留病检测的试剂盒的制作方法
本实用新型涉及生物技术领域,尤其涉及一种用于T细胞白血病微小残留病检测的试剂盒。
背景技术:
急性淋巴细胞白血病(ALL)是最常见的成人急性白血病之一,它是一类以原幼淋巴细胞恶性增殖、蓄积、浸润为特点的恶性血液病。多项研究报道采用系统治疗方案,ALL患者完全缓解率(CR)70%-90%, 3-5年无病生存率为60%。尽管成人ALL的初治CR率己有明显提高,但复发率高,长期生存率仍较低。同样,儿童急性髓细胞白血病占儿童急性白血病的20%左右,却占儿童AL病死人数的50%以上。目前使用新型药物及造血干细胞移植的先进治疗方案可使患者获得接近70%的长期无病生存和超过50%的5年无事件生存率,但是复发率和病死率同样较高。发生类似以上复发死亡的主要原因就是微小残留(MRD) 所引起。急性淋巴细胞白血病在发病时体内大约有1012左右的白血病细胞,但经过多种化疗药物的联合应用,在达完全缓解时,体内仍剩余108-1010左右的白血病细胞,但这些残余白血病细胞通过现行形态学检测己无法做出准确的测评,且这些残存白血病细胞即是白血病复发的根源,因此这种白血病完全缓解后体内仍残存白血病细胞的状态称为微小残留病变。
目前MRD检测技术主要是流式细胞术及多聚酶链式反应技术。虽然PCR灵敏度高,但可用于PCR监测的融合基因较少,使用范围窄;基因突变、原癌基因过表达虽然覆盖率高,但是灵敏度低。虽然mpFC 对于复发疾病的检测灵敏度为10-4,但是复杂的多维数据依赖于实验人员分析,人为因素影响大,不利于临床标准化检测。此外,在化疗后白血病抗原的表达水平对MRD的mpFC检测具有干扰作用。依赖于分子手段可以提高检测MRD的灵敏度,可以达到10-5;然而,实时定量PCR需根据患者设计特殊的引物将多样性丰富的重排序列扩增出来,其检测费用昂贵、劳动力密集、很难形成标准化实验流程,目前在进行检测时多使用试剂盒进行检测,但是现有的检测盒,结构简单,仅能够起承载作用,不能根据试剂瓶的大小进行调节,且不能储存试剂瓶,很不方便,为此,我们提出了一种用于T细胞白血病微小残留病检测的试剂盒来解决上述问题。
技术实现要素:
本实用新型的目的是为了解决现有技术中存在的缺点,而提出的一种用于T细胞白血病微小残留病检测的试剂盒。
为了实现上述目的,本实用新型采用了如下技术方案:
一种用于T细胞白血病微小残留病检测的试剂盒,包括盒体,所述盒体上铰接有盒盖,所述盒盖的上端中部设有限位槽,所述限位槽内转动连接有提手,所述盒体的两侧均设有开口,所述开口上贯穿设有放置板,所述放置板的两侧均设有滑块,所述盒体内相对的侧壁上设有和滑块对应的滑槽,且滑块位于滑槽内,所述放置板上设有放置槽,所述放置槽内等间距设有多个吸盘,所述吸盘上设有放气口,所述放气口上设有密封塞,所述吸盘的上端固定有支撑杆,所述支撑杆远离吸盘的一端固定有承载板,所述承载板上固定有试剂瓶夹紧装置,所述放置板的一侧设有握把,所述盒体内的底部从左至右等间距设有两个隔板,两个隔板将盒体的内部等间距分隔三个大小相等的第一试剂瓶储存区、第二试剂瓶储存区和第三试剂瓶储存区,所述三个试剂瓶储存区的底部等间距设有多个试剂瓶放置槽。
优选地,所述试剂瓶夹紧装置包括设置在承载板上的固定管,所述固定管为一端封闭的桶体,所述固定管封闭的一端焊接在承载板上,所述固定管上设有螺纹通孔,所述螺纹通孔内贯穿设有螺杆,所述螺杆的一端设有转动块,所述螺杆远离转动块的一端设有挤压块,且挤压块上包覆有海绵垫。
优选地,所述提手和握把上均设有防滑纹。
优选地,所述盒盖上设有锁扣,所述盒体上设有和锁扣对应的锁孔。
优选地,所述盒体内的侧壁上均设有保温层。
优选地,所述第一试剂瓶储存区的试剂瓶放置槽大于第二试剂瓶储存区的试剂瓶放置槽,所述第二试剂瓶储存区的试剂瓶放置槽大于第三试剂瓶储存区的试剂瓶放置槽。
本实用新型中,使用时,利用锁扣和锁孔将盒盖打开,将吸盘取出,根据需要从试剂瓶放置区取出对应的试剂瓶,可通过螺杆以及固定管来对不同的试剂瓶夹紧固定,从而进行检测,提手的设置方便进行携带,本实用新型通过固定管、螺杆以及吸盘的结合,实现了对不同试剂瓶的夹取,同时还可以储存不同类型的试剂瓶,方便操作,还便于携带,适宜推广。
附图说明
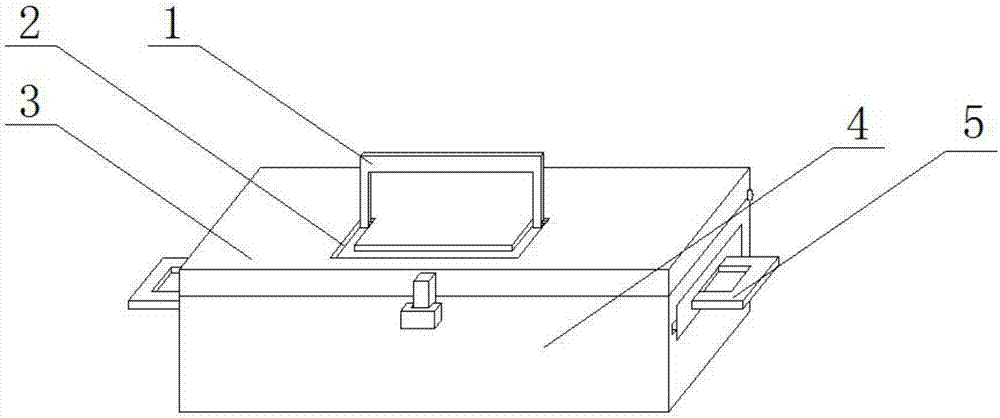
图1为本实用新型提出的一种用于T细胞白血病微小残留病检测的试剂盒的结构示意图;
图2为本实用新型提出的一种用于T细胞白血病微小残留病检测的试剂盒的内部结构示意图。
图中:1提手、2限位槽、3盒盖、4盒体、5握把、6滑槽、7 隔板、8固定管、9吸盘、10放置板、11螺杆、12支撑杆、13滑块。
具体实施方式
下面将结合本实用新型实施例中的附图,对本实用新型实施例中的技术方案进行清楚、完整地描述,显然,所描述的实施例仅仅是本实用新型一部分实施例,而不是全部的实施例。
参照图1-2,一种可用于T细胞白血病微小残留病检测的试剂盒,使用步骤如下:
1、一步法RT-PCR步骤;
2、磁珠纯化步骤
1)取出磁珠振荡混匀5min取出45μl/个样本的量放于室温 10min;
2)RT-PCR的产物各取出20μl,剩余5μljustincase,再每个样本加入30μlH2O,最后按照45μl/个加入磁珠,用枪吸吹约10次混匀,放于室温2min;
3)开盖放于磁力架上1min左右,液体变得澄清即可洗出液体,加入125μl85%的乙醇,1min后洗出弃掉,磁珠放于室温8min(5-10min)晾干。
3、用Nanodrop测定DNA的浓度。如果浓度是20ng/μl,稀释5 倍;如果接近40ng/μl,稀释10倍。
4、末端修复:在1.5ml离心管中混合以下成分(50μl)
1)34μl纯化的病人样本基因组DNA(或补水至34μl)
2)5μl10×末端修复缓冲液
3)5μl2.5mMdNTP混合物
4)5μl10mMATP
5)1μl末端修复酶
室温放置45分钟。用QIAquickPCR纯化柱纯化,用34μl缓冲液洗脱。
5、3’末端加A:在1.5ml离心管中混合以下成分(50μl):
1)34μl步骤4的末端修复后的DNA
2)5μlKlenow缓冲液=NEBbuffer2
3)10μl1mMdATP
4)1μlKlenow片段(3’à5’外切酶活性)
(1mMdATP用100mMdATP母液稀释,每管25μl分装,只能冻融一次)
用MinElutePCR纯化柱纯化,12μl缓冲液洗脱。
6、接头连接:在1.5ml离心管中混合以下成分(30ul)
1)11μl步骤5的DNA
2)15μlDNA连接缓冲液
3)1μl1:20稀释的接头寡核苷酸
4)3μlDNA连接酶
如果同时做多个重复,确保每个平行反应加入不同的接头,标记清楚。
7、凝胶筛选除去多余的接头:
将6μl稀释10倍的上样缓冲液加入到30μl第6步的反应液中,上样至两个E-gel胶孔中。另外取20μl稀释10倍的50bpDNAladder 上样。电泳20分钟。
切取大小在150bp到450bp之间的DNA,用QIAquick凝胶纯化试剂盒纯化,
30μl洗脱缓冲液洗脱。
8、用Illumina引物PCR:
用Gibco水将IlluminaPCR引物1.1和2.1进行1:1稀释
在PCR管中混合以下成分(60ul):
1)30μl步骤4的DNA
2)28μlPhusion PCR预混液
3)1μl稀释的引物1.1
4)1μl稀释的引物2.1
PCR循环:
9、2%琼脂糖凝胶上进行分子量筛选:
将1μl稀释的上样缓冲液加入到上一步的PCR反应液中,上样至三个E-gel胶孔中。另外分别取20μl稀释10倍的50bp和 100bpDNAladder上样。电泳30分钟。切取大小在400bp左右的DNA。用QIAquick凝胶纯化试剂盒纯化DNA,用30μl洗脱缓冲液洗脱。
10、测定DNA浓度。用NanoDrop测定所得DNA的浓度。
本实用新型中,使用时,利用锁扣和锁孔将盒盖3打开,将吸盘 9取出,根据需要从试剂瓶放置区取出对应的试剂瓶,可通过螺杆11 以及固定管8来对不同的试剂瓶夹紧固定,从而进行检测,提手1的设置方便进行携带。
以上所述,仅为本实用新型较佳的具体实施方式,但本实用新型的保护范围并不局限于此,任何熟悉本技术领域的技术人员在本实用新型揭露的技术范围内,根据本实用新型的技术方案及其实用新型构思加以等同替换或改变,都应涵盖在本实用新型的保护范围之内。
- 还没有人留言评论。精彩留言会获得点赞!