一种定性检测幽门螺旋杆菌并进行基因分型的试剂盒的制作方法
本发明属于荧光定量pcr领域,具体涉及一种多重荧光pcr法定性检测幽门螺旋杆菌并进行基因分型的试剂盒。
背景技术:
幽门螺旋杆菌(helicobacterpylori,hp)是一种高感染率的慢性感染性致病菌。hp的感染可引起人类发生慢性胃炎、胃和十二指肠溃疡、与消化性胃粘膜相关的淋巴样组织淋巴瘤和胃腺癌。大多数患者无临床症状;然而约10%至20%的患者会发展为消化性溃疡,1%的患者会发展为胃癌。幽门螺旋杆菌被iarc(internationalagencyforresearchoncancer)划分为一种致癌物,被公认为能够产生癌症的唯一的细菌。
幽门螺旋杆菌种分为i型和ii型。i型幽门螺旋杆菌表达caga毒力蛋白,而ii型幽门螺旋杆菌缺乏整个caga基因,不具有caga基因,体外无毒素。临床分析表明,相比于ii型,i型幽门螺旋杆菌与十二指肠炎、十二指肠溃疡及胃癌密切相关。
流行病学研究表明幽门螺杆菌感染了世界范围内一半以上的人口,其发病率各个国家不同,甚至同一国家的各个地区也不相同。发病率的高低与社会经济水平,人口密集程度,公共卫生条件以及水源供应有较密切的关系。也有报道指出,hp的感染有明显的季节分布特征,以7~8月份为高峰。在亚洲地区,中国内地、中国香港、越南、印度等少年幽门螺杆菌的感染率分别60%、50%、40%、70%。
慢性胃炎患者的胃粘膜活检标本中hp检出率可达80%~90%,而消化性溃疡患者更高,可达95%以上,甚至接近100%。胃癌由于局部上皮细胞已发生异化,因此检出率高低报道不一。
在自然人群中初出生的新生儿血清中抗hp-igg水平很高,接近成人水平,可能从母体获得被动免疫抗体之故。半年后迅速下降。在我国及大多数发展中国家中阳性率待降至10%~20%后又迅速回升。大约在10岁以后即迅速上升达到或接近成人阳性检出率水平。
中国及大多数发展中国家人群hp感染因地区有所不同。低达20%,高达90%,人群中总感染率高于发达国家。
现阶段,临床上检测幽门螺旋杆菌主要采取组织活检、免疫学检测、c14呼气检查和荧光pcr法检测。(1)组织活检:取得胃黏膜样本涂片染色后进行镜检,特异性较高,但检测依赖于检验医师的经验与技术,已造成人为判读误差导致结果不准确。(2)免疫学检测:检测灵敏度不高,且易与空肠弯曲菌等病原体发生交叉反应,从而影响检测结果。(3)c14呼气检查:有出现假阳性的可能。(4)荧光pcr法检测:直接检测幽门螺旋杆菌核酸,灵敏度高、特异性好,操作简单且通过多重荧光pcr技术,能够在同一反应中检测幽门螺旋杆菌并对其进行基因分型。
技术实现要素:
本发明的目的在于提供一种多重荧光pcr法定性检测幽门螺旋杆菌并进行基因分型的试剂盒。
为实现上述目的,本发明采用如下技术方案:
本发明能对胃粘膜活检标本中幽门螺旋杆菌进行定性检测并对幽门螺旋杆菌进行分型,在检测是否为幽门螺旋杆菌感染的同时判断幽门螺旋杆菌的型别,可用于临床上幽门螺旋杆菌感染的辅助诊断、疗效检测以及流行病学调查。
试剂盒共包含4个组分:hp反应缓冲液,酶混合液,阳性对照,阴性对照,
hp反应缓冲液包含hp引物及探针、hp-1型引物及探针、内控引物及探针、dntps、mgcl2、kcl;
酶混合液包含热启动taq酶及ung酶;
阳性对照包含hp特异性质粒、hp-1特异性质粒、内控质粒及te水;
阴性对照包含te水。
引物探针序列:
各质粒的序列为:
质粒制备方法:
委托厦门纽克泰生物技术有限公司合成上述质粒序列,然后通过ta克隆的方法,将该序列连接至pgem-t载体上,转化到jm109大肠杆菌中进行培养,然后提取质粒并稀释至5.0×108copies/ml备用。
试剂组分配方:
hp反应缓冲液配方:tris(三羟甲基氨基甲烷)(ph9.0)40mmol/l,kcl(氯化钾)80mmol/l,mgcl2(氯化镁)2.5mmol/l,甲酰胺5wt.%,dntps(datp:dgtp:dctp:dttp:dutp为2:2:2:2:1)0.9mmol/l,hp上游引物333nmol/l,hp下游引物333nmol/l,hp探针125nmol/l,hp-1上游引物333nmol/l,hp-1下游引物333nmol/l,hp-1探针125nmol/l,内控上游引物200nmol/l,内控下游引物200nmol/l,内控探针50nmol/l。
酶混合液配方:热启动taq酶2u/µl,ung酶0.1u/µl。
pcr扩增条件为:38℃5分钟,95℃10分钟;进入以下循环:95℃15秒,58℃40秒(采集荧光),40循环。
本发明的优点在于:
优点:本发明具有以下优势:1、灵敏度达到500copies/ml;2、在同一管反应中既能检测幽门螺旋杆菌,又能对其进行基因分型;3、在反应中加入内控,能够实时监控反应成功与否。
有益效果:1、在检测幽门螺旋杆菌的同时进行基因分型,能够评估患者感染的严重程度;2、采用多重实时荧光pcr法检测,一个反应管中同时进行3个pcr反应,降低检测成本;3、降低患者经济负担。
附图说明
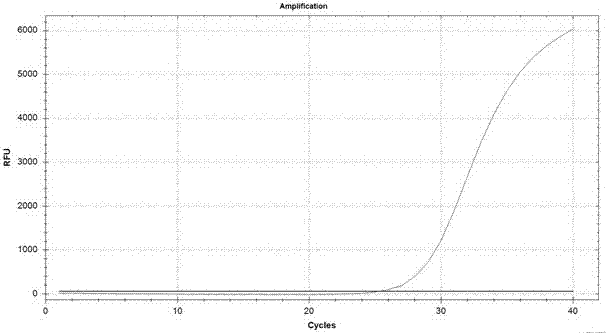
图1hp阳性检测结果图。
图2hp-1阳性检测结果图。
图3内控结果图。
图4i型幽门螺旋杆菌患者检测结果图。
图5ii型幽门螺旋杆菌患者检测结果图。
图6幽门螺旋杆菌阴性检测结果图。
具体实施方式
实施例1
1、试剂配制
(1)hp反应缓冲液的配制
取10ml容量瓶,分别加入0.5mol/l的trizma®hcl80μl,0.5mol/l的trizma®base720μl,100mmol/l的mgcl2250μl,5mol/l的kcl160μl,甲酰胺500μl,100mmol/l的dntps90μl,100μmol/l的hp上游引物33.3µl,100μmol/l的hp下游引物33.3µl,100μmol/l的hp探针12.5μl,100μmol/l的hp-1上游引物33.3µl,100μmol/l的hp-1下游引物33.3µl,100μmol/l的hp-1探针12.5μl,100μmol/l的内控上游引物20µl,100μmol/l的内控下游引物20µl,100μmol/l的内控探针5μl。用灭菌超纯水补足体积到10ml,混匀后,按1.5ml/支分装到离心管中,-20℃保存备用。
(2)酶混合液的配制
取10ml容量瓶,分别加入5000u/ml的热启动taq酶4ml,5000u/ml的ung酶0.2ml。用灭菌超纯水补足体积到10ml,混匀后,按25µl/支分装到离心管中,-20℃保存备用。
(3)阴性对照的配制
取10ml容量瓶,加入te水定容至10ml,按50µl/支分装到离心管中,-20℃保存备用。
(4)阳性对照的配制(浓度为5.0×103copies/ml)
取10ml容量瓶,分别加入5.0×105copies/ml的hp特异性质粒、hp-1特异性质粒和内控质粒(质粒委托厦门纽克泰生物技术有限公司合成)各100µl。用te水定容至100ml,混匀后,按50µl/支分装到离心管中,-20℃保存备用。
2、核酸提取
采用已备案的核酸提取试剂盒进行核酸提取,提取后用微量紫外分光光度计测核酸纯度,其od260/od280应在1.6~2.0之间。
3、加样上机
(1)反应混合物配制
取出hp反应缓冲液、酶混合液室温放置,使其充分溶解,配制反应混合物(每测试配置体系:29.5µl反应液+0.5µl酶混合液),按照需要计算好试剂用量,充分混合均匀后,3000-5000g离心5秒。
(2)加样
取28μl的上述pcr反应液分装至pcr反应管、八连条或96孔pcr反应板的n个上样孔中,分别加入样本dna、hp阳性对照或hp阴性对照各2μl。将管盖或封膜密封后,轻轻混匀并短暂离心,置入荧光pcr扩增仪内。
(3)上机检测
(1)循环条件设置
(2)检测模式:
4、结果判断
(1)阴性对照fam通道、hex通道的cp/ct应>36或无读值,rox通道的cp/ct应cp/ct>33或无读值;阳性对照fam通道、hex通道的cp/ct应≦36,rox通道的cp/ct应≦33;
(2)样本测试结果应以下表判断:
实施例2
1、试剂特异性验证
(1)实验样本
采取6份特异性样本对试剂的特异性进行验证,分别为:大肠杆菌、空肠弯曲菌、沙门氏菌、肠道病毒71型、科萨奇病毒16型、轮状病毒。
(2)实验过程
采用本方法所述试剂分别检测以上6份特异性样本,分析检测结果,验证试剂的特异性。
(3)实验结果
6份特异性样本检测结果皆为阴性,表明试剂特异性好,无交叉反应情况。具体结果见下表:
特异性检测结果
2、试剂精密性验证
(1)实验样本
采取1份i型幽门螺旋杆菌样本对试剂的精密性进行验证。
(2)实验过程
用本方法所述试剂重复检测以上样本20次,分析检测结果,验证试剂的精密性。
(3)实验结果
本试剂盒检测精密性样本的批内变异系数(cv值)<5%,表明试剂重复性好。具体结果见下表:
精密性检测结果
3、试剂最低检测限验证
(1)实验样本
将hp质粒及hp-1质粒分别稀释为500copies/ml,作为最低检测限样本。
(2)实验过程
本方法所述试剂分别重复检测以上最低检测限样本20次,分析检测结果,验证试剂的最低检测限。
(3)实验结果
检测两种质粒最低检测限样本均为阳性,试剂的最低检测限为500copies/ml。具体结果见下表:
实施例3:检测100例临床样本的结果
1、按照实施例1所示的配制方法,配制试剂盒相关组分,于-20℃保存备用。
2、于南京军区福州总院获得100例临床胃黏膜石蜡切片样本,采用嘉兴雅康博贝南生物科技有限公司石蜡组织核酸提取试剂(磁珠法)提取100例临床样本的基因组dna,用紫外分光光度计检测dna样本的纯度,100例样本od260/od280皆在1.6~2.0之间。
3、按照实施例1所示的步骤,进行dna加样并上荧光定量pcr仪进行检测,本次使用的仪器为bio-radcfx96。
4、采用测序法检测上述100例样本。
5、按照实施例1所示判断标准,对结果进行判读并统计,结果如下表:
检测结果见附图1~6。
图1为阳性对照中hp的扩增曲线;图2为阳性对照中hp-1的扩增曲线;图3为阳性对照中内控的扩增曲线;图4为i型幽门螺旋杆菌患者样本的扩增曲线,其中hp、hp-1、内控均为阳性;图5为ii型幽门螺旋杆菌患者样本的扩增曲线,其中hp、内控为阳性,hp-1为阴性;图6为幽门螺旋杆菌阴性患者样本的扩增曲线,其中hp、hp-1、内控均为阴性。
以上所述仅为本发明的较佳实施例,凡依本发明申请专利范围所做的均等变化与修饰,皆应属本发明的涵盖范围。
sequencelisting
<110>嘉兴雅康博贝南生物科技有限公司
<120>一种定性检测幽门螺旋杆菌并进行基因分型的试剂盒
<130>10
<160>9
<170>patentinversion3.3
<210>1
<211>20
<212>dna
<213>人工序列
<400>1
tcaataggggtatgcacggt20
<210>2
<211>20
<212>dna
<213>人工序列
<400>2
aaagactgcggctgaattga20
<210>3
<211>20
<212>dna
<213>人工序列
<400>3
tcccatcaggaaacatcgct20
<210>4
<211>20
<212>dna
<213>人工序列
<400>4
tcatgggcgtgtttgatgaa20
<210>5
<211>20
<212>dna
<213>人工序列
<400>5
tatgtcggtggtggtagtgg20
<210>6
<211>20
<212>dna
<213>人工序列
<400>6
atcaagagccaaggcctgat20
<210>7
<211>149
<212>dna
<213>人工序列
<400>7
cggctgaattgatgcaagaaggacgcactcttttaaaacctgatgatgtgatggatggcg60
tggcaagcatgatccatgaagtgggtattgaagcgatgtttcctgatgggaccaaactcg120
taaccgtgcatacccctattgaggccaat149
<210>8
<211>197
<212>dna
<213>人工序列
<400>8
tcatgggtgtgtttgatgaatctttgaaagcaaggcaagaagcagaaaaaaatgcagagc60
ctgctggtggagattggcttgatatttttttatcatttgtgtttaacaaaaaacaatctt120
ccgatctcaaagaaacactcaatcaagagccaaggcctgattttgaacaaaatttagcca180
ctaccaccaccgacata197
<210>9
<211>175
<212>dna
<213>人工序列
<400>9
caacgtgtcagtggtggacctgacctgccgtctagaaaaacctgccaaatatgatgacat60
caagaaggtggtgaagcaggcgtcggagggccccctcaagggcatcctgggctacactga120
gcaccaggtggtctcctctgacttcaacagcgacacccactcctccacctttgac175
- 还没有人留言评论。精彩留言会获得点赞!