可用于激活与调节免疫系统的配合物及其制备方法和应用与流程
本发明涉及一类配合物材料,特别是基于1-甲基-2 -((3-(吡啶-2-基)咪唑并[1,5-a]吡啶-1-基)甲基)-1H-苯并[d]咪唑及其衍生物的配合物材料,该材料具有良好的光敏性,可应用于多种肿瘤细胞(MDA-MB-231,CT26,MCF-7,HT-29等)的高效光动力治疗,并且能够激活与调节动物免疫系统对肿瘤的识别、清除,达到治愈的目的。
背景技术:
光动力疗法(photodynamic therapy)是将三种无毒组分(光敏剂(photosensitizer),光和氧)汇聚于靶组织,从而产生具有细胞毒性的活性氧(reactive oxygen species),特别是单线态氧(1O2),导致细胞凋亡和坏死。与其他全身治疗方式相比,通过局部给予光敏剂和光照,光动力治疗可以减少对正常组织的附带损伤,因此近年来已被用于治疗癌症和其他疾病。越来越多的报导指出,存在某些化学治疗药物可以调节免疫系统,并引发免疫反应,从而维持长期持久的治疗效果。已经提出这些化疗药物(例如蒽环类抗生素,紫杉烷和吉西他滨)的治疗功效至少部分取决于这种脱靶的免疫系统调节作用。化疗药物参与肿瘤特异性免疫应答的其中一种途径是通过引发免疫原性细胞死亡(immunogenic cell death),由此垂死的癌细胞开始强有力的免疫应答,起到“抗癌疫苗”的作用。而对于光疗药物能够引起免疫原性细胞死亡清除肿瘤细胞,提高治疗效果,并且维持长期持久的治疗效果的报导甚少。
技术实现要素:
本发明的目的是提供一类基于1-甲基-2 -((3-(吡啶-2-基)咪唑并[1,5-a]吡啶-1-基)甲基)-1H-苯并[d]咪唑及其衍生物的配合物材料;
本发明的另一个目的是提供上述配合物材料的制备方法;
本发明的第三个目的是提供上述配合物材料应用于多种肿瘤细胞(MDA-MB-231,CT26,MCF-7,HT-29等)的高效光动力治疗,通过激活与调节动物免疫系统达到对肿瘤的识别、清除目的。
本发明实现过程如下:
结构通式(1)表示的配合物,
其中,M为Mn2+、Fe2+、Co2+、Ni2+、Cu2+、Zn2+;
R1、R2独立地选自氢原子,C1-C4的烷基(如甲基,乙基,丙基,异丙基,正丁基,异丁基,叔丁基),C1-C3的烷氧基(如甲氧基,乙氧基),苯基,羧基,羟基,硝基,氰基,三氟甲基,卤素基,环己基;
X为卤素原子(如F,Cl,Br)。
当R1、R2选自氢原子,X选自Cl时,所述配合物材料属于单斜晶系,P21/c空间群,晶胞参数为a = 8.65225(12) Å, b = 13.29863(17) Å, c = 16.5913(2) Å, α = 90 (deg), β = 94.9653(13) (deg), γ = 90 (deg)。
上述配合物的制备方法:
将化学计量比的N-甲基苯并咪唑-2-甲醛衍生物a与2-氨甲基吡啶衍生物b溶于有机溶剂中,加入可溶性卤代盐MX2,在100~180 ℃反应得到结构式(I)所示的配合物。
所述有机溶剂选自甲醇、乙醇、乙腈、DMF。
所述可溶性卤代盐MX2为Mn2+、Fe2+、Co2+、Ni2+、Cu2+、Zn2+的F、Cl或Br盐。
反应温度优选为120~160 ℃。
溶剂热金属离子原位配位催化通常用于无机功能材料的合成制备,在热液/溶剂热法条件下,经常观察到金属离子辅助的原位反应。当金属离子参与时,原位金属/配体在一锅中逐步反应,有时能够合成得到结构罕见的有机化合物及其金属配合物。溶剂热原位反应为新的氮杂环及其配合物类光敏剂的发现和扩展提供了机会。
本发明反应过程为:两分子的b首先发生偶联反应,接着通过关环反应得到中间体化合物,再进一步与a发生亲核反应得到最终产物。
本发明配合物具有良好的光敏性能,金属活性位点高,可应用于多种肿瘤细胞(三阴乳腺癌MDA-Mb-231细胞,小鼠结肠癌CT26细胞,乳腺癌细胞MCF-7细胞,人结肠癌HT-29细胞)的高效光动力治疗,并且能够激活与调节动物免疫系统对肿瘤的识别、清除,达到治愈的目的。
附图说明
图1为配合物Fe(L3)Cl2的结构图;
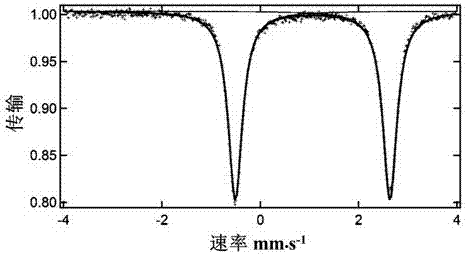
图2为配合物Fe(L3)Cl2的穆斯堡尔谱图;
图3为配合物Fe(L3)Cl2的热重分析图;
图4为配合物Fe(L3)Cl2的粉末衍射图;
图5为配合物Zn(L3)Cl2的结构图;
图6为配合物Mn(L3)Cl2的结构图;
图7为配合物Mn(L3)Br2的结构图;
图8为配合物Co(L3)Cl2的结构图;
图9为配合物Fe(L3)Cl2的生成机理图;
图10为配合物Fe(L3)Cl2的对各种不同细胞(MDA-Mb-231,CT26,MCF-7,HT-29)杀伤作用效果图;
图11为配合物Fe(L3)Cl2的荧光光谱图;
图12为配合物Fe(L3)Cl2与配体L3对MDA-MB-231细胞的杀伤作用对比图。
具体实施方式
为了更清楚的理解本发明,以下通过发明人给出的依本发明技术方案所完成的具体的实施例对本发明进一步的详细描述。
实施例1: Fe(L3)Cl2的合成
将1.00 mmol的N-甲基苯并咪唑-2-甲醛(a, 0.1700 g) 加入到15 mL容量的聚四氟乙烯的反应釜中,加入10 mL的甲醇溶解后,再加入0.5 mmol的氯化亚铁(0.0811 g) ,在搅拌的条件下加入0.25 mmol的2-氨甲基吡啶(b, 26 μL),继续搅拌3分钟,密封,放入140 ℃的烘箱保温48 h,然后缓慢降温得到红色块状晶体(大概10 h降至室温),产率为71% (基于b)。晶胞参数为a = 8.65225(12) Å, b = 13.29863(17) Å, c = 16.5913(2) Å, α = 90 (deg), β = 94.9653(13) (deg), γ = 90 (deg)。
本发明具体反应过程:两分子的b首先发生偶联反应,接着通过关环反应得到,再与a发生亲核反应得到最终产物(详细机理见图9)。
如图1所示,配合物Fe(L3)Cl2的空间群是P21/c,不对称单元由一个Fe,一个L3和两个Cl组成。金属中心(Fe)与螯合配体L3提供的N3和两个弱配位Cl原子发生配位,Fe1-Cl1(2.336 Å)、Fe1-Cl2(2.340 Å)和Cl1-Fe1-Cl2(109.47°)。平面型有机配体位于与氯原子相反的一侧,并且有机配体L3处于的平面平分角Cl1-Fe1-Cl2。在配位氯原子的方向上容易发生反应,几乎没有阻碍。
如图2所示,配合物Fe(L3)Cl2的穆斯堡尔谱证实Fe处于+2价态。
如图3所示,配合物Fe(L3)Cl2的热重分析图,实验温度控制为室温到800 ℃,流速为15 cm3/min,升温速率为5 ℃/min,氮气条件下的热重分析表明,配合物Fe(L3)Cl2没有溶剂分子,并且在接近360 ℃时才开始分解,说明其热稳定性好。到800 ℃时,仍然剩余42.23%。
如图4为配合物Fe(L3)Cl2的粉末衍射图。通过粉末衍射的实验值和拟合值对比可以看出,通过上述方法合成的配合物Fe(L3)Cl2为纯相。
实施例2:Zn(L3)Cl2的合成
将1.00 mmol的N甲基-苯并咪唑-2-甲醛(0.1700 g) 加入到15 mL容量的聚四氟乙烯的反应釜中,加入10 mL的甲醇溶解后,再加入0.5 mmol的氯化锌(0.0685 g) ,在搅拌的条件下加入0.25 mmol的2-氨甲基吡啶(26 μL),继续搅拌3分钟,密封,放入140 ℃的烘箱保温72 h,然后缓慢降温得到橘黄色块状晶体(大概10 h降至室温) ,产率为63% (基于2-氨甲基吡啶)。晶胞参数为a = 8.6279(4) Å, b = 13.3115(6) Å, c = 16.4043(2) Å, α = 90 (deg), β = 95.531(1) (deg), γ = 90 (deg)。
如图5所示,配合物Zn(L3)Cl2的空间群是P21/c,结构与Fe(L3)Cl2相似。
实施例3:Mn(L3)Cl2的合成
将1.00 mmol的N甲基-苯并咪唑-2-甲醛(0.1700 g) 加入到15 mL容量的聚四氟乙烯的反应釜中,加入10 mL的甲醇溶解后,再加入0.5 mmol的四水氯化锰(0.099 g) ,在搅拌的条件下加入0.25 mmol的2-氨甲基吡啶(26 μL),继续搅拌3分钟,密封,放入160 ℃的烘箱保温72 h,然后缓慢降温得到黄色块状晶体(大概10 h降至室温) ,产率为61% (基于2-氨甲基吡啶)。晶胞参数为a = 8.7596(4) Å, b = 13.3602(7) Å, c = 16.7930(9) Å, α = 90 (deg), β = 95.375(4) (deg), γ = 90 (deg)。
如图6所示,配合物Mn(L3)Cl2的空间群是P21/c,结构与Fe(L3)Cl2相似。
实施例4:Mn(L3)Br2的合成
将1.00 mmol的N甲基-苯并咪唑-2-甲醛(0.1700 g) 加入到15 mL容量的聚四氟乙烯的反应釜中,加入10 mL的甲醇溶解后,再加入0.5 mmol的溴化锰(0.1074 g) ,在搅拌的条件下加入0.25 mmol的2-氨甲基吡啶(26 μL),继续搅拌3分钟,密封,放入160 ℃的烘箱保温72 h,然后缓慢降温得到黄色块状晶体(大概10 h降至室温) ,产率为58% (基于2-氨甲基吡啶)。晶胞参数为a = 8.9665(5) Å, b = 13.2430(8) Å, c = 16.9733(10) Å, α = 90 (deg), β = 96.832(2) (deg), γ = 90 (deg)。
如图7所示,配合物Mn(L3)Br2的空间群是P21/c,结构与Fe(L3)Cl2相似。
实施例5:Co(L3)Cl2的合成
将1.00 mmol的N甲基-苯并咪唑-2-甲醛(0.1700 g) 加入到15 mL容量的聚四氟乙烯的反应釜中,加入10 mL的甲醇溶解后,再加入0.5 mmol的四水氯化钴(0.119 g) ,在搅拌的条件下加入0.25 mmol的2-氨甲基吡啶(26 μL),继续搅拌3分钟,密封,放入160 ℃的烘箱保温48 h,然后缓慢降温得到黄色块状晶体(大概10 h降至室温) ,产率为46% (基于2-氨甲基吡啶)。晶胞参数为a = 8.5965(5) Å, b = 13.3363(8) Å, c = 16.4927(10) Å, α = 90 (deg), β = 94.615(5) (deg), γ = 90 (deg)。
如图8所示,配合物Co(L3)Cl2的空间群是P21/c,结构与Fe(L3)Cl2相似。
实施例6:
发明人通过使用不同的反应原料均可获得目标配合物,具体列表如下:
实施例7:实施例1制备得到的Fe(L3)Cl2应用于肿瘤细胞的光动力治疗
利用MTT比色法来分析Fe(L3)Cl2对各类肿瘤细胞的抗增殖效应。MTT,中文名叫噻唑蓝,是一种四唑盐,在活细胞中,线粒体内的琥珀酸脱氢酶可将MTT还原,生成一种蓝紫色产物-甲臜(可溶于DMSO),且该产物在490 nm处有吸收峰,故可用A490nm来分析细胞增殖情况。
MTT实验步骤如下:①先各复苏1管肿瘤细胞,用新鲜培养液(DMEM培养基+10%胎牛血清)培养,传代2次后使用。②待细胞到达对数生长期时,以8000个/孔的细胞密度接种至2块96孔板中(每孔用100 μL培养液培养细胞,一板为光照组,另一板为黑暗对照组),送入恒温箱(37 °C,5% CO2)中培养。③待其贴壁后,每孔加入100 μL含有不同浓度Fe1的新鲜培养液,轻轻晃匀,在恒温箱中避光孵育4 h后,将光照组的细胞培养板置于100 W卤钨灯下光照1 h(每照射20 min休息5 min,功率密度:25 mW/cm2),然后放回温箱接着避光孵育19 h(黑暗对照组的细胞一直置于温箱中避光培养)。④ 弃两板内原有培养基,用PBS漂洗细胞一次,每孔换成200 μL新鲜的含药培养液。37 °C避光孵育4 h后,将光照组的细胞培养板置于卤钨灯下继续间断式光照1 h(黑暗对照组的细胞不做处理),然后接着避光孵育19 h。⑤ 每孔加入20 μL MTT (5 mg/mL),于37 °C温箱中孵育4 h后检测A490nm。
如图10所示,MTT法检测配合物Fe(L3)Cl2(Fe1-NBM)在黑暗与光照处理条件下对多种肿瘤细胞(三阴乳腺癌MDA-Mb-231细胞,小鼠结肠癌CT26细胞,乳腺癌细胞MCF-7细胞,人结肠癌HT-29细胞)的生长抑制效果,同时该生长抑制作用可以被还原剂N-乙酰半胱氨酸(NAC)清除。
如图11所示,配合物Fe(L3)Cl2的浓度为5*10-4mol/L,测试电压为500V,狭缝宽度为5nm的测试条件下,使用300nm和400nm激发得到的样品光致发光(荧光)光谱图。
如图12所示,MTT法检测相同浓度的配合物Fe(L3)Cl2与配体L3通过黑暗与光照处理之后对MDA-MB-231细胞的杀伤作用效果;明显看出,配合物Fe(L3)Cl2在光照条件下对MDA-MB-231细胞杀伤作用非常强,而在黑暗条件下杀伤作用非常弱;配体L3无论是否光照均无有效的杀伤效果。
- 还没有人留言评论。精彩留言会获得点赞!