检测FGD1基因突变的引物和方法与流程
本发明属生命科学和生物技术领域,特别涉及检测fgd1659+27t>c和482-113c>t位点突变的引物,采用普通pcr结合sanger测序技术,可用于快速检测fgd1位点的突变情况。
背景技术:
aarskog综合征(aarskogsyndrome,aas)是一种罕见的遗传性面-指-生殖器异常综合征,主要临床表现为身材矮小、面部、指(趾)和生殖器形态改变,但程度各异,还可合并其他多种异常,目前诊断必备的表型尚不明确。aas是由位于xp11.21的fgd1基因突变所致的一种x连锁隐性遗传性疾病。
fgd1基因(fyve,rhogefandphdomaincontainingl,nc_000023)共含有18个外显子,能够编码形成一种鸟嘌呤核苷酸转化因子(guaninenucleotideexchangefactor,gef)。目前已经发现有多种fgd1的突变可导致aas的发生,包括第4,6,9-12及17号外显子区的缺失突变,第3和7号外显子区的插入突变,第3-8及15号外显子区的错义突变,以及在7、8、11号内含子剪切位点上的突变等。fgd1基因的突变可导致其编码的gef的结构域发生空间结构改变,从而干扰了fgd1/cdc42正常的信号传递系统,导致aas的发生。
aas患者可出现身材矮小、智力缺陷及生育障碍等多种复杂、严重的临床症状,严重威胁着患者的身体健康和生活质量。通过检测fgd1基因突变情况,将有望据此对高危的可疑人群(如有相关家族史,或有放射性辐射接触史等)开展早期筛查和干预,从而将有利于对该病进行基因筛查、产前诊断、植入前遗传学分析、靶位治疗和新药研发等,最终对该病的早期预防与诊断、优生与优育等产生重要意义。
技术实现要素:
本发明的目的是提供一种检测fgd1659+27t>c和482-113c>t位点突变的引物,采用pcr结合sanger测序技术,可用于快速检测fgd1659+27t>c和482-113c>t位点的突变情况。所述检测fgd1659+27t>c和482-113c>t位点突变情况的引物,包括:扩增fgd1659+27t>c和482-113c>t位点5号外显子的引物,其碱基序列为:
fgd1-exon-3-f:tgtaaaacgacggccagtgcctcctgagttcaagcaat
fgd1-exon-3-r:aacagctatgaccatgtctgaggtgggtggtggac。
进一步地,还包括测序引物,其碱基序列为:
m13f:tgtaaaacgacggccagt
m13r:aacagctatgaccatg
本发明提供了检测fgd1659+27t>c和482-113c>t位点突变情况的方法,包括以下步骤:
(1)抽提血液中的基因组dna;
(2)用pcr扩增步骤1中提取的dna;
(3)对步骤2中的扩增产物进行测序;
(4)对测序结果进行判断,确定fgd1659+27t>c和482-113c>t位点是否发生突变。
本发明还提供了一种检测fgd1659+27t>c和482-113c>t位点突变的试剂盒,包括
(i)血液dna抽提试剂;
(ii)检测体系pcr扩增反应液;
(iii)测序体系试剂。
本发明还提供了一种检测fgd1659+27t>c和482-113c>t位点突变的试剂盒,所述试剂盒包括检测体系pcr扩增反应液、测序体系反应液,所述检测体系pcr扩增反应液包括至少fgd1-exon-3-f和fgd1-exon-3-r这对扩增引物,所述测序体系反应液包括m13f和m13r这对测序引物。
进一步地,所述检测体系pcr扩增反应液还包括2×pcrbuffer、dntps和kodfxdnapolymerase。
进一步地,所述测序体系反应液还包括edta、无水乙醇、75%乙醇、hidi和bigdyeterminatorv3.1。
有益效果:本发明设计了扩增fgd1659+27t>c和482-113c>t位点的引物。采用pcr技术,构建了稳定的扩增体系。通过调整引物浓度、退火温度等反应条件,可使扩增效率达到最佳。本发明利用sanger测序技术检测fgd1659+27t>c和482-113c>t位点突变的方法,可以准确将fgd1659+27t>c和482-113c>t位点突变类型检测出来,相比较荧光定量pcr法降低了检测的成本和难度。荧光定量pcr法要针对不同的突变类型设计2个探针,而且不能在同一管里检测,成本高,检测难度大。
附图说明
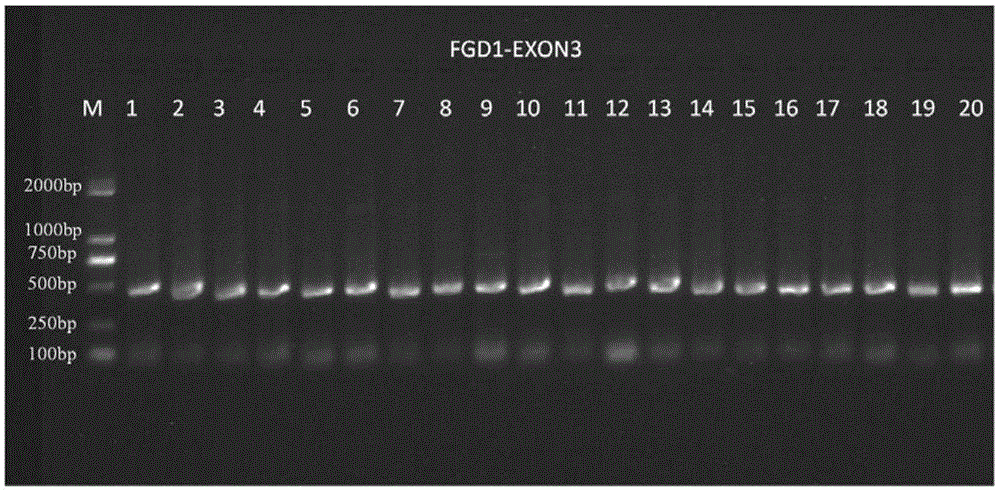
图1为20例临床样本引物扩增后的琼脂糖凝胶电泳图,m为markerdl2000,1-20为20例血液样本,经验证,引物扩增有效,且目的条带清晰,产物大小正确。
图2为样本3fgd1659+27t位点的测序截图,表明为阴性样本。
图3为样本1fgd1659+27t位点的测序截图,表明为阳性样本。
图4为样本3fgd1482-113c位点的测序截图,表明为阴性样本。
图5为样本1fgd1482-113c位点的测序截图,表明为阳性样本。
具体实施方式
实施例1
下面结合具体实施例和附图,进一步阐述本发明。应当注意的是,实施例中未说明的常规条件和方法,通常按照所属领域实验人员常规采用方法:譬如,奥斯柏和金斯顿主编的《精编分子生物学实验指南》第四版,或者按照制造厂商所建议的步骤和条件。
一种检测fgd1659+27t>c和482-113c>t位点突变的引物和方法,该引物是针对扩增fgd1659+27t>c和482-113c>t位点突变所设计的特异性扩增引物,其碱基序列为:
fgd1-exon-3-f:tgtaaaacgacggccagtgcctcctgagttcaagcaat
fgd1-exon-3-r:aacagctatgaccatgtctgaggtgggtggtggac。
一种检测fgd1659+27t>c和482-113c>t位点突变的试剂盒,包括
(i)血液dna抽提试剂;
(ii)检测体系pcr反应液;
(iii)测序体系试剂;
(iv)阳性对照品和阴性对照品。
其中,血液dna抽提试剂可购自天根dna抽提试剂盒等商品化试剂。
检测体系pcr扩增反应液包括:2×pcrbuffer;2mmdntps;kodfxdnapolymerase(1u/μl);fgd1659+27t>c和482-113c>t位点上、下游引物(10μm)。
测序体系试剂包括:测序纯化液(exoi:0.6u,cip:1.2u)、edta(125mmol)、无水乙醇、75%乙醇、hidi(高度去离子甲酰胺)、测序引物:m13f和m13r(3.2μm)。
实施例2
血液基因组dna抽提试剂盒(天根生物)的操作流程:
(1)抽提血液中的基因组dna
1)抽取300μl血液加入900μl红细胞裂解液,颠倒混匀,室温放置5分钟,期间再颠倒混匀几次。12,000rpm离心1min,吸去上清,留下白细胞沉淀,加200μl缓冲液ga,振荡至彻底混匀。
2)加入20μl蛋白酶k溶液,混匀。
3)加入200μl缓冲液gb,充分颠倒混匀,70℃放置10分钟,溶液应变清亮,简短离心以去除管盖内壁的水珠。
4)加入200μl无水乙醇,充分振荡混匀15秒,此时可能会出现絮状沉淀,简短离心以去除管盖内壁的水珠。
5)将上一步所得溶液和絮状沉淀都加入一个吸附柱cb3中(吸附柱放入收集管中),12,000rpm离心30秒,倒掉废液,将吸附柱cb3放回收集管中。
6)向吸附柱cb3中加入500μl缓冲液gd(使用前请先检查是否已加入无水乙醇),12,000rpm离心30秒,倒掉废液,将吸附柱cb3放入收集管中。
7)向吸附柱cb3中加入700μl漂洗液pw(使用前请先检查是否已加入无水乙醇),12,000rpm离心30秒,倒掉废液,将吸附柱cb3放入收集管中。
8)向吸附柱cb3中加入500μl漂洗液pw,12,000rpm离心30秒,倒掉废液。
9)将吸附柱cb3放回收集管中,12,000rpm离心2分钟,倒掉废液。将吸附柱cb3置于室温放置数分钟,以彻底晾干吸附材料中残余的漂洗液。
10)将吸附柱cb3转入一个干净的离心管中,向吸附膜的中间部位悬空滴加100μl洗脱缓冲液te,室温放置2-5分钟,12,000rpm离心2分钟,将溶液收集到离心管中。
(2)试剂配置:按检测人份数配置检测体系pcr反应液各xμl,每人份18μl分装:
x=18μl反应液×(n份标本+1份阳性对照+1份阴性对照+1份空白对照)
n为检测标本数。
(3)加样:加入检测体系pcr反应液中2μldna;阳性对照和阴性对照直接加2μl阳性对照品和阴性对照品;空白对照加2μl生理盐水或不加任何物质。
(4)扩增:检测在常规pcr仪上进行,可用仪器包括abiveriti(美国appliedbiosystems公司)等。反应条件如下:
pcr扩增体系试剂配制方法如下:
其中,引物序列为:
fgd1-exon-3-f:tgtaaaacgacggccagtgcctcctgagttcaagcaat;
fgd1-exon-3-r:aacagctatgaccatgtctgaggtgggtggtggac。
(5)电泳:1.5%琼脂糖凝胶电泳,110v,35min,凝胶成像系统观察。
如图1所示,即为2例血液样本以相应的引物扩增后所得产物的电泳图谱。通过电泳图的分析表明本发明所述扩增有效,且条带清晰。
(6)sanger测序:
取9pcr产物与2μl纯化体系。按照以下程序进行纯化:
将1μl纯化产物分别与上、下测序引物按照如下体系进行混合:
测序反应程序:
沉淀环节:
向完成测序反应的产物中加入2μl125mmol的edta,静置5min;加入15μl无水乙醇,漩涡混匀;3700rpm离心30min;倒置离心15sec,加入50ml70%乙醇,漩涡混匀;3700rpm离心15min;倒置离心15sec,置于95℃金属浴上;加入10μlcbl后进行变性5min,最后-20℃2min上测序仪(abi3730)测序。
(7)结果判断:分别将测序结果与fgd1(nc_000023)阴性参考序列进行比对,根据实际突变情况对结果进行报告。
实施例3
取20例临床样品,按实施例1和2所述方法提取基因组、配制试剂并检测。样本加入检测体系pcr反应液中1μl,同时做阳性,阴性,空白对照各一份。电泳结果如图1所示,表明本发明所述引物对血液样本能有效扩增,且条带单一。
测序后发现共有8例样本发生fgd1659+27t>c和482-113c>t突变,分别为样本1、2、6、10、11、12、13、18,两种突变在样本中同时发生,且全部为纯合突变。样本1(阳性样本)和样本3(阴性样本)的测序结果如图2-5所示。图2和图3为fgd1659+27t位点阴性和阳性样本的测序截图。图4和图5为fgd1482-113c位点阴性和阳性样本的测序截图。
序列表
<110>杭州艾迪康医学检验中心有限公司
<120>检测fgd1基因突变的引物和方法
<160>4
<170>siposequencelisting1.0
<210>1
<211>38
<212>dna
<213>人工序列(artificialsequence)
<400>1
tgtaaaacgacggccagtgcctcctgagttcaagcaat38
<210>2
<211>35
<212>dna
<213>人工序列(artificialsequence)
<400>2
aacagctatgaccatgtctgaggtgggtggtggac35
<210>3
<211>18
<212>dna
<213>人工序列(artificialsequence)
<400>3
tgtaaaacgacggccagt18
<210>4
<211>16
<212>dna
<213>人工序列(artificialsequence)
<400>4
aacagctatgaccatg16
- 还没有人留言评论。精彩留言会获得点赞!