一种扇贝类胡萝卜素氧化裂解酶基因及其应用的制作方法
本发明属于生物工程技术领域,具体涉及一种扇贝类胡萝卜素氧化裂解酶基因及其应用。
背景技术:
虾夷扇贝(patinopectenyessoensis)于上世纪80年代由日本引入我国,已成为中国北方重要的海水养殖贝类。普通虾夷扇贝的闭壳肌为白色,但在我国虾夷扇贝养殖群体中有的个体其闭壳肌呈橘红色。研究表明,呈橘红色的闭壳肌内积累扇贝醇酮和梳黄质两种类胡萝卜素,而在普通虾夷扇贝的白色闭壳肌中则检测不到扇贝醇酮和梳黄质。进一步的家系和多组学分析显示,闭壳肌呈橘红色为单基因决定的隐性性状,类胡萝卜素氧化裂解酶基因的表达下调是闭壳肌积累类胡萝卜素,从而呈橘红色的原因,该基因是扇贝代谢类胡萝卜素的关键基因。
类胡萝卜素是亲脂性的黄色、橙色或红色的天然色素,在自然界中广泛分布并具有结构和功能多样性。类胡萝卜素通过氧化降解产生的代谢物参与广泛的生物学过程。比如其中一种降解产物视黄醛,是11-顺式-视黄醛(视觉发色团)和全反式视黄酸等信号分子的前体。
虾夷扇贝是我国重要海产经济贝类,其主要的食物微藻中含有大量类胡萝卜素,因此制备虾夷扇贝类胡萝卜素氧化裂解酶对研究贝类类胡萝卜素代谢机制有重要意义。
技术实现要素:
本发明的目的是提供一种具有降解虾夷扇贝类胡萝卜素的蛋白酶,通过抑制该蛋白酶的表达可提高扇贝闭壳肌的类胡萝卜素含量,从而弥补现有技术的不足。
本发明提供一种具有降解虾夷扇贝类胡萝卜素的蛋白酶,所述的蛋白酶包含有:
1)氨基酸序列为seqidno:1的蛋白酶;
2)在1)的氨基酸序列上经过取代、缺失或添加一个或几个氨基酸且具有1)中蛋白酶活性的,从虾夷扇贝中获得的蛋白酶。
编码上述蛋白酶的基因,其一种核苷酸序列为seqidno:2;
本发明还提供一种大肠杆菌重组菌株,所述的大肠杆菌重组菌株用于重组表达氨基酸序列为氨基酸序列为seqidno:1的蛋白酶;
本发明再提供一种制备氨基酸序列为seqidno:1的蛋白酶的方法,是使用上述的大肠杆菌重组菌株进行发酵制备的。
所述的方法,其步骤如下:
第一步,构建表达质粒。对虾夷扇贝类胡萝卜素氧化裂解酶基因的编码区进行扩增,将扩增得到的片段连接至pet-28a表达载体;
第二步,蛋白的原核表达:将重组质粒转入大肠杆菌感受态细胞,添加诱导剂iptg以诱导蛋白表达。离心收集菌体,在收集到的菌体中加入缓冲液,并使用超声破碎仪使其充分溶解。离心后分别处理上清和沉淀,进行sds-page检测;
第三步,蛋白的纯化。根据sds-page检测结果,选择适当诱导条件进行大量表达,离心收集菌体。用缓冲液溶解菌体,超声破碎后,离心收集上清粗蛋白。使用ni-nta柱对蛋白进行纯化,对粗蛋白、洗杂流出、洗脱流出分别处理、制样,并进行sds-page检测。将纯度较好的组分进行透析、浓缩以及过滤,分装后于-80℃保存。本发明属于生物工程技术领域,具体涉及一种贝类类胡萝卜素氧化裂解酶的制备方法。
本发明利用基因工程技术,将虾夷扇贝类胡萝卜素氧化裂解酶基因的编码区域克隆到原核表达载体中,然后将重组质粒转化至大肠杆菌,并用异丙基-β-d-硫代半乳糖苷(iptg)诱导融合蛋白表达,最后将融合蛋白进行纯化和透析浓缩。通过本发明所提供的原核表达及蛋白纯化方法,可高效制备扇贝类胡萝卜素氧化裂解酶,为从蛋白水平深入研究贝类胡萝卜素代谢机制提供了必要的实验工具。
附图说明
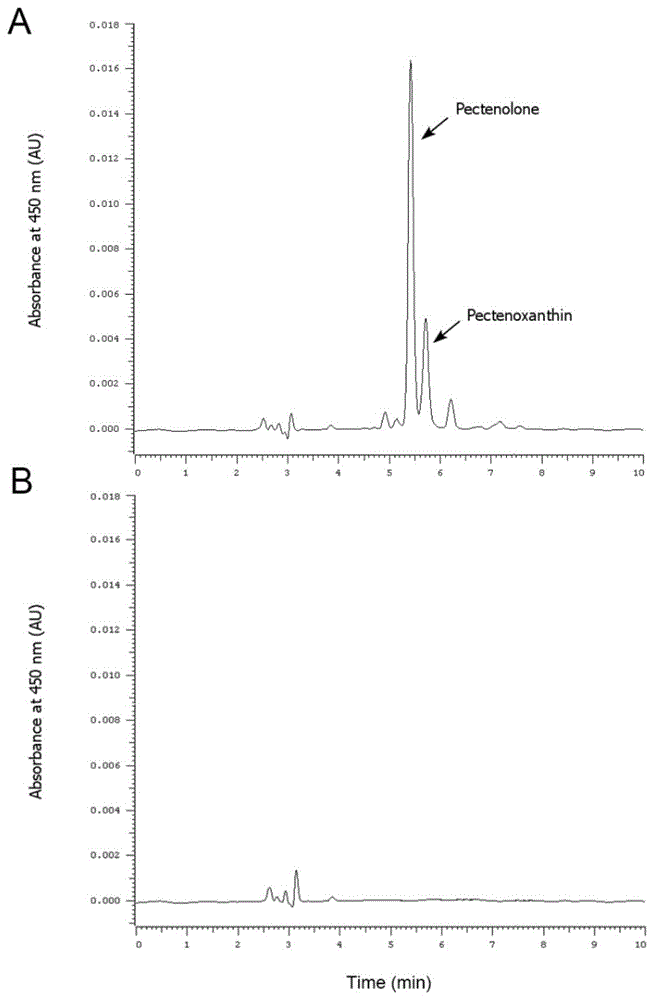
图1:hplc检测实验组及对照组闭壳肌中的类胡萝卜素。a:dsrna注射实验组,b:对照组。
图2:融合蛋白原核表达sds-page分析图。m:proteinmarker;1:诱导前总蛋白;2:20℃上清;3:20℃沉淀;4:37℃上清;5:37℃沉淀。
图3:类胡萝卜素氧化裂解酶表达引起的β-胡萝卜素积累菌株颜色变化,(c-):导入空pet-28a质粒的β-胡萝卜素积累菌株;(c+):导入类胡萝卜素氧化裂解酶表达质粒的β-胡萝卜素积累菌株。
图4:融合蛋白镍琼脂糖亲和层析纯化sds-page分析图。m:proteinmarker;1:上样;2:流出;3-4:20mmimidazole洗脱组分;5:50mmimidazole洗脱组分;6:500mmimidazole洗脱组分。
图5:最终纯化蛋白sds-page分析图。m:proteinmarker;1:融合目的蛋白。
具体实施方式
下面结合实施例对本发明的蛋白酶进行详细的描述。
实施例1:筛选蛋白酶
申请人通过全基因组连锁分析、关联分析、表达谱分析等多组学研究发现,扇贝橘红色闭壳肌积累类胡萝卜素的原因是类胡萝卜素氧化裂解酶下调表达,使类胡萝卜素降解效率降低。
最终从虾夷扇贝基因组和转录组数据库中获得目的基因,该基因全长9107bp,cdna长度2682bp,其中cds长度为1566bp(seqidno:2),编码521个氨基酸(seqidno:1),预测蛋白分子量59.2kda,等电点为6.54;5′utr长度为510bp,3′utr长度为609bp。
通过注射dsrna,干扰该基因表达。qrt-pcr检测干扰成效,通过观察闭壳肌颜色变化以及hplc分析,证明干扰后扇贝的肌肉中有类胡萝卜素积累(图1),即筛选的基因具有降解类胡萝卜素的功能。
通过rna干扰(rnai)技术抑制该基因的表达,检测干扰后所述基因表达量的变化,以及扇贝闭壳肌中类胡萝卜素的含量,证明所筛选的基因具有降解虾夷扇贝类胡萝卜素的功能,为一种虾夷扇贝类胡萝卜素氧化裂解酶。
实施例2
本发明中虾夷扇贝类胡萝卜素氧化裂解酶蛋白的原核表达包括下列步骤:
a)类胡萝卜素氧化裂解酶编码序列的扩增;
b)表达质粒的构建;
c)类胡萝卜素氧化裂解酶的原核表达;
d)原核体系中类胡萝卜素氧化裂解酶活性验证。
具体操作如下:
a)类胡萝卜素氧化裂解酶编码序列的扩增。以虾夷扇贝闭壳肌cdna为模板,使用含有pet-28a载体相应酶切位点及保护碱基的引物:
5′-ccggaattcgtcccaccagc-3′;
5′-tcccaagctttcaagggatgttaaagaacc-3′
对目的片段进行扩增,反应体系(20μl)为:
扩增所用pcr反应程序:98℃预变性30s;98℃变性10s,62℃退火30s,72℃延伸50s,30个循环;72℃延伸10min。
b)表达质粒的构建。对扩增得到的目的片段以及pet-28a载体进行双酶切,酶切体系为:
37℃酶切15min,酶切产物用qiaquickpcrpurificationkit进行纯化。
用t4连接酶将纯化后的片段和载体进行连接,连接体系(25ul)为:
于pcr仪16℃连接过夜。经转化、提取等步骤得到重组质粒后,进行测序以验证导入序列的正确性。
c)类胡萝卜素氧化裂解酶的原核表达。将重组质粒转入rosetta(de3)感受态细胞,涂布于lb固体培养基(50μg/ml卡那霉素)。挑取单克隆到含有抗生素的液体培养基中进行培养,当od值达到0.6时,添加诱导剂iptg。分别于20℃条件下培养16h、37℃条件下培养4h,未添加诱导剂的为阴性对照。离心收集菌体,弃上清,在收集到的菌体中加入缓冲液a,使用超声破碎仪使其充分溶解。再次进行离心,离心后的沉淀使用缓冲液b进行溶解。分别对上清和沉淀进行处理、制样,并准备sds-page检测,根据检测结果确定最佳表达条件(图2)。
d)原核体系中类胡萝卜素氧化裂解酶活性验证。将重组质粒转入积累β-胡萝卜素且呈橘黄色的大肠杆菌中,涂布于lb固体培养基(50μg/ml卡那霉素)。挑取单克隆在液体培养基(50μg/ml卡那霉素,25μg/ml氯霉素)中培养至od600值达0.6。加入iptg诱导剂后,降低温度避光继续培养16小时。同时也将空pet-28a质粒导入β-胡萝卜素积累感受态中,用同样方法培养和诱导,作为对照组。离心收集细胞,观察细菌颜色的变化,发现相对于导入空pet-28a质粒的β-胡萝卜素积累菌株,表达类胡萝卜素氧化裂解酶蛋白的共转化菌株颜色明显变浅,证明所述酶在原核体系中具有活性(图3)。
实施例3
本发明中的虾夷扇贝类胡萝卜素氧化裂解酶蛋白纯化包括下列步骤:
a)类胡萝卜素氧化裂解酶蛋白的大量表达;
b)蛋白纯化;
c)纯化检测;
d)透析浓缩。
具体操作如下:
a)类胡萝卜素氧化裂解酶蛋白的大量表达。在含50μg/ml卡那霉素的液体培养基中培养细菌,当od值达到0.6时,添加0.5mm诱导剂iptg,20℃条件下培养16h进行大量表达,离心收集菌体。
b)蛋白纯化。菌体用缓冲液c溶解后进行超声破碎,离心收集上清粗蛋白。取5mlni-nta,用5倍柱床体积的bindingbuffer清洗平衡柱子,流速5ml/min。将粗蛋白与平衡后的柱填料孵育1h,然后将孵育后的产物上柱,收集流出。用bindingbuffer清洗平衡柱子,用washingbuffer洗柱子,并收集流出。最后用elutionbuffer洗脱,收集流出。
c)纯化检测。对粗蛋白、洗杂流出、洗脱流出分别进行处理,制样,并准备sds-page检测(图4)。
d)透析浓缩。将纯度较好的组分6透析到蛋白保存缓冲液(1×pbs,20%glycerol,2mmdtt,0.1%skl,ph=8.0)中。透析结束后用peg20000浓缩,经0.22μm滤膜过滤后进行分装,-80℃保存。最后通过验证获得5mg,纯度>85%的类胡萝卜素氧化裂解酶重组蛋白(图5)。
上述缓冲液配方如下:
本发明所制备的类胡萝卜素氧化裂解酶可以用于体外降解类胡萝卜素。
序列表
<110>中国海洋大学
<120>一种扇贝类胡萝卜素氧化裂解酶基因及其应用
<160>2
<170>siposequencelisting1.0
<210>1
<211>521
<212>prt
<213>虾夷扇贝(patinopectenyessoensis)
<400>1
metlysserargsercysleuvalvalserleuleuleuthrleucys
151015
aspvalileglyleuglualavalproproalaaspaspaspasppro
202530
glyphegluaspilephelysthrasnthrlyssertyrgluasnphe
354045
hisvalglnpheasnglnproleuprolystrpleuargglyileleu
505560
valargasnglyalaglylysleuglumetglyserarglystyrleu
65707580
asntyrpheaspglytyralalysleuhissertrpthrphethrgly
859095
asnglyseralaphepheseralaglumetleumetserlysserphe
100105110
leusersergluarglysasnaspilegluprotyrleuthrphegly
115120125
glyvalasnpropropheaspvalalaglulysphealatrpmettyr
130135140
phelysmetasnasnmetasnvalasnvalphelystyralaasnarg
145150155160
thrvalalaileasnaspleutrpvalsertyrglupheaspleugln
165170175
thrleuasnthrileglypheargasnproprovalproproserlys
180185190
phetrpasnileglylysgluvalaspmetserseralahisproval
195200205
proglutyrglythrserserargphegluileilethrthrleuser
210215220
pheileproglythrlysglyargleuglyvalvalargilethrser
225230235240
leuaspthrthrglumetvalalaglutrpgluthrglulysserhis
245250255
tyrmethisserpheservalthrproasntyrvalileleupheala
260265270
alaprotyrthrvalserilethrlysmetleugluthrcysserval
275280285
gluglyglymetvaltrpaspglyasnalaasnthrthriletyrile
290295300
valgluilelysthrglythrleuhisthrleuglnthrgluasnval
305310315320
phevalthrhishisileasnalaphegluleuproaspglyargile
325330335
valleuaspleuprothrglnlysasnprophealapheasntyrphe
340345350
aspphesertyrilepheasnlysthralaargmetasnileileser
355360365
metproileleulysargtyrthrileaspilehislyslysserval
370375380
leulyslysthrphelysasnglyprolysalaprocysalaglyala
385390395400
leugluleuprovalileasngluasntyrarghisleuasntyrcys
405410415
tyriletyrglyhisvalileasntyrasnglylysglypheserhis
420425430
metalaleuvallyslysaspvalcysaspglualaglyaspleumet
435440445
tyralaalaprohisglntyrphethrgluprotrpphevalproasn
450455460
proleuglylysglugluaspaspglyvalleumetthrseralaphe
465470475480
aspglyaspmetlysglnsertyrleualaileleuaspprolysthr
485490495
metthrleuthrasnargalalysmetprothrthrvalpropheasn
500505510
phehisglyargphepheasnilepro
515520
<210>2
<211>1566
<212>dna
<213>虾夷扇贝(patinopectenyessoensis)
<400>2
atgaagtccagaagctgtctggtagtgtcacttttgcttaccctgtgtgacgtcattggt60
ttagaagcagtcccaccagcagacgacgatgacccagggtttgaagacatatttaagacc120
aacacgaagtcctacgagaatttccatgtacagtttaaccaacctttaccaaaatggctt180
cgtggaatattggtcagaaatggtgctgggaaactggaaatgggcagtaggaaatacctg240
aactattttgacgggtatgcaaaacttcacagttggacgtttactggaaacggatcggcc300
tttttttccgcggaaatgctaatgtcgaaatccttcttgtcttctgagaggaaaaatgac360
attgaaccttatctaacgttcgggggtgtcaatcctcccttcgatgtagctgaaaaattt420
gcttggatgtatttcaaaatgaataacatgaacgttaatgttttcaagtatgccaacaga480
acggtcgccatcaacgacttgtgggtttcctacgagttcgatcttcaaacattgaatact540
ataggatttaggaatccaccagttcctccgtcaaagttttggaatattggcaaagaagtt600
gacatgtcttctgctcatccagttccggagtatgggacgtcgtcaaggtttgaaattatc660
acaacattgagttttattcccggaaccaaaggtcggttaggcgtggtccggataacgtcc720
ctagataccacagagatggtggctgagtgggagacggagaaaagtcactacatgcattcg780
ttctctgtcacaccaaactatgtcatcctgttcgccgctccgtacaccgtcagcattacg840
aaaatgctggagacctgttcagtagagggtggaatggtttgggatgggaacgccaacacc900
accatatatattgtggagatcaagacaggaacgctacacacactacagacggagaacgtc960
ttcgttactcatcatataaatgcttttgaactgccagacggtagaatcgtgttggatctt1020
ccgacacagaaaaatcctttcgcttttaattatttcgacttttcatatatttttaataaa1080
actgctcggatgaatattatatcaatgcccatcctcaaacgatataccattgatattcac1140
aaaaaatctgtgttgaaaaagacattcaagaatggacctaaagctccctgcgcaggcgca1200
cttgaattgccggtgattaacgagaactaccgccacttgaactactgttacatctacggt1260
catgtgataaactataacgggaagggtttcagtcacatggctctggtcaaaaaggatgtg1320
tgtgacgaagccggggacctgatgtatgccgcaccccaccagtactttacagagccttgg1380
ttcgtccccaaccccttgggcaaggaggaggatgacggcgtgcttatgacgtcagctttt1440
gacggtgatatgaagcagagctaccttgccatactagaccctaaaacaatgacattgaca1500
aatcgcgccaaaatgcctacaactgtcccatttaactttcacggccggttctttaacatc1560
ccttga1566
- 还没有人留言评论。精彩留言会获得点赞!