一种用于组胺检测的电化学发光传感方法与流程
本发明涉及一种用于组胺检测的电化学发光传感方法,属于电化学传感器领域。
背景技术:
组胺(Histamine),又叫做:组胺双盐酸盐,组织胺等,分子式为:C5H9N3。组胺是一种自体活性物质,同时也是众多生物胺中的一种,在生命体中可以通过组氨酸脱羧基后形成。少量的组胺对机体有一定的好处,可以适当的调节神经活动,控制血压。但是在某些食品中,如鱼类、发酵食品、酒、饮料等,在组氨酸脱羧酶的作用下会形成组胺。机体中组胺过量时会产生危害,造成机体中毒。当机体摄入的组胺含量大于0.1g时,就会引起过敏性的食物中毒。因此,对加强对组胺的检测十分重要。
目前,检测组胺常用的方法有高效液相色谱(HPLC)、薄层色谱法(TLC)、气相色谱法(GC)、毛细管电泳(CE)、酶联免疫吸附法(ELISA)、放射性免疫法(RIA)、放射性酶法(REA)、毛细管电泳色谱法(CEC)等。其中,酶联免疫吸附法、放射性免疫法和放射性酶法是在抗原-抗体特异性识别的基础上建立的,选择性较好。早在1999年,Osman等人利用酶联免疫吸附法检测奶酪中的组胺,检测限达到10mg/kg。随后,A.Marcobal等人将此方法用于啤酒中组胺的检测,同样得到了很好的检测效果。单克隆抗体或多克隆抗体的制备是免疫检测方法的关键步骤,但是组胺属于小分子半抗原,分子量极小,不具有免疫原性,因此利用组胺作为免疫原,制备具有高特异性的组胺抗体非常困难。色谱方法由于检测灵敏度高,在实际中广泛应用,并且它可以和其他质谱检测方法联合使用,使检测效果得到进一步的提高,目前是大部分物质的国家标准检测方法。Vida等人利用高效液相色谱法检测了水产品中的组胺,得到了很好的检测结果。但这些利用大型仪器的检测方法要求对样品进行严格的前处理,并且前处理的效果直接关系到检测的结果,同时大型仪器一般价格比较昂贵,需要具有较高专业水平的操作人员。所以需要研制一种便捷、快速、灵敏度高、费用低的方法,应用于组胺的检测。
20世纪80年代电化学发光物质三联吡啶钌是这一阶段电化学传感研究的热点之一,主要将它用于有机酸、氨基酸、胺类化合物、草酸和丙酮酸等物质的测定。Bard小组在1984年将三联吡啶钌作为免疫标记物用于生物分子的研究;90年代,电化学发光分析方法的应用领域继续扩大。在电极材料研究方面,关于氧化铟锡(ITO)电极电化学发光实际应用领域的研究取得进展,并且将其和光导纤维技术进行结合,使电化学发光检测技术向便捷微电极和超微电极方向发展,这使得电化学发光分析法更适用于生物分子或具有活性的物质的研究。阵列电极技术和超声技术则使电极发光特性进一步提高。在电化学发光机理研究方面,表面活性剂对电化学发光的增强作用得到证明,有利于检测的灵敏度的提高。21世纪以后,电化学发光更加受到人们的关注。在食品安全、免疫分析、环境监测和临床等领域已经得到了成功的应用,正朝着快速、普适、低检测限、特异、固相方向发展;电化学发光设备朝着微型化、自动化和高速检测方向发展。
技术实现要素:
本发明利用含有阳离子的高分子材料Nafion膜修饰玻碳电极,通过与三联吡啶钌上的阳离子之间的离子交换作用将三联吡啶钌固定到电极表面,同时,在Nafion膜中掺入了两种纳米材料分别为多壁碳纳米管和纳米氧化锌颗粒,有效的解决了Nafion膜结构致密,不利于物质通过的缺点。MWCNTs的加入明显的增强了氧化还原峰电流,降低了氧化还原峰电位差。除此之外,MWCNTs带负电荷,可以吸附一定量的带正电荷的三联吡啶钌,增大了复合物膜对三联吡啶钌的固定量,从而增强了电化学发光信号,从另一方面提高了传感器的灵敏度,同时由于纳米材料具有比表面积大、导电性和光传导性好等优点,增加了检测的灵敏度,对传感器的信号起到了显著的放大作用。本发明利用胺基对三联吡啶钌的电化学发光的促进作用实现了对组胺的检测。本发明的优点是利用MWCNTs/ZnO/Nafion复合物膜修饰电极固定三联吡啶钌,减少了三联吡啶钌的用量,降低了实验的成本,减少了对环境的危害,也提高了实验的稳定性和重复利用率。本发明一种电化学传感方法对组胺的检测具有较宽范围宽和较低的检出限并且具有良好的稳定性,可以重复使用,可应用于实际样品中组胺的检测。
本发明的第一个目的是提供一种新型固化三联吡啶钌电化学发光传感器复合物膜
本发明的第二个目的是提供一种新型的固化三联吡啶钌电化学发光传感器检测组胺的方法
本发明的技术方案概述如下:利用胺基对三联吡啶钌电化学发光的促进作用制备用于组胺检测的电化学发光传感器。首先通过溶胶-凝胶法制备ZnO溶胶-凝胶,将其与Nafion溶液按一定的比例充分混合后加入一定量的MWCNTs,制得MWCNTs/ZnO/Nafion复合物膜,作为三联吡啶钌的固定基质。将制备的MWCNTs/ZnO/Nafion复合物膜通过悬涂的方式修饰到玻碳电极表面,得到MWCNTs/ZnO/Nafion修饰的玻碳电极,将此电极在三联吡啶钌的PBS溶液中孵育,固定三联吡啶钌,最后用于组胺浓度的检测,得到组胺浓度与电化学发光信号之间的线性关系。
本发明的有益效果是首次使用电化学传感方法检测了组胺,并且具有较宽的线性范围和较低的检出限,本发明一种检测组胺的电化学发光传感方法,由以下具体步骤实现:
1.裸玻碳电极的打磨
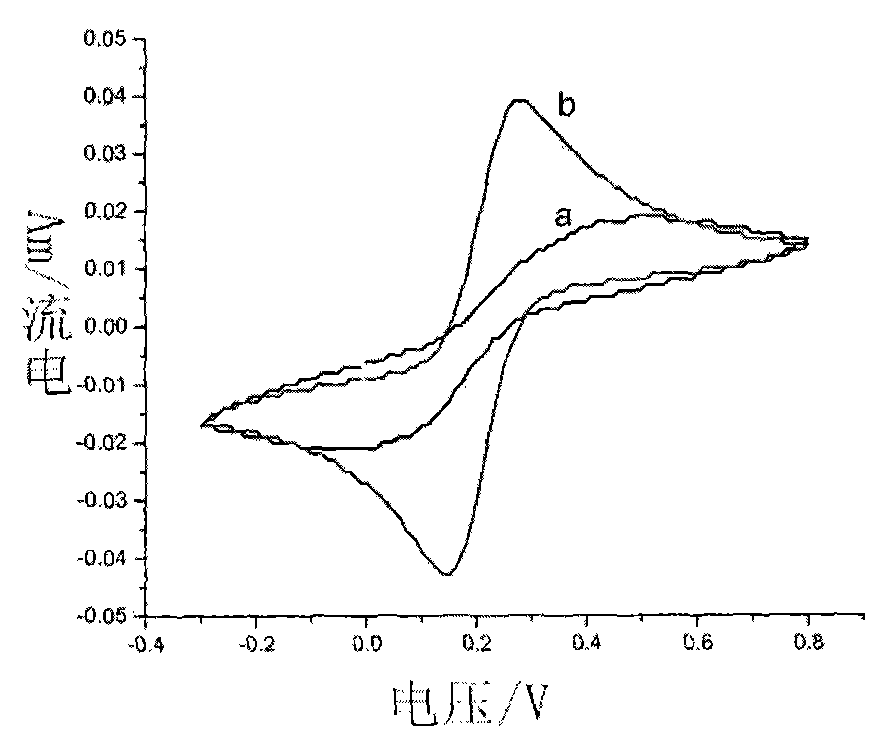
首先,将适量的30~50nm的Al2O3抛光粉放置在干净的麂皮上,滴加适量的去离子水后轻轻搅拌,调成匀浆。之后将玻碳电极竖直握住,肘部均匀用力,按照“8”字形或者圆形的路径在麂皮上缓慢的移动打磨。打磨后分别用无水乙醇和去离子水冲洗电极的表面。然后将裸玻碳电极、Ag/AgCl参比电极、铂丝对电极连接成三电极体系,组装到电化学工作站上,在含有2.5mmol/L的K3[Fe(CN)6]和2.5mmol/L的K4[Fe(CN)6]的混合溶液(v∶v=1∶1)中进行循环伏安法扫描。扫描的电压范围为-0.3V~0.8V,扫描速率为100mV/s。当得到的玻碳电极的循环伏安图中氧化还原峰电位差应在100mV以下,并且尽量接近64mV时,电极才可以后续使用。否则需要重新打磨处理,直到达到要求。将打磨前后的电极在含有2.5mmol/L的K3[Fe(CN)6]和2.5mmol/L的K4[Fe(CN)6]的混合溶液中的循环伏安图进行对比,如图1所示,电极经过 Al2O3打磨以后,氧化还原峰电流明显增强,氧化还原电位差减小。(注:a表示玻碳电极打磨之前;b表示玻碳电极打磨之后)
2. MWCNTs/ZnO/Nafion复合物膜修饰玻碳电极
首先将Zn(Ac)2的乙醇溶液在70℃搅拌至完全溶解得到Zn(Ac)2的乙醇溶液,取0.25ml 0.1mol/L的Zn(Ac)2的乙醇溶液冰浴15min后加入0.25ml 0.15mol/L的LiOH乙醇溶液和1.5ml的去离子水,冰浴条件搅拌4h,得到ZnO sol-gel。然后将制备的ZnO sol-gel与5%的Nafion溶液等体积混合,超声混匀制得ZnO/Nafion复合物。最后在ZnO/Nafion复合物中加入MWCNTs,得到MWCNTs/ZnO/Nafion复合物。用微量移液枪吸取10ul的MWCNTs/ZnO/Nafion复合溶液轻轻滴涂到打磨好的电极表面,确保没有气泡产生,然后室温晾干备用。通过MWCNTs/ZnO/Nafion复合物修饰的玻碳电极和不含MWCNTs的ZnO/Nafion复合物修饰的玻碳电极在0.5mol/LTPA的PBS(pH=7.8)溶液中的循环伏安曲线对比。如图2所示,MWCNTs对电信号有一个非常明显的放大作用,氧化还原峰电流从40uA左右上升到180uA左右,同时氧化还原电位差下降也非常明显。
3. Ru(bpy)32+的固定
将制备好的MWCNTs/ZnO/Nafion修饰的玻碳电极在0.01M Ru(bpy)32+的PBS溶液中循环伏安法连续扫描50圈,电压范围为0.6-1.5V,扫描速率为100mv/s。然后用去离子水反复冲洗,氮气吹干。此过程便将Ru(bpy)32+固定到了MWCNTs/ZnO/Nafion电极表面,通过循环伏安法电流的变化表征固定过程。
4 制备及检测条件的优化
4.1 MWCNTs/金属氧化物/Nafion复合物膜中金属氧化物的选择
(1)TiO2sol-gel的制备:将0.15mol/L Ti(OC4H9)4的异丙醇溶液1ml,去离子水5ml,0.1mol/L HCl(催化剂)混合,室温磁力搅拌1.5h后得到TiO2溶胶-凝胶(sol-gel)。
(2)ZnO sol-gel的制备:首先将Zn(Ac)2的乙醇溶液在70℃搅拌至完全溶解得到Zn(Ac)2的乙醇溶液,取0.25ml 0.1mol/L的Zn(Ac)2的乙醇溶液冰浴15min后加入0.25ml 0.15mol/L的LiOH乙醇溶液和1.5ml的去离子水,冰浴条件搅拌4h,得到ZnO sol-gel。
(3)SiO2sol-gel的制备:将50ul的TEOS,200ul的去离子水和10ul 0.1mol/L HCl混合后搅拌2h,得到SiO2sol-gel。
(4)Fe3O4sol-gel的制备:将10ml的KOH溶液和10ml的KNO3溶液混合,然后在混合溶液中缓慢的加入5ml的Fe3SO4溶液,充分搅拌以后在90℃水浴中陈化4h,便得到黑色的Fe3O4sol-gel。分别将制备的TiO2、ZnO、SiO2、Fe3O4sol-gel与5%的Nafion溶液等体积混合,超声混匀制得TiO2/Nafion、ZnO/Nafion、SiO2/Nafion、Fe3O4/Nafion四种复合物,然后分别在四种复合物中加入MWCNTs制得 MWCNTs/TiO2/Nafion、MWCNTs/ZnO/Nafion、MWCNTs/SiO2/Nafion、MWCNTs/Fe3O4/Nafion四种复合物。分别吸取10ul MWCNTs/TiO2/Nafion、MWCNTs/ZnO/Nafion、MWCNTs/SiO2/Nafion及MWCNTs/Fe3O4/Nafion复合物溶液滴涂到打磨好的玻碳电极表面,室温晾干。然后在Ru(bpy)32+的PBS溶液中循环伏安法连续扫描50圈,电压范围为0.6-1.5V,扫描速率为100mv/s。然后用去离子水冲洗,氮气吹干,制得固定有Ru(bpy)32+的不同复合物膜修饰的电极,将此电极在0.5mol/L TPA的PBS(pH=7.8)溶液中检测电化学信号和发光信号。通过对制备的含有四种不同金属氧化物(TiO2、ZnO、SiO2、Fe3O4)的MWCNTs/金属氧化物/Nafion复合物膜进行电化学以及化学发光检测结果对比发现,含有ZnO的MWCNTs/ZnO/Nafion复合物膜是最佳的选择。如图3所示,含有ZnO、SiO2的复合物膜的氧化还原峰几乎处在同一水平,明显优于含有TiO2、Fe3O4的两种复合物膜,如图4中,含有ZnO的复合物膜的光信号明显优于其他三种复合物膜。所以最终选择MWCNTs/ZnO/Nafion复合物膜作为Ru(bpy)32+固定的基底。
4.2 MWCNTs对电化学信号的影响
按照步骤2的方法制备了MWCNTs/ZnO/Nafion复合物修饰的玻碳电极和不含MWCNTs的ZnO/Nafion复合物修饰的玻碳电极。将制备好的电极在0.5mol/L TPA的PBS(pH=7.8)溶液中进行循环伏安法扫描,电压范围为0.2-1.3V,扫描速率为100mV/s。观察二者的电信号。分别制备MWCNTs浓度为0.25、0.50、0.75、1.00、1.25和1.5mg/ml的MWCNTs/ZnO/Nafion复合物膜,通过观察ECL信号检测的结果可以发现,如图5所示,当ECL信号随着MWCNTs浓度上升而上升,当浓度达到1.00mg/ml时,ECL信号达到最大值,之后随着MWCNTs浓度上升ECL开始下降,所以MWCNTs在MWCNTs/ZnO/Nafion复合物膜中的最佳浓度为1.00mg/ml。
4.3 组胺溶液pH对传感器电化学发光信号的影响
按照步骤2和步骤3的方法制备了Ru/MWCNTs/ZnO/Nafion修饰的玻碳电极,然后分别在pH为5.4、5.7、6.0、6.6、7.0、7.8、8.8、9.8的0.5mol/L组胺的PBS溶液中进行电化学发光信号的检测,电压范围为0.3-1.25V,扫描速率为100mV/s,每个pH值进行3次平行检测,记录检测结果。结果如图6所示,pH为7.8的时候,ECL信号最强,所以选择pH=7.8为最佳条件。
4.4 扫描速率对传感器电化学发光信号的影响
按照步骤2和步骤3的方法制备了Ru/MWCNTs/ZnO/Nafion修饰的玻碳电极,在0.5mol/L TPA的PBS溶液中进行电化学发光信号的检测,电压范围为0.3-1.25V,扫描速率为20、40、60、80、100、120、140、160和180mV/s,每个扫描速率进行3次平行检测,记录检测结果。如图7所示,随着扫描速率的增加,ECL信号也有一个明显的增加,当增加到100mV/s时,ECL信号达到最大值,之后随着扫描速率的增加,ECL信号反而逐渐下降。所以最佳的扫描速率为100mV/s。
4.5 电倍增管电压对传感器电化学发光信号的影响
按照步骤2和步骤3的方法制备了Ru/MWCNTs/ZnO/Nafion修饰的玻碳电极,在0.5mol/L TPA的PBS溶液中进行电化学发光信号的检测,电压范围为0.3-1.25V,光电倍增管电压分别为650、700、750、800、850、900、950、1000、1050、1100和1150V,每个电压水平进行3次平行检测,记录检测结果。如图8所示,光电倍增管电压为900V时,ECL信号最强,大于或小于900V,ECL信号均会下降。故900V为最适宜的光电倍增管电压强度。
5. 电化学发光传感器性能评价
5.1 传感器对组胺的响应实验
按步骤2和3制备好修饰有Ru/MWCNTs/ZnO/Nafion的玻碳电极,在PBS缓冲溶液和含有1×10-7mol/L组胺的PBS缓冲溶液中进行电化学发光信号的检测,检测条件是:光电倍增管电压为900V,扫面范围0.2-1.25V,扫描速率100mV/s。对比得到的两组结果。结果如图9所示(a:PBS缓冲溶液;b:组胺溶液),与在PBS缓冲溶液相比,在1×10-7mol/l的组胺PBS溶液中,Ru(bpy)32+的电化学发光信号得到明显增强,这表明组胺对三联吡啶钌的电化学发光具有增强作用。
5.2 干扰性实验
配置含有干扰物质Mg2+、CO32+、SO42+、Ca2+、K+、NH+、Cl-、BSA、5-羟色胺、1-咪唑乙酸和组氨酸的1×10-6g/ml的组胺溶液,其中Mg2+、CO32+、SO42+、Ca2+、K+、NH+、Cl-浓度为组胺浓度的200倍,BSA浓度为组胺浓度的300倍,5-羟色胺、1-咪唑乙酸和组氨酸浓度为组胺浓度的400倍。将修饰有Ru/MWCNTs/ZnO/Nafion的玻碳电极在上述各溶液中进行电化学发光检测,检测条件是:光电倍增管电压为900V,扫面范围0.2-1.25V,扫描速率100mV/s。记录各检测结果。如图10所示,加入干扰物质及结构类似物以后,并没有对组胺的检测造成干扰,含有干扰物质和不含干扰物质的组胺的检测结果(电化学发光信号)处在同一水平。这表明此传感器用于组胺检测的特异性和抗干扰能力良好,非常适用于组胺的检测。
5.3 重复性、稳定性实验
将修饰有Ru/MWCNTs/ZnO/Nafion的玻碳电极在1×10-7g/ml组胺溶液中进行电化学发光检测,连续扫描5次,观察其变化。按照相同的方法制备了五根Ru/MWCNT/ZnO/Nafion修饰的玻碳电极,在相同的条件下检测1×10-8g/mL的组胺的PBS,记录检测结果。将制备的Ru/MWCNT/ZnO/Nafion修饰的玻碳电极4℃冰箱保存,每隔一周用此电极检测一次1×10-6g/mL组胺的PBS溶液,持续5周,记录检测结果。检测条件是:光电倍增管电压为900V,扫面范围0.2-1.25V,扫描速率100mV/s。由图11所示,5次连续扫描的电化学发光信号基本上没有变化,处在同一检测水平,变化差值在误差允许范围之内。在相同的实验条件下制备5根Ru/MWCNT/ZnO/Nafion修饰的玻碳电极,在相同条件下分别将其用于1×10-8g/mL的组胺的PBS溶液的电化学发光信号的检测。由图12所示,5根电极的检测结果处在同一水平,测量差值在误差允许范围内。每隔一周将制备的Ru/MWCNT/ZnO/Nafion修饰的玻碳电极用于组胺检测,连续检测 5周,观察其电化学发光信号的衰减情况。如图13所示,其电化学发光信号下降幅度非常小,在误差允许的范围内。
5.4 检测范围及检测限
根据步骤2和步骤3制备Ru/MWCNT/ZnO/Nafion电极,然后在浓度为1×10-10-1.0mg/ml的组胺的PBS溶液中进行电化学发光检测。检测条件是:光电倍增管电压为900V,扫面范围0.2-1.25V,扫描速率100mV/s。记录检测数据,观察电化学发光信号与组胺浓度之间的关系。在1×10-9~1×10-5g/mL范围内时,组胺浓度的lg值(lgC)与电化学发光信号(I)的峰强呈现良好的线性关系,即随着组胺浓度的增大,电化学发光信号也会逐渐增强,如图14所示,经过拟合后得到的线性方程为I=326.71gC+4917.9,R2=0.9968,通过计算得到此传感器的检出限(3N/S)为6.4×10-9g/mL。
附图说明
图1玻碳电极打磨前后对比
图2MWCNTs放大效果
图3分别含有TiO2、ZnO、SiO2、Fe3O4复合物膜的电化学信号对比图
图4分别含有TiO2、ZnO、SiO2、Fe3O4复合物膜的电化学发光对比图
图5MWCNTs/ZnO/Nafion复合物膜中MWCNTs浓度的优化
图6组胺溶液pH值的优化
图7扫描速率的优化
图8光电倍增管电压的优化
图9组胺增强Ru(bpy)32+电化学发光图
图10传感器对不同干扰物的特异性曲线
图11连续扫描5次1×10-7g/ml组胺溶液的ECL信号
图12 5根相同条件电极对1×10-8g/mL组胺溶液的ECL信号
图13连续检测5周的ECL信号
图14ECL信号与不同组胺浓度lg值之间的线性关系
具体实施方式
以下的实施例便于更好地理解本发明,但并不限定本发明。下述实施例中的实验方法,如无特殊说明,均为常规方法。下述实施例中所用的试剂与材料,如无特殊说明,均可从常规试剂公司购买得到。
本发明的技术方案:一种用于组胺检测的电化学发光传感方法:
实施例1
根据步骤2和步骤3制备Ru/MWCNT/ZnO/Nafion电极,然后在浓度为1×10-10-1.0mg/ml的组胺的PBS溶液中进行电化学发光检测。检测条件是:光电倍增管电压为900V,扫面范围0.2-1.25V,扫描速率100mV/s。记录检测数据,观察电化学发光信号与组胺浓度之间的关系。在1×10-9~1×10-5g/mL范围内时,组胺浓度的lg值(lgC)与电化学发光信号(I)的峰强呈现良好的线性关系,即随着组胺浓度的增大,电化学发光信号也会逐渐增强,如图14所示,经过拟合后得到的线性方程为I=326.71gC+4917.9,R2=0.9968,通过计算得到此传感器的检出限(3N/S)为6.4×10-9g/mL。
实际样品加标回收实验
取5g市售的鱼肉,捣碎,将捣碎后的均质置于20ml的去离子水中,充分搅拌,室温下离心,取1ml上清液加入到9ml PBS缓冲溶液中,即得到待测实际样品,对其进行检测。同时将实际样品均分为三等份,分别添加组胺,得到加标量分别为2×10-6、2×10-7、2×10-8g/ml的组胺加标溶液,对其进行加标量的检测。加标实验结果如表所示,加标回收率范围为98.00%-103.00%,相对标准偏差(RSD)范围为2.23%-3.70%。
实际样品加标回收结果
- 还没有人留言评论。精彩留言会获得点赞!
- 一种固定三联吡啶钌及电化学发光检测亮蓝的方法与制造工艺
- 一种基于双极电极阵列的可视化电化学发光传感器检测葡萄糖的方法与制造工艺
- 一种电化学发光快速检测抗生素ZwittermicinA浓度的方法与制造工艺
- 一种纳米金铜猝灭硫化锌镉电致发光胰岛素传感器的制备方法与制造工艺
- 一种基于CdSe/ZnS量子点纳米簇的电化学发光生物传感器及其制法和应用的制造方法与工艺
- 一种Fe3O4固载Ru(bpy)32+检测刀豆凝集素A的电化学发光传感器的制造方法与工艺
- 一种基于纸电化学发光芯片的POCT装置的制造方法
- 免疫分析系统及其开盖装置的制造方法
- 一种电化学发光免疫分析仪及其固体废物装置的制造方法
- 一种电化学发光免疫分析仪及其搅拌装置的制造方法