一种基于普鲁士蓝膜生物电极对葡萄糖的检测方法与流程
本发明涉及一种基于普鲁士蓝膜生物电极对葡萄糖的检测方法,属于发酵工业技术领域。
背景技术:
葡萄糖是很多发酵产物的主要碳源,葡萄糖的调控必需符合菌种的代谢特点,防止出现因为葡萄糖浓度偏大或偏小的情况,即要严格控制其在发酵液中的浓度。在发酵前期,如果葡萄糖浓度太高,容易对菌体生长产生阻遏、抑制和限制作用;在发酵后期,如果葡萄糖浓度过低,则会限制菌体生长和产物合成。因此目前工业中常使用过程流加葡萄糖,辅助在线检测葡萄糖浓度,从而实现葡萄糖的稳定控制,取得良好的性结果。葡萄糖作为生物体内重要的供能物质,与人类的日常生活息息相关。对葡萄糖的检测,在食品工业中的质量监测、化工发酵过程的控制及糖尿病病情诊断有着重要的意义。葡萄糖的传统检测方法有光学法和电化学法。其中,电化学法中的酶电极法因具有高的灵敏度、优良的选择性和操作简便等优点受到广泛关注。近年来,酶生物传感器的研究得到了飞速的发展。普鲁士蓝(pb)是一种无机铁氰配位化合物,由于其优良的电化学可逆性、稳定性以及h2o2具有特异性的电催化活性,被誉为“人工过氧化物酶”。而h2o2是酶促反应中常见的产物之一,因此,pb薄膜被广泛应用于酶电化学生物传感器的构建。一种高灵敏度、低成本的葡萄糖生物传感器这个技术是基于在丝网印刷碳电极上,采用层层自组装法制备普鲁士蓝薄膜,同时基于戊二醛交联法在薄膜上固定葡萄糖氧化。
现有相似的技术是在基于电子传递的葡萄糖电化学生物传感器使用的酶墨不稳定、检测灵敏度缺陷而制备了一种用于葡萄糖检测的酶墨,它的方法是将不同浓度的葡萄糖加入检测装置,用线性伏安法进行测量,得到不同浓度的葡萄糖溶液的电流随电位变化的关系图,结合极化电阻的倒数与葡萄糖浓度间的标准曲线便可得到葡萄糖溶液的浓度。
技术实现要素:
现有技术的所有缺点:目前检测葡萄糖的方法主要有高效液相色谱法、气相色谱法、分光光度法、近红外、电化学生物传感器等。其中,高效液相色谱法应用范围最为广阔,但其需要昂贵的大型仪器设备,且不便于携带;气相色谱法精度相对较高,但需对葡萄糖进行硅醚处理,操作复杂;分光光度法需加入显色剂,会污染葡萄糖溶液,操作过程比较繁琐,检测精度低。
为解决现有技术存在的缺陷,解决上述技术问题,本发明的目的是提出基于普鲁士蓝膜生物电极而设计的一种检测葡萄糖的方法,普鲁士蓝膜生物电极是属于电化学传感器,其具有线性检测范围宽、成本低、操作简便、灵敏度高等优点,在葡萄糖检测中具备很好的应用前景。
本发明是在一种基于普鲁士蓝膜生物电极的检测装置上而设计的一种检测方法,检测装置由样品池,蠕动泵,磁力搅拌器构成,把电磁学和化学很好的结合了起来,使用磁力搅拌器带动搅拌子旋转,使得加入的葡萄糖与培养液迅速均匀混合从而使得检测的葡萄糖更准确,也使得检测时间减短,通过蠕动泵来进样使得样品池的每次检测葡萄糖的时候液位是相同的,也使得测量准确。
本发明采用如下技术方案:一种基于普鲁士蓝膜生物电极对葡萄糖的检测方法,其特征在于,具体包括如下步骤:
步骤ss1:将普鲁士蓝膜生物电极的插入端插入样品池中,所述普鲁士蓝膜生物电极的插入端上设置有与葡萄糖反应的酶,普鲁士蓝膜生物电极的输出端电联接检测电路,进行样品池清洗;
步骤ss2:向样品池中加入定量已知浓度的葡萄糖溶液,检测电路的电流值稳定后,用来激活所述普鲁士蓝膜生物电极上的与葡萄糖反应的酶,再按照所述步骤ss1的方法进行样品池清洗;
步骤ss3:向样品池中加入定量已知浓度的葡萄糖溶液,检测电路的电流值稳定后进行高点标定,再按照所述步骤ss1的方法进行样品池清洗;
步骤ss4:向样品池中加入定量已知浓度的葡萄糖溶液,所述检测电路进行测试,检测电路的电流值稳定后,若测得葡萄糖溶液的浓度范围在所述已知浓度的95%~105%以内,判定高点标定成功,按照步骤ss1的方法进行样品池清洗,并转入步骤ss6;否则继续判断测试次数是否超过三次,若没有则转入步骤ss3,否则更换普鲁士蓝膜生物电极,按照步骤ss1的方法进行样品池清洗;
步骤ss5:不向样品池中注入葡萄糖溶液,检测电路的电流值稳定后进行低点标定;
步骤ss6:向样品池中加入定量未知的葡萄糖溶液,待检测电路的电流值稳定后,所述检测电路显示浓度则为待测葡萄糖溶液的浓度;
步骤ss7:每次检测未知的葡萄糖溶液前就按照步骤ss1的方法进行样品池清洗一次。
作为一种较佳的实施例,所述步骤ss1中的样品池清洗包括如下步骤:通过控制一个进水蠕动泵和一个出水蠕动泵对样品池进行清洗,先是出水蠕动泵将样品池原有的溶液抽干,然后进水蠕动泵将缓冲溶液pbs注入样品池,接着进水蠕动泵泵和出水蠕动泵泵同进同出一段时间,然后进水蠕动泵停止,出水蠕动泵再将样品池中的缓冲溶液pbs抽干后,进水蠕动泵再将缓冲溶液pbs注入样品池中。
作为一种较佳的实施例,所述已知浓度的葡萄糖溶液和所述未知浓度的葡萄糖溶液的定量为20微升。
作为一种较佳的实施例,所述已知浓度的葡萄糖溶液的浓度为100g/l。
作为一种较佳的实施例,所述步骤ss2中的检测电路的电流值为1900~2100na。
作为一种较佳的实施例,所述步骤ss3中的检测电路的电流值为1900~2100na。
作为一种较佳的实施例,所述步骤ss4中的检测电路的电流值为1900~2100na。
作为一种较佳的实施例,所述步骤ss5中的检测电路的电流值为380~420na。
作为一种较佳的实施例,所述步骤ss6中的检测电路的电流值为1900~2100na。
作为一种较佳的实施例,所述样品池的内部设置有若干搅拌转子,所述样品池的外部设置有与所述搅拌转子相配合的磁力搅拌机,所述磁力搅拌机带动所述搅拌转子在样品池的葡萄糖溶液中转动,使得加入葡萄糖溶液时迅速均匀混合,加快检测速度,同时也使测量更准确。
作为一种较佳的实施例,葡萄糖反应的酶为葡萄糖氧化酶溶液与明胶溶液的混合溶液。
本发明所达到的有益效果:第一,本发明提出的针对葡萄糖的检测方法是基于普鲁士蓝膜生物电极而设计的;第二,本发明清洗样品池的方法,通过清洗两次使得样品池干净,不含有杂质,使得检测浓度更精确;第三,本发明在检测葡萄糖溶液的培养液的液位是相同的,这是通过蠕动泵来控制的,减少测量误差;第四,本发明加入了磁力搅拌机和搅拌转子,使得加入葡萄糖溶液迅速均匀混合,使得检测时间减短,也使得测量误差减小。
附图说明
图1是本发明的一种基于普鲁士蓝膜生物电极对葡萄糖的检测方法的流程图。
图2是本发明的样品池的一个实施例的结构示意图。
图3是本发明的磁力搅拌装置的一个实施例的结构示意图。
图4是本发明的支架的一个实施例的结构示意图。
图5是本发明的硅胶密封垫的一个实施例的结构示意图。
图6是本发明的普鲁士蓝膜生物传感器的一个实施例的结构示意图。
图7是本发明的空心池体的一个实施例的剖视图的结构示意图。
图8是图7的俯视图的结构示意图。
图9是本发明的旋紧盖的一个实施例的剖视图的结构示意图。
图10是图9的俯视图的结构示意图。
图11是本发明的检测电路的一个实施例的电路结构图。
图12是检测电路的lmp91000芯片的电路原理图。
具体实施方式
下面结合附图对本发明作进一步描述。以下实施例仅用于更加清楚地说明本发明的技术方案,而不能以此来限制本发明的保护范围。
图1是本发明的一种基于普鲁士蓝膜生物电极对葡萄糖的检测方法的流程图。本发明提出一种基于普鲁士蓝膜生物电极对葡萄糖的检测方法,其特征在于,具体包括如下步骤:
步骤ss1:将普鲁士蓝膜生物电极的插入端插入样品池中,所述普鲁士蓝膜生物电极的插入端上设置有与葡萄糖反应的酶,普鲁士蓝膜生物电极的输出端电联接检测电路,进行样品池清洗;
步骤ss2:向样品池中加入定量已知浓度的葡萄糖溶液,检测电路的电流值稳定后,用来激活所述普鲁士蓝膜生物电极上的与葡萄糖反应的酶,再按照所述步骤ss1的方法进行样品池清洗;
步骤ss3:向样品池中加入定量已知浓度的葡萄糖溶液,检测电路的电流值稳定后进行高点标定,再按照所述步骤ss1的方法进行样品池清洗;
步骤ss4:向样品池中加入定量已知浓度的葡萄糖溶液,所述检测电路进行测试,检测电路的电流值稳定后,若测得葡萄糖溶液的浓度范围在所述已知浓度的95%~105%以内,判定高点标定成功,按照步骤ss1的方法进行样品池清洗,并转入步骤ss6;否则继续判断测试次数是否超过三次,若没有则转入步骤ss3,否则更换普鲁士蓝膜生物电极,按照步骤ss1的方法进行样品池清洗;
步骤ss5:不向样品池中注入葡萄糖溶液,检测电路的电流值稳定后进行低点标定;
步骤ss6:向样品池中加入定量未知的葡萄糖溶液,待检测电路的电流值稳定后,所述检测电路显示浓度则为待测葡萄糖溶液的浓度;
步骤ss7:每次检测未知的葡萄糖溶液前就按照步骤ss1的方法进行样品池清洗一次。
作为一种较佳的实施例,所述步骤ss1中的样品池清洗包括如下步骤:通过控制一个进水蠕动泵和一个出水蠕动泵对样品池进行清洗,先是出水蠕动泵将样品池原有的溶液抽干,然后进水蠕动泵将缓冲溶液pbs注入样品池,接着进水蠕动泵泵和出水蠕动泵泵同进同出一段时间,然后进水蠕动泵停止,出水蠕动泵再将样品池中的缓冲溶液pbs抽干后,进水蠕动泵再将缓冲溶液pbs注入样品池中。
作为一种较佳的实施例,所述已知浓度的葡萄糖溶液和所述未知浓度的葡萄糖溶液的定量为20微升。
作为一种较佳的实施例,所述已知浓度的葡萄糖溶液的浓度为100g/l。
作为一种较佳的实施例,所述步骤ss2中的检测电路的电流值为1900~2100na。
作为一种较佳的实施例,所述步骤ss3中的检测电路的电流值为1900~2100na。
作为一种较佳的实施例,所述步骤ss4中的检测电路的电流值为1900~2100na。
作为一种较佳的实施例,所述步骤ss5中的检测电路的电流值为380~420na。
作为一种较佳的实施例,所述步骤ss6中的检测电路的电流值为1900~2100na。
作为一种较佳的实施例,所述样品池的内部设置有若干搅拌转子,所述样品池的外部设置有与所述搅拌转子相配合的磁力搅拌机,所述磁力搅拌机带动所述搅拌转子在样品池的葡萄糖溶液中转动,使得加入葡萄糖溶液时迅速均匀混合,加快检测速度,同时也使测量更准确。
作为一种较佳的实施例,葡萄糖反应的酶为葡萄糖氧化酶溶液与明胶溶液的混合溶液,其具体的制备过程参考中国专利cn101105471a。
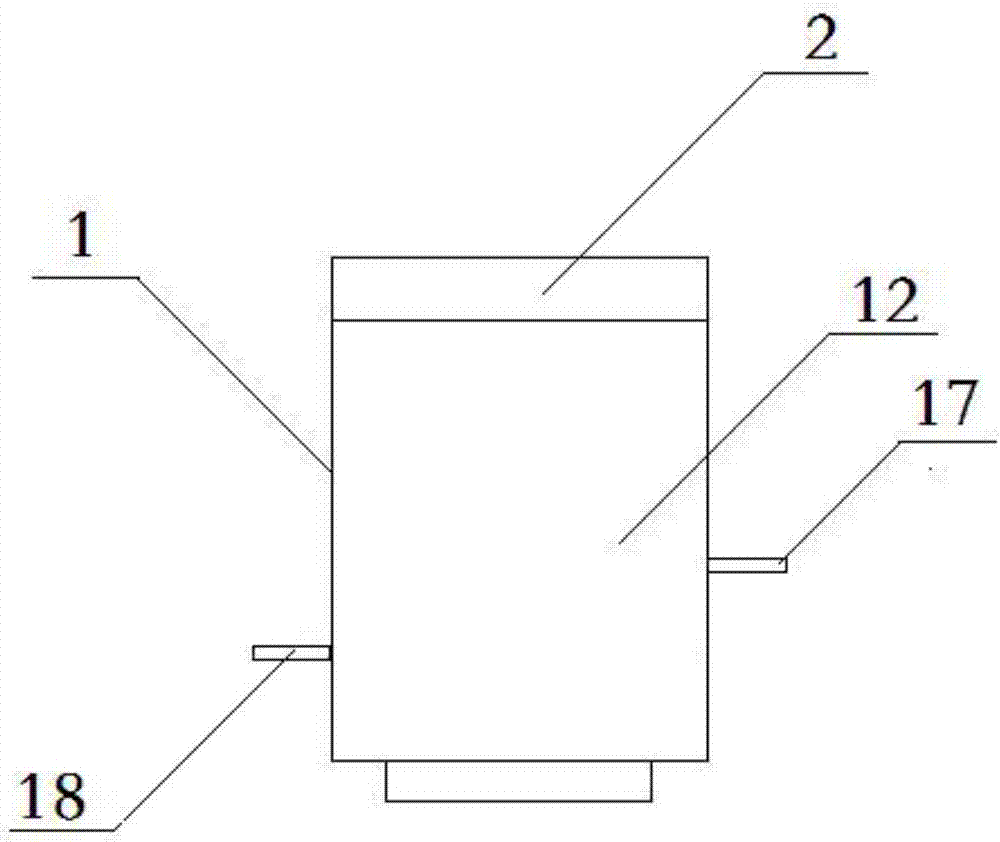
图2是本发明的样品池的一个实施例的结构示意图。图3是本发明的磁力搅拌装置的一个实施例的结构示意图。图4是本发明的支架的一个实施例的结构示意图。本发明提出一种基于普鲁士蓝膜生物电极检测的装置,包括样品池1、磁力搅拌装置3、支架4,样品池1固定设置于支架4的上方,磁力搅拌装置3固定设置于支架4的下方;样品池1包括空心的池体12、中空的旋紧盖2、硅胶密封垫5,池体12的顶部外壁与旋紧盖2的底部内壁采用螺纹连接,池体12的内部设置有中空的腔体、包裹腔体的池体内壁13,硅胶密封垫5嵌套设置于池体12的腔体中,腔体中设置有溶液,硅胶密封垫5上插装有普鲁士蓝膜生物电极传感器6;池体12的底部分别设置有进水口14、出水口15,进水口14的外端、出水口15的外端分别连通用来进出水的蠕动泵,池体12的腔体内还设置有与磁力搅拌装置3相配合的用来搅拌溶液用的从动转子。
作为一种较佳的实施例,池体12的腔体采用倒圆台设计,防止转子搅拌溶液时出现大量的漩涡而干扰普鲁士蓝膜生物电极传感器6正常工作,具备一定的抗干扰能力。
作为一种较佳的实施例,进水口14设置于出水口15的上方,有利于将样品池1内的溶液排净;进水口14通过外接的进水管17与蠕动泵相连通,出水口15通过外接的出水管18与蠕动泵相连通。
作为一种较佳的实施例,池体12的底部设置有圆柱体状的池底16,用于与支架4相连接。
作为一种较佳的实施例,旋紧盖2包括中间镂空的旋紧盖体22,旋紧盖体22的上部中间设置有镂空圆柱体内壁21,旋紧盖体22的下部内壁刻设有用来与池体12连接的连接内螺纹23;旋紧盖体22用来实现样品池1的密封,中空镂空的设计一方面是为了将普鲁士蓝膜生物电极传感器6的电极的接线引出,另一方面方便注射溶液。
图5是本发明的硅胶密封垫的一个实施例的结构示意图。作为一种较佳的实施例,硅胶密封垫5的中间开设有电极条缝51,电极条缝51用来插装普鲁士蓝膜生物电极传感器6,硅胶密封垫5上还设置有用来注射葡萄糖溶液的注射孔52。
作为一种较佳的实施例,磁力搅拌装置3包括直流电机31、主动转子32、电机传动轴33、旋转托盘34、支架安装板35,直流电机31固定设置于支架安装板35的底部,电机传动轴33设置于支架安装板35的上方,直流电机31的输出端与电机传动轴33的底端配合联接,电机传动轴33的顶端与旋转托盘34的中间固定连接,旋转托盘34随电机传动轴33同向转动,主动转子32对称固定设置于旋转托盘34上,主动转子32与样品池1中的从动转子磁力配合,支架安装板35的两侧与支架4的两侧固定连接。
作为一种较佳的实施例,支架4的顶部开设有与样品池1的底部相配合的池底安装槽41,支架4的两侧分别开设有紧固连接孔42,支架4的两侧通过紧固连接孔42与磁力搅拌装置3固定连接。
图6是本发明的普鲁士蓝膜生物传感器的一个实施例的结构示意图。作为一种较佳的实施例,普鲁士蓝膜生物电极传感器6为三电极传感器。
作为一种较佳的实施例,从动转子为内嵌磁铁外包裹硅胶的可浮动式转子。
下面分别从具体的材料、结构和使用方法上对本发明作出进一步的说明。
材料方面:①样品池1的主体即池体12和旋紧盖2均采用有机玻璃,其优点高度透明,能观察到样品池内部情况,耐腐蚀,耐湿,绝缘性能好,不会影响电极工作;②硅胶密封垫5上可插普鲁士蓝膜生物电极传感器6,其优点一方面方便经常更换普鲁士蓝膜生物电极传感器的电极,另一方面实现样品池1的密封,硅胶密封垫5具有很好的弹性及耐磨性,硅胶密封垫5置于池体12与旋紧盖2之间,一旦将旋紧盖2旋紧,硅胶密封垫5受力均匀,会将普鲁士蓝膜生物电极传感器6卡紧,即可实现样品池1的密封性,同时也使得普鲁士蓝膜生物传感器6的电极不会被浸湿;③进水管17和出水管18采用的是直径3mm的不锈钢毛细管;④底部的支架4采用绝缘材料,比如如塑料、陶瓷等,避免干扰主动转子32和从动转子旋转。
结构方面:①样品池1的腔体内采用倒圆台的设计,为了防止从动转子搅拌溶液时出现大量的漩涡而干扰普鲁士蓝膜电极传感器正常工作,具备一定的抗干扰能力;②池体12的底部两侧分别设置有进水口14和出水口15,进水口14在上,出水口15在下,出水口15在下的优点是有利于样品池1内的溶液排净,通过蠕动泵进行进出水,不必对样品池1拆卸即可完成清洗、进样等操作;③池体12的底部池底16为凸圆柱体,用于与底部的支架4的连接;④旋紧盖2为中间镂空的圆柱体,旋紧盖2能够实现样品池1的密封,中空设计一方面是为了将普鲁士蓝膜生物电极传感器6的三个电极的接线引出,另一方面方便通过注射孔52注射葡糖糖溶液;⑤样品池1的腔体和旋紧盖2之间通过螺纹旋紧,其间加入一硅胶密封垫5,一方面用于普鲁士蓝膜生物电极传感器6的电极的安装,另一方面实现密封性,三者配合使用操作简单,便于安装和拆卸。
支架4的材料选择:采用绝缘材料,以防止干扰主动转子32和从动转子的转速,从而避免影响普鲁士蓝膜生物电极传感器6检测溶液的浓度,具备一定的抗干扰能力。
结构方面:支架4顶部有一直径比样品池1底部稍大的凹槽(即池底安装槽41),这样方便与样品池1相连接,起到对样品池1的固定作用。
使用方法:首先,将两个蠕动泵接在进水口14、出水口15上,并将从动转子放入样品池1的腔体中,然后将普鲁士蓝膜生物电极传感器6插在硅胶密封垫5上,将硅胶密封垫5置于腔体的顶部,用中空的旋紧盖2旋紧,支架4置于磁力搅拌装置3的直流电机31之上,并将样品池1置于支架4上即可。
图7是本发明的空心池体的一个实施例的剖视图的结构示意图。图8是图7的俯视图的结构示意图。图9是本发明的旋紧盖的一个实施例的剖视图的结构示意图。图10是图9的俯视图的结构示意图。
材料:池体12、旋紧盖体22均采用有机玻璃,进水口14连通的进水管17、出水口15连通的出水管18均采用3mm不锈钢毛细管。
结构:池体12的外观上为三段圆柱体,顶部圆柱体为池体12的颈部,刻设有连接外螺纹11,用于与旋紧盖2相连接;中间部分的圆柱体为池体12的腔体,其池体内壁13为倒圆台设计,用于存放溶液;池体12的左右两侧钻有进水口14、出水口15,进水口14在上,出水口15在下;底部为凸圆柱体(即池底16)主要用于与支架4相连。旋紧盖2的外观上为圆柱体,内部为上下两个直径上小下大镂空的圆柱体,镂空大圆柱体设有连接内螺纹23,用于与池体12颈部的连接外螺纹11相连。
图11是本发明的一个实施例的电路结构图。本发明提出一种针对普鲁士蓝膜生物电极的检测电路,其特征在于,包括主芯片62、lmp91000芯片61、第一接线端子64、第二接线端子63、三芯屏蔽线65、连接器66、鲁士蓝膜生物电极传感器67、基准电源68,主芯片62与lmp91000芯片61相连接,lmp91000芯片61分别与第二接线端子63、基准电源68相连接,第二接线端子63与第一接线端子64相连接,第一接线端子64通过三芯屏蔽线65与连接器66相连接,连接器66与普鲁士蓝膜生物电极传感器67相连接,lmp91000芯片61与第二接线端子63之间、第一接线端子64与三芯屏蔽线65之间均设置有屏蔽层69。
作为一种较佳的实施例,稳压电源68采用精密的稳压芯片,型号如adr4533。
作为一种较佳的实施例,lmp91000芯片61的12号引脚、13号引脚、14号引脚、15号引脚分别接第二接线端子63的工作电极we、参考电极re、对电极ce、lmp91000芯片61与第二接线端子63之间的屏蔽层69,第一接线端子64的工作电极we、参考电极re、对电极ce分别接三芯屏蔽线65的工作电极we、参考电极re、对电极ce,三芯屏蔽线65的工作电极we、参考电极re、对电极ce分别与连接器66的工作电极we、参考电极re、对电极ce相连接。
作为一种较佳的实施例,lmp91000芯片61的1号引脚接地;lmp91000芯片61的2号引脚接主芯片62,作为模块使能;lmp91000芯片61的3号引脚接电阻r2的一端,电阻r2的另一端连接主芯片62,用来给i2c接口兼容接口时钟信号;lmp91000芯片61的4号引脚接电阻r3的一端,电阻r3的另一端连接主芯片62,用来给i2c接口兼容接口数据;lmp91000芯片61的3号引脚与lmp91000芯片61的4号引脚之间连接有电阻r4、电阻r5,用来防止通讯信号回波;如图1所示的②③可实现串行通讯。
作为一种较佳的实施例,lmp91000芯片61的6号引脚分别接电源vcc、电容c6的一端,电容c6的另一端接地,用来对供电电压进行滤波,电源vcc的电压为5v;lmp91000芯片61的7号引脚接地。
作为一种较佳的实施例,lmp91000芯片61的8号引脚接电阻r1的一端,电阻r1的另一端与主芯片62、电容c5的一端并联,电容c5的另一端接地,用来对输出信号进行滤波,如图1所示④实现了ad采集。
作为一种较佳的实施例,lmp91000芯片61的9号引脚与lmp91000芯片61的10号引脚之间接入电容c3,用来实现信号放大滤波。
作为一种较佳的实施例,lmp91000芯片61的11号引脚分别接基准电源68、电容c4的一端,电容c4的另一端接地,用来对基准电源68的电压进行滤波;基准电源68的电压为3v。
作为一种较佳的实施例,连接器66的型号为5-520315-3,主芯片62的型号为stm32f407vgt6,可以替换为带有i2c接口并且自带adc转换的芯片或者替换为带有i2c的芯片,同时需要一个ad转换器通过i/o口与主芯片62连接。
作为一种较佳的实施例,第一接线端子64的型号为kf2edgk的4p接线端子;第二接线端子63的型号为kf2edgr的4p接线端子。
图12是本发明的lmp91000芯片的电路原理图。作为一种较佳的实施例,lmp91000芯片61的内部设置有控制放大器611、可调偏置电阻612、参考分配器613、i2c接口614、控制寄存器615、温度传感器616、跨导放大器617,控制放大器611的输出端通过ce接口与普鲁士蓝膜生物电极传感器67的对电极ce相连接,控制放大器611的反向输入端通过re接口与普鲁士蓝膜生物电极传感器67的参考电极re相连接,控制放大器611的反向输入端依次通过开关元件k1、可调电阻rload、we接口与普鲁士蓝膜生物电极传感器67的工作电极we相连接,控制放大器611的同向输入端接可调偏置电阻612的一端,可调偏置电阻612的另一端接参考分配器613,参考分配器613与跨导放大器617的同向输入端相连接,跨导放大器617的反向输入端分别与开关元件k1、可调电阻rload相连接,跨导放大器617的反向输入端与跨导放大器617的输出端接入可调电阻rtia,跨导放大器617的输出端、温度传感器616分别通过开关元件k2接用来模拟输出的vout接口,参考分配器613通过开关元件k3分别接用来电压基准输入的vref接口、用来提供电源电压的vdd接口,we接口与vout接口之间串联依次设置有内部无连接的nc接口、用来作为外部滤波器连接器的c1接口和c2接口、用来连接lmp91000芯片61的agnd的dap接口、agnd接口;lmp91000芯片61的we接口用来驱动普鲁士蓝膜生物电极传感器67的工作电极we的输出,lmp91000芯片61的re接口用来驱动普鲁士蓝膜生物电极传感器67的对电极ce的输入,lmp91000芯片61的ce接口用来驱动普鲁士蓝膜生物电极传感器67的对电极ce的输出;i2c接口614与控制寄存器615相连接,i2c接口614分别接用来兼容i2c接口614时钟信号的scl接口、用来兼容i2c接口614数据的sda接口,控制寄存器615接menb接口,menb接口具有模块使能,低电平有效;menb接口与vout接口之间还连接用来接地的有dgnd接口。
本发明的优点在于:第一,本发明是针对普鲁士蓝膜生物电极的检测电路;第二,本发明的电容c6实现供电电压滤波;电容c3实现信号放大滤波;电容c4实现基准电压滤波;电容c5实现输出信号滤波;第三,本发明通过连接器66,三芯屏蔽线65,第一接线端子64、第二接线端子63将基于普鲁士蓝膜生物电极的传感器67与lmp91000芯片61连接起来,接口插拔稳定;第四,本发明可以针对不同酶的活性,可通过对i2c接口编程实现对信号不同程度的放大;第五,本发明的基准电源,采用精密的稳压芯片,如adr4533,可以很好的稳定电压,能保证本发明的检测电路的电流值稳定,从而根据检测电路的电流推导出普鲁士生物蓝膜电极传感器的采集的溶液浓度;第六,本发明的基于普鲁士蓝膜生物电极生物传感器67具有高灵敏度,宽的线性范围,低的检测极限,同时具有优良的重复性、稳定性和抗干扰能力,成本低廉;第八,本发明与基于普鲁士蓝膜生物电极传感器连接的检测电路采用三芯屏蔽双绞线,保护信号,抗干扰性强,同时多处采用滤波,使信号输出稳定。
名词解释:普鲁士蓝(pb)是一种无机铁氰配位化合物,由于其优良的电化学可逆性、稳定性以及h2o2具有特异性的电催化活性,被誉为“人工过氧化物酶”。而h2o2是酶促反应中常见的产物之一,因此,pb薄膜被广泛应用于酶电化学生物传感器的构建。
以上所述仅是本发明的优选实施方式,应当指出,对于本技术领域的普通技术人员来说,在不脱离本发明技术原理的前提下,还可以做出若干改进和变形,这些改进和变形也应视为本发明的保护范围。
- 还没有人留言评论。精彩留言会获得点赞!